一种阿托伐他汀钙中有关物质的检测方法与流程
本发明属于生物医药
技术领域:
,具体涉及一种阿托伐他汀钙中有关物质(阿托伐他汀钙安奈德叔丁酯)的检测方法。
背景技术:
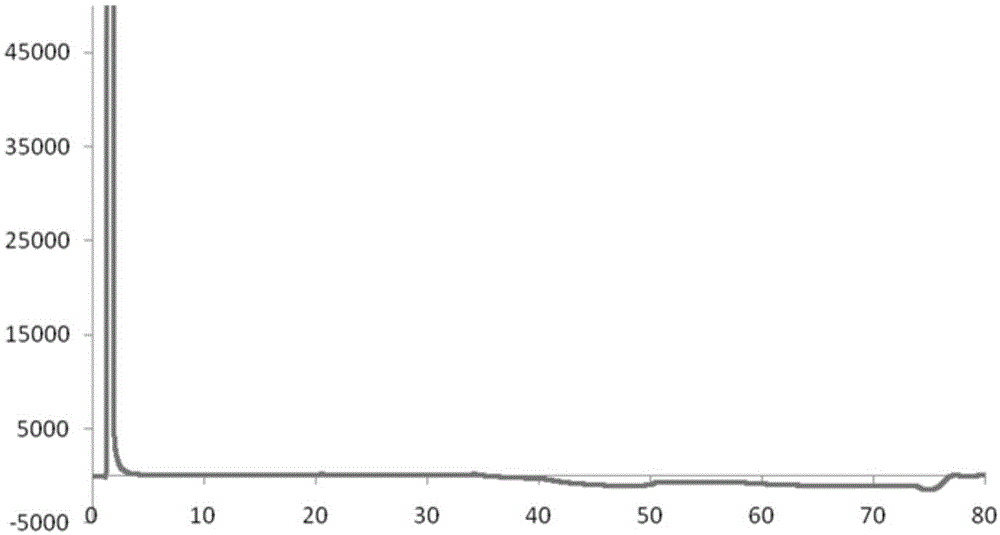
:阿托伐他汀钙是第三代他汀类调血脂药,是hmg-coa还原酶的选择性、竞争性抑制剂,通过抑制肝脏内hmg-coa还原酶(3-羟基-3-甲基戊二酸单酰辅酶a还原酶)和胆固醇的合成,从而降低血浆中胆固醇和脂蛋白水平,并通过增加细胞表面的肝脏ldl受体,以增强ldl的摄取和代谢。阿托伐他汀钙的有关物质能引起肌痛等不良反应,该分析方法提高了对杂质的检出和识别能力,提高了质量控制水平,从而更有效的保证产品的安全性。现有技术中已经报道了几种阿托伐他汀钙有关物质的测定方法,如专利201110197172.9阿托伐他汀钙胶囊有关物质的检测方法,专利201310239929.5阿托伐他汀钙制剂溶出度的测定方法,专利200910087797.2一种用高效液相色谱法测定阿托伐他汀钙有关物质的方法,专利201510178001.x公开了一种如何测定阿托伐他汀钙中杂质e的方法,药物分析杂质chinjpharmanal2014,34(8)公开了以乙腈-四氢呋喃-醋酸铵缓冲溶液,采用hplc法,检测阿托伐他汀钙中有关物质的方法。在参考质量标准:usp41质量标准中,采用高效液相色谱进行分离,流动相采用单一的流动相体系,即乙腈,不含稳定剂的四氢呋喃和缓冲液,其中缓冲液为磷酸二氢铵缓冲液,采用该流动相体系可以将阿托伐他汀钙和杂质h等物质实现分离和检测,但是对于杂质i(阿托伐他汀钙安奈德叔丁酯),该体系并不能实现有效分离,检测结果的准确性不能得到保证。技术实现要素:发明要解决的问题为了解决现有技术中对于杂质i(阿托伐他汀钙安奈德叔丁酯)不能有效分离和检测的问题,本发明的目的是提供一种阿托伐他汀钙中的阿托伐他汀钙安奈德叔丁酯的分离和检测方法。用于解决问题的方案本发明提供的技术方案是:一种阿托伐他汀钙中有关物质的检测方法,包括采用高效液相色谱进行检测的步骤,所述液相色谱采用的色谱柱为反向色谱柱,以流动相a和流动相b进行梯度洗脱,所述的流动相a为体积比为35~45:55~65的溶液a和缓冲溶液的混合溶液,所述溶液a是体积比为800~950:50~200的乙腈-四氢呋喃溶液,所述流动相b是体积比为40~80:10~30:10~50的溶液a-缓冲溶液-甲醇的混合溶液。进一步的,所述有关物质包括阿托伐他汀钙安奈德叔丁酯,所述的反向色谱柱为c18色谱柱,c8色谱柱,苯基色谱柱或氨基色谱柱。进一步的,所述的缓冲溶液为醋酸盐溶液或磷酸盐溶液。进一步的,缓冲溶液为10-100mmol/l醋酸盐溶液,ph值为3.0~4.0。进一步的,所述的溶液a为体积比为900:100的乙腈-四氢呋喃溶液,流动相a为体积比为41:59的溶液a和缓冲溶液的混合溶液,流动相b是体积比为60:15:25的溶液a-缓冲溶液-甲醇的混合溶液。进一步的,色谱条件为检测波长为240-250nm,优选为244nm;柱温为25-40℃,优选为柱温为30℃,流动相的流速为1-2ml/min,优选为1.4-1.8ml/min。进一步的,所述阿托伐他汀钙以原料药、固体制剂、半固体制剂或液体制剂形式存在。进一步的,所述流动相a和流动相b进行梯度洗脱采用下表洗脱程序进行洗脱:时间(min)流动相a(%)流动相b(%)流速(ml/min)0100~900~101.830100~900~101.84520~3080~701.4~1.75020~3080~701.4~1.75515~2585~751.4~1.77015~2585~751.4~1.773100~900~101.880100~900~101.8其中流动相a和b的百分比为体积百分比。进一步的,洗脱程序中时间为45~55min时的流速为1.5~1.7ml/min。进一步的,在采用高效液相色谱进行检测的步骤之前,将所述阿托伐他汀钙加入溶剂中配制成待处理溶液。发明的效果本发明所涉及的检测方法,可将阿托伐他汀钙有关物质各组分实现充分的分离,同时在参考方法中不能检测的杂质i也能准确有效的检测,能够有效提高阿托伐他汀钙的药品质量和安全性。附图说明图1空白辅料溶液的色谱图;图2空白溶剂的色谱图;图3供试品溶剂的色谱图;图4-10不同色谱条件下混合溶液分离的色谱图;图11参考方法混合溶液的色谱图。具体实施方式首先,本发明提供了一种阿托伐他汀钙中有关物质的检测方法,所述有关物质为阿托伐他汀钙安奈德叔丁酯,该方法包括采用高效液相色谱进行检测的步骤,所述液相色谱采用的色谱柱为反向色谱柱,以流动相a和流动相b进行梯度洗脱,所述的流动相a为体积比为35~45:55~65的溶液a和缓冲溶液的混合溶液,所述溶液a是体积比为800~950:200~50的乙腈-四氢呋喃溶液,所述流动相b是体积比为40~80:10~30:10~50的溶液a-缓冲溶液-甲醇的混合溶液。在本发明的上下文中,术语“阿托伐他汀钙”的分子式为c66h68caf2n4o10,英文名为atorvastatincalcium,cas号为134523-03-8,在本发明的具体方案中,所述阿托伐他汀钙以原料药、固体制剂、半固体制剂或液体制剂形式存在。优选所述固体制剂包括片剂、胶囊剂、栓剂、颗粒剂、膜剂、糊剂或丸剂,所述半固体制剂包括凝胶剂和软膏剂,所述液体制剂包括注射剂、合剂和溶液剂。在本发明的上下文中,术语“阿托伐他汀钙安奈德叔丁酯”,为阿托伐他汀钙中的杂质i,是阿托伐他汀钙的杂质。在本发明的上下文中,术语“流动相”,是指色谱过程中携带待测组分向前移动的物质。在本发明的上下文中,术语“反向色谱柱”,是指流动相极性大于固定相极性的色谱柱。本发明可使用本领域常规的反相色谱柱。例如在具体方案中使用包括c18色谱柱,c8色谱柱,苯基色谱柱或氨基色谱柱等。c18色谱柱是指十八烷基硅烷键合硅胶为填充剂的色谱柱。在一项优选的实施方案中,所述的缓冲溶液为10-100mmol/l醋酸盐溶液,ph值为3.0~4.0,调节缓冲溶液ph值的酸为磷酸、冰醋酸或酸水混合物。在一项更优选的实施方案中,缓冲溶液为醋酸铵溶液,ph值为3.5。在一项优选的实施方案中,所述的溶液a为体积比为900:100的乙腈-四氢呋喃溶液,流动相a为体积比为41:59的溶液a和缓冲溶液的混合溶液。在一项优选的实施方案中,所述流动相b是体积比为60:15:25的溶液a-缓冲溶液-甲醇的混合溶液。在一项优选的实施方案中,色谱条件为检测波长为240-250nm,优选为244nm,柱温为25-40℃,优选为30℃,流动相的流速为1-2ml/min,优选1.4-1.8ml/min。在一项优选的实施方案中,所述流动相a和流动相b进行梯度洗脱采用采用下表洗脱程序进行洗脱:时间(min)流动相a(%)流动相b(%)流速(ml/min)0100~900~101.830100~900~101.84520~3080~701.4~1.75020~3080~701.4~1.75515~2585~751.4~1.77015~2585~751.4~1.773100~900~101.880100~900~101.8其中流动相a和b的百分比为体积百分比。在一项优选的实施方案中,洗脱程序中时间为45~55min时的流速为1.5-1.7ml/min。在一项优选的实施方案中,在采用高效液相色谱进行检测的步骤之前,将所述阿托伐他汀钙配制成待处理溶液。在一项优选的实施方案中,还包括供试样品溶液配制的过程。溶剂:dmf空白辅料溶液的配制:取空白辅料适量(按处方比例约相当于阿托伐他汀钙10mg),精密称定,置20ml量瓶中,加入约80%溶剂,振摇10min,加溶剂稀释至刻度,摇匀,滤过,取续滤液作为空白辅料溶液。各杂质对照品贮备液①的配制:分别精密称取杂质a、pd140728、杂质b、杂质c、pd130694、pd148996、pd153824、阿托伐他汀钙甲酯、阿托伐他汀钙环氧四氢呋喃、pd139884、阿托伐他汀钙叔丁酯、杂质i对照品各适量,加溶剂溶解并稀释制成每1ml中含相应杂质约为0.1mg的溶液。混合溶液的配制:取阿托伐他汀钙对照品约10mg,精密称定,置20ml量瓶中,加溶剂适量使溶解,加入上述杂质a、b、c、阿托伐他汀钙甲酯、阿托伐他汀钙叔丁酯、杂质i对照品贮备液①各0.2ml,pd140728、pd148996、pd153824对照品贮备液①各0.5ml,pd130694对照品贮备液①1.0ml、阿托伐他汀钙环氧四氢呋喃对照品贮备液①0.25ml、d139884对照品贮备液①0.35ml,用溶剂稀释至刻度,摇匀。下表是上述杂质的缩写与全称的对照表:供试品溶液的配制:取本品细粉适量(约相当于阿托伐他汀钙10mg),精密称定,置20ml量瓶中,加约80%溶剂振摇10min,用溶剂稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。对照溶液的配制:精密量取供试品溶液1ml置50ml量瓶中,用溶剂稀释至刻度,摇匀,精密量取1ml置10ml量瓶中,用溶剂稀释至刻度,摇匀。下面通过具体实施例对本发明的
发明内容做进一步的详细说明,但并不因此限定本发明的内容。实施例1供试样品溶液配制空白辅料溶液的配制:取空白辅料适量(按处方比例约相当于阿托伐他汀钙10mg),精密称定,置20ml量瓶中,加入约80%dmf,振摇10min,加溶剂稀释至刻度,摇匀,滤过,取续滤液作为空白辅料溶液。各杂质对照品贮备液①的配制:分别精密称取杂质a、pd140728、杂质b、杂质c、pd130694、pd148996、pd153824、阿托伐他汀钙甲酯、阿托伐他汀钙环氧四氢呋喃、pd139884、阿托伐他汀钙叔丁酯、杂质i对照品各适量,加dmf溶剂溶解并稀释制成每1ml中含相应杂质约为0.1mg的溶液。混合溶液的配制:取阿托伐他汀钙对照品约10mg,精密称定,置20ml量瓶中,加dmf溶剂适量使溶解,加入上述杂质a、b、c、阿托伐他汀钙甲酯、阿托伐他汀钙叔丁酯、杂质i对照品贮备液①各0.2ml,pd140728、pd148996、pd153824对照品贮备液①各0.5ml,pd130694对照品贮备液①1.0ml、阿托伐他汀钙环氧四氢呋喃对照品贮备液①0.25ml、d139884对照品贮备液①0.35ml,用dmf稀释至刻度,摇匀。供试品溶液的配制:取本品细粉适量(约相当于阿托伐他汀钙10mg),精密称定,置20ml量瓶中,加约80%dmf溶液振摇10min,用dmf溶液稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。对照溶液的配制:精密量取供试品溶液1ml置50ml量瓶中,用dmf溶液稀释至刻度,摇匀,精密量取1ml置10ml量瓶中,用dmf溶液稀释至刻度,摇匀。检测仪器与色谱条件检测仪器:高效液相色谱仪(hplc)色谱条件:选择十八烷基硅烷键合硅胶为填充剂的色谱柱(c18色谱柱)。以乙腈-四氢呋喃(90∶10,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶15∶25,v/v)作为流动相b,梯度洗脱程序见下表1,检测波长为244nm,柱温为30℃。表1时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84522781.65022781.65518821.67018821.6739821.8809821.81、干扰试验取空白溶剂、空白辅料溶液和供试品溶液各20微升分别进样分析,见附图1~附图3。结果表明,空白溶剂和空白辅料均不干扰阿托伐他汀钙片有关物质的检测,从附图3的供试品色谱图中可以明确的检测出供试品中含有杂质i。2、杂质混合分离实验取混合溶液20微升,进样考察各组分理论板数、分离度、拖尾因子(见附图4)。实验结果见表2。表2组分保留时间(min)分离度理论塔板数拖尾因子杂质a17.38--134000.95pd14072818.291.3288000.98杂质b19.461.59149000.93阿托伐他汀钙20.651.73128001.00杂质c22.552.60132001.00pd13069440.5122.41393000.97pd14899643.804.33616001.03甲酯45.122.081049000.96pd15382446.362.231123000.98环氧四氢呋喃47.973.522792000.96pd13988450.567.373582000.98叔丁酯58.9819.832126001.00杂质i71.6023.591989000.983、仪器精密度供试品溶液的配制:取本品细粉适量(约相当于阿托伐他汀钙10mg),精密称定,置20ml量瓶中,加约80%溶剂振摇10min,用溶剂稀释至刻度,摇匀,滤过,取续滤液作为供试品溶液。精密量取供试品溶液1ml置50ml量瓶中,用溶剂稀释至刻度,摇匀,精密量取1ml置10ml量瓶中,用溶剂稀释至刻度,摇匀,即得对照溶液。精密量取对照溶液20μl,注入液相色谱仪,连续进样6次考察仪器精密度结果见表3表3进针序号自身对照峰面积128186228035328401428165528433628248平均值28245rsd(%)0.5结论:各对照品色谱峰的相对标准偏差(rsd)均小于2%,重复性符合要求。4、破坏试验制备阿托伐他汀钙的酸破坏溶液,碱破坏溶液,氧化破坏溶液,高温破坏溶液和光照破坏溶液。精密吸取酸破坏溶液,碱破坏溶液,氧化破坏溶液,高温破坏溶液和光照破坏溶液各20微升,分别进样考察各有关物质峰的个数及含量,并检测峰纯度。阿托伐他汀钙峰与有关物质峰能得到很好的分离,阿托伐他汀钙片各破坏样品破坏前后物料基本平衡;采用二极管阵列检测器,对阿托伐他汀钙片的酸、碱、氧化、高温、光照破坏试验的主峰阿托伐他汀钙色谱峰进行峰纯度分析,所有峰均为单一色谱峰,峰纯度>99%,结果见表4。说明本检测方法可用于阿托伐他汀钙胶囊有关物质的检查。表4结论:①阿托伐他汀钙在氧化、碱强降解条件下,无明显降解。在光照条件下,阿托伐他汀钙的已知降解产物为pd148996;在高温条件下,阿托伐他汀钙的已知主降解产物均为pd130694;在酸条件下原料药与阿托伐他汀钙的已知主降解产物均为pd130694。各降解产物均可与主峰完全分离。②经峰纯度考察,各条件下均未检测到不纯物,峰纯度合格,验证色谱条件专属性好。③以未破坏含量为100%,按外标法计算上述各破坏条件下的主成分物料平衡情况,物料均守恒,进一步验证了该色谱条件专属性好。5、最低检测限取各杂质对照品适量,精密称定,加溶剂逐级稀释至适宜浓度,在上述色谱条件下,以信噪比为3:1时注入仪器的量作为检测限。结果见下表5:表5结论:拟定阿托伐他汀钙检查浓度为0.5mg/ml,检测限为0.2ng,杂质在0.002%以上可检测,表明本品色谱条件灵敏度高,适合进行杂质控制。实施例2混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(90∶10,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶15∶25,v/v)作为流动相b,梯度洗脱程序见下表6,检测波长为244nm,柱温为30℃。表6时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84525751.65025751.65520801.67020801.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图5所示。结果显示:阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。实施例3混合溶液配制方法与实施例1相同。检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(90∶10,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶15∶25,v/v)作为流动相b,梯度洗脱程序见下表7,检测波长为244nm,柱温为30℃。表7时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84521791.65021791.65516841.67016841.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图6所示。结果显示:实施例2和3结果汇总见表8,阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。表8结果显示:上述两个实施例条件下,阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出。实施例4混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(90∶10,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶20∶20,v/v)作为流动相b,梯度洗脱程序见下表9,检测波长为244nm,柱温为30℃。表9时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84522781.65022781.65518821.67018821.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图7所示。结果显示:阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。实施例5混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(90∶10,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶10∶30,v/v)作为流动相b,梯度洗脱程序见下表10,检测波长为244nm,柱温为30℃。表10时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84522781.65022781.65518821.67018821.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图8所示。结果显示:实施例4、5结果汇总见表11,阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。表11结果显示:上述两个实施例条件下,阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出。实施例6混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(88∶12,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶15∶25,v/v)作为流动相b,梯度洗脱程序见下表12,检测波长为244nm,柱温为30℃。表12时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84522781.65022781.65518821.67018821.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图9所示。结果显示:阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。实施例7混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(92∶8,v/v)作为溶液a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a(59:41,v/v)作为流动相a,50mmol/l醋酸铵(用冰醋酸调节ph至3.5±0.1)-溶液a-甲醇(60∶15∶25,v/v)作为流动相b,梯度洗脱程序见下表13,检测波长为244nm,柱温为30℃。表13时间(min)流动相a(%)流动相b(%)流速(ml/min)09821.8309821.84522781.65022781.65518821.67018821.6739821.8809821.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图10所示。结果显示:实施例6、7结果汇总见表14阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出,该方法适用阿托伐他汀钙有关物质检测。表14结果显示:上述两个实施例条件下,阿托伐他汀钙有关物质各组分能够很好的分离,杂质i能够有效检测出。实施例8(完全参照usp41方法)混合溶液配制方法与实施例1相同。检测仪器与色谱条件检测仪器:高效液相色谱仪色谱条件:十八烷基硅烷键合硅胶为填充剂的色谱柱。以乙腈-四氢呋喃(925∶75,v/v)作为溶液a,5.75g/l的磷酸二氢铵水溶液(用稀10%乙酸或10%的氨水调节至ph4.3±0.05)-溶液a(58:42,v/v)作为流动相a,5.75g/l的磷酸二氢铵水溶液(用稀10%乙酸或10%的氨水调节至ph4.3±0.05)-溶液a-甲醇(60∶20∶20,v/v)作为流动相b,梯度洗脱程序见下表15,检测波长为244nm,柱温为30℃。表15时间(min)流动相a(%)流动相b(%)流速(ml/min)010001.83010001.84525751.55025751.55520801.55810001.86510001.8测定方法:量取混合溶液20μl,注入液相色谱仪,记录色谱图,完成测定;所得色谱图如图11所示。结果显示:实施例8结果汇总见表16阿托伐他汀钙有关物质各组分能够很好的分离,杂质i未能检测出,该方法不适用阿托伐他汀钙有关物质检测。表16从上述实施结果可看出,在本发明的条件下,阿托伐他汀钙有关物质各组分能够很好的分离,参考方法中不能检测的杂质i,发明方法也能准确有效的检测。所以本发明用于阿托伐他汀钙有关物质的检测是一行之有效的方法。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1