一种醒脑静注射液血液中冰片与麝香酮含量测定方法与流程
本发明涉及药物有效成分的检测方法,具体涉及将醒脑静注射液注入体内后检测血液中冰片与麝香酮含量的方法。
背景技术:
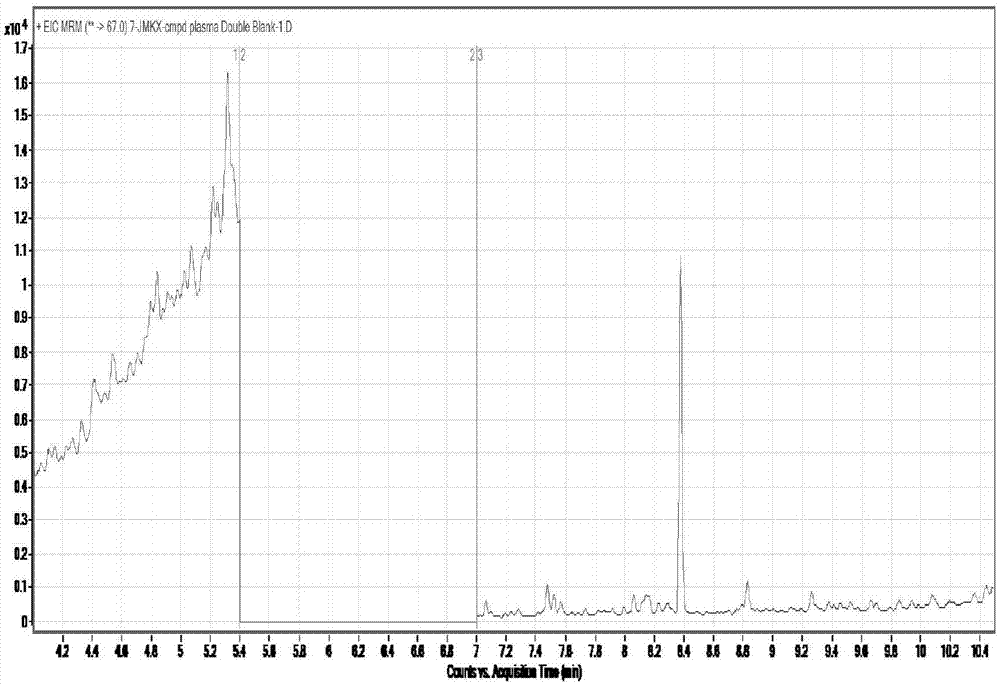
醒脑静注射液是由麝香、冰片、郁金和栀子经水蒸气蒸馏提取精制而成的复方中药注射液,始创于上世纪70年代,组方由中医名方安宫牛黄丸化裁而得,具有清热解毒,凉血活血,开窍醒脑功效。为阐明醒脑静作用机制并找到控制质量的关键指标,制定更科学更合理的质量内控标准,生产更加优质而有竞争力的醒脑静注射剂,需开展物质基础的研究工作,从而为大幅度拓展国内市场并力争推向国际奠定坚实的基础,已有的醒脑静注射液质量控制的文献报道,全部是以麝香酮和冰片为质控指标,检测方法主要为气相色谱法(gc)和气质联用法(gc-ms),目前未有血液中麝香酮和冰片的测定方法,缺乏有效成分在血液中的检测手段,为了确定有效成分在血液中的变化情况,需要开发一种准确可靠的检测技术,为阐明醒脑静注射液的药效物质基础提供科学依据。技术实现要素:本发明的目的在于提供一种醒脑静注射液血液中冰片与麝香酮含量测定方法。本发明通过对醒脑静注射液血液中冰片与麝香酮含量研究,提供了醒脑静注射液血液中冰片与麝香酮含量测定方法,弥补了现有体内醒脑静注射液药效活性物质研究的不足的缺点,使醒脑静注射液后期物质基础研究手段更为完善,也更为科学。一种醒脑静注射液在血液中的冰片与麝香酮含量测定方法,采用气质联用色谱法,所述方法,步骤如下1)供试品溶液的制备:将醒脑静注射液静脉注射进入体内,在给药10min-60min采集血液样品,分离血浆2)将分离的血浆注入气质联用色谱仪,得到色谱图,根据色谱图,用标准曲线法计算血浆中冰片与麝香酮的含量。其中所述气质联用色谱仪采用以下色谱条件:气质联用色谱仪色谱系统条件:气相色谱:安捷伦7890a,色谱柱:岛津rtx-wax,30m,0.25id,0.25um(rt-12423),程序升温条件:初始温度150℃,15℃/min升温至250℃,维持5min。进样口温度:250℃,载气:高纯氦气,流速:2ml/min,压力:19.4psi,自动进样器:安捷伦7693。自动进样器温度:室温,保留时间:待测物内标冰片=~5.3分钟萘=~5.6分钟麝香酮=~9.2分钟运行时间:12.83min进样量:1μl质谱仪:7000qqq-ms离子化模式:电子电离极性:正离子监测模式:mrm离子源温度:230℃碰撞气:高纯氮气emv:2386或2441离子对和参数:其中,所述标准曲线,以冰片和麝香酮作为检测目标,配制成已知的不同浓度的样品溶液,按照上述气质联用色谱仪色谱系统条件进行检测,得到色谱图,根据色谱图峰面积得到不同含量的冰片和麝香酮的标准曲线。其中根据需要,还要用到内标溶液,本发明用到的内标溶液是萘的溶液。其中,优选的,冰片,麝香酮以及内标的峰面积和/或峰高由qqqquantitativeanalysis软件获得,并用标准样品建立标准曲线。其中,优选的,利用qqqquantitativeanalysis软件对待测物/内标的峰面积比与待测物的浓度进行线性回归得到标准曲线,得到色谱图后,进行数据处理,方法如下:待测样品浓度由qqqquantitativeanalysis软件经线性方程式来确定。其他实验数据的统计分析利用microsoftexcel软件计算本发明进一步包括供试液的制备,制备方法如下:动物或人静脉给药醒脑静注射液,剂量为5ml/kg,在给药后10min-60min时采集血液样品,采集量为5.0ml,转移至装有200μl400u的肝素钠的离心管,混匀,将全血分到1.5毫升离心管,在4℃、转速10000g条件下,离心10分钟得到含药的血浆样本。本发明还包括空白液的制备,制备方法如下:采集空白血液样品,采集量为5.0ml,转移至装有200μl400u的肝素钠的离心管,混匀,将全血分到1.5毫升离心管,在4℃、转速10000g条件下,离心10分钟得到空白的血浆样本。本发明进一步包括制备标准曲线用的标准溶液的制备,制备方法如下:将冰片和麝香酮溶于无水乙醇,配制成5mg/ml的冰片和麝香酮的混合储备溶液。一份冰片和麝香酮储备液用无水乙醇进一步用稀释液稀释成1000,2,500,5,000,10,000,25,000,100,000,200,000和400,000ng/ml的标曲工作溶液。另一份冰片和麝香酮储备液用无水乙醇进一步用稀释液稀释成1,000,3,000,20,000和320,000ng/ml的定量下限、低、中、高浓度的质控样品工作溶液。本发明进一步包括制备标准曲线用的内标溶液的制备,制备方法如下:萘用无水乙醇制成10mg/ml的内标储备液,然后继续用乙酸乙酯稀释成600ng/ml的内标溶液。储备液检查时,将萘储备液用乙酸乙酯稀释成600ng/ml进行系统适应性检查。本发明的检测方法是经过筛选获得的,筛选过程如下:1.提取溶剂考察分别采用不同溶剂进行液液萃取考察,分别考察正己烷、乙酸乙酯提取效果成分正己烷乙酸乙酯麝香酮1536816527冰片3602636800通过考察乙酸乙酯萃取含量较好,提取溶剂使用可使用乙酸乙酯。2.供试品稳定性短期稳定性:冰片和麝香酮在sd大鼠血浆中的短期稳定性样品将至少冷冻24小时以上再进行测定。稳定性血浆样品将在室温下解冻,并在室温下保存至少4小时才可进行样品制备和分析。冻融循环稳定性:冰片和麝香酮在sd大鼠脑匀浆或血浆中冻/融的稳定性测试应有三个冻/融循环确定,每个低,高浓度样品应储存在-75±15oc。所有的样品将冷冻储存至少24小时,不借助任何条件在室温下融化进行处理,再次冷冻至少12小时,进入下一循环。长期稳定性:冰片和麝香酮在sd大鼠血浆中的长期稳定性,通过测定储存在-75±15oc至少3天以上的低、高浓度样品来评价。结果:每个浓度水平的平均浓度的准确度在理论浓度的85%-115%区间,变异系数不超过15%。附图说明:附图1冰片和麝香酮在血浆中的双空白样品图谱附图2冰片和麝香酮在血浆中的样品图谱具体实施方式通过以下具体实施例对本发明做进一步的说明,但不作为限制。实施例1:本发明提供提供一种醒脑静注射液血液中冰片与麝香酮含量测定方法,其特征在于,步骤如下:(1)供试品溶液的制备:a)大鼠经尾静脉缓慢注射给药,单次给药,动物给药醒脑静注射液,剂量为5ml/kg,b)分别在给药10min、20min、60min从sd大鼠采集血液样品,每只大鼠大约采集5.0ml全血,转移至装有200μl400u的肝素钠的离心管,颠倒数次以充分混匀,使用前放置在湿冰或5±3℃条件下,每个时间点雌雄动物各一只。c)取血后60分钟以内,将全血等分到1.5毫升离心管,在4℃、转速10000g条件下,离心10分钟以获取血浆,分离的血浆样本分别分成3等份,保存在-80±5℃冰箱直至取出分析。d)按照步骤a)到c)获取大鼠空白血浆:肝素钠抗凝(每毫升血液肝素用量为(15±2.5)u),冷冻保存在-80±5℃的冰箱内。2)储备液和工作液的配制:a)将冰片和麝香酮溶于无水乙醇,配制成5mg/ml的冰片和麝香酮的混合储备溶液。一份冰片和麝香酮储备液用无水乙醇进一步用稀释液稀释成1000,2,500,5,000,10,000,25,000,100,000,200,000和400,000ng/ml的标曲工作溶液。另一份冰片和麝香酮储备液用无水乙醇进一步用稀释液稀释成1,000,3,000,20,000和320,000ng/ml的定量下限、低、中、高浓度的质控样品工作溶液。b)萘用无水乙醇制成10mg/ml的内标储备液,然后继续用乙酸乙酯稀释成600ng/ml的内标溶液。储备液检查时,将萘储备液用乙酸乙酯稀释成600ng/ml进行系统适应性检查。3)标曲和质控样品配制标准样品和质控血浆样品时,向495μl空白鼠血浆中分别加入每个浓度的5μl的工作溶液。定量下限样品(lloq)和乙酸乙酯(含内标萘)用于系统适应性检查。4)样品处理步骤a)双空白样品、零样品、标曲样品和质控样品:向已加有5μl工作溶液和495μl空白鼠血浆或的离心管中加入500μl含内标的乙酸乙酯,充分涡旋,放入-20±5℃冰箱过夜萃取,室温融化,充分涡旋,在4℃,20000g离心条件下离心20分钟,取大约250μl上清过滤膜,转入带玻璃衬管的进样小瓶,用gc-ms/ms分析。双空白样品以不含内标的乙酸乙酯代替,其他步骤不变。b)待测样品:取495μl待测血浆样品至1.5毫升离心管,加入5μl无水乙醇,随后加入500μl含内标的乙酸乙酯,其他步骤与标曲样品一致。个别超限样品,用空白血浆稀释10倍后,再按上述步骤处理。5)液相色谱系统条件:气相色谱:安捷伦7890a色谱柱:岛津rtx‐wax,30m,0.25id,0.25um(rt‐12423)程序升温条件:初始温度150℃,15℃/min升温至250℃,维持5min。进样口温度:250℃载气:高纯氦气流速:2ml/min压力:19.4psi自动进样器:安捷伦7693自动进样器温度:室温保留时间:待测物内标冰片=~5.3分钟萘=~5.6分钟麝香酮=~9.2分钟运行时间:12.83min进样量:1μl质谱仪:7000qqq‐ms离子化模式:电子电离极性:正离子监测模式:mrm离子源温度:230℃碰撞气:高纯氮气emv:2386或2441离子对和参数:6)数据处理:冰片,麝香酮以及内标的峰面积和/或峰高由qqqquantitativeanalysis软件获得,并用标准样品建立标准曲线。利用qqqquantitativeanalysis软件对待测物/内标的峰面积比与待测物的浓度进行线性回归得到标准曲线,质量控制样品,待测样品浓度由qqqquantitativeanalysis软件经线性方程式来确定。其他实验数据的统计分析利用microsoftexcel软件计算。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1