一种橘红珠药材质量检测方法与流程
本发明属于中药质量检测领域,特别是涉及橘红珠药材质量检测方法。
背景技术:
橘红珠为芸香科植物化州柚(citrusgrandis‘tomentosa’)的未成熟幼小果实,又称橘珠、橘胎、橘红胎。化州柚生长于广东化州及其周边地域,始种于梁朝,至今已有约一千五百年的栽培历史。化州柚是柚而不是橘,其幼果之所以称为“橘红珠”,是借助了宋、明以来橘红的声誉。相关的文字记载,始见于1675年(康熙14年)《广东通志》,在高州府药之属类别下有如下描述:“粤中虽称沃壤,然风土浅薄赋质柔脆,人物同之,至于灵奇珍异,物亦独擅其美者,若…化州之橘红,增城之荔枝,琼南之香犀、象贝”。《广东省化州志》(1827年)卷十一引《橘红辨》:“化州所产橘红,医家以之利气化痰,功峻于他药。(果实)有红白瓤两种,明明柚也,无毫发异,而混呼之曰橘,且饰其色曰红。夫果有利于用,即存其名以著其实可也。奚必橘之贵而柚之贱哉。或曰柚诚柚也,何以他产不利于用,予曰此正所谓道地也。”清光绪十五年(1890年)《广东省高州府志》记载:“若夫化州之橘非橘也,柚也,天下之人皆橘之,吾亦不得不橘之。”
化州柚早期作为药用时,其炮制方法也效仿橘红“去白取皮”,使用外果皮入药,即化橘红药材。而由于化州柚皮厚肉酸,不中食,在实际使用中,逐渐演变为使用未成熟幼果入药。化州柚幼果中大部分都是中果皮,其中柚皮苷、野漆树苷等药理活性成分含量很高,将其除去无疑是一种浪费,且耗费人力物力,不利于资源的合理利用。橘红珠最早收载于《广西中药志》(1963年)第二辑,用于“止渴,助消化,除胸中气滞。治食积,症瘕”;后亦收载于《中药大辞典》、《中华本草》。经过近50年的市场流通,橘红珠临床疗效确证,目前已成为化州柚的主流加工规格。
橘红珠用药广泛,尤其是在两广地区;但是现行版国家药典及地方标准均尚未收载该品种。缺乏统一的质量标准,造成流通及使用中的混乱。
技术实现要素:
本发明公开了橘红珠中药药材的质量检测方法,包括外观性状鉴别、显微鉴别、薄层鉴别、水分测定、总灰分测定、特征图谱鉴别和含量测定方法。为建立统一的、可行的橘红珠药材质量标准提供可操作性手段。
本发明所述的橘红珠外观性状鉴别方法包括如下步骤:
鉴别方法:检视供试品的外观性状,并拍照记录;使用游标卡尺测量果实横向直径与纵向直径,以其平均值作为果实直径;
供试品外观应呈近球形、半球形或圆柱形,表面墨绿色或灰绿色,密布茸毛,有皱纹及小油室,先端有花柱脱落的痕迹,基部有呈圆形果柄的疤痕;质坚硬,不易切开,断面平整,黄白色或淡红棕色,有脉络纹。外缘有一列不整齐的下凹的油室。气芳香,味苦、微辛。
选定果实直径作为外观性状指标,可将橘红珠药材分为一等、二等、三等、四等4个等级,一等:果实直径不超过4cm;二等:果实直径不超过5cm;三等、四等:果实直径不超过6cm。
本发明所述的橘红珠显微鉴别包括如下步骤:
供试品制备:供试品粉碎,过二号筛,混合均匀。取适量于载玻片上,滴数滴水合氯醛溶液将粉末浸润后,酒精灯加热,再滴加适量稀甘油溶液,充分混合,盖上盖玻片;
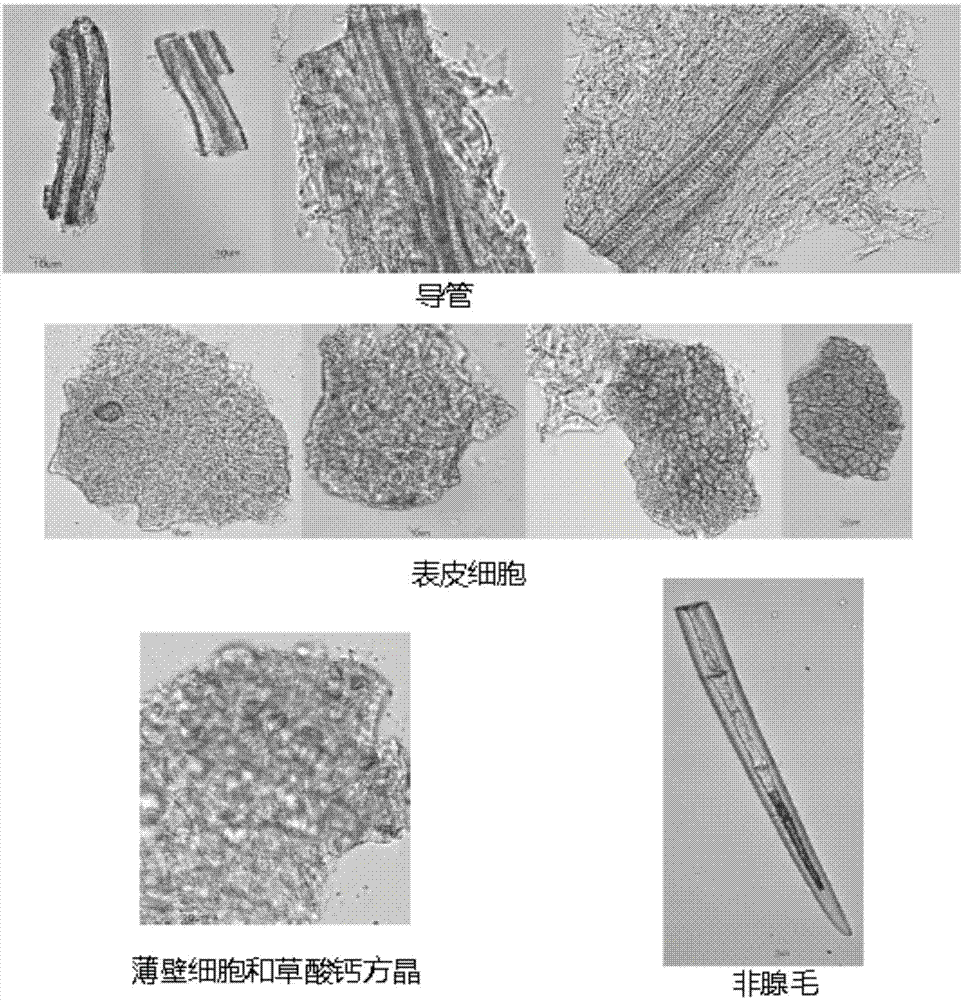
鉴别方法:将制好的玻片置于显微镜下观察,供试品粉末黄棕色至棕褐色。中果皮薄壁细胞形状不规则,壁不均匀增厚,有的作连珠状或在角隅处特厚。果皮表皮细胞表面观多角形、类方形或长方形,垂周壁增厚,气孔类圆形,直径18~31μm,副卫细胞5~7个,侧面观外被角质层,靠外方的径向壁增厚。可见碎断的非腺毛,碎断细胞多至十数个,最宽处直径约33μm,具壁疣或外壁光滑、内壁粗糙,胞腔内含淡黄色或棕色颗粒状物。草酸钙方晶成片或成行存在于中果皮薄壁细胞中,呈多面形、菱形、棱柱形、长方形或形状不规则,直径1~32μm,长5~40μm。导管为螺纹导管和网纹导管。偶见石细胞及纤维。
本发明所述的橘红珠薄层鉴别方法包括如下步骤:
供试品溶液的制备:取供试品粉末0.5g,加甲醇5ml,超声处理15分钟,离心,取上清液作为供试品溶液;
对照品溶液的制备:取柚皮苷对照品,加甲醇制成每1ml含1mg的溶液,作为对照品溶液;
展开剂:乙酸乙酯∶丙酮∶冰乙酸∶水=8∶4∶0.3∶1;
鉴别方法:吸取供试品溶液和对照品溶液各2μl,分别点于同一高效硅胶g薄层板上,展开,取出,晾干,喷5%三氯化铝乙醇溶液,在105℃加热1分钟,置波长365nm紫外光灯下检视;供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点。
本发明所述的橘红珠水分测定方法包括如下步骤:
供试品制备:供试品粉碎,过二号筛,取2~5g,平铺于干燥至恒重的扁形称量瓶中;
测定方法:精密称定装有供试品的称量瓶,开启瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,放冷30分钟,精密称定,再在上述温度干燥1小时,放冷,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量小于12.0%。
本发明所述的橘红珠总灰分测定方法包括如下步骤:
供试品制备:供试品粉碎,过二号筛,混合均匀后,取2~3g,置炽灼至恒重的坩埚中,称定重量(准确至0.01g),缓缓炽热,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化并至恒重;
测定方法:根据残渣重量,计算供试品中总灰分的含量小于4.5%。
本发明所述的橘红珠特征图谱方法包括如下步骤:
供试品溶液的制备:取供试品粉末,过二号筛约0.5g,精密称定,置具塞锥形瓶中,精密加甲醇10ml,称定重量,超声处理,30分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液;
参照物溶液的制备:取柚皮苷对照品适量,精密称定,加甲醇制成每1ml含柚皮苷500μg的溶液,作为参照物溶液。
色谱条件:以十八烷基硅烷键合硅胶为填充剂,以甲醇为流动相a,以2%醋酸溶液为流动相b,梯度洗脱程序为:0~25分钟,30%流动相a,70%流动相b;25~75分钟,30%→45%流动相a,70%→55%流动相b;75~110分钟,45%→100%流动相a,55%→0%流动相b;110~120分钟,100%流动相a,0%流动相b;流速为每分钟1ml,检测波长为320nm;
测定方法:分别精密吸取参照物溶液和供试品溶液各5μl,注入液相色谱仪,记录120分钟的色谱图;供试品特征图谱中应呈现4个特征峰,其中特征峰1应与相应的参照物峰保留时间相同;与柚皮苷参照物峰相应的峰为s峰,计算特征峰2~4的相对保留时间,特征峰2、3的相对保留时间应在规定值的±5%之内,特征峰4的相对保留时间应在规定值的±6%之内,规定值为:1.49(峰2)、1.74(峰3)、3.19(峰4)。
本发明所述的橘红珠含量测定方法包括如下步骤:
供试品溶液的制备:取供试品粉末,过二号筛,取约50mg,精密称定,置10ml容量瓶中,精密加入甲醇5ml,超声处理30分钟(150w,40khz),放冷,加50%甲醇至刻度,摇匀,滤过,取续滤液,作为供试品溶液;
对照品溶液的制备:取柚皮苷、野漆树苷对照品适量,精密称定,加甲醇制成每1ml分别含柚皮苷400μg、野漆树苷10μg的溶液,作为对照品溶液;
色谱条件:以十八烷基硅烷键合硅胶为填充剂;以甲醇-0.3%醋酸溶液(体积比为35∶65)为流动相;检测波长为283nm、338nm;
测定方法:分别精密吸取对照品溶液与供试品溶液各5μl,注入液相色谱仪,测定,按外标法以峰面积计算含量;选定柚皮苷和野漆树苷含量作为内在指标,将橘红珠药材分为一等、二等、三等、四等4个等级,一等:含柚皮苷不少于11.8%,野漆树苷不少于0.93%;二等:含柚皮苷不少于8.5%,野漆树苷不少于0.77%;三等:含柚皮苷不少于7.5%,野漆树苷不少于0.50%;四等:含柚皮苷不少于6.5%,野漆树苷不少于0.37%。
本发明是首次对橘红珠中药材所做的质量检测提供了专属性、重现性强,全面可行的检测方法,为建立了统一的、可行的橘红珠药材质量标准,及进一步对其质量等级进行划分提供了全面可行的检测手段,以利于保护优质药材,避免以次充好,大大提高了橘红珠药材的质量控制水平。
附图说明:
图1是橘红珠的显微鉴别特征图示;
图2是薄层检测点样体积的考察结果图示;
图3是1~11批橘红珠样品薄层鉴别结果图;
图4是橘红珠对照特征图谱;
图5是28批橘红珠样品的聚类分析结果图。
具体实施方式:
下面结合具体实施例对本发明的权利要求做进一步的详细说明。
实施例1橘红珠药材的外观性状鉴别
从橘红珠药材道地产区收集了具代表性的样品28批,如表1所示。检视各批样品的外观性状。橘红珠样品呈近球形、半球形或圆柱形,直径3~6cm。表面墨绿色或灰绿色,密布茸毛,有皱纹及小油室,先端有花柱脱落的痕迹,基部有呈圆形果柄的疤痕;质坚硬,不易切开,断面平整,黄白色或淡红棕色,有脉络纹。外缘有一列不整齐的下凹的油室。气芳香,味苦、微辛。
表1橘红珠样品列表
实施例2橘红珠药材的显微鉴别
供试品粉碎,过二号筛,混合均匀。取适量于载玻片上,滴数滴水合氯醛溶液将粉末浸润后,酒精灯加热,再滴加适量稀甘油溶液,充分混合,盖上盖玻片,置于显微镜下观察。代表性显微特征见图1。样品粉末黄棕色至棕褐色,中果皮薄壁细胞形状不规则,壁不均匀增厚,有的作连珠状或在角隅处特厚。果皮表皮细胞表面观多角形、类方形或长方形,垂周壁增厚,气孔类圆形,直径18~31μm,副卫细胞5~7个。可见碎断的非腺毛,碎段细胞多至十数个,最宽处直径约33μm,胞腔内含淡黄色或棕色颗粒状物。草酸钙方晶成片或成行存在于中果皮薄壁细胞中,呈多面形、菱形、棱柱形、长方形或形状不规则,直径1~32μm,长5~40μm.导管为螺纹导管和网纹导管。偶见石细胞及纤维。
实施例3橘红珠药材的薄层鉴别
1仪器
卡玛薄层色谱自动点样仪(ats4)、自动展开仪(adc2)、紫外成像系统(camag,muttenz,switzerland)。
2试剂
乙酸乙酯,丙酮,冰醋酸,甲醇,乙醇,均为分析纯。
柚皮苷对照品(110722-200610,中国食品药品检定研究院),橙皮内酯水合物对照品(bbp00486,云南西力生物技术股份有限公司),野漆树苷对照品(12110232,上海同田生物技术股份有限公司)。
3供试品制备方法考察
(1)提取溶剂的考察
配制含柚皮苷对照品0.98mg/ml,橙皮内酯水合物对照品0.19mg/ml的混合溶液。
对不同提取溶剂进行考察:甲醇、甲醇水溶液(7:3,v/v)、乙醇、乙醇水溶液(7:3,v/v)。供试品制备步骤如下:
取5号样品,粉碎过二号筛,取0.5g粉末于锥形瓶中,分别加入5ml上述不同提取溶剂,超声15分钟,离心,取上清液作为供试品溶液。各取2μl供试品溶液,点样于高效薄层硅胶g板。展开剂根据预实验结果,选择乙酸乙酯,丙酮,乙酸和水(8:4:0.3:1),点好样的薄层板于饱和展开缸中展开至8cm。取出薄层板,干燥,喷适量5%三氯化铝乙醇溶液显色剂后,于105℃加热一分钟,并在365nm紫外波长下观察。结果表明,提取溶剂对供试品溶液薄层展开效果并无明显影响,最终选用甲醇作为提取溶剂。
(2)提取溶剂体积的考察
取0.5g样品粉末于锥形瓶中,分别加入5ml,10ml,15ml,20ml甲醇,超声15分钟,离心,取上清液作为供试品溶液。各取2μl供试品溶液点样,同法展开、显色结果表明,随着提取体积的降低,柚皮苷及橙皮内酯水合物条带清晰度增加。因此选用5ml提取体积进行后续实验。
(3)提取时间的考察
取0.5g样品粉末于锥形瓶中,加入5ml甲醇,分别超声5min、15min、25min和35min,离心,取上清液作为供试品溶液。各取2μl供试品溶液点样,同法展开、显色。结果表明,超声时间对提取效果无明显影响。选择15分钟作为提取时间。
4点样方法的考察
(1)点样体积的考察
分别取0.5μl,1μl,2μl,5μl,8μl供试品溶液点于高效薄层板展开,干燥,喷显色剂,于105°加热1分钟后,置于365nm紫外波长下观察。结果见图2。结果表明,随着点样体积增加,柚皮苷及橙皮内酯水合物条带清晰度增加。但当点样体积为8μl时,柚皮苷条带与下方条带分离较差。因此最终选用2μl作为点样体积。
(2)条带宽度的考察
取2μl供试品溶液点在高效薄层板上,条带宽度分别为2mm,4mm,6mm,8mmand10mm,于饱和展开缸中展开,干燥,喷适量显色剂后于105°干燥1分钟,并在365nm紫外波长下观察。结果表明,条带随着点样宽度的增加显得更加狭细,分离度更好。因此选用8mm的条带宽度进行后续试验。
5方法学考察
(1)专属性
根据确定好的条件,制备供试品溶液,化橘红对照药材溶液(0.10g/ml,甲醇溶解),柚皮苷对照品溶液(0.98mg/ml,甲醇溶解),野漆树苷对照品溶液(0.46mg/ml,甲醇溶解),橙皮内酯水合物对照品溶液(0.36mg/ml,甲醇溶解)。
以上溶液各取2μl点于高效薄层板展开,干燥,喷适量显色剂,于105°加热1分钟后,置于365nm波长紫外光下观察。365nm波长紫外光结果:供试品溶液中,蓝色条带为rf0.52,与橙皮内酯水合物对照品对应,两条绿色条带rf分别为0.21,0.18,分别对应柚皮苷对照品和野漆树苷对照品。结果显示专属性符合测试要求。
(2)稳定性
供试品溶液于室温放置不同时间(0,1,2,3天)后,点样、展开、显色,置于365nm波长紫外光下观察。结果表明,供试品溶液在3天内稳定性良好。
(3)耐用性
不同粒径硅胶薄层板
样品分别点于不同粒径薄层板上(tlc和hptlc板)。展开、显色,置365nm波长紫外光下观察。结果表明,高效薄层板条带更为清晰,但普通薄层板也可达到鉴别要求。
荧光板的考察
样品分别点于gf254板与硅胶g薄层板。展开、显色,置365nm波长紫外光下观察。结果表明,硅胶g薄层板的条带更为集中、狭窄,gf254板对于本实验不适用。
不同品牌薄层板
样品分别点于不同品牌薄层板上,展开、显色,置365nm波长紫外光下观察。结果表明,不同品牌薄层板对供试品溶液条带无明显影响。
展开湿度的影响
点样后,分别在不同湿度(46%、65%、75%、84%)条件下展开,显色后,置于365nm波长紫外光下观察。结果表明,不同湿度下,条带清晰度无明显区别。
耐用性考察结果表明,不同粒径(高效薄层板或普通薄层板),不同品牌和湿度对样品及对照品溶液薄层展开结果无明显影响。
6橘红珠样品的薄层鉴别
利用建立的薄层鉴别方法,对收集到的橘红珠样品进行鉴别。代表性结果如图3所示。供试品溶液中,在与柚皮苷对照品相应的位置上,均显相同的绿色荧光斑点,rf约为0.28。
实施例4橘红珠药材的特征图谱
1材料
1.1仪器
电子分析天平(bp211d,瑞士sartorius公司);万分之一电子分析天平(me204,瑞士mettlertoledo公司,仪器编号:tp604-2);ultimate3000高效液相色谱仪(美国dionex公司,dgp-3600sd双三元泵、srd-3600脱气机、ups-3000sl自动进样器、tcc3000-rs柱温箱、dad检测器、chromeleon7.2数据处理软件;仪器编号:418-3);色谱柱:welchxb-c18(4.6×250mm,5μm,s.n.211604929),依利特hypersilbdsc18(4.6mm×250mm,5μm),戴安acclaim120c18(4.6mm×250mm,5μm);数控超声波清洗器(kq500de,昆山市超声仪器有限公司;仪器编号:cs605-1);超纯水器(simplicity185personal,美国millipore公司);10ml移液管。
1.2试药
柚皮苷、异欧前胡素对照品,购自中国药品生物制品检定所;野漆树苷对照品,购自上海同田生物技术有限公司;橙皮内酯水合物对照品为实验室自制,hplc检测纯度高于98%。甲醇(天津市大茂化学试剂厂,分析纯);甲醇(honeywell,批号:r11g4h,色谱纯);冰醋酸(aladdin,批号:e1519047,色谱纯)。
1.3样品
条件摸索及方法学考察所用样品为18号橘红珠样品,特征图谱的建立所用样品为1~15号。
2实验方法的摸索
2.1色谱条件
以甲醇为流动相a,以6%醋酸溶液为流动相b,按表2中的规定进行梯度洗脱;流速为1ml/min,检测波长为320nm。
表2流动相洗脱梯度
2.2供试品溶液制备方法的考察
分别比较不同提取方法(水浴回流、超声)及不同提取时间(超声20min、超声30min)对检测结果的影响。
取18号样品粉末(过二号筛)0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇50ml,称定重量,水浴回流提取1h,放冷,再称定重量,用甲醇补足减失的重量,摇匀,取25ml续滤液,浓缩至近干,加甲醇定量转移至5ml量瓶中,并加甲醇至刻度,作为供试品溶液1;
另取18号样品粉末(过二号筛)0.5g,精密称定,置具塞锥形瓶中,精密加入甲醇10ml,称定重量,超声20min或30min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,取其续滤液,作为供试品溶液2、供试品溶液3。
按2.1“色谱条件”分别进样测定,以超声30min与水浴回流1h两种提取方法所得的峰面积计算提取率。结果表明(见表3):超声和水浴回流两种方法提取效率没有明显差异,均可作为供试品溶液的制备方法,超声操作更为方便省时;但是超声处理时间不宜小于30min。
表3不同提取方法的峰面积对比
2.3检测波长的选择
检测波长应保证全谱主要色谱峰都有很好响应,应用二极管阵列检测器考察不同波长下色谱图情况,优选检测波长为320nm。
2.4色谱柱的选择
分别考察依利特hypersilbdsc18(4.6mm×250mm,5μm)、戴安acclaim120c18(4.6mm×250mm,5μm)、welthxb-c18(4.6mm×250mm,5μm)三根色谱柱分离度、保留时间和理论塔板数,结果表明不同品牌的c18均可用于橘红珠特征图谱鉴别,结果见表4最终确定使用welchxb-c18(4.6mm×250mm,5μm)色谱柱进行后续实验。
表4色谱柱的比较
3方法学考察
3.1溶液的制备
对照品溶液的制备:精密称取柚皮苷对照品10.16mg、野漆树苷对照品10.25mg、橙皮内酯水合物对照品10.45mg、异欧前胡素5.48mg,加甲醇溶解,摇匀,分别制成每1ml含柚皮苷508μg、野漆树苷16.4μg、橙皮内酯水合物8.36μg、异欧前胡素54.8μg的对照品溶液。
供试品溶液的制备:取供试品粉末(过二号筛)约0.5g,精密称定,置具塞锥形瓶中,精密加甲醇10ml,称定重量,超声处理(功率120w,频率40khz)30min,放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,取续滤液,作为供试品溶液。
3.2色谱条件
同2.1“色谱条件”。
3.3精密度试验
取18号样品,制成供试品溶液,连续测定6次,并使用中药色谱指纹图谱相似度评价系统(2004a版)软件进行相似度评价,结果见表5。结果表明仪器精密度良好。
表5精密度相似度评价结果
3.4重复性试验
取18号样品,平行制备6份供试品溶液,进样测定,并使用中药色谱指纹图谱相似度评价系统(2004a版)软件进行相似度评价,结果见表6。结果表明重复性良好。
表6重复性相似度评价结果
3.5稳定性试验
取18号样品,制成供试品溶液,分别在室温下放置0、2、4、6、12、24h后进样测定,并使用中药色谱指纹图谱相似度评价系统(2004a版)软件进行相似度评价,结果见表7。结果表明供试品溶液在24h内稳定性良好。
表7稳定性相似度评价
4样品的检测及特征图谱的确立
取1-15批橘红珠样品,分别制成供试品溶液,测定。使用中药色谱指纹图谱相似度评价系统(2004a版)软件,对主要色谱峰进行匹配,生成对照图谱,见图4。结果表明,橘红珠样品中呈现4个主要特征峰,分别为柚皮苷、野漆树苷、橙皮内酯水合物、异欧前胡素。图中,峰1(s):柚皮苷峰2:野漆树苷峰3:橙皮内酯水合物峰4:异欧前胡素。
5相对保留时间规定值的确定
采用不同色谱柱(依利特hypersilbdsc18、戴安acclaim120c18、welchxb-c18)进行考察。以柚皮苷对照品、异欧前胡素对照品为参照,以柚皮苷峰(峰1)为s峰,计算野漆树苷、橙皮内酯水合物的相对保留时间,见表8。根据不同色谱柱特征峰相对保留时间的平均值,规定特征峰2、3、4的相对保留时间为1.49(峰2)、1.74(峰3)、3.19(峰4),峰2、3的测定结果应在规定值的±5%之内;峰4异欧前胡素因出峰较慢,相对保留时间的rsd较大,将限度放宽至规定值的±6%之内。
表8相对保留时间规定值的计算结果
所检测样品的相对保留时间如表9所示,各峰的相对保留时间均符合上述规定。
表9橘红珠样品特征图谱相对保留时间结果
*括号内为规定值范围
实施例5橘红珠药材含量测定方法的建立
橘红珠的主要活性成分为黄酮类物质,以柚皮苷(c27h32o14)和野漆树苷(c27h30o14)为代表。其中柚皮苷占总黄酮的80%以上;药理实验结果表明,其具有良好的止咳化痰作用,同时具有较好的抗气道炎症作用:不仅能显著抑制脂多糖诱导的小鼠急性肺部炎症,而且对于慢性气道炎症也有很好的保护作用;还具有一定的抗氧化作用。野漆树苷具有一定的抗炎及抗氧化作用,对nf诱导的基因毒性有显著保护作用,同时还具保肝作用。因此,本发明选择柚皮苷和野漆树苷作为橘红珠含量测定的指标成分。
1材料
1.1仪器
万分之一电子分析天平(me204,瑞士mettlertoledo公司);ultimate3000高效液相色谱仪(美国dionex公司,dgp-3600sd双三元泵、srd-3600脱气机、ups-3000sl自动进样器、tcc3000-rs柱温箱、dad检测器、chromeleon7.2数据处理软件);色谱柱:dionexacclaim120c18(4.6×150mm,3μm),welchxb-c18(4.6×250mm,5μm);数控超声波清洗器(kq500de,昆山市超声仪器有限公司);超纯水器(simplicity185personal,美国millipore公司);移液管。
1.2试药
柚皮苷对照品(中国药品生物制品检定所,批号:110722-201111,纯度:93.2%),野漆树苷对照品(中国药品生物制品检定所,批号:111919-201102,纯度:95.0%)。甲醇(天津市大茂化学试剂厂,分析纯);甲醇(honeywell,批号:r11g4h,色谱纯);冰醋酸(aladdin,批号:e1519047,色谱纯)。
1.3样品:条件摸索及方法学考察所用样品为18号样品。
2供试品制备方法的考察
2.1色谱条件
色谱柱:dionexacclaim120c18(4.6×150mm,3μm);流动相:甲醇(a)-0.3%醋酸溶液(b)=35∶65;流速:1.0ml/min;检测波长:320nm;进样量:10μl;柱温:35℃。
2.2对照品溶液的制备
精密称取适量柚皮苷对照品、野漆树苷对照品和橙皮内酯水合物对照品,加甲醇制成每1ml分别含柚皮苷496.5μg、野漆树苷20.23μg、橙皮内酯水合物9.12μg的溶液。
2.3供试品溶液的制备
使用水浴回流及超声两种方法对样品进行提取,其中超声时间分别考察20分钟、30分钟,比较以上三种方法的柚皮苷、野漆树苷及橙皮内酯水合物提取效果。
供试品溶液a(水浴回流):取供试品粉末(过二号筛)0.5g,精密称定,置150ml圆底烧瓶中,精密加入甲醇50ml,称定重量,水浴回流提取60分钟,放冷,再称定重量,用甲醇补足减失的重量,摇匀,取25ml续滤液,加甲醇定量转移至5ml量瓶中,并加甲醇至刻度,摇匀,过0.45μm滤膜,取续滤液即得。
供试品溶液b(超声20min):取供试品粉末(过二号筛)0.5g,精密称定,置100ml具塞锥形瓶中,精密加入甲醇50ml,称定重量,超声20分钟(150w,40khz),放冷,再称定重量,用甲醇补足减失的重量,摇匀,过0.45μm滤膜,取续滤液即得。
供试品溶液c(超声30min):取供试品粉末(过二号筛)0.5g,精密称定,置100ml具塞锥形瓶中,精密加入甲醇50ml,称定重量,超声30分钟(150w,40khz),放冷,再称定重量,用甲醇补足减失的重量,摇匀,过0.45μm滤膜,取续滤液即得。
分别进样以上3种供试品溶液10μl,记录所需成分的峰面积。结果表明见表10,超声30分钟与水浴回流60分钟的提取效果相近,且两种成分的峰面积均略高于水浴回流,说明此法提取效果较好,且更加省时、便利。故选择超声30分钟作为样品的提取方法。
表10不同提取方法的比较
最终确定的供试品溶液制备方法为:取样品粉末(过二号筛)约0.5g,精密称定,置100ml具塞锥形瓶中,精密加入甲醇50ml,称定重量,超声处理30分钟(150w,40khz),放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml容量瓶中,加50%甲醇至刻度,摇匀,滤过,取续滤液,即得。
为节约溶剂,本标准草案中将供试品制备方法调整为:取本品粉末(过二号筛)约50mg,精密称定,置10ml容量瓶中,精密加入甲醇5ml,超声处理30分钟(150w,40khz),放冷,加50%甲醇至刻度,摇匀,滤过,取续滤液,即得。
3色谱系统考察
3.1溶液的制备
(1)对照品溶液的制备
精密称取适量柚皮苷对照品、野漆树苷对照品,加甲醇制成每1ml分别含柚皮苷420.2μg、野漆树苷12.42μg的溶液。
(2)供试品溶液的制备
取供试品粉末(过二号筛)约0.5g,精密称定,置100ml具塞锥形瓶中,精密加入甲醇50ml,称定重量,超声处理30min(150w,40khz),放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml容量瓶中,加50%甲醇至刻度,摇匀。过0.45μm滤膜,取续滤液,即得。
3.2色谱条件
流动相及比例选择甲醇-0.3%醋酸溶液(35:65)等度洗脱。
3.3检测波长的选择
根据柚皮苷、野漆树苷对照品溶液的紫外波长扫描结果,确定最大吸收波长λmax。分别选择283nm和338nm作为柚皮苷和野漆树苷的检测波长。
3.4色谱柱的选择
(1)不同品牌色谱柱的考察
共考察三种不同品牌色谱柱:dionexacclaimc18(5μm,4.6×250mm),agilenteclipseplusc18(5μm,2.1×250mm),welchxbc18(5μm,4.6×250mm)。使用同一对照品溶液,比较柚皮苷、野漆树苷的保留时间、理论塔板数和拖尾因子。结果表明表11,对于以上三种品牌色谱柱,柚皮苷、野漆树苷均能获得较好的分离效果。
表11色谱柱的选择
(2)不同柱长的考察
使用同一供试品溶液,考察不同柱长色谱柱的分离效果:dionexacclaim120c18(3μm,4.6×150mm)、dionexacclaim120c18(5μm,4.6×250mm)。结果表明见表12,两种长度的色谱柱对于柚皮苷和野漆树苷皆有较好的分离度。考虑到缩短保留时间,选用150mm柱长的色谱柱进行后续试验。
表12色谱柱长的考察
3.5流动相的选择
(1)ph值
使用同一供试品溶液,考察流动相ph值分别为2.6、2.8、3.0、3.2时的分离效果。结果表明见表13,随着ph值的降低,保留时间变长。但ph为2.8、3.0、3.2时,保留时间区别很小。考虑到获得更好的柱效及分离度,选择流动相ph值为3.0。
表13流动相ph值的选择
(2)流动相比例
使用同一供试品溶液,考察流动相中不同甲醇比例(30%、33%、35%、37%、40%)对分离的影响。结果表明见表14,不同比例甲醇对两种待测成分的保留时间有显著影响。甲醇比例越高,保留时间越短。考虑到分离度及缩短分析时间,最终选择甲醇比例为35%。
表14流动相甲醇比例的选择
(3)流速
使用同一供试品溶液,考察不同流速(0.8、1.0、1.2ml/min)对分离效果的影响。结果见表15。结果表明:除保留时间外,流速对各参数无明显影响。最终选用1.0ml/min进行后续实验。
表15流速的选择
3.6柱温的选择
使用同一供试品溶液,考察不同柱温(25、30、35、40℃)对分离效果的影响。结果表明见表16,随着柱温上升,柚皮苷与野漆树苷的分离度减小。考虑到二者之间合适的分离度,最终选用35℃进行后续实验。
表16柱温的选择
最后确定的色谱条件为:色谱柱:dionexacclaim120c18(4.6×150mm,3μm);流动相:甲醇(a)-0.3%醋酸溶液(b)=35∶65;流速:1.0ml/min;检测波长:柚皮苷283nm,野漆树苷338nm;进样量:10μl;柱温:35℃。
4方法学考察
通过混合对照品溶液以及供试品溶液,使用外标法计算柚皮苷和野漆树苷在样品中的含量。其公式如下:
(ru/rs)×(cs/cu)×100
ru为在供试品溶液中,柚皮苷在283nm波长下、野漆树苷在338nm波长下的峰面积;rs为在混合标准品溶液中,柚皮苷在283nm波长下、野漆树苷在338nm波长下的峰面积。cu为供试品溶液的浓度,单位为mg/ml;cs分别为柚皮苷、野漆树苷在混合标准品溶液中的浓度,单位mg/ml。
4.1线性范围
对照品母液的制备:精密称取16.34mg野漆树苷对照品于10ml容量瓶中,甲醇定容,制成野漆树苷对照品母液。根据纯度,计算出野漆树苷母液的浓度为1.552mg/ml。
精密称取42.02mg柚皮苷对照品于10ml容量瓶中,加少量甲醇溶解,再加入上述野漆树苷对照品母溶液0.8ml,甲醇定容,摇匀,即得混合对照品母液,其中柚皮苷、野漆树苷浓度分别为4.202、0.1242mg/ml。
线性对照品溶液的制备:分别定量移取不同体积0.1、0.2、0.5、1.0、1.5、2.0、2.5ml上述混合对照品母液于10ml容量瓶中,加50%甲醇定容,混匀。
分别进样各浓度的线性对照品溶液,记录283nm波长下柚皮苷峰面积、338nm波长下野漆树苷峰面积。根据各浓度下测得的峰面积,获得以下校正曲线见表17,结果表明,柚皮苷和野漆树苷都具有良好的线性。
表17柚皮苷、野漆树苷及橙皮内酯水合物的标准曲线
4.2重复性试验
取同一批样品,平行制备六份供试品溶液,进样测定。结果表明见表19),两种待测成分含量的rsd均小于2%。
表19重复性试验结果
4.3中间精密度试验
不同日期:取同一批样品,在3个不同日期制备供试品溶液,每次平行3份,进样测定,结果见表20,rsd小于2%。
不同分析人员:取同一批样品,由三名分析人员分别平行制备3份供试品溶液,进样检测,结果见表21,rsd小于2%。
表20中间精密度试验结果-不同日期
表21中间精密度试验结果-不同分析人员
4.4准确性试验
通过检测已知加入量的两种待测成分的回收率来判断方法的准确性。分别制备低、中、高三个浓度的供试品溶液,每个浓度平行制备三份,方法如下:
低浓度:精密移取甲醇50ml,置100ml具塞锥形瓶中,再精密移出1.0ml。取柚皮苷对照品10mg、样品粉末250mg,精密称定,移至上述锥形瓶中,并加入1.0ml野漆树苷对照品溶液(浓度为0.3105mg/ml,溶剂为甲醇)。称定重量,超声处理30min(150w,40khz),放冷,再称定重量,用甲醇补足减失的重量,摇匀,滤过,精密量取续滤液5ml,置10ml量瓶中,加50%甲醇至刻度,摇匀。过0.45μm滤膜,取续滤液即得。
中浓度:精密移取甲醇50ml,置100ml具塞锥形瓶中,再精密移出2.0ml。取柚皮苷对照品20mg、样品粉末250mg,精密称定,移至上述锥形瓶中,并加入2.0ml野漆树苷对照品溶液(浓度为0.3105mg/ml,溶剂为甲醇),其余步骤同上。
高浓度:精密移取甲醇50ml,置100ml具塞锥形瓶中,再精密移出3.0ml。取柚皮苷对照品30mg、样品粉末250mg,精密称定,移至上述锥形瓶中,并加入3.0ml野漆树苷对照品溶液(浓度为0.3105mg/ml,溶剂为甲醇),其余步骤同上。
根据样品的测得量、原有量及加入量,计算其回收率。结果表明(表22、表23),回收率范围在95%-105%之间,且rsd<3%。
表22柚皮苷回收率试验结果
回收率(%)=100×(测得量-原有量)/加入量,下同
表23野漆树苷回收率试验结果
4.5稳定性试验
使用同一供试品溶液,在室温存放不同时间后进样检测,比较三种待测成分的峰面积,并计算rsd。结果显示(表24),供试品溶液中三种成分在24小时内稳定性良好。
表24供试品溶液稳定性试验结果
4.6耐用性试验
使用两种长度的色谱柱(150mm,250mm),分别检测柚皮苷、野漆树苷含量,通过相对平均偏差(rad)评估两种柱长的含量测定误差。结果表明(表25),两种成分含量计算结果的rad均小于3%,说明色谱柱长对检测结果的影响小。
表25耐用性试验结果——色谱柱长
*色谱柱品牌均为dionexacclaim
实施例6橘红珠药材样品各指标测定结果及综合分析
水分测定:供试品粉碎,过二号筛,取2~5g,平铺于干燥至恒重的扁形称量瓶中,精密称定,开启瓶盖在100~105℃干燥5小时,将瓶盖盖好,移置干燥器中,放冷30分钟,精密称定,再在上述温度干燥1小时,放冷,称重,至连续两次称重的差异不超过5mg为止。根据减失的重量,计算供试品中含水量(%)。水分测定结果如表26所示。
总灰分测定:供试品粉碎,过二号筛,混合均匀后,取2~3g,置炽灼至恒重的坩埚中,称定重量(准确至0.01g),缓缓炽热,至完全炭化时,逐渐升高温度至500~600℃,使完全灰化并至恒重,根据残渣重量,计算供试品中总灰分的含量(%)。总灰分测定结果如表26所示。
柚皮苷、野漆树苷含量测定:根据已建立的含量测定方法,对28批橘红珠样品进行柚皮苷、野漆树苷含量测定,结果如表26所示。
表2628批橘红珠样品各指标测定结果
表27橘红珠各指标的相关性分析
数据分析:利用spss19.0软件处理数据。对所检测的5项可量化指标进行统计分析,筛选橘红珠药材等级划分指标及限度。
由表26可知,水分和总灰分的变异系数较小,说明离散程度小,差异不明显,提示不适合作为样品等级划分的指标。因此,统一以平均值上浮20%作为水分和总灰分的限度,规定分别不得过12.0%和4.5%。
由表27可知,柚皮苷和野漆树苷与果实直径均呈负相关,其中果实直径为外观性状指标,柚皮苷、野漆树苷含量为内在质量指标,故结合这三个指标,来对橘红珠药材质量优劣进行评价。
根据评价指标检测数据,将28批橘红珠样品进行系统聚类分析,结果如5所示。谱系图中的距离代表相似度,距离越远差异越大,其中20号样品在距离为25时才可单独与其他样品归为一类,故不作为均值聚类数值。进一步对3个评价指标作k-均值聚类分析,结果见表28。
表28橘红珠样品的最终聚类中心值
结合分析结果及实际情况,最终将橘红珠分为一等、二等、三等和四等:
一等:果实直径不超过4cm,含柚皮苷不少于11.8%、野漆树苷不少于0.93%;二等:果实直径不超过5cm,含柚皮苷不少于8.5%、野漆树苷不少于0.77%;三等:果实直径不超过6cm,含柚皮苷不少于7.5%、野漆树苷不少于0.50%;四等:果实直径不超过6cm,含柚皮苷不少于6.5%、野漆树苷不少于0.37%。28批样品的等级划分结果见表26,划分为一等的样品有4批、二等6批、三等11批、四等4批,另有3批不合格样品。说明本发明建立的橘红珠药材检测方法及由该方法建立的等级质量标准科学、有效、可行。
- 还没有人留言评论。精彩留言会获得点赞!