糖化蛋白质的测定的制作方法
本公开涉及糖化蛋白质的测定,更具体而言,涉及使用阿马道里酶的糖化蛋白质的测定方法、装置、系统。
背景技术:
由于当蛋白质与葡萄糖等糖共存时形成阿马多利化合物,因此能够通过阿马多利化合物量的测定来知道糖的量。关于糖的量,在人或动物的血液中、食品等中测定。
糖化蛋白质量的测定尤其在糖尿病的诊断、治疗中是重要的。作为糖化蛋白质量的测定方法,存在仅仅测定糖化蛋白质量的方法、测定糖化蛋白质量和蛋白质量而计算比率的方法等,关于作为对象的蛋白质,还存在没有特别限制的情况、局限于特定蛋白质的情况、局限于特定蛋白质的特定部位的情况。
作为这样的糖化蛋白质量的测定,存在果糖胺、糖化白蛋白、糖化血红蛋白以及血红蛋白a1c等。
例如,关于果糖胺,测定血清、血浆中的蛋白质或白蛋白的糖化量,关于糖化白蛋白,测定血清、血浆中的白蛋白的糖化量与白蛋白量之间的比率。关于糖化血红蛋白,测定血液中的血红蛋白的糖化量、或者与血红蛋白量之间的比率。关于血红蛋白a1c,测定血液中的血红蛋白的β链n末端糖化量(hba1c量)、或者与血红蛋白量之间的比率。
作为这些糖化蛋白质的测定方法,使用了与糖化氨基酸、糖化肽反应的阿马道里酶的酶法通常被使用。
日本专利3034698中示出果糖胺的测定法、日本专利4341809以及日本专利特开2008-295305中示出糖化白蛋白的测定法,日本专利5878096等中示出仅针对糖化血红蛋白量的测定法。
其中,糖化血红蛋白比率的测定在糖尿病的诊断、治疗中是重要的。作为糖化血红蛋白之一的血红蛋白a1c(hba1c)的测定尤其被广泛测定。
为了糖化血红蛋白比率的测定,广泛使用测定糖化血红蛋白量与血红蛋白量的方法。
作为糖化血红蛋白量的测定方法,使用了与糖化氨基酸、糖化肽反应的阿马道里酶的酶法通常被使用。作为阿马道里酶,存在生成过氧化氢等的果糖基肽氧化酶(日本专利4231668)、提高了脱氢酶活性的果糖基肽脱氢酶(wo2016-63984)等。
用于现有的酶法中的阿马道里酶具有从糖化氨基酸对糖化肽的基质特异性。因此,在通过阿马道里酶来测定糖化血红蛋白量的情况下,有必要通过蛋白酶等来预先处理糖化血红蛋白而分解成糖化氨基酸、糖化肽,以使得阿马道里酶容易作用(wo2006-120976)。在通过蛋白酶来分解糖化血红蛋白的情况下,由于用于测定的阿马道里酶不会被蛋白酶分解,有必要调制成其他试剂。
另一方面,由于因hb与试剂(尤其蛋白酶)反应而hb的色调变化、以及通过阿马道里酶的作用而根据糖化血红蛋白浓度生成的显色染料与hb的色调重叠从而对糖化血红蛋白值带来影响等,因此难以在试样、阿马道里酶以及蛋白酶混合之后测定血红蛋白量。
作为由酶法进行的糖化血红蛋白量的测定的试剂,当前使用双试剂系统或三试剂系统的试剂。作为双试剂系统的试剂的构成,可以举出以下的构成1~4。
构成1
第一试剂:阿马道里酶、缓冲剂
第二试剂:蛋白酶、显色剂、缓冲剂
构成2
第一试剂:蛋白酶、缓冲剂
第二试剂:阿马道里酶、显色剂、缓冲剂
构成3
第一试剂:阿马道里酶、显色剂、缓冲剂
第二试剂:蛋白酶、缓冲剂
构成4
第一试剂:蛋白酶、显色剂、缓冲剂
第二试剂:阿马道里酶、缓冲剂
近年来,阿马道里酶被改良,发现了对糖化蛋白质具有基质特异性(直接作用于糖化蛋白质)的阿马道里酶(以下,还称为“糖化蛋白直接型阿马道里酶”)(wo2015-005257以及wo2015-060429)。作为使用了糖化蛋白直接型阿马道里酶的糖化血红蛋白量的测定方法,例如,公开有包括依次进行下述(i)~(ii)工序的测定方法。
(i)将糖化蛋白直接型阿马道里酶作用于试样中的糖化血红蛋白而使糖化血红蛋白氧化的工序。
(ii)测定上述工程(i)中生成的物质或者所消耗的物质的工序。
此外,关于血红蛋白量的测定,使用测定血红蛋白的血红素的红色的方法。血红蛋白包括氧化型和还原型,根据型而血红素的电荷状态变化、光谱变化,因此有必要使用用于设为某一定型的变性剂。
技术实现要素:
在通过双试剂系统的酶法试剂进行糖化蛋白质比率的测定的情况下,存在依次添加两种溶液的工序。即,存在如下两个工序:使试样与第一试剂混合的工序、以及在其中混合第二试剂的工序。因此,在由双试剂系统的试剂进行的糖化蛋白质比率的测定方法中,工序较繁杂。另外,由于具有两个工序,因此分注、混合等作业需要时间从而难以缩短时间。
本公开在一个方式中提供一种工序被简化的测定方法,该测定方法是通过酶法进行的糖化蛋白质的测定方法。
本公开在一个方式中涉及包括下述(1)至(3)的试样中的糖化蛋白质的测定方法,其中,为了进行下述(2)和(3)而与试样混合的试剂是一个。以下,将该测定法方法还称为“本公开涉及的测定方法”,将为了进行下述(2)和(3)而与试样混合的试剂还称为“单试剂系统试剂”。此外,在本公开中,单试剂系统试剂还可以是为了进行下述(1)至(3)而与试样混合的试剂。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与阿马道里酶的反应,使显色剂显色。
(3)测定(1)和(2)之后的试样的显色信号,并计算糖化蛋白质量。
本公开在其他一个方式中,涉及执行本公开涉及的测定方法的糖化蛋白质的测定装置或测定系统。
根据本公开,例如,能够简化由酶法进行的糖化蛋白质的测定方法的工序。根据本公开,例如,能够将向溶血试样添加双试剂或三试剂的工序设为混合单试剂的工序。由此,例如,能够缩短血红蛋白a1c比率(hba1c%)的测定中所需的时间。另外,例如,由于是单试剂的混合,因此能够在相同溶液内进行糖化血红蛋白量的测定和血红蛋白量的测定,从而能够提高测定准确性、精度。
附图说明
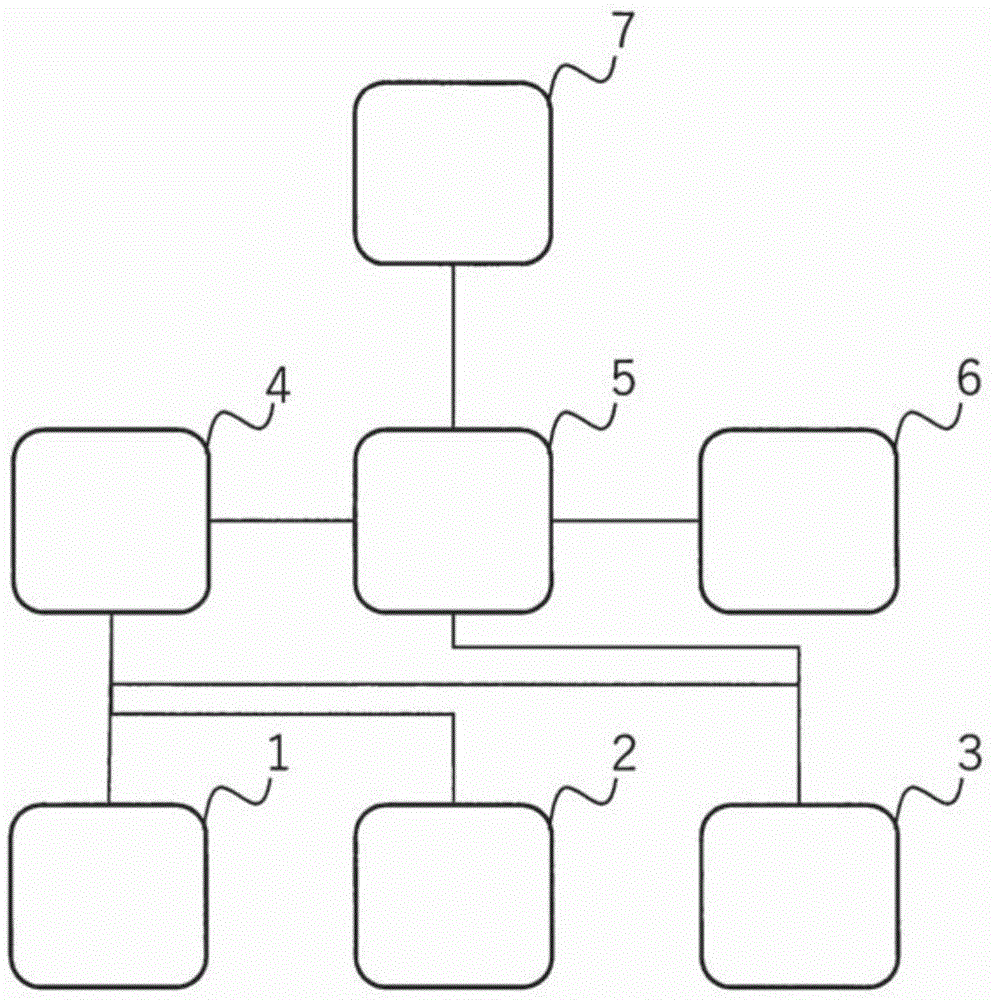
图1是执行本公开涉及的测定方法的糖化蛋白质的测定装置或测定系统的一个例子的说明图。
具体实施方式
在本公开中,关于糖化蛋白质的测定,在一个实施方式中,包括糖化蛋白质量的测定,在其他一个实施方式中,包括糖化蛋白质量以及蛋白质量的测定,在又一其他一个实施方式中,能够包括测定糖化蛋白质量以及蛋白质量而求出它们之比的情况。
在本公开中,在没有特别提及的情况下,“蛋白质”可以包括“糖化蛋白质”。
在本公开中,单试剂系统试剂的“与试样之间的混合”包括:向试样添加单试剂系统试剂;以及向单试剂系统试剂添加试样。
本公开涉及的测定方法在一个或多个实施方式中,通过试样与单试剂系统试剂的一次混合、且在一个容器(例如,测光小室)内能够进行蛋白质的变性、糖化蛋白质与阿马道里酶的反应、使显色剂显色、显色剂的吸光度的测定、以及选择性地测定变性的蛋白质的吸光度。
在本公开中,通过单试剂系统试剂使试样中的蛋白质变性是指,单试剂系统试剂包括能够使试样中的蛋白质变性的变性剂(或者具有变性作用的物质)。如后面叙述,混合前的试样为了溶血等而可以包括表面活性剂(变性剂)。
作为本公开涉及的测定方法中测定的糖化蛋白质,可以举出果糖胺、糖化白蛋白、糖化血红蛋白等,在一个实施方式中,为糖化白蛋白或糖化血红蛋白。作为糖化血红蛋白,可以举出hbβ链n末端被糖化的血红蛋白a1c(hba1c)。
作为本公开涉及的测定对象试样,可以举出包含糖化蛋白质的试样。在糖化蛋白质为糖化血红蛋白的情况下,作为测定对象试样,可以举出包含血红蛋白和糖化血红蛋白的试样。作为测定对象试样,在不受限的一个或多个实施方式中,可以举出全血、包含血球等红细胞的试样、使该试样的溶血的试样。在测定对象试样为包含红细胞的试样的情况下,可以由单试剂系统试剂溶血,也可以由与单试剂系统试剂不同的手段溶血并作为溶血试样。红细胞的溶血能够通过现有的方法实施。例如,存在使用渗透压的方法(例如,水)、使用表面活性剂的方法、冷冻的方法、使用超声波的方法等。若使用表面活性剂等具有变性作用的物质,则溶血的同时还进行蛋白质的变性。
在一个或多个实施方式中,关于基于试样的显色信号的hba1c等的糖化蛋白质量、血红蛋白等的蛋白质量的计算,能够通过公知的方法来进行。
因此,本公开在一个方式中涉及一种包括下述(1)至(4)的、试样中的糖化血红蛋白的测定方法,其中,为了进行下述(1)至(4)而与试样混合的试剂为一个。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与阿马道里酶的反应,使显色剂显色。
(3)测定(1)和(2)之后的试样的显色信号,并计算糖化血红蛋白量。
(4)测定(1)和(2)之后的试样的显色信号,并计算血红蛋白量。
另外,在测定对象试样为包含红细胞的试样的情况下,可以通过与单试剂系统试剂不同的手段来进行溶血和血红蛋白的变性。即,本公开在一个方式中,涉及包括下述(0)至(4)的、试样中的糖化血红蛋白的测定方法,其中,为了进行上述(2)至(4)而与试样混合的试剂为一个。
(0)使试样中的红细胞溶血,并从红细胞放出血红蛋白。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与阿马道里酶的反应,使显色剂显色。
(3)测定(1)和(2)之后的试样的显色信号,并计算糖化血红蛋白量。
(4)测定(1)和(2)之后的试样的显色信号,并计算血红蛋白量。
[使用糖化蛋白直接型阿马道里酶的实施方式]
本公开涉及的测定方法在一个实施方式中,作为阿马道里酶而使用针对糖化蛋白质具有基质特异性(直接作用于糖化蛋白质)的阿马道里酶(糖化蛋白直接型阿马道里酶)。
在本公开中,“糖化蛋白直接型阿马道里酶”是指,即使没有将糖化蛋白质由蛋白酶等分解为肽,也能够将糖化蛋白质的糖化部分作为基质而进行反应的阿马道里酶。
作为糖化蛋白直接型阿马道里酶,可以举出糖化蛋白直接型果糖基肽氧化酶(直接型fpox)、以及糖化蛋白直接型果糖基肽脱氢酶(直接型fpdh)(wo2015-005257以及wo2015-060429)。
[使用直接型fpox的实施方式a]
本公开涉及的测定方法在未受限制的实施方式a中,涉及一种包括下述(1)至(4)的、糖化蛋白质的测定方法,其中,为了进行下述(1)至(4)、或者为了进行下述(2)至(4),包括:使一个试剂(单试剂系统试剂)与试样混合。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与直接型fpox的反应,生成过氧化氢。
(3)通过所生成的过氧化氢与过氧化物酶(pod)的反应,使氧化显色剂显色。
(4)测定所显色的氧化显色剂的显色信号,并计算糖化蛋白质量。
在不受限的一个或多个实施方式中,作为实施方式a中的单试剂系统试剂,可以举出下述构成a1~a3。但是,本公开涉及的试剂不局限于这些实施方式。单试剂系统试剂还可以包括其他成分。
构成a1
单试剂系统试剂:缓冲剂、变性剂、直接型fpox、pod、氧化显色剂
构成a2
单试剂系统试剂:缓冲剂、直接型fpox、pod、氧化显色剂
构成a3
单试剂系统试剂:缓冲剂、直接型fpox、pod、隐色型染料、下述式(i)的化合物
在式(i)中,r表示碳数8-17的烃基。
作为实施方式a中的缓冲剂,能够使用能调整到中性附近、且不损伤反应系统的缓冲剂。作为缓冲剂的不受限的例子,可以举出n,n-双(2-羟乙基)-2-氨基乙磺酸(bes,n,n-bis(2-hydroxyethyl)-2-aminoethanesulfonicacid)、3-吗啉代丙磺酸(mops,3-morpholinopropanesulfonicacid)、n-三(羟甲基)甲基-2-氨基乙磺酸(tes,n-tris(hydroxymethyl)methyl-2-aminoethanesulfonicacid)、2-[4-(2-羟乙基)-1-哌嗪基]乙磺酸(hepes,2-[4-(2-hydroxyethyl)-1-piperazinyl]ethanesulfonicacid)、n-[三(羟甲基)甲基]甘氨酸(tricine,n-[tris(hydroxymethyl)methyl]glycine)、哌嗪-1,4-双(2-乙磺酸)(pipes,piperazine-1,4-bis(2-ethanesulfonicacid))、哌嗪-1,4-双(2-羟基-3-丙磺酸)脱水(popso,piperazine-1,4-bis(2-hydroxy-3-propanesulfonicacid)dehydrate)、碳酸、磷酸、硼酸、甘氨酸、丙氨酸、亮氨酸、精氨酸、赖氨酸、组氨酸、牛磺酸、天冬氨酸、天冬酰胺、羟脯氨酸、脯氨酸、苏氨酸、丝氨酸、谷氨酸、谷氨酰胺、缬氨酸、半胱氨酸、蛋氨酸、异亮氨酸、亮氨酸、酪氨酸、苯丙氨酸、鸟氨酸、色氨酸、羟甲基氨基甲烷、二甲基氨基乙醇、三乙醇胺、二乙醇胺、单乙醇胺、n-甲基氨基乙醇、肌酐、咪唑、巴比妥、氨、乙胺、二乙胺、三乙胺等。
作为实施方式a中的过氧化物酶(pod),能够使用与过氧化氢反应而使作为显色基质的隐色型染料等氧化显色剂发光的酶。pod来源的生物种等不受特别限制。作为不受限的例子,可以举出源自辣根的过氧化物酶。
作为实施方式a的构成a1中的变性剂,能够使用能变性蛋白质、且不会显著损伤酶的活性的变性剂。作为变性剂的不受限的例子,可以举出下述(1)至(8)。此外,(1)~(7)还可以与亚硝酸并用。
(1)3-月桂基二甲基氨基丁酸(3-lauryldimethylaminobutyricacid)
(2)3-肉豆蔻基二甲基氨基丁酸(3-myristyldimethylaminobutyricacid)
(3)月桂基二甲基氨基丙磺酸(lauryldimethylaminopropanesulfonicacid)
(4)肉豆蔻基二甲基氨基丙磺酸(myristyldimethylaminopropanesulfonicacid)
(5)月桂酰胺基二甲基氨基丁酸(laurylamidepropyldimethylaminobutyricacid)
(6)肉豆蔻酰胺丙基甜菜碱(myristamidepropylbetaine)
(7)n-十二烷基-βd-麦芽糖苷(n-dodecyl-βd-maltoside)
(8)wst-3(2-(4-碘苯基)-3-(2,4-二硝基苯基)-5-(2,4-二磺基苯基)-2h-四氮唑)(wst-3(2-(4-iodophenyl)-3-(2,4-dinitrophenyl)-5-(2,4-disulfophenyl)-2h-tetrazolium))
实施方式a的构成a1和a2中的氧化显色剂在进行糖化血红蛋白量、血红蛋白量的测定的情况下,优选为隐色型染料。
作为所述隐色型染料,例如可以举出容易入手的n-(羧甲基氨基羰基)-4,4'-双(二甲基氨基)二苯胺(da-64)、10-(羧甲基氨基羰基)-3,7-双(二甲基氨基)吩噻嗪(da-67)、2,2'-氨基双(3-乙基苯并噻唑啉酮-6-磺酸)(abts)、双-(4-二乙基氨基苯基)-2-磺基苯基甲烷(bspm)、双[3-双(4-氯苯基)甲基-4-二甲基氨基苯基]胺(bcma)、10-n-甲基氨基甲酰基-3,7-二甲氨基-10h-吩噻嗪(mcdp)、邻联甲苯胺、3,3'-二氨基联苯胺·4hcl(dab)、3-(4-羟基苯基)丙酸(hppa)、3,3',5,5'-四甲基联苯胺(tmbz)、n-(3-磺丙基)-3,3',5,5'-四甲基联苯胺·na(tmbz-ps)、n,n',n',n”,n”-己基(3-磺丙基)-4,4',4”-三氨基三苯基甲烷·6na(tpm-ps)等。
关于实施方式a的构成a1和a2中的氧化显色剂,在果糖胺、糖化白蛋白的测定的情况下,能够使用通过4-氨基安替比林(4-aa)或者3-甲基-2-苯并噻唑啉酮腙(mbth)等的偶合剂与苯酚等的色原体的氧化缩合来生成染料的特林德试剂(trinderreagent)、或者隐色型染料。
作为特林德试剂的氢供体,能够使用苯酚衍生物、苯胺衍生物、甲苯胺衍生物等,作为具体例子,举出n-(3-磺丙基)苯胺钠一水合物(halps)、n-乙基-n-(3-磺丙基)-3-甲基苯胺钠一水合物(tops)、n-乙基-n-(2-羟基-3-磺丙基)-3,5-二甲氧基苯胺钠一水合物(maos)、n-(3-磺丙基)-3,5-二甲氧基苯胺钠一水合物(hdaps)、n-(2-羟基-3-磺丙基)-3,5-二甲氧基苯胺钠(hdaos)、n-乙基-n-(3-磺丙基)-3,5-二甲氧基苯胺钠一水合物(daps)、n-乙基-n-(2-羟基-3-磺丙基)-3,5-二甲氧基苯胺钠(daos)、n-乙基-n-(3-磺丙基)苯胺钠(alps)、n-乙基-n-(3-磺丙基)-3-甲氧基苯胺钠一水合物(adps)、n-乙基-n-(2-羟基-3-磺丙基)-3-甲氧基苯胺钠二水合物(ados)、n-乙基-n-(2-羟基-3-磺丙基)-间甲苯胺(toos)、n,n-双(4-磺丁基)-3-甲基苯胺二钠(todb)等。
实施方式a的构成a1和a2还可以包括染料稳定剂,例如可以包括还原剂、表面活性剂等。
实施方式a的构成a3中包括能够发挥变性剂和染料稳定剂的两个功能的式(i)的化合物。在式(i)中,从不阻碍酶法测定的观点以及提高隐色型染料的稳定性的观点出发,r的碳数优选为8至17,更优选为12至16,进一步优选为14。从相同的观点出发,r的烃基优选为烷基,更优选为直链烷基。从相同的观点出发,r优选为十二烷基以及十四烷基,更优选为十四烷基。
作为实施方式a中的测定对象试样,可以举出包含血红蛋白以及糖化血红蛋白的试样。作为测定对象试样,在不受限的一个或多个实施方式中,可以举出全血、包含血球等红细胞的试样、使该试样溶血的试样。在测定对象试样为包含红细胞的试样的情况下,可以由单试剂系统试剂溶血,也可以由与单试剂系统试剂不同的单元溶血并作为溶血试样。红细胞的溶血能够通过现有的方法实施。例如,存在利用渗透压的方法(例如,水)、利用表面活性剂的方法、利用冷冻的方法、超音波的方法等。
在一个或多个实施方式中,作为本公开的显色信号,可以举出吸光度、反射率以及透过率等。
在一个或多个实施方式中,糖化蛋白质量的计算包括将由测定得到的显色信号基于预定的换算因素换算为糖化蛋白质量。在一个或多个实施方式中,基于预定的换算因素的糖化蛋白质量的换算能够通过将由测定得到的吸光度等的显色信号基于下述(i)~(iv)中任一者的换算规则换算为糖化蛋白质量而进行。(iv)可以与(i)~(iii)组合而进行。
(i)基于试样中的某已知的校准物质来求出校准曲线,将源自hba1c的吸光度基于校准曲线换算为hba1c量。
(ii)将显色染料作为校准物质(校正用物质),求出显色染料的校准曲线,将显色染料的吸光度基于该显色染料的校准曲线换算为糖化蛋白质量。
(iii)取不同的波长中求出的吸光度比,基于相对于吸光度比的校准曲线换算为糖化蛋白质量。
(iv)取在试样与试剂的混合后紧接以及混合预定时间经过后测定的吸光度之差而求出吸光度变化量,基于相对于吸光度变化量的校准曲线换算为糖化蛋白质量。
在一个或多个实施方式中,作为(i)中的已知的校准物质,可以举出含有已知量的hba1c的校正用标准物质。在一个或多个实施方式中,作为含有已知量的hba1c的校正用标准物质,可以举出全血或血细胞的冷冻品、提炼它们的含有hba1c的hb溶液、或者在它们之中含有缓冲液组成物以及hb的稳定剂等的物质等。在一个或多个实施方式中,作为已知的校准物质,可以举出公共机构提供的一级标准物质或常用标准物质、试剂盒附带的校正物质等。
在一个或多个实施方式中,作为(iv)中的混合后紧接,可以举出从试样与试剂的混合至5秒~30秒左右。在一个或多个实施方式中,作为预定时间经过后,可以举出从试样与试剂的混合至1分钟~3分钟左右。
此外,上述方式是显色信号为吸光度的情况的一个例子,即使是吸光度以外的反射率以及透过率,也能够以同样的方式进行。
实施方式a中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式aa,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(1)至(5),包括为了进行下述(1)至(5)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式aa
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与直接型fpox的反应,生成过氧化氢。
(3)通过所生成的过氧化氢与过氧化物酶(pod)的反应,使隐色型染料显色。
(4)测定所显色的隐色型染料的显色信号并计算糖化血红蛋白量。
(5)测定所变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式a中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式ab,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(0)至(5),包括为了进行下述(2)至(5)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式ab
(0)使试样中的红细胞溶血并将血红蛋白从红细胞放出。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与直接型fpox的反应,生成过氧化氢。
(3)通过所生成的过氧化氢与过氧化物酶(pod),使隐色型染料显色。
(4)测定所显色的隐色型染料的显色信号并计算糖化血红蛋白量。
(5)测定所变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式aa和ab还可以包括根据糖化血红蛋白量与血红蛋白量计算糖化血红蛋白比率。
另外,在实施方式aa和ab中,糖化血红蛋白在一个或多个实施方式中为血红蛋白a1c。
实施方式a中的测定对象是糖化血红蛋白以外的糖化蛋白质(例如,糖化白蛋白等),在测定糖化蛋白质比率(糖化蛋白质量相对于蛋白质量的比率)的情况下,在一个或多个实施方式中,能够根据本公开涉及的测定中得到的糖化蛋白质量与通过其他方法得到的蛋白质量,求出糖化蛋白质比率。糖化血红蛋白比率也可以通过该方法得到。
作为求出蛋白质量的方法,例如可以举出双缩脲反应法、利用福林酚(folinphenol)试剂的劳里法(lowry法)、利用考马斯(coomassie)g-250的bradford(布拉德福)(coomassie)法等,在白蛋白的情况下,可以举出bcg法、bcp法。
[实施方式a的现配方式]
实施方式a中的单试剂系统试剂在流通阶段中,从试剂的稳定性的观点等出发,可以不是一个试剂。可以在进行本公开涉及的测定方法的阶段中进行现配。用于调制这样的实施方式中的单试剂系统试剂的、作为不受限的双试剂的构成,可以举出下述构成a4至a9。但是,本公开涉及的试剂不局限于这样的实施方式。试剂还可以包括其他成分。
构成a4
试剂1:缓冲剂、变性剂、直接型fpox、pod
试剂2:缓冲剂、氧化显色剂
构成a5
试剂1:缓冲剂、直接型fpox、pod
试剂2:缓冲剂、变性剂、氧化显色剂
构成a6
试剂1:缓冲剂、pod
试剂2:缓冲剂、变性剂、直接型fpox、氧化显色剂
构成a7
试剂1:缓冲剂、变性剂、pod
试剂2:缓冲剂、直接型fpox、氧化显色剂
构成a8
试剂1:缓冲剂、直接型fpox、pod
试剂2:缓冲剂、氧化显色剂
构成a9
试剂1:缓冲剂、pod
试剂2:缓冲剂、直接型fpox、氧化显色剂
实施方式a的构成a4至a9还可以包括染料稳定剂,例如还原剂、表面活性剂等。另外,作为构成a4至a9中的缓冲剂、变性剂、氧化显色剂,能够使用上述的。另外,在构成a4至a9中,变性剂以及/或者染料稳定剂可以是式(i)的化合物。
本公开中的“现配方式”是指,针对一个或多个试样,在采用本公开涉及的测定方法的情况下,包括为了用于一个或多个试样而从多个试剂中调制单试剂系统试剂的方式。
[使用直接型fpdh的实施方式b]
在不受限的实施方式b中,本公开涉及的测定方法为糖化蛋白质的测定方法,该测定方法包括下述(1)至(3),包括为了进行下述(1)至(3)、或者为了进行下述(2)至(3)而使一个试剂(单试剂系统试剂)与试样混合。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与直接型fpdh的反应,使还原显色剂显色。
(3)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
在不受限的一个或多个实施方式中,作为实施方式b中的单试剂系统试剂,可以举出下述构成b1和b2。但是,本公开涉及的试剂不局限于这些实施方式。单试剂系统试剂还可以包括其他成分。
构成b1
单试剂系统试剂:缓冲剂、变性剂、直接型fpdh、还原显色剂
构成b2
单试剂系统试剂:缓冲剂、直接型fpdh、还原显色剂
实施方式b中的缓冲剂、变性剂和测定对象试样与实施方式a相同。
作为实施方式b中的还原显色剂,能够使用四唑盐等。
作为四唑盐,可以举出2,5-二苯基-3-(1-萘基)-2h-氯化四唑<简称为四唑紫>、3,3'-(3,3'-二甲氧基-4,4'-亚联苯基)-双[2-(对硝基苯基)-5-苯基四唑氯化物]<简称为硝基蓝四唑>、3,3'-(3,3'-二甲氧基-4,4'-亚联苯基)-双(2,5-二苯基四唑氯化物)<简称为蓝四唑>、3-(4,5-二甲基-2-噻唑基)-2,5-二苯基四唑溴化物<简称为mtt>、3-(对碘苯基)-2-(对硝基苯基)-5-苯基-四唑氯化物、2,2',5,5'-四-(对硝基苯基)-3,3'-(3-二甲氧基-4-二亚苯基)-二硝基氯化物<简称为硝基蓝四唑>、2,3,5-三苯基四唑氯化物、3,3'-(3,3'-二甲氧基-4,4'-亚联苯基)-双-[2,5-双(对硝基苯基)四唑氯化物]、3,3'-(4,4'-亚联苯基)-双(2,5-二苯基四氮唑氯化物)、2-(4-碘苯基)-3-(4-硝基苯基)-5-苯基-2h-四唑氯化物<简称为int>、3,3'-[3,3'-二甲氧基-(1,1'-联苯基)-4,4'-二基]-双[2-(4-硝基苯基)-5-苯基]-2h四唑氯化物<简称为硝基-tb>、2-苯并噻唑基-3-(4-羧基-2-甲氧基苯基)-5-[4-(2-磺乙基氨基甲酰基)苯基]-2h-四唑<简称为wst-4>、2,2'-二苯并噻唑基-5,5'-双[4-二(2-磺乙基)氨基甲酰基苯基]-3,3'-(3,3'-二甲氧基-4,4'-二亚苯基)二四氮唑二钠盐<简称为wst-5>等。
这些之中,wst-4和wst-5除了水溶性高且作为试剂容易调整之外,还在长波长区域具有吸收,并且难以受到血红蛋白等的蛋白质的吸收的影响的特征。
实施方式b的构成b1和b2还可以包括染料稳定剂。作为染料稳定剂,可以举出叠氮化钠(wo2003/029229)、ph调节剂(日本专利特开2009-072136)等。
实施方式b中的显色信号以及糖化蛋白质量的测定与实施方式a相同。
实施方式b的构成b1和b2中可以包括电子转移剂(electrontransferagent)。作为电子转移剂,可以举出黄递酶、n-甲基吩嗪·甲基硫酸酯类(例如,n-甲基吩嗪·甲基硫酸酯、1-甲氧基-5-甲基吩嗪·甲基硫酸酯(1-甲氧基pms)等)、麦尔多拉蓝、亚甲蓝等。
实施方式b中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式ba,可以举出一种糖化血红蛋白比率的测定方法,该测定方法包括下述(1)至(4),包括为了进行下述(1)至(4)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式ba
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与直接型fpdh的反应,使还原显色剂显色。
(3)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
(4)测定所变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式b中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式bb,举出一种糖化血红蛋白比率的测定方法,该测定方法包括下述(0)至(4),包括为了进行下述(2)至(4)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式bb
(0)使试样中的红细胞溶血并将血红蛋白从红细胞放出。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与直接型fpdh的反应,使还原显色剂显色。
(3)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
(4)测定所变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式ba和bb还可以包括根据糖化血红蛋白量和血红蛋白量来计算糖化血红蛋白比率。
另外,在本实施方式ba和bb中,在一个或多个实施方式中,糖化血红蛋白为血红蛋白a1c。
实施方式b中的测定对象是糖化血红蛋白以外的糖化蛋白质(例如,糖化白蛋白等),在测定糖化蛋白质比率(糖化蛋白质量相对于蛋白质量的比率)的情况下,在一个或多个实施方式中,能够根据本公开涉及的测定中得到的糖化蛋白质量、以及通过其他方法得到的蛋白质量,求出糖化蛋白质比率。糖化血红蛋白比率也可以通过该方法求出。作为求出蛋白质量的方法,例如可以举出上述的方法。
[实施方式b的现配方式]
关于实施方式b中的单试剂系统试剂,在流通阶段中,从试剂的稳定性的观点等出发,可以不是一个试剂。可以在进行本公开涉及的测定方法的阶段中进行现配。作为用于调制这样的实施方式中的单试剂系统试剂的、不受限的双试剂的构成,可以举出下述构成b3和b4。
构成b3
试剂1:缓冲剂、变性剂、直接型fpdh
试剂2:缓冲剂、还原显色剂
构成b4
试剂1:缓冲剂、直接型fpdh
试剂2:缓冲剂、还原显色剂
实施方式b的构成b3和b4还可以包括上述的染料稳定剂和/或电子转移剂。
另外,构成b3和b4中的缓冲剂、变性剂以及还原显色剂能够使用上述的。
[利用阿马道里酶和蛋白酶的实施方式]
本公开涉及的测定方法在其他一个实施方式中,作为阿马道里酶而使用相对于n末端糖化肽和糖化氨基酸(以下,简单称为“糖化肽”)具有基质特异性的阿马道里酶。作为该阿马道里酶,可以举出果糖基肽氧化酶(fpox)以及果糖基肽脱氢酶(fpdh)。
作为用于果糖胺、糖化白蛋白的测定的阿马道里酶,能够使用较好作用于赖氨酸的ε氨基被糖化的氨基酸和/或ε氨基被糖化的肽的、作用于糖化氨基酸和/或糖化肽的酶。作为例子,可以举出源自赤霉菌(gibberella)属、曲霉菌(aspergillus)属、念珠菌(candida)属、青霉菌(penicillium)属、镰刀霉(fusarium)属、枝顶孢霉(acremonium)属或者德巴利氏酵母(debaryomyces)属的氧化酶等。
[利用fpox的实施方式c]
在不受限的实施方式c中,本公开涉及的测定方法为糖化蛋白质的测定方法,该测定方法包括下述(1)至(5),包括为了进行下述(1)至(5)或为了进行下述(2)至(5)而使一个试剂(单试剂系统试剂)与试样混合。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与蛋白酶的反应,生成糖化肽。
(3)通过糖化肽与fpox的反应,生成过氧化氢。
(4)通过所生成的过氧化氢与过氧化物酶的反应,使氧化显色剂显色。
(5)测定所显色的氧化显色剂的显色信号并计算糖化蛋白质量。
在不受限的一个或多个实施方式中,作为实施方式c中的单试剂系统试剂,可以举出下述构成c1至c3。但是,本公开涉及的试剂不局限于这些实施方式。单试剂系统试剂还可以包括其他成分。
构成c1
单试剂系统试剂:缓冲剂、变性剂、蛋白酶、fpox、pod、氧化显色剂
构成c2
单试剂系统试剂:缓冲剂、蛋白酶、fpox、pod、氧化显色剂
构成c3
单试剂系统试剂:缓冲剂、蛋白酶、fpox、pod、隐色型染料、式(i)的化合物
实施方式c的构成c1至c3还可以包括上述染料稳定剂。
构成c1至c3中的缓冲剂、变性剂、pod、氧化显色剂、隐色型染料、式(i)的化合物、以及测定对象试样与实施方式a相同。
作为实施方式c中的蛋白酶,能够使用在中性附近具有活性、且与糖化血红蛋白反应而能够生成n末端糖化肽(在本公开中,包括糖化氨基酸)的酶。产生生物种、酶家族未受特别限制。作为蛋白酶的不受限的例子,可以举出丝氨酸蛋白酶、苏氨酸蛋白酶、谷氨酸蛋白酶、天冬氨酸蛋白酶、金属蛋白酶等。
作为实施方式c中的蛋白酶,可以举出源自芽孢杆菌属、曲霉菌属、链霉菌属等微生物的蛋白酶。除此之外,优选丝氨酸蛋白酶。
另外,在测定对象为糖化白蛋白的情况下,由于芽孢杆菌属和链霉菌属的源自微生物的蛋白酶针对人白蛋白的作用较大,因此更优选,特别优选源自芽孢杆菌属的蛋白酶、例如枯草杆菌(subtilisin)、枯草菌蛋白酶、蛋白酶-类型-viii、-ix、-x、-xv、-xxiv、-xxvii、-xxxi(以上西格玛社制)、嗜热菌蛋白酶(thermolysin)、中性蛋白酶、esperase(注册商标)、savinase(注册商标)、durazym(注册商标)、biofeedpr(注册商标)、alcalase(注册商标)(以上是诺和诺德社制)等,进一步特别优选枯草杆菌、枯草菌蛋白酶、蛋白酶-类型-xxvii等。
实施方式c中的显色信号以及糖化蛋白质量的测定与实施方式a相同。
实施方式c中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式ca,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(1)至(6),包括为了进行下述(1)至(6)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式ca
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与蛋白酶的反应来生成糖化肽。
(3)通过糖化肽与fpox的反应来生成过氧化氢。
(4)通过所生成的过氧化氢与过氧化物酶的反应,使氧化显色剂显色。
(5)测定所显色的氧化显色剂的显色信号并计算糖化蛋白质量。
(6)测定变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式c中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式cb,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(0)至(6),包括为了进行下述(2)至(6)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式cb
(0)使试样中的红细胞溶血并将血红蛋白从红细胞放出。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与蛋白酶的反应来生成糖化肽。
(3)通过糖化肽与fpox的反应来生成过氧化氢。
(4)通过所生成的过氧化氢与过氧化物酶的反应,使氧化显色剂显色。
(5)测定所显色的氧化显色剂的显色信号并计算糖化蛋白质量。
(6)测定变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式ca以及cb还可以包括根据糖化血红蛋白量和血红蛋白量来计算糖化血红蛋白比率。
另外,在实施方式ca以及cb中,在一个或多个实施方式中,糖化血红蛋白为血红蛋白a1c。
实施方式c中的测定对象是糖化血红蛋白以外的糖化蛋白质(例如,糖化白蛋白等),在测定糖化蛋白质比率(糖化蛋白质量相对于蛋白质量的比率)的情况下,在一个或多个实施方式中,能够根据本公开涉及的测定中得到的糖化蛋白质量以及通过其他方法得到的蛋白质量来求出糖化蛋白质比率。糖化血红蛋白比率也可以通过该方法求出。作为求出蛋白质量的方法,例如可以举出上述的方法。
[实施方式c的现配方式]
实施方式c中的单试剂系统试剂在流通阶段中从试剂的稳定性的观点等出发,可以不是一个试剂。在进行本公开涉及的测定方法的阶段中可以进行现配。作为用于调制这样的实施方式中的单试剂系统试剂的、不受限的双试剂的构成,可以举出下述构成c4至c11。
构成c4
第一试剂:缓冲剂、变性剂、fpox、pod
第二试剂:缓冲剂、蛋白酶、氧化显色剂
构成c5
第一试剂:缓冲剂、变性剂、蛋白酶、pod
第二试剂:缓冲剂、fpox、氧化显色剂
构成c6
第一试剂:缓冲剂、变性剂、fpox、氧化显色剂
第二试剂:缓冲剂、蛋白酶、pod
构成c7
第一试剂:缓冲剂、变性剂、蛋白酶、氧化显色剂
第二试剂:缓冲剂、fpox、pod
构成c8
第一试剂:缓冲剂、fpox、pod
第二试剂:缓冲剂、蛋白酶、氧化显色剂
构成c9
第一试剂:缓冲剂、蛋白酶、pod
第二试剂:缓冲剂、fpox、氧化显色剂
构成c10
第一试剂:缓冲剂、fpox、氧化显色剂
第二试剂:缓冲剂、蛋白酶、pod
构成c11
第一试剂:缓冲剂、蛋白酶、氧化显色剂
第二试剂:缓冲剂、fpox、pod
实施方式c的构成c4至c11还可以包括染料稳定剂,例如还原剂、表面活性剂等。另外,构成c4至c11中的缓冲剂、变性剂、氧化显色剂以及测定对象试样与实施方式a相同。另外,在构成c4至c11中,变性剂以及/或者染料稳定剂也可以是式(i)的化合物。
[利用fpdh的实施方式d]
在不受限的实施方式d中,本公开涉及的测定方法为糖化蛋白质的测定方法,该测定方法包括下述(1)至(4),包括为了进行下述(1)至(4)或者为了进行下述(2)至(4)而使一个试剂(单试剂系统试剂)与试样混合。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与蛋白酶的反应来生成糖化肽。
(3)通过糖化肽与fpdh的反应,使还原显色剂显色。
(4)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
在不受限的一个或多个实施方式中,作为实施方式d中的单试剂系统试剂,可以举出下述构成d1以及d2。但是,本公开涉及的试剂不局限于这些实施方式。单试剂系统试剂还可以包括其他成分。
构成d1
单试剂系统试剂:缓冲剂、变性剂、蛋白酶、fpdh、还原显色剂
构成d2
单试剂系统试剂:缓冲剂、fpdh、还原显色剂
实施方式d的构成d1以及d2还可以包括上述的染料稳定剂以及/或者电子转移剂。
构成d1以及d2中的缓冲剂、变性剂、还原显色剂以及测定对象试样与实施方式b相同,蛋白酶与实施方式c相同。
实施方式d中的显色信号以及糖化蛋白质量的测定与实施方式a相同。
实施方式d中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式da,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(1)至(5),包括为了进行下述(1)至(5)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式da
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与蛋白酶的反应来生成糖化肽。
(3)通过糖化肽与fpdh的反应,使还原显色剂显色。
(4)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
(5)测定变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式d中的测定对象是糖化血红蛋白,作为测定糖化血红蛋白比率(糖化血红蛋白量相对于血红蛋白量的比率)的实施方式db,可以举出糖化血红蛋白比率的测定方法,该测定方法包括下述(0至(5),包括为了进行下述(2)至(5)而使一个试剂(单试剂系统试剂)与试样混合。
实施方式db
(0)使试样中的红细胞溶血并将血红蛋白从红细胞放出。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与蛋白酶的反应来生成糖化肽。
(3)通过糖化肽与fpdh的反应,使还原显色剂显色。
(4)测定所显色的还原显色剂的显色信号并计算糖化蛋白质量。
(5)测定变性的血红蛋白的显色信号并计算血红蛋白量。
实施方式da以及db还可以包括根据糖化血红蛋白量以及血红蛋白量来计算糖化血红蛋白比率。
另外,在实施方式da以及db中,在一个或多个实施方式中,糖化血红蛋白为血红蛋白a1c。
实施方式d中的测定对象是糖化血红蛋白以外的糖化蛋白质(例如糖化白蛋白等),在测定糖化蛋白质比率(糖化蛋白质量相对于蛋白质量的比率)的情况下,在一个或多个实施方式中,能够根据本公开涉及的测定中得到的糖化蛋白质量以及通过其他方法得到的蛋白质量来求出糖化蛋白质比率。糖化血红蛋白比率也可以通过该方法求出。作为求出蛋白质量的方法,例如可以举出上述的方法。
[实施方式d的现配方式]
实施方式d中的单试剂系统试剂在流通阶段中从试剂的稳定性的观点等出发,可以不是一个试剂。在进行本公开涉及的测定方法的阶段中,可以进行现配。作为用于调制这样的实施方式中的单试剂系统试剂的、不受限的双试剂的构成,可以举出下述构成d3至d10。
构成d3
第一试剂:缓冲剂、变性剂、fpdh
第二试剂:缓冲剂、蛋白酶、还原显色剂
构成d4
第一试剂:缓冲剂、变性剂、蛋白酶
第二试剂:缓冲剂、fpdh、还原显色剂
构成d5
第一试剂:缓冲剂、变性剂、fpdh、还原显色剂
第二试剂:缓冲剂、蛋白酶
构成d6
第一试剂:缓冲剂、变性剂、蛋白酶、还原显色剂
第二试剂:缓冲剂、fpdh
构成d7
第一试剂:缓冲剂、fpdh
第二试剂:缓冲剂、蛋白酶、还原显色剂
构成d8
第一试剂:缓冲剂、蛋白酶
第二试剂:缓冲剂、fpdh、还原显色剂
构成d9
第一试剂:缓冲剂、fpdh、还原显色剂
第二试剂:缓冲剂、蛋白酶
构成d10
第一试剂:缓冲剂、蛋白酶、还原显色剂
第二试剂:缓冲剂、fpdh
实施方式d的构成d3至d10还可以包括上述的染料稳定剂以及/或者电子转移剂。
构成d3からd10中的缓冲剂、变性剂、还原显色剂以及测定对象试样与实施方式b相同,蛋白酶与实施方式c相同。
[测定装置/测定系统]
本公开在其他方式中,涉及执行本公开涉及的测定方法的、糖化蛋白质的测定装置或者测定系统。
在一个或多个实施方式中(图1),本公开涉及的测定装置或者系统包括向反应容器(测光小室)供应试样的采样部1、向反应容器(测光小室)供应单试剂系统试剂的试剂供应部2、测定测光小室的吸光度等的显色信号的测光部3、控制采样部1与试剂供应部2与测光部3的控制部4、记录测光数据等的记录部5、计算糖化蛋白质量等的运算部6、以及数据输出部7。这些各部可以包含于一个装置,也可以包含于不同的装置而构成系统。
作为测定糖化蛋白质量的方法,除了本公开涉及的测定方法之外,还存在hplc(高效液相色谱,highperformanceliquidchromatography)法。hplc法近年来已高速化,若(仅仅)一个待测体则约1分钟能够测定,对于多个待测体,每10个待测体能够以约5.5分钟的速度(一个待测体约30秒)进行测定。
另一方面,酶法在现有的双试剂系统的情况下,针对一个待测体需要8-10分钟的测定时间。但是,由于反应时间能够并行进行、且能够以采样间隔进行测光(测定),因此待测体数量越多越能够使一个待测体的测定时间更接近采样间隔的时间,能够进行比hplc更高速的处理。
只要是本公开涉及的测定方法,在一个或多个实施方式中,从试样与单试剂系统试剂的混合后10秒-180秒就能够进行测定,并且能够与双试剂系统相比进一步高速化。
因此,在一个或多个实施方式中,本公开涉及的装置能够适用于一次处理多个待测体的大型的自动分析装置。
或者,本公开涉及的测定方法在一个或多个实施方式中,比现有的酶法比,能够通过使用单试剂系统试剂来缩短需要的时间,因此能够适用于测定对象试样少的小型的自动分析装置。
针对本公开涉及的装置或者系统的不受限的一个或多个实施方式进行说明。
通过在采样部1中直接设置采血中所用的采血管、或者将血液等移动到试样杯或在采血管中设置采样工具,待测体被供应到采样部1。在直接设置采血管的情况下,也能够使用能贯通盖子的穿孔喷嘴。
在采样部1中,试样从所供应的待测体向反应容器(测光小室)移动。作为采样量,例如可以举出0.1-10μl。在直接移动到测光小室的情况下,从稀释率的观点出发,优选0.1-2μl。另一方面,可以从待测体经由稀释槽将试样移动到测光小室,在该情况下的采样量例如为0.5-10μl。
待测体中的红细胞的溶血在使用稀释槽的情况下,在稀释槽中,能够通过将待测体与包含精制水和/或表面活性剂的溶液等(以下,这些也被称为“溶血溶液”)混合来溶血。溶血后,作为测定对象的试样而移动到测光小室。因此,本公开涉及的装置或者系统也可以具备供应溶血溶液的溶血溶液供应部。
另一方面,也可以将待测体直接向测光小室移动。在该情况下,可以向测光小室供应溶血溶液而溶血,可以通过供应单试剂系统试剂来溶血。
在任意情况下,也能够在溶血中使用基于搅拌器的物理搅拌、基于超声波的搅拌。
从试剂供应部2向测光小室供应单试剂系统试剂。在试剂供应部2中,可以设置作为一种液体而供应的单试剂系统试剂的溶液,也可以设置以必要的待测体分量混合作为两种液体(作为现配方式)供应的试剂而制作的单试剂系统试剂。例如,可以制作一日量、数日量,例如可以制作数个待测体量至数千个待测体量。
在本申请说明书中,可以现配单试剂系统试剂。在一个或多个实施方式中,可以在与试样的混合前5分钟以内调制单试剂系统试剂。在一个或多个实施方式中,该调制是指,所有的与试剂成分接触时所需的最终工序。在不受特别限制的一个或多个实施方式中,可以将含有酶的第一试剂与含有显色剂的第二试剂组合而形成单试剂系统试剂。朝向测光小室的试样和单试剂系统试剂的供应可以是任意顺序进行,也可以是同时进行。在全血试样的情况下,试样与试剂的混合比率例如为1:30~2000的比率、优选为1:100~1000、更优选为1:150~500。在血球试样的情况下,试样与试剂的混合比率例如为1:50~4000的比率、优选为1:100~2000、更优选为1:250~1000。
在试样与单试剂系统试剂的混合后、到测定为止的时间例如能够设定为10秒至180秒之间。混合后到测定为止的时间例如为30秒以上、45秒以上或者60秒以上。另外,混合后到测定为止的时间例如为30秒以下、45秒以下、60秒以下、90秒以下、120秒以下或者180秒以下。
测定能够通过在测光部3中测定测光小室的吸光度等的显色信号来进行。
糖化蛋白质的测定在添加测定试剂之后迅速进行第一次测定,在测定结束时刻进行第二次测定,将第二次与第一次的测光之差设为测定值。
在有hb的吸收的波长下测定血红蛋白,但优选不受糖化血红蛋白的显色反应影响的波长,例如在显色剂为da-67的情况下,例如在550nm以下、优选在500nm以下、更优选在450~480nm附近进行测定。
测定小室或者溶血小室可以是进行清洗来多次使用的方式,但也可以是使用一次而丢弃的方式。
控制部4进行控制以使得例如采样部1、试剂供应部2、测光部3、以及可选的溶血溶液供应部如上述的方式操作。
测光部中测定的数据由记录部5记录。另外,基于该数据,通过运算部6来计算糖化蛋白质量、蛋白质量、和/或糖化蛋白质比率,并记录到记录部5。所记录的数据从数据输出部输出。
运算部6将测光部中得到的测定值(例如,吸光度变化量)基于相对于测定值的校准曲线换算为糖化蛋白质量而计算出糖化蛋白质量。
本公开可以涉及以下的不受限的一个或多个实施方式。
〔1〕一种试样中的糖化蛋白质的测定方法,其中,该测定方法包括下述(1)至(3),并且为了进行下述(2)至(3)而与试样混合的试剂为一个。
(1)使试样中的蛋白质变性。
(2)通过试样中的糖化蛋白质与阿马道里酶的反应,使显色剂显色。
(3)测定(1)以及(2)之后的试样的吸光度并计算糖化蛋白质量。
〔2〕根据〔1〕所述的测定方法,其中,所述糖化蛋白质是糖化血红蛋白或者糖化白蛋白,所述蛋白质是血红蛋白或者白蛋白。
〔3〕一种试样中的糖化血红蛋白的测定方法,其中,该测定方法包括下述(1)至(4),并且为了进行下述(1)至(4)而与试样混合的试剂为一个。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与阿马道里酶的反应,使显色剂显色。
(3)测定(1)以及(2)之后的试样的吸光度并计算糖化血红蛋白量。
(4)测定(1)以及(2)之后的试样的吸光度并计算血红蛋白量。
〔4〕一种包括下述(0)至(4)的、试样中的糖化血红蛋白的测定方法,为了进行下述(2)至(4)而与试样混合的试剂为一个。
(0)使试样中的红细胞溶血并将血红蛋白从红细胞放出。
(1)使试样中的血红蛋白变性。
(2)通过试样中的糖化血红蛋白与阿马道里酶的反应,使显色剂显色。
(3)测定(1)以及(2)之后的试样的吸光度并计算糖化血红蛋白量。
(4)测定(1)以及(2)之后的试样的吸光度并计算血红蛋白量。
〔5〕根据〔2〕至〔4〕中任一项所述的测定方法,其中,糖化血红蛋白是血红蛋白a1c。
〔6〕根据〔1〕至〔5〕中任一项所述的测定方法,其中,所述阿马道里酶是糖化蛋白直接型阿马道里酶。
〔7〕根据〔1〕至〔6〕中任一项所述的测定方法,其中,所添加的试剂含有变性剂、糖化蛋白直接型果糖基肽氧化酶、过氧化物酶以及氧化显色剂。
〔8〕根据〔1〕至〔6〕中任一项所述的测定方法,其中,所添加的试剂含有变性剂、糖化蛋白直接型果糖基肽脱氢酶以及还原显色剂。
〔9〕根据〔2〕至〔8〕中任一项所述的测定方法,其中,所述(2)是通过试样中的糖化血红蛋白与蛋白酶的反应来生成n末端糖化肽、以及通过n末端糖化肽与阿马道里酶的反应而使显色剂显色。
〔10〕根据〔1〕至〔5〕以及〔9〕中任一项所述的测定方法,其中,所添加的试剂含有变性剂、蛋白酶、果糖基肽氧化酶、过氧化物酶以及显色剂。
〔11〕根据〔1〕至〔5〕以及〔9〕中任一项所述的测定方法,其中,所添加的试剂含有变性剂、蛋白酶、果糖基肽脱氢酶以及显色剂。
〔12〕一种糖化血红蛋白的测定装置或者测定系统,其执行〔1〕至〔11〕中任一项所述的测定方法。
以下,通过实施例进一步详细说明本公开,但这些仅仅是示例而已,本公开并不局限于这些实施例。
实施例
[实施例1]
单试剂系统试剂
糖化蛋白直接型果糖基肽氧化酶3000u/l
肉豆蔻基二甲基氨基丙磺酸(东京化成工业)3g/l
pod10ku/l
da-67(和光纯药工业)0.1mmol/l
mops(同仁化学研究所)50mmol/l
naohph6.5
测定装置
bm-6010(日本电子制)
操作
使人全血2μl与单试剂系统试剂148μl混合,并在37℃下培养2分钟。
吸光度测定
糖化血红蛋白测定:在主波长654nm、次波长694nm下测定从单试剂系统试剂的混合至约20秒后与约2分钟后的吸光度,并通过从约2分钟后的吸光度中减去约20秒后的吸光度来求出吸光度变化量。
血红蛋白测定:在主波长478nm、次波长694nm下测定从单试剂系统试剂的混合至约2分钟后的吸光度。
糖化血红蛋白量的计算
基于相对于吸光度变化量的校准曲线换算为糖化血红蛋白而计算出糖化血红蛋白量。
[实施例2]
单试剂系统试剂的现配用第一试剂(酶试剂)
糖化蛋白直接型果糖基肽氧化酶400u/l
pod20ku/l
mops(同仁化学研究所)50mmol/l
naohph6.5
单试剂系统试剂的现配用第二试剂(显色剂试剂)
肉豆蔻基二甲基氨基丙磺酸(东京化成工业)30g/l
da-67(和光纯药工业)1.0mmol/l
mops(同仁化学研究所)50mmol/l
naohph6.5
测定装置
bm-6010(日本电子制)
操作
使第一试剂9ml与第二试剂1ml混合,并制作单试剂系统试剂。
使人全血2μl与单试剂系统试剂148μl混合,并在37℃下培养2分钟。
吸光度测定
糖化血红蛋白测定:在主波长654nm、次波长694nm下测定从单试剂系统试剂的混合至约20秒后与约2分钟后的吸光度,并通过从2分钟后的吸光度中减去约20秒后的吸光度来求出吸光度变化量。
血红蛋白测定:在主波长478nm、次波长694nm下测定从单试剂系统试剂的混合至约2分钟后的吸光度。
糖化血红蛋白量的计算
基于相对于吸光度变化量的校准曲线换算为糖化血红蛋白而计算出糖化血红蛋白量。
[实施例3]
单试剂系统试剂的现配用第一试剂(酶试剂)
果糖基肽脱氢酶500u/l
1-甲氧基pms(同仁化学研究所)1mmol/l
mops(同仁化学研究所)50mmol/l
naohph6.5
单试剂系统试剂的现配用第二试剂(显色剂试剂)
金属蛋白酶20000ku/l
肉豆蔻基二甲基氨基丙磺酸(东京化成工业)30g/l
wst-4(同仁化学研究所)1mmol/l
mops(同仁化学研究所)50mmol/l
naohph6.5
测定装置
bm-6010(日本电子制)
操作
使第一试剂9ml与第二试剂1ml混合,并制作单试剂系统试剂。
使人全血2μl与单试剂系统试剂148μl混合,并在37℃下培养2分钟。
吸光度测定
糖化血红蛋白测定:在主波长694nm、次波长805nm下测定从单试剂系统试剂的混合至约20秒后与约2分钟后的吸光度,并通过从约2分钟后的吸光度中减去约20秒后的吸光度来求出吸光度变化量。
血红蛋白测定:在主波长478nm、次波长694nm下测定从单试剂系统试剂的混合至约2分钟后的吸光度。
糖化血红蛋白量的计算
基于相对于吸光度变化量的校准曲线换算为糖化血红蛋白而计算出糖化血红蛋白量。
[实施例4]
单试剂系统试剂的现配用第一试剂(酶试剂)
果糖基肽氧化酶500u/l
pod20ku/l
mops(同仁化学研究所)50mmol/l
naohph6.5
单试剂系统试剂的现配用第二试剂(显色剂试剂)
金属蛋白酶30000ku/l
肉豆蔻基二甲基氨基丙磺酸(东京化成工业)30g/l
da-67(和光纯药工业)1.0mmol/l
mops(同仁化学研究所)50mmol/l
naohph6.5
测定装置
bm-6010(日本电子制)
操作
使第一试剂9ml与第二试剂1ml混合,并制作单试剂系统试剂。
使人全血2μl与单试剂系统试剂148μl混合,并在37℃下培养2分钟。
吸光度测定
糖化血红蛋白测定:在主波长658nm、次波长694nm下测定从单试剂系统试剂的混合至约20秒后、约1分钟后、约2分钟后、约5分钟后的吸光度,并通过从约1分钟后、约2分钟后、约5分钟后的吸光度中减去约20秒后的吸光度来求出各自的吸光度变化量。
血红蛋白测定:在主波长478nm、次波长694nm下测定从单试剂系统试剂的混合至约2分钟后的吸光度。
糖化血红蛋白量的计算
基于相对于吸光度变化量的校准曲线换算为糖化血红蛋白而计算出糖化血红蛋白量。
结果
在约1分钟后、约2分钟后以及约5分钟后的任何一者中,也能够得到相同的测定结果。
- 还没有人留言评论。精彩留言会获得点赞!