一种用于骨肉瘤诊断的外泌体蛋白及其即时检测方法与流程
本发明涉及生物标志物领域,具体涉及一种用于骨肉瘤诊断的外泌体蛋白及其即时检测方法。
背景技术:
骨肉瘤是肿瘤细胞能直接形成肿瘤性类骨组织或骨组织的恶性肿瘤,约占全部原发恶性骨肿瘤的20—34%,是最常见的恶性原发骨肿瘤。骨肉瘤为高度恶性肿瘤,发病率在男性略高,可发生于各级年龄,但最多见于11~20岁,其次为21~30岁,年龄越大,发病率越低。骨肉瘤多发生在骨骼生长发育的旺盛时期,其恶性程度又较高,因此是严重影响劳动生产力并危及生命的重要肿瘤之一,早期诊断及早期治疗具有特别重要意义。在临床诊断中,需与慢性化脓性骨髓炎、尤文氏肉瘤、转移性骨肿瘤、骨关节结核等鉴别,目前尚缺乏能准确区分慢性化脓性骨髓炎、尤文氏肉瘤、转移性骨肿瘤与骨肉瘤的生物标记物。
肿瘤微环境对肿瘤细胞的发生发展起到了关键作用,外泌体(exosomes)作为肿瘤微环境中的重要成分,可以改变肿瘤微环境,通过传递蛋白质、rna、mirna等介导细胞间物质交换和信息交流,参与肿瘤细胞生长、细胞迁移、血管新生、肿瘤耐药等过程。外泌体是大小在30-150nm大小的细胞外囊泡,天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中,已知肿瘤细胞分泌的外泌体的量可以作为肿瘤早期诊断,监测和预后的重要指标。其和ctdna,循环肿瘤细胞成为目前液体活检的研究对象。生物化学和蛋白质组学分析显示,外泌体具有特定的脂质(如胆固醇、鞘脂类、神经酰胺、甘油磷脂等)和蛋白成分,还含有mrna和mirna等核酸成分,外泌体所含有的特定成分有可能作为肿瘤的特异性标志物。本申请通过对骨肉瘤患者的外泌体进行蛋白组学的分析和比较,获得在骨肉瘤患者外泌体中特异性的标志物。
技术实现要素:
为了解决上述技术问题,本发明提供了如下方案:
提供一种检测血清外泌体来源的c19orf43蛋白的表达水平的试剂在制备诊断骨肉瘤的试剂盒中的用途。
优选地,所述诊断骨肉瘤包括区分骨肉瘤与慢性化脓性骨髓炎、尤文氏肉瘤、转移性骨肿瘤、骨关节结核。
优选地,其中外泌体来源的c19orf43蛋白的表达水平通过即时检测平台检测。
优选地,所述即时检测平台包括:
样品粘贴区:用于滴加体液;
滤血膜粘贴区:所述滤血膜粘贴区与所述样品粘贴区连接,所述滤血膜粘贴区上设有滤血膜,所述滤血膜与所述滤血膜粘贴区固定连接,所述滤血膜对血液进行分离纯化;
微孔滤膜粘贴区:所述微孔滤膜粘贴区上设有微孔滤膜,所述微孔滤膜与所述滤血膜粘贴区连接,用于进一步分离体液;
芯片粘贴区:所述芯片粘贴区上设有芯片,所述芯片与所述芯片粘贴区连接,所述芯片用于进一步分离纯化并得到尺寸小于150nm的外泌体,所述芯片粘贴区与所述微孔滤膜粘贴区连接;
喷金垫粘贴区:所述喷金垫粘贴区上设有被颗粒标记的抗体,所述被颗粒标记的抗体与所述体液中外泌体的c19orf43蛋白结合,所述喷金垫粘贴区与所述芯片粘贴区连接;
硝酸纤维素膜粘贴区:用做多组t线和c线的承载体,多组t线用于检测外泌体的含量,所述c线作为控制线,所述硝酸纤维素膜粘贴区与所述喷金垫粘贴区连接;t线的划线抗体为与目的抗原c19orf43结合的另外一种抗体,c线的划线抗体为被标记的羊兔抗体;当t线为三组或三组以上时,所述t线中的多组呈相互水平对称设置;
吸水垫粘贴区:吸水垫粘贴区上设有吸水垫,所述吸水垫粘贴区与所述吸水垫固定连接,所述吸水垫粘贴区与所述硝酸纤维素膜粘贴区连接。
优选地,所述微孔滤膜的孔径为大于1um并且小于110um。
优选地,所述芯片为微流控芯片或纸芯片中的任一种。
优选地,所述芯片的孔径为150-200nm。
优选地,所述被颗粒标记的抗体中的颗粒为胶金体或荧光材料中的任一种。
优选地,利用即时检测平台检测的具体步骤如下:
1)将血液分别通过滤血膜和微孔滤膜进行分离;
2)将第一步分离后的液体通过芯片进一步分离纯化,得到尺寸小于150nm的外泌体;
3)被颗粒标记的抗体与尺寸小于150nm的外泌体中的抗原结合;
4)硝酸纤维素膜粘贴区上的多组t线中的一组显色,证明外泌体通过了t线,根据显色的t线组数及显色程度判断该外泌体目的蛋白的含量。
本发明具有以下积极效果:
1、我们对骨肉瘤患者的血清外泌体进行分析,获得能够用于诊断骨肉瘤的血清外泌体标志物c19orf43蛋白,该标志物可用于准确鉴别骨肉瘤,尤其是区分骨肉瘤与慢性化脓性骨髓炎、尤文氏肉瘤、转移性骨肿瘤、骨关节结核,对于辅助临床诊断具有很大的价值。
2、我们采用了外泌体蛋白即时检测平台来检测c19orf43蛋白,集外泌体分离纯化和外泌体蛋白定量检测于一体,其使用操作简单,检测方便,低成本。极大地简化了整个标志物检测的过程。
附图说明
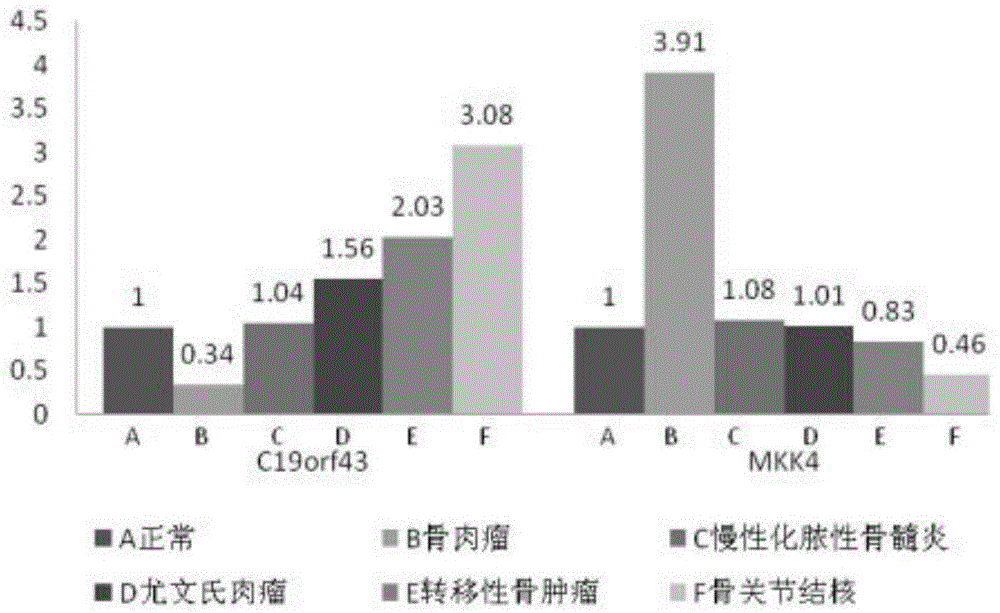
图1为外泌体蛋白标志物在各类样本中的表达情况。
图2为基于外泌体的体外即时检测平台的主视图;
其中:1.样品粘贴区,2.滤血膜粘贴区,3.微孔滤膜粘贴区,4.芯片粘贴区,5.喷金垫粘贴区,6.硝酸纤维素膜粘贴区,7.吸水垫粘贴区,8.t线,81.第一t线,82.第二t线,83.第三t线,9.c线,10.被颗粒标记的抗体,11.t线的划线抗体,12.c线的划线抗体。
具体实施方式
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1骨肉瘤外泌体蛋白标志物的筛选
1、血清外泌体样本的选择、分离与鉴定
为了研究骨肉瘤与慢性化脓性骨髓炎、尤文氏肉瘤、转移性骨肿瘤、骨关节结核之间的区别,我们选择了32例骨肉瘤,30例慢性化脓性骨髓炎,29例尤文氏肉瘤、30例转移性骨肉瘤、28例骨关节结核与32例正常人的血清样本,从中分离出细胞外囊泡(ev)作为研究对象。
通过使用纳米粒子跟踪分析(nta)、圆形形态(透射电子显微镜)、大小和标记物(免疫印迹检测cd9、cd63和cd81)表明,所分离的细胞外囊泡是外泌体。
2、蛋白质组学筛选骨肉瘤标志物
通过蛋白质组学分析鉴定病理样本外泌体中的差异表达蛋白,在健康人外泌体鉴定到501个蛋白,骨肉瘤外泌体鉴定到490个蛋白,慢性化脓性骨髓炎外泌体鉴定到417个蛋白,尤文氏肉瘤鉴定到524个蛋白,转移性骨肉瘤外泌体鉴定到378个蛋白,骨关节结核外泌体鉴定到489个蛋白,然后对这些蛋白进行统计分析,并且进行两两比较。
具体的实验步骤如下:
(1)蛋白样品的制备
将5倍体积预冷的丙酮加入己裂解的蛋白质样品中,-20℃沉淀过夜后离心取蛋白沉淀,室温放置10min晾干,并溶解。对蛋白进行定量,操作按说明书进行。sds—page对样品质量进行检测。根据蛋白浓度进行调整,保证取相同的质量和体积的蛋白样品进行后续实验。对蛋白样品进行烷基化和酶解反应。
(2)质谱分析
真空抽干酶解后的蛋白样品复溶于流动相a(98%水,2%乙腈,ph值为10.0),样品在高ph值条件下以0.6ml/min的流速用xbridgepeptidebehcl8(4.6mmx250mm)进行第一维多肽分离。从第5min开始收集馏分,每2min收集一管,首尾收集的馏分适当合并后得到22个馏分。将第一维分离后的馏分进行脱盐处理后真空抽干,复溶于流动相a进行lc.ms/ms分析。质谱采用esi正离子模式,质谱扫描分辨率为60000;二级质谱扫描分辨率为1500,用cid碰撞模式完成。电喷雾电压采用1.5kv。
(3)质谱数据处理
获取质谱的原始数据,采用高置信度的肽段(大于95%),用proteomediscovery软件的sequest搜索器进行搜索和匹配,数据库为uniprot库中物种为human的数据库。
通过分析发现骨肉瘤外泌体中c19orf43的表达量相对于正常样本显著下调(p<0.001),而其它类型样本相对于正常样本无显著性改变或者显著上调,mkk4蛋白的表达量相对于正常样本显著上调(p<0.001),而其它类型样本相对于正常样本无显著性改变或者显著下调,具体参见图1。图1显示了各类样本血清外泌体c19orf43蛋白的表达水平,将正常样本的值设定为1,其他样本的数值相对正常样本标准化。
3、elisa验证蛋白表达水平
采用elisa实验验证筛选出的骨肉瘤外泌体标志物,具体步骤如下:
在每个检测孔中加入100μl经超声破碎的外泌体重悬液,配制标准品,加入阴性对照进行检测。室温孵育2h后进行洗板,重新加入100μl检测抗体,孵育2h并洗板。加入辣根过氧化物酶标记的链霉亲和素20min后洗板,最后加入底物孵育20min并加入终止液,在450nm波长处进行测定,根据标准品的吸光度(a)计算标本浓度。
elisa实验表明与其他样本相比,骨肉瘤患者血清外泌体中的c19orf43显著性低表达,与质谱数据一致。但是对于mkk4蛋白,其在骨肉瘤血清外泌体中的表达水平的elisa结果与质谱数据不完全一致,其中转移性骨肉瘤外泌体中的mkk4蛋白的表达比骨肉瘤外泌体中的要高,其余样本类型的外泌体mkk4蛋白表达水平低于骨肉瘤。因此,选中c19orf43进一步在扩大的样本中进行验证。
实施例2扩大样本验证c19orf43对骨肉瘤的诊断价值
另外选择30例样本(包括5例骨肉瘤、5例慢性化脓性骨髓炎,5例尤文氏肉瘤、5例转移性骨肉瘤、5例骨关节结核、5例正常样本),采用我们之前研究的外泌体即时检测平台对实施例1所筛选到的c19orf43蛋白在血清外泌体中的表达水平进行检测。该体外即时检测平台集外泌体分离纯化和肿瘤特异性外泌体半定量检测为一体,其使用操作简单,检测方便,低成本。另外同时采用elisa检测方法对上述样本外泌体的c19orf43蛋白水平进行检测。
1、即时检测
(1)外泌体的体外即时检测平台如图2所示,包括:
样品粘贴区1:用于滴加体液;
滤血膜粘贴区2:所述滤血膜粘贴区2与所述样品粘贴区1连接,所述滤血膜粘贴区2上设有滤血膜,所述滤血膜与所述滤血膜粘贴区2固定连接,所述滤血膜2对血液进行分离纯化。
微孔滤膜粘贴区:所述微孔滤膜粘贴区上设有微孔滤膜,所述空滤膜与所述滤血膜粘贴区连接,用于进一步分离体液,所述微孔滤膜粘贴区与所述样品粘贴区连接;
芯片粘贴区:所述芯片粘贴区上设有芯片,所述芯片与所述芯片粘贴区连接,所述芯片用于进一步分离纯化并得到尺寸小于150nm的外泌体,所述芯片粘贴区与所述微孔滤膜粘贴区连接;
喷金垫粘贴区:所述喷金垫粘贴区上设有被颗粒标记的抗体,所述被颗粒标记的抗体与所述体液中外泌体的目的抗原结合,所述喷金垫粘贴区与所述芯片粘贴区连接;
硝酸纤维素膜粘贴区:用做多组t线和c线的承载体,多组t线用于检测外泌体的含量,所述c线作为控制线,所述硝酸纤维素膜粘贴区与所述喷金垫粘贴区连接;t线的划线抗体为与目的抗原结合的另外一种抗体,c线的划线抗体为被标记的羊兔抗体。当t线为三组或三组以上时,所述t线中的多组呈相互水平对称设置,以三组为例,三组呈相互水平对称设置的t线为第一t线、第二t线和第三t线;
吸水垫粘贴区:吸水垫粘贴区上设有吸水垫,所述吸水垫粘贴区与所述吸水垫固定连接,所述吸水垫粘贴区与所述硝酸纤维素膜粘贴区连接。
所述微孔滤膜的孔径为大于1um并且小于110um。
所述芯片为微流控芯片或纸芯片中的任一种。
所述芯片的孔径为150-200nm。
所述被颗粒标记的抗体中的颗粒为胶金体或荧光材料中的任一种。
所述样品粘贴区1、所述滤血膜粘贴区2、所述微孔滤膜粘贴区3、所述芯片粘贴区4、所述喷金垫粘贴区5、所述硝酸纤维素膜粘贴区6和所述吸水垫粘贴区7均呈阶梯状,其结构简单,便于对外泌体c19orf43的水平进行定量检测。
(2)即时检测步骤:
1)将血液通过滤血膜和微孔滤膜进行第一步分离;
2)将第一步分离后的液体通过芯片进一步分离纯化,得到尺寸小于150nm的外泌体;
3)被颗粒标记的抗体与尺寸小于150nm的外泌体的抗原结合;
4)硝酸纤维素膜粘贴区上的多组t线中的一组显色,证明外泌体通过了t线,根据显色的t线组数及颜色深浅判断该外泌体蛋白(例如c19orf43)的含量。
结果表明,5例骨肉瘤患者血清外泌体的检测结果中仅有1条t线显色,且显色程度明显弱于其他各类样本,而正常样本显色显色条数为两条,且颜色明显强于骨肉瘤,其余样本外泌体的t线检测结果为2条或3条。进一步根据显色程度对免疫层析的检测结果进行定量分析,表明骨肉瘤患者血清外泌体的c19orf43蛋白水平显著低于正常组以及其他组(p<0.001)。由此可见,根据血清外泌体c19orf43蛋白水平可以将骨肉瘤与其他样本区分开来。
2、elisa检测
采用elisa实验对本实施例另外选择30例样本的血清外泌体c19orf43蛋白水平进行检测,具体步骤参见实施例1。
elisa实验表明与其他病理组以及正常组相比,5例骨肉瘤患者血清外泌体中的c19orf43显著性低表达,与即时平台的检测数据一致。
以上的仅是本发明的优选实施方式,应当指出,对于本领域的普通技术人员来说,在不脱离本发明创造构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!