一种基于涡旋萃取的薄荷醇异构体分离测定方法与流程
本发明属于分析化学研究领域,具体是一种薄荷醇精油及添加剂中薄荷醇异构体的分离测定方法及应用。
背景技术:
薄荷醇是薄荷精油及薄荷醇添加剂的主要成分,可用作牙膏、香水、饮料、烟草和糖果等的赋香剂,在医药上用作刺激药,作用于皮肤或粘膜,有清凉止痒作用,内服可用于头痛及鼻、咽、喉炎症等。近年来国内市场对薄荷醇的需要日益增长,天然提取的薄荷醇的已无法满足市场日益旺盛的需求,合成薄荷醇的用量也在不断增长。
薄荷醇的立体异构体呈香性质各不相同,l-薄荷醇具有薄荷香气并有清凉的作用,dl-薄荷醇也有清凉作用,其他的异构体无清凉作用,甚至有刺激作用。由于不同薄荷醇异构体具有不同物理性质,然而不同来源的薄荷醇中异构体含量和分布各异,其构型组成影响其特征和功效,表现出不同的应用价值,从产品质量控制、质量评价和应用出发,需要建立一个薄荷醇异构体的分离检测方法,从而对薄荷醇精油及添加剂中薄荷醇异构体进行检测。
目前主要采用色谱法对薄荷醇异构体分离,但目前报道的方法不能完全分离8个薄荷醇异构体。采用19fnmr核磁共振谱可以将8个薄荷醇异构体进行分离,但19fnmr核磁共振谱仪器昂贵,并需要特殊试剂、复杂的前处理和化学反应步骤,且只能用于薄荷醇纯品检测,不能用于复杂样品基质中薄荷醇异构体的分离和检测。同时,薄荷醇精油及添加剂中的薄荷醇分离十分困难,现有技术中并没有有效的样品分离方法及其检测方法。
技术实现要素:
本发明的目的正是基于上述现有技术状况的不足和薄荷醇异构体的检测需求,提供一种基于涡旋萃取的薄荷醇异构体分离测定方法,可以分离和检测薄荷醇精油及添加剂中的8个薄荷醇异构体,该方法简便快速,分离度高,检测灵敏,方法具有推广应用价值。
本发明采用的技术方案具体如下:
一种基于涡旋萃取的薄荷醇异构体分离测定方法,包括以下步骤:
步骤(1)、涡旋萃取:
准确称量一定质量样品于离心管中,加入含内标溶液的萃取溶剂,其中,萃取溶剂的用量与样品质量的比例为50:1~500:1,ml:g;内标溶液浓度为10~1000mg/l,加盖后进行涡旋萃取,涡旋振荡的转速为1000~2500rpm,涡旋振荡的时间为2~5min;
步骤(2)、气相色谱分离:
萃取液经0.22μm~0.45μm微孔滤膜过滤后,进入气相色谱进行分离;
步骤(3)、薄荷醇异构体含量测定:
通过质谱法对分离的薄荷醇异构体进行检测,内标法定量,根据标准曲线计算各薄荷醇异构体含量。
进一步地,步骤(1)中,样品的质量为0.01~0.5g。
进一步地,步骤(1)中,萃取溶剂为甲醇、乙醇、异丙醇或正丙醇。
进一步地,步骤(1)中,内标溶液为乙酸苯乙酯。
进一步地,步骤(2)中,气相色谱的色谱柱为两根手性弹性毛细管柱串联,第一根色谱柱通过毛细管柱连接专用接头与第二根色谱柱相连接。
进一步地,步骤(2)中,第一根色谱柱固定相为20%叔丁基二甲基氯硅烷-β-环糊精溶解于bgb-15,规格为长度25m~35m×内径0.25mmid×膜厚0.25μmdf。其中,bgb-15为15%的苯基取代和85%的甲基取代的聚硅氧烷。
进一步地,步骤(2)中,第二根色谱柱固定相为30%七-(2,3-二-o-甲基-6-o-叔丁基二甲基硅基)-β-环糊精溶解于db-1701,规格为长度30m~40m×内径0.25mmid×膜厚0.25μmdf。
进一步地,步骤(2)中,气相色谱条件如下:
进样口温度:180~200℃;载气:氦气,纯度≥99.999%;柱流量:恒流1.4~2.0ml/min;进样量:1μl;分流进样,分流比5:1~50:1;升温程序:初始温度80~100℃,然后以2~5℃/min的速率升温至120℃,并保持15~20min,最后以10℃/min的速率升温至200℃,保持5min。
进一步地,步骤(3)中,质谱条件如下:电子轰击源ei;传输线温度:200~220℃;离子源温度:180~200℃;电离能量:70ev;溶剂延迟:12min;扫描模式为选择离子监测模式,8个薄荷醇的定性、定量离子均为71/81/95,乙酸苯乙酯定性、定量离子均为43/91/104。
进一步地,步骤(3)中,标准曲线绘制方法如下:
用萃取溶剂配制8个薄荷醇异构体的混合标准溶液,浓度范围为:0.5mg/l~5000mg/l,系列标准溶液加入内标物,内标物浓度与样品提取液中内标浓度相同,内标物浓度为10~1000mg/l,对系列标准溶液进行气相色谱-质谱联用仪分析,以各物质定量离子峰面积与内标物定量离子峰面积的比值为纵坐标,以各物质浓度与内标物浓度比值为横坐标,作各测定物质的标准曲线。
与现有技术相比,本发明有益效果具体如下:
(1)方法选用的萃取溶剂对样品溶解或分散效果较好,结合涡旋萃取可实现样品中薄荷醇快速、均匀溶解于萃取剂中,前处理过程简便快速。
(2)借助两根手性色谱柱的串联组合,结合两根手性色谱柱的分离能力,可实现8个薄荷醇异构体完全分离,解决一根色谱柱无法将8个薄荷醇异构体分离的难题,分离效率高,效果好;
(3)方法检测灵敏度高,精密度小于3.7%,回收率在93%~105%,准确可靠,具有推广应用价值。
附图说明
以上说明为本发明技术方案的概述,为了更清楚的了解本发明的技术手段,而可依照说明书的内容予以实施,并且为了让本发明的上述和其它目的、特征和优点能够更明显易懂,现特举较佳实施例,并配合附图,详细说明如下:
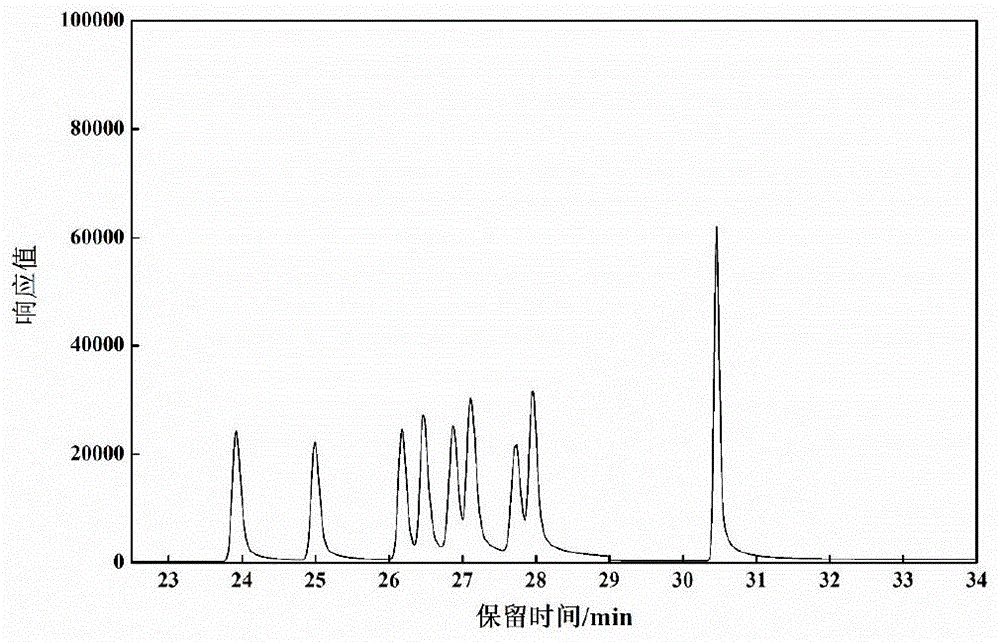
图1为8种薄荷醇异构体标准溶液测定的气相色谱-质谱图;
图2为合成薄荷醇添加剂中荷醇异构体测定的气相色谱-质谱图;
图3为薄荷醇天然精油中荷醇异构体测定的气相色谱-质谱图;
图4为烟用爆珠添加剂中荷醇异构体测定的气相色谱-质谱图。
具体实施方式
下面结合实施例对本发明作进一步的详细描述,但其并不限制本发明。
本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限定本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可以通过购买获得的常规产品。
实施例1
本实施例的基于涡旋萃取的薄荷醇异构体分离测定方法,包括以下步骤:
步骤(1)、涡旋萃取:
本实施例的样品为某合成薄荷醇添加剂。
准确称量0.02g合成薄荷醇添加剂于离心管中,加入5ml含乙酸苯乙酯浓度为100mg/l的甲醇溶液,加盖后置于涡旋振荡仪上于1500rpm转速下涡旋2min;
步骤(2)、气相色谱分离:
萃取液经0.22μm微孔滤膜过滤后,进样,进入气相色谱分离,气相色谱条件如下:
色谱柱为两根手性弹性毛细管柱串联,第一根色谱柱通过毛细管柱连接专用接头与第二根色谱柱相连接。
第一根色谱柱固定相为20%叔丁基二甲基氯硅烷-β-环糊精溶解于bgb-15(15%苯基,85%甲基聚硅氧烷),规格为长度30m×内径0.25mmid×膜厚0.25μmdf。
第二根色谱柱固定相为30%七-(2,3-二-o-甲基-6-o-叔丁基二甲基硅基)-β-环糊精溶解于db-1701((14%-氰丙基-苯基)甲基聚硅氧烷),规格为长度35m×内径0.25mmid×膜厚0.25μmdf。
进样口温度:180℃;载气:氦气(纯度≥99.999%),柱流量:恒流1.5ml/min;进样量:1μl;分流进样,分流比5:1;升温程序:初始温度100℃,然后以5℃/min的速率升温至120℃,并保持20min,最后以10℃/min的速率升温至200℃,保持5min。
步骤(3)、薄荷醇异构体含量测定:
通过质谱法对分离的薄荷醇异构体进行检测,内标法定量,根据标准曲线计算各薄荷醇异构体含量,质谱条件如下:
电子轰击源(ei);传输线温度:200℃;离子源温度:190℃;电离能量:70ev;溶剂延迟:12min;扫描模式为选择离子监测模式,8个薄荷醇的定性、定量离子均为71/81/95,乙酸苯乙酯定性、定量离子为43/91/104。
标准曲线绘制方法如下:
用萃取溶剂配制8个薄荷醇异构体的混合标准溶液,浓度范围为:0.5mg/l~5000mg/l,系列标准溶液加入内标物,内标物浓度与样品提取液中内标浓度相同,内标物浓度为10~1000mg/l,对系列标准溶液进行气相色谱-质谱联用仪分析,以各物质定量离子峰面积与内标物定量离子峰面积的比值为纵坐标,以各物质浓度与内标物浓度比值为横坐标,作各测定物质的标准曲线。
图1为8种薄荷醇异构体标准溶液测定的气相色谱-质谱图,图中9个峰从左到右分别为d-新薄荷醇、l-新薄荷醇、l-新异薄荷醇、d-薄荷醇、l-薄荷醇、l-异薄荷醇、d-新异薄荷醇、d-异薄荷醇、乙酸苯乙酯,8个薄荷醇异构体分离情况良好。
表1是采用本方法测定8种薄荷醇异构体的方法评价数据,给出了本实验方法的线性相关系数、精密度(rsd)、检出限和回收率,表明该方法灵敏度高,精密度和准确度好,适用于薄荷醇精油及添加剂中薄荷醇异构体的分离和定量测定。
表1线性相关系数、精密度(rsd)、检出限和回收率
图2为无糖薄荷糖中荷醇异构体测定的气相色谱-质谱图,检出的薄荷醇异构体从左到右为d-薄荷醇、l-薄荷醇,根据标准曲线计算其含量分别为163mg/g、214mg/g;该方法对薄荷醇异构体定性、定量分析准确可靠,适用于薄荷醇添加剂中薄荷醇异构体的测定。
实施例2
本实施例的基于涡旋萃取的薄荷醇异构体分离测定方法,包括以下步骤:
步骤(1)、涡旋萃取:
本实施例的样品为某薄荷醇天然精油。
准确称量0.5g薄荷醇天然精油于离心管中,加入25ml含乙酸苯乙酯浓度为10mg/l的乙醇溶液,加盖后置于涡旋振荡仪上于2000rpm转速下涡旋3.5min。
步骤(2)、气相色谱分离:
萃取液经0.45μm微孔滤膜过滤后,进样,进入气相色谱分离,气相色谱条件如下:
色谱柱为两根手性弹性毛细管柱串联,第一根色谱柱通过毛细管柱连接专用接头与第二根色谱柱相连接。
第一根色谱柱固定相为20%叔丁基二甲基氯硅烷-β-环糊精溶解于bgb-15(15%苯基,85%甲基聚硅氧烷),规格为长度25m×内径0.25mmid×膜厚0.25μmdf。
第二根色谱柱固定相为30%七-(2,3-二-o-甲基-6-o-叔丁基二甲基硅基)-β-环糊精溶解于db-1701((14%-氰丙基-苯基)甲基聚硅氧烷),规格为长度40m×内径0.25mmid×膜厚0.25μmdf。
进样口温度:190℃;载气:氦气(纯度≥99.999%),柱流量:恒流2.0ml/min;进样量:1μl;分流进样,分流比30:1;升温程序:初始温度80℃,然后以3℃/min的速率升温至120℃,并保持15min,最后以10℃/min的速率升温至200℃,保持5min。
步骤(3)、薄荷醇异构体含量测定:
通过质谱法对分离的薄荷醇异构体进行检测,内标法定量,根据标准曲线计算各薄荷醇异构体含量,质谱条件如下:
电子轰击源(ei);传输线温度:210℃;离子源温度:200℃;电离能量:70ev;溶剂延迟:12min;扫描模式为选择离子监测模式,8个薄荷醇的定性、定量离子均为71/81/95,乙酸苯乙酯定性、定量离子为43/91/104。
图3为薄荷醇天然精油测定的气相色谱-质谱图,检出的薄荷醇异构体从左到右为d-新薄荷醇、l-新薄荷醇、d-薄荷醇、l-薄荷醇、l-异薄荷醇、d-新异薄荷醇、d-异薄荷醇,根据标准曲线计算其含量分别为74.2mg/g、82.5mg/g、3.7mg/g、68.9mg/g、8.5mg/g、6.1mg/g、7.6mg/g。
其余与实施例1相同。
实施例3
本实施例的基于涡旋萃取的薄荷醇异构体分离测定方法,包括以下步骤:
步骤(1)、涡旋萃取:
本实施例的样品为某烟用爆珠添加剂。
准确称量0.1g烟用爆珠添加剂于离心管中,加入50ml含乙酸苯乙酯浓度为1000mg/l的异丙醇溶液,加盖后置于涡旋振荡仪上于2500rpm转速下涡旋5min;
步骤(2)、气相色谱分离:
萃取液经0.22μm微孔滤膜过滤后,进样,进入气相色谱分离,气相色谱条件如下:
色谱柱为两根手性弹性毛细管柱串联,第一根色谱柱通过毛细管柱连接专用接头与第二根色谱柱相连接。
第一根色谱柱固定相为20%叔丁基二甲基氯硅烷-β-环糊精溶解于bgb-15(15%苯基,85%甲基聚硅氧烷),规格为长度35m×内径0.25mmid×膜厚0.25μmdf。
第二根色谱柱固定相为30%七-(2,3-二-o-甲基-6-o-叔丁基二甲基硅基)-β-环糊精溶解于db-1701((14%-氰丙基-苯基)甲基聚硅氧烷),规格为长度30m×内径0.25mmid×膜厚0.25μmdf。
进样口温度:200℃;载气:氦气(纯度≥99.999%),柱流量:恒流1.4ml/min;进样量:1μl;分流进样,分流比50:1;升温程序:初始温度90℃,然后以2℃/min的速率升温至120℃,并保持17min,最后以10℃/min的速率升温至200℃,保持5min。
步骤(3)、薄荷醇异构体含量测定:
通过质谱法对分离的薄荷醇异构体进行检测,内标法定量,根据标准曲线计算各薄荷醇异构体含量,质谱条件如下:
电子轰击源(ei);传输线温度:220℃;离子源温度:180℃;电离能量:70ev;溶剂延迟:12min;扫描模式为选择离子监测模式,8个薄荷醇的定性、定量离子均为71/81/95,乙酸苯乙酯定性、定量离子为43/91/104。
图4为烟用爆珠添加剂中荷醇异构体测定的气相色谱-串联质谱图,检出的薄荷醇异构体从左到右为d-新薄荷醇、l-新薄荷醇、d-薄荷醇、l-薄荷醇,根据标准曲线计算其含量分别为0.54mg/g、0.69mg/g、0.58mg/g、216.6mg/g。
其余与实施例1相同。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!