一种林下山参的指纹图谱的检测方法与流程
本发明属于中药成分分析检测
技术领域:
,涉及一种林下山参的指纹图谱的检测方法。
背景技术:
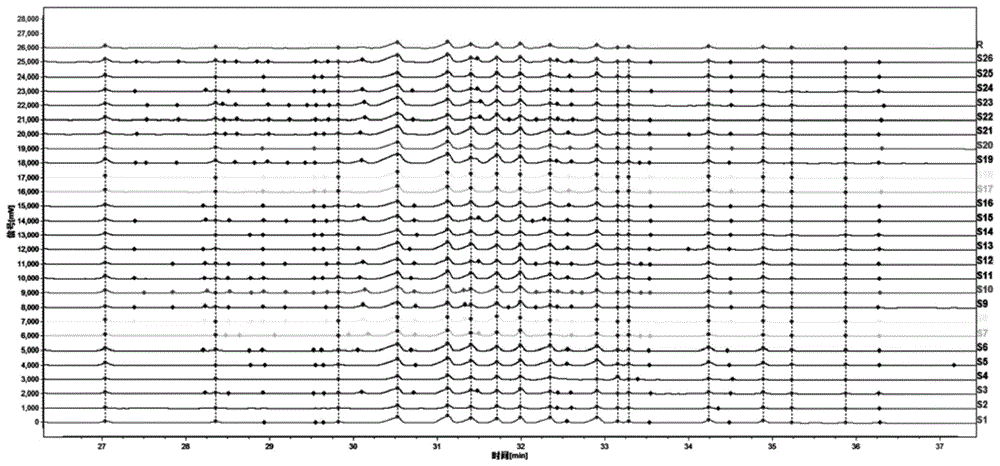
:林下山参为五加科植物人参(panaxginsengc.a.mey.)的干燥根和根茎,是一味常见名贵中药,《神农本草经》将其列为上品,认为其具有大补元气、复脉固脱、补脾益肺、安神益智的功效。现代临床药理研究表明,人参的主要药效成分为人参皂苷,其具有多个方面药效,如陈颉等人认为人参能够提升免疫力(人参皂苷免疫调节作用的研究进展[j].山西中医学院学报,2014(05):75-77),姜卫卫等人认为人参能够抗肿瘤(人参皂苷rb1、rg3、rh2抗肿瘤作用与机制概况[j].世界科学技术-中医药现代化,2013(07):1634-1637),蔡晓月等人认为人参能够改善心血管(人参治疗心血管疾病的药理学研究[j].长春中医药大学学报,2012(01):158-159),吴晓民等人认为人参能够抗氧化(人参多糖的药理作用与临床研究进展[j].人参研究,2016(05):40-46),李成鹏等人认为人参能够抗衰老(人参皂苷rg_1延缓脑衰老机制研究[j].中国中药杂志,2014(22):4442-4447),郑友生等人认为人参能够抗老年痴呆(人参皂苷rg1促进神经干细胞增殖的实验研究[j].世界中西医结合杂志,2011(12):1021-1024),张彩等人认为人参能够降血糖(人参化学成分和药理作用研究进展[j].食品与药品,2016(04):300-304),彭雪等人认为人参能够抑菌抗炎(人参挥发油研究[j].吉林中医药,2017(01):71-74)。近年来,随着林下山参在食品、药品方面应用的逐步广泛,其质量愈加成为人们关注的焦点,由于林下山参资源稀缺,价格昂贵且市场需求大,假冒林下山参及掺伪现象不断增多,制定林下山参科学准确的质控方法,完善林下山参质量标准,显得尤为重要。在《中国药典》2015年版(一部),以人参皂苷rg1、rb1和re的最低含量限定来控制其质量,但是仅以这三种人参皂苷为指标难以全面的评判药材的质量。另外,林下山参作为多年生草本植物,采收年限是影响其质量的重要因素,更是制定其市场价格的主要依据。因为无论是在临床疗效上还是大部分消费者的认知中,参龄高的林下山参其药效要优于参龄低的林下山参。当前对参龄的鉴别方式主要靠性状鉴别和老药工老参农的经验判断,难免有一定程度的主观性,随着商品加工的多样化,性状鉴别的局限性愈发明显。因而,当前市场对林下山参客观准确的生长年限鉴定及质量评价方法有着迫切的需要。中药指纹图谱具有整体、宏观、模糊分析等特点,可通过对中药整体特征的描述,采用适当模糊处理方式,达到整体质量控制的目的,因此成为中药质量控制的有效手段。其中色谱指纹图谱分析可以使中药所含多种化学组分的整体特征可视化,从而披露出常规检验难以发现的质量问题。技术实现要素:鉴于以上所述现有技术的缺点,本发明的目的在于提供一种林下山参的指纹图谱的检测方法,采用优化条件的高效液相色谱方法建立林下山参的指纹图谱,并且同时一次对林下山参中多种成分进行定量分析,并可通过相似度比较及正交偏最小二乘法判别分析(opls-da),对辽宁省桓仁县10年生、15年生和20年生林下山参生长年限进行鉴定,与园参样品进行鉴别,比较全面的反映林下山参的现状,提高林下山参的质控水平。为实现上述目的及其他相关目的,本发明第一方面提供一种林下山参的指纹图谱的检测方法,将含有林下山参的供试品溶液和含有参照品的参照品溶液,采用高效液相色谱法进行测定,将获得的供试品溶液和参照品溶液的指纹谱图,与林下山参的标准指纹谱图进行比较,根据相对保留时间,指认出共有特征峰,从而获得供试品溶液中林下山参的指纹图谱。优选地,所述供试品溶液是将林下山参加入甲醇溶液后超声提取,第一次过滤后取续滤液,旋转蒸发至干,加入甲醇溶液溶解定容后进行第二次过滤,即得。更优选地,所述林下山参经研磨成粉末状后过筛而得。进一步优选地,所述过筛的筛孔孔径为75-85目。最优选地,所述过筛的筛孔孔径为80目。更优选地,所述林下山参加入的重量g与所述甲醇溶液加入的体积ml之比为2:15-25。进一步优选地,所述林下山参加入的重量g与所述甲醇溶液加入的体积ml之比为2:20。更优选地,所述林下山参加入甲醇溶液后,需精密称重。更优选地,所述超声提取的温度为45-55℃。最优选地,所述超声提取的温度为50℃。更优选地,所述超声提取时间为90-110min。最优选地,所述超声提取时间为100min。更优选地,所述超声提取后需再称重,并用甲醇溶液补足失重。所述续滤液是指:过滤时,初滤液后的溶液即为续滤液。更优选地,所述续滤液的取样量为8.0-12.0ml。进一步优选地,所述续滤液的取样量为10.0ml。所述旋转蒸发至干是指采用旋转蒸发仪将续滤液旋转蒸发至干。更优选地,旋转蒸发前的所述续滤液与旋转蒸发后加入甲醇溶液的体积之比为8-12:2。进一步优选地,旋转蒸发前的所述续滤液与旋转蒸发后加入甲醇溶液的体积之比为10:2。更优选地,所述第一次过滤为滤纸过滤。所述滤纸为定性滤纸(中速)。更优选地,所述第二次过滤为滤膜过滤。所述滤膜为0.22μm滤膜。更优选地,所述甲醇溶液为体积百分比65-75%的甲醇水溶液。更优选地,所述甲醇溶液为体积百分比70%的甲醇水溶液。优选地,所述参照品溶液是将参照品加入甲醇后溶解定容制得。更优选地,所述参照品包括有人参皂苷rg1(cas号为22427-39-0)、人参皂苷re(cas号为51542-56-4)、人参皂苷rb1(cas号为41753-43-9)、人参皂苷rc(cas号为11021-14-0)、人参皂苷rd(cas号为52705-93-8)。更优选地,所述参照品溶液中人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd的浓度均为0.5-2.0mg/ml。进一步优选地,所述参照品溶液中人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd的浓度均为1.0mg/ml。优选地,所述高效液相色谱法的色谱条件为:色谱柱:c18柱;柱温:20-40℃;检测波长:200-205nm;流速:0.5-2.0ml/min;进样量:1-10μl;流动相:0.05-0.15v/v%甲酸水溶液-0.05-0.15v/v%甲酸乙腈溶液,其中,a相为0.05-0.15v/v%甲酸水溶液,b相为0.05-0.15v/v%甲酸乙腈溶液;分析时间:60min;梯度洗脱。更优选地,所述高效液相色谱法的色谱条件为:色谱柱:waterscortecsc18柱(150mm×4.6mm,2.7μm);柱温:30℃;检测波长:203nm;流速:1.0ml/min;进样量:5μl;流动相:0.1v/v%甲酸水溶液-0.1v/v%甲酸乙腈溶液,其中,a相为0.1v/v%甲酸水溶液,b相为0.1v/v%甲酸乙腈溶液;分析时间:60min;梯度洗脱。进一步优选地,所述梯度洗脱的具体程序为:0-20min,a相:b相体积比为85:15-75:25;20-37min,a相:b相体积比为75:25-60:40;37-45min,a相:b相体积比为60:40-40:60;45-49min,a相:b相体积比为40:60-21:79;49-58min,a相:b相体积比为21:79-5:95;58-60min,a相:b相体积比为5:95-85:15。所述林下山参的标准指纹谱图是指按照国家食品药品监督管理局2000年8月15日颁布的《中药注射剂指纹图谱研究的技术要求(暂行)》中的规定,取同一种至少10个批次的林下山参,分别制备供试品溶液和参照品溶液,再按上述的hplc条件进行测定后,分别获得指纹图谱,再将指纹图谱导入《中药色谱指纹图谱相似度评价软件2012版》,生成对照图谱,最终确定林下山参的标准指纹谱图。在实际检测时,被检样品与标准指纹图谱进行相似度比较,当相似度≥0.9,即为合格,说明获得被检样品中林下山参的指纹全谱图。优选地,所述供试品溶液和参照品溶液的指纹谱图与林下山参的标准指纹谱图进行的比较时,采用国家药典委员会发布的《中药色谱指纹图谱相似度评价软件2012版》进行相似度比较,以参照品溶液的指纹谱图中的参照品色谱峰为参比峰,根据相对保留时间,指认出供试品溶液的指纹图谱中的相应特征峰,从而对供试品溶液指纹图谱中的指标成分进行归属定位,从而指认出供试品溶液的指纹谱图中的共有特征峰。本发明第二方面提供一种林下山参的指纹图谱的检测方法在林下山参中成分的质量检测中的用途。本发明第三方面提供一种林下山参的质量检测方法,包括采用前述林下山参的指纹图谱的检测方法获得林下山参指纹图谱,将得到的林下山参指纹图谱与相同指纹图谱检测条件下获得的林下山参的标准指纹图谱进行相似度比较。优选地,将林下山参指纹图谱与林下山参的标准指纹图谱进行相似度的比较时,采用国家药典委员会发布的《中药色谱指纹图谱相似度评价系统》2012版软件进行比较。更优选地,本发明测得的林下山参的指纹图谱与林下山参的标准指纹图谱的相似度≥0.90。优选地,采用与前述林下山参指纹图谱的检测方法相同的条件得到林下山参的标准指纹图谱,所述林下山参的标准指纹图谱包括33个共有指纹峰,以2号峰为定位峰(s峰,相对保留时间为1.000),其他32个共有指纹峰的相对保留时间依次为1号峰(0.9793-0.9803)、3号峰(1.0949-1.1049)、4号峰(1.1408-1.1433)、5号峰(1.1870-1.2747)、6号峰(1.2704-1.2824)、7号峰(1.5468-1.5613)、8号峰(1.5962-1.6072)、9号峰(1.6678-1.6879)、10号峰(1.7159-1.7742)、11号峰(1.8003-1.8793)、12号峰(1.8369-1.8513)、13号峰(1.8524-1.8680)、14号峰(1.8579-1.8852)、15号峰(1.8708-1.9028)、17号峰(1.9075-1.9584)、18号峰(1.9424-1.9729)、19号峰(1.9575-1.9801)、20号峰(2.0217-2.0361)、21号峰(2.0600-2.0752)、22号峰(2.0798-2.0968)、23号峰(2.1182-2.1326)、24号峰(2.7044-2.7358)、25号峰(2.8304-2.8658)、26号峰(2.8561-2.8918)、27号峰(2.9297-2.9679)、28号峰(2.9865-3.0260)、29号峰(3.1100-3.1501)、30号峰(3.1208-3.1620)、31号峰(3.1371-3.1778)、32号峰(3.2340-3.2767)、33号峰(3.2628-3.3052)。优选地,所述林下山参的指纹图谱与参照品溶液的指纹图谱进行比较,定位确定所述1号峰为人参皂苷rg1的指纹峰,所述2号峰为人参皂苷re的指纹峰,所述11号峰为人参皂苷rb1的指纹峰,所述13号峰为人参皂苷rc的指纹峰,所述20号峰为人参皂苷rd的指纹峰。本发明第四方面提供一种林下山参的指纹图谱的检测方法在林下山参中人参皂苷成分含量测定中的应用。本发明第五方面提供一种林下山参中人参皂苷成分含量的测定方法,包括以下步骤:a)供试品溶液的制备:按上述林下山参的指纹图谱的检测方法的相同步骤制备供试品溶液;b)对照品溶液的制备:将一种或多种人参皂苷成分的对照品,加入甲醇溶解定容,即得对照品溶液;c)测定:采用上述林下山参的指纹图谱的检测方法中相同的高效液相色谱(hplc)条件,分别测定步骤a)中的供试品溶液和步骤b)中的对照品溶液,并采用外标法计算供试品溶液中人参皂苷成分的含量。优选地,步骤b)中,所述对照品溶液选自人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd的对照品溶液中的一种或多种。更优选地,所述对照品溶液中,人参皂苷rg1的浓度为0.59~3.90mg/ml,人参皂苷re的浓度为0.58~3.89mg/ml,人参皂苷rb1的浓度为0.61~4.06mg/ml,人参皂苷rc的浓度为0.58~3.86mg/ml,人参皂苷rd的浓度为0.40~2.67mg/ml。所述外标法是指:分别移取一定体积的步骤b)所述对照品溶液,配成一定浓度的对照品标准溶液,采用高效液相色谱仪进样分析,获得对照品标准溶液中人参皂苷成分含量与峰面积的线性关系,以每一种人参皂苷成分色谱峰面积对应其相应的含量,绘制相应的标准工作曲线,计算得到各标准工作曲线的回归方程。再将步骤a)所述供试品溶液采用高效液相色谱仪检测,将获得的供试品溶液中人参皂苷成分的色谱峰面积,分别代入所述各标准工作曲线的回归方程中,可得到林下山参中相应人参皂苷成分的含量。本发明中所述林下山参为野生环境自然生长的林下参,所述园参为人工种植的平地栽参。如上所述,本发明提供的一种林下山参的指纹图谱的检测方法,采用优化条件的高效液相色谱方法建立林下山参的指纹图谱,对林下山参中多种成分进行定量分析,并可通过相似度比较及正交偏最小二乘法判别分析(opls-da),比较全面的反映林下山参的现状,与园参进行鉴别,提高林下山参的质控水平,对科学有效评价林下山参质量,改善市场环境,科学有效区分不同参龄林下山参有一定意义。本发明建立的林下山参的指纹图谱的检测方法,其精密度、稳定性和重复性、加样回收率良好,确定了33个共有峰,方法学考察各共有峰的相对保留时间和相对峰面积的rsd≤3%,多批次林下山参样品的相似度评价结果均大于0.90。附图说明图1显示为本发明中的26批林下山参样品的指纹图谱。图2显示为本发明中的林下山参的指纹图谱。图3显示为本发明中的34批样品的聚类树图。图4显示为本发明中的34批样品的opls-da得分图。具体实施方式下面结合具体实施例进一步阐述本发明,应理解,这些实施例仅用于说明本发明而不用于限制本发明的保护范围。以下通过特定的具体实例说明本发明的实施方式,本领域技术人员可由本说明书所揭露的内容轻易地了解本发明的其他优点与功效。本发明还可以通过另外不同的具体实施方式加以实施或应用,本说明书中的各项细节也可以基于不同观点与应用,在没有背离本发明的精神下进行各种修饰或改变。以下实施例使用的试剂和仪器如下:1、试剂乙腈、甲醇(色谱纯,merck公司);甲酸(分析纯,国药集团化学试剂有限责任公司);水(纯净水);人参皂苷rg1(hplc色谱纯≥99.7%)、人参皂苷re(hplc色谱纯≥99.2%)、人参皂苷rb1(hplc色谱纯≥99.9%)、人参皂苷rc(hplc色谱纯≥99.6%)、人参皂苷rd(hplc色谱纯≥99.6%),上述对照品均来自上海源叶生物科技有限公司。林下山参及园参上海上药神象健康药业有限公司提供,林下山参药材共26份,园参样本共8份,具体情况见下表1。表12、仪器watersacquityarc高效液相色谱仪(美国waters公司);kq5200de型数控超声波清洗器(昆山市超声仪器有限公司);eyelan-1100型旋转蒸发仪(上海爱朗仪器有限公司);eyelacca-1112型冷却水循环装置(上海爱朗仪器有限公司);sartoriusbs124s电子天平(赛多利斯科学仪器(北京)有限公司);sartoriussqpquintix65-1cn十万分之一分析天平(赛多利斯科学仪器(北京)有限公司)。实施例11、样品前处理供试品溶液的制备:将林下山参研磨成粉末状过75-85目筛,精密称定,加入65-75%甲醇水溶液,林下山参加入的重量g与甲醇溶液加入的体积ml之比为2:15-25。称重后,在45-55℃下超声提取90-110min,再称重,并用65-75%甲醇水溶液补足失重。采用定性滤纸进行第一次过滤,取8-12ml续滤液,旋转蒸发至干,加入65-75%甲醇水溶液溶解定容,旋转蒸发前的所述续滤液与旋转蒸发后加入甲醇的体积之比为8-12:2。再采用0.22μm滤膜进行第二次过滤,即得供试品溶液。参照品溶液的制备:将参照品加入甲醇后溶解定容,制得参照品溶液。参照品包括有人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd。参照品溶液中人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd的浓度均为0.5-2.0mg/ml。2、色谱条件所述高效液相色谱法的色谱条件为:色谱柱:c18柱;柱温:20-40℃;检测波长:200-205nm;流速:0.5-2.0ml/min;进样量:1-10μl;流动相:0.05-0.15v/v%甲酸水溶液-0.05-0.15v/v%甲酸乙腈溶液,其中,a相为0.05-0.15v/v%甲酸水溶液,b相为0.05-0.15v/v%甲酸乙腈溶液;分析时间:60min;梯度洗脱。所述梯度洗脱的具体程序为:0-20min,a相:b相体积比为85:15-75:25;20-37min,a相:b相体积比为75:25-60:40;37-45min,a相:b相体积比为60:40-40:60;45-49min,a相:b相体积比为40:60-21:79;49-58min,a相:b相体积比为21:79-5:95;58-60min,a相:b相体积比为5:95-85:15。3、测定采用上述2中的色谱条件的高效液相色谱法分别测定上述1中供试品溶液和参照品溶液,获得的供试品溶液和参照品溶液的指纹谱图,与林下山参的标准指纹谱图进行比较,根据相对保留时间,指认出共有特征峰,从而获得供试品溶液中林下山参的指纹图谱。其中,所述供试品溶液和参照品溶液的指纹谱图与林下山参的标准指纹谱图进行的比较时,采用国家药典委员会发布的《中药色谱指纹图谱相似度评价软件2012版》进行相似度比较,以参照品溶液的指纹谱图中的参照品色谱峰为参比峰,根据相对保留时间,指认出供试品溶液的指纹图谱中的相应特征峰,从而对供试品溶液指纹图谱中的指标成分进行归属定位,从而指认出供试品溶液的指纹谱图中的共有特征峰。实施例21、样品前处理供试品溶液的制备:取林下山参研磨后过80目筛的粉末2.0g,精密称定,置25ml具塞锥形瓶中,加70%甲醇水溶液20.0ml称重后,于50℃下超声100min,再称重,并用70%甲醇水溶液补足失重。采用定性滤纸进行第一次过滤,取10.0ml续滤液,旋转蒸发至干,用70%甲醇水溶液复溶后转移至2ml容量瓶中,用70%甲醇水溶液溶解定容,再采用0.22μm滤膜进行第二次过滤,即得供试品溶液。参照品溶液的制备:将各种含量均为5.0mg的参照品置5ml容量瓶中,加入甲醇后溶解定容,制得参照品溶液。参照品包括有人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd。参照品溶液中人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd的浓度均为1.0mg/ml。2、色谱条件所述高效液相色谱法的色谱条件为:色谱柱:waterscortecsc18柱(150mm×4.6mm,2.7μm);柱温:30℃;检测波长:203nm;流速:1.0ml/min;进样量:5μl;流动相:0.1v/v%甲酸水溶液-0.1v/v%甲酸乙腈溶液,其中,a相为0.1v/v%甲酸水溶液,b相为0.1v/v%甲酸乙腈溶液;分析时间:60min;梯度洗脱。所述梯度洗脱的具体程序为:0-20min,a相:b相体积比为85:15-75:25;20-37min,a相:b相体积比为75:25-60:40;37-45min,a相:b相体积比为60:40-40:60;45-49min,a相:b相体积比为40:60-21:79;49-58min,a相:b相体积比为21:79-5:95;58-60min,a相:b相体积比为5:95-85:15。3、测定采用上述2中的色谱条件的高效液相色谱法分别测定上述1中供试品溶液和参照品溶液,获得的供试品溶液和参照品溶液的指纹谱图,与林下山参的标准指纹谱图进行比较,根据相对保留时间,指认出共有特征峰,从而获得供试品溶液中林下山参的指纹图谱,具体指纹图谱见图2。其中,所述供试品溶液和参照品溶液的指纹谱图与林下山参的标准指纹谱图进行的比较时,采用国家药典委员会发布的《中药色谱指纹图谱相似度评价软件2012版》进行相似度比较,以参照品溶液的指纹谱图中的参照品色谱峰为参比峰,根据相对保留时间,指认出供试品溶液的指纹图谱中的相应特征峰,从而对供试品溶液指纹图谱中的指标成分进行归属定位,从而指认出供试品溶液的指纹谱图中的共有特征峰。实施例3采用上述实施例2中建立的林下山参的指纹图谱的检测方法对26批林下山参样品进行检测,获得林下山参指纹图谱,将得到的林下山参指纹图谱与相同指纹图谱检测条件下获得的林下山参的标准指纹图谱进行相似度评价,指纹图谱叠加图如图1所示。26批林下山参样品的指纹图谱与林下山参的标准指纹图谱的相似度均大于0.90。同时,如图2所示,林下山参的标准指纹图谱包括33个共有指纹峰,以2号峰为定位峰(s峰,相对保留时间为1.000),其他32个共有指纹峰的相对保留时间依次为1号峰(0.9793-0.9803)、3号峰(1.0949-1.1049)、4号峰(1.1408-1.1433)、5号峰(1.1870-1.2747)、6号峰(1.2704-1.2824)、7号峰(1.5468-1.5613)、8号峰(1.5962-1.6072)、9号峰(1.6678-1.6879)、10号峰(1.7159-1.7742)、11号峰(1.8003-1.8793)、12号峰(1.8369-1.8513)、13号峰(1.8524-1.8680)、14号峰(1.8579-1.8852)、15号峰(1.8708-1.9028)、17号峰(1.9075-1.9584)、18号峰(1.9424-1.9729)、19号峰(1.9575-1.9801)、20号峰(2.0217-2.0361)、21号峰(2.0600-2.0752)、22号峰(2.0798-2.0968)、23号峰(2.1182-2.1326)、24号峰(2.7044-2.7358)、25号峰(2.8304-2.8658)、26号峰(2.8561-2.8918)、27号峰(2.9297-2.9679)、28号峰(2.9865-3.0260)、29号峰(3.1100-3.1501)、30号峰(3.1208-3.1620)、31号峰(3.1371-3.1778)、32号峰(3.2340-3.2767)、33号峰(3.2628-3.3052)。其中,所述1号峰为人参皂苷rg1的指纹峰,所述2号峰为人参皂苷re的指纹峰,所述11号峰为人参皂苷rb1的指纹峰,所述13号峰为人参皂苷rc的指纹峰,所述20号峰为人参皂苷rd的指纹峰。实施例4取编号a10的林下山参样品1份,采用上述实施例2中建立的林下山参的指纹图谱的检测方法,连续进样5次,考察指纹图谱中各主要色谱峰保留时间及其峰面积的一致性,具体结果见表2、3,其中规定的共有峰的相对保留时间rsd≤3.0%,相对峰面积rsd≤3.0%。结果表明,该方法的精密度良好。表2保留时间表3峰面积实施例5取编号a10的林下山参样品1份,采用上述实施例2中建立的林下山参的指纹图谱的检测方法,制备供试品溶液后分别放置0h、2h、4h、10h、12h、24h进行检测,计算得出各共有峰相对保留时间和相对峰面积的rsd,具体结果见表4、5,结果表明各共有峰相对保留时间的rsd≤3.0%,相对峰面积的rsd%≤3.0%。表明本发明中样品在24h内检测稳定性良好。表4保留时间表5峰面积实施例6取编号a10的林下山参样品5份,采用上述实施例2中建立的林下山参的指纹图谱的检测方法进行检测,计算各共有峰的相对保留时间和相对峰面积的rsd,具体结果见表6、7,其中规定的共有峰相对保留时间的rsd≤3.0%,相对峰面积的rsd≤3.0%。表明本发明中方法的重复性良好,准确度较高。表6保留时间表7峰面积实施例7按上述实施例2中建立的林下山参的指纹图谱的检测方法中的相同步骤制备供试品溶液。取5种人参皂苷成分的对照品,加入甲醇溶解定容,获得对照品溶液。5种人参皂苷成分分别为人参皂苷rg1、人参皂苷re、人参皂苷rb1、人参皂苷rc、人参皂苷rd。对照品溶液中,人参皂苷rg1的浓度为0.59~3.90mg/ml,人参皂苷re的浓度为0.58~3.89mg/ml,人参皂苷rb1的浓度为0.61~4.06mg/ml,人参皂苷rc的浓度为0.58~3.86mg/ml,人参皂苷rd的浓度为0.40~2.67mg/ml。按上述实施例2中建立的林下山参的指纹图谱的检测方法中的相同的高效液相色谱(hplc)条件,分别测定供试品溶液和对照品溶液,并采用外标法计算供试品溶液中人参皂苷成分的含量。实施例8精密称取对照品溶液适量,按上述实施例7中制备成含有不同质量浓度成分的对照品溶液,并按上述实施例7中的高效液相色谱(hplc)条件进行测定,计算获得5种人参皂苷成分的标准回归方程、相关系数和线性范围,具体结果见表8。表8化合物标准曲线r线性范围(mg/ml)人参皂苷rg1y=0.8331x-2455000.99910.59~3.90人参皂苷rey=0.8678x-2154540.99940.58~3.89人参皂苷rb1y=0.9941x-1616390.99950.61~4.06人参皂苷rcy=0.8835x-1538940.99980.58~3.86人参皂苷rdy=0.83x-103987.711.00000.40~2.67根据表8可知,标准回归方程以色谱峰面积为纵坐标(y),化合物质量为横坐标(x),同时,5种成分在一定线性范围内均呈良好的线性关系,其标准回归方程的相关系数均大于0.9990。同时,以s/n=3确定检测限,以s/n=10确定定量限,具体结果见表9。表9人参皂苷rg1人参皂苷re人参皂苷rb1人参皂苷rc人参皂苷rd进样体积(μl)55555进样浓度(mg/ml)0.1160.1160.1160.1160.08s/n1010101010进样浓度(mg/ml)0.0420.0420.030.030.0336s/n33333定量限(μg)580580625625400检测限(μg)210210150150168实施例9精密称取对照品溶液适量,分别准确加入一定含量的5种人参皂苷成分,按上述实施例7中的高效液相色谱(hplc)条件进行测定,结果见表10-14。由表10-14可知,5种人参皂苷成分的含量测定方法的加样回收率均在90-110%之间,rsd均小于3.0%,其测定结果的回收率良好。表10人参皂苷rg1表11人参皂苷re表12人参皂苷rb1表13人参皂苷rc表14人参皂苷rd实施例10按上述实施例7中的林下山参中人参皂苷成分含量的测定方法,对表1中的26批次林下山参样品进行检测,其含量测定结果见表15。由表15可知,本发明中的测定方法能够有效测定林下山参中人参皂苷成分的含量。表15实施例11将上述实施例2中建立的林下山参的指纹图谱的检测方法,对如表1所示的34批样品进行检测,获得指纹图谱。将获得的指纹图谱中的33个共有峰的峰面积导入simca-p14.0软件中,进行聚类分析,得到的聚类树图如图3所示。结果显示34批样品聚为两大组,一组为园参,一组为林下山参。表明园参和林下山参之间存在质量差异。林下山参又分成三组,一组为10年,一组为15年,一组为20年。说明不同参龄的林下山参之间质量存在差异。本发明中方法可对辽宁省桓仁县10年生、15年生和20年生林下山参生长年限进行鉴定。实施例12将上述实施例2中建立的林下山参的指纹图谱的检测方法,对如表1所示的34批样品进行检测,获得林下山参和园参的色谱图。将获得的图谱中的34批样品色谱数据导入simca-p14.0软件进行正交偏最小二乘法判别分析(opls-da)分析处理,opls-da得分图如图4所示。从图4中可以看出样品被明显分为林下山参和园参两大类,且林下山参又被分为10年生、15年生和20年生三类,与聚类分析结果一致。本发明中方法可对辽宁省桓仁县10年生、15年生和20年生林下山参生长年限进行鉴定。综上所述,本发明提供的一种林下山参的指纹图谱的检测方法,建立林下山参的指纹图谱,对林下山参中多种成分进行定量分析,全面反映林下山参的现状,提高林下山参的质控水平。所以,本发明有效克服了现有技术中的种种缺点而具高度产业利用价值。上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属
技术领域:
中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1