一种减肥类中成药及食品中N-丁基-3-(三氟甲基)-α-甲基苯乙胺的检测方法与流程
本发明属于化学分析领域,涉及化学物质的色谱、质谱联用检测方法,具体涉及一种减肥类中成药及食品中n-丁基-3-(三氟甲基)-α-甲基苯乙胺的分析方法。
背景技术:
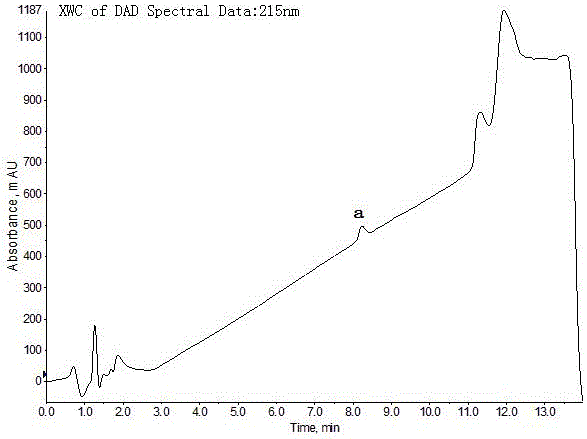
:芬氟拉明(n-乙基-α-甲基-3-三氟甲基苯乙胺)是一种苯丙胺类食欲抑制药,具有一定的中枢兴奋作用,能加强周围组织对葡萄糖的利用而降低血糖;还有降低胆固醇、三酰甘油、血浆总脂质的作用。所以,临床上常用于单纯性肥胖及伴有糖尿病、高血压、焦虑症、心血管疾病的肥胖患者。近年来,该药被不法商家添加进减肥类中成药或保健食品中,这种行为已违反了国家法律。目前,国家法定检验标准(国家药品监督管理局药品检验补充检验方法和检验项目批准件编号:2006004、食品中西布曲明等化合物的测定bjs201701)都已收载了芬氟拉明的检测方法,为禁用成分。n-丁基-3-(三氟甲基)-α-甲基苯乙胺(cas号:52742-18-4,分子式:c14h20f3n,分子量:259.1547)为芬氟拉明的修饰物(结构式见下),其与芬氟拉明具有相同的结构骨架,因而具有一定的减肥作用。不法分子为了躲避监管,往减肥中成药或食品中添加这种物质以达到增加销量,逃脱法律制裁的目的。日前在市售减肥类中成药中发现有添加这种成分,但尚无此物质的检验方法,本发明建立n-丁基-3-(三氟甲基)-α-甲基苯乙胺的快速筛查、定量方法,以填补监管漏洞。a:n-丁基-3-(三氟甲基)-α-甲基苯乙胺b:芬氟拉明技术实现要素:本发明的目的是提供一种针对减肥类中成药和食品中添加n-丁基-3-(三氟甲基)-α-甲基苯乙胺的检验方法,该方法的原理为:将供试品用甲醇提取稀释,c18色谱柱分离,经紫外光谱检测器和线性离子阱质谱仪检测,采集化合物的紫外吸收光谱,一级质谱离子、二级主要碎片离子进行定性确证,并采用mrm模式建立外标方法测定含量。本发明解决上述技术问题采用的技术方案为:一种减肥类中成药及食品中n-丁基-3-(三氟甲基)-α-甲基苯乙胺的检测方法,包括以下步骤:(1)测定条件:色谱条件:色谱柱:c18色谱柱,100mm/50mm×2.1mm,1.7μm/1.8μm;检测器:二极管阵列检测器、线性离子阱质谱仪;流动相:a-0.1%甲酸溶液、b-0.1%甲酸-甲醇;流速:0.2-0.6ml/min;柱温:25-40℃;进样量:0.1-10μl;洗脱梯度程序:0-1min,30%b;10-10.2min,75%-95%b;12-12.2min,95%-30%b;紫外检测波长:200-400nm;质谱条件:离子源:esi+;脱溶剂温度(℃):550;离子化电压(v):5500;喷雾气(psi):55;辅助加热气(psi):55;采集模式:mrm,ms2;气帘气:25;碰撞气:medium;化合物离子对参数:注:*定量离子对(2)精密称量n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品约10mg,置于100ml容量瓶中,用甲醇溶解稀释至刻度,作为对照品溶液一;再移取适量,用甲醇逐级稀释,配成浓度约为10ng/ml的对照品溶液二。(3)将供试品制成细粉(胶囊剂倾取内容物,片剂及固体食品研细),混合均匀,精密称取适量(固体中成药取用量为一次服用量,固体食品称取1g,液体样品直接移取1ml),置于100ml容量瓶中,加甲醇70ml,涡旋1min,室温水浴超声提取30min,静置,加甲醇定容至刻度,混匀,13000r/min离心5min,移取上清液,进样,测定。(4)采用超高效液相色谱-二极管阵列检测器-线性离子阱质谱法进行定性筛查,分别取空白溶液、供试品溶液和对照品溶液一,注入液质联用仪,采集色谱图,比对供试品与对照品的色谱峰保留时间及紫外吸收光谱,如果均一致,则将供试品溶液适当稀释,与空白溶液和对照品溶液二,注入液质联用仪,采集质谱图,比对一、二级质谱特征。结果判断:供试品色谱图中,如果出现与n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品保留时间一致的色谱峰,紫外吸收光谱都一致,且其质谱一级母离子,二级主要子离子质量数均相同,主要子离子的相对丰度比接近(满足下表1规定值),则确定添加了n-丁基-3-(三氟甲基)-α-甲基苯乙胺,则利用mrm模式建立标准曲线进行含量测定。如果未出现与n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品保留时间一致的色谱峰,或者出现了与n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品保留时间一致的色谱峰,但是不能同时满足紫外吸收光谱一致,质谱一级母离子,二级主要子离子质量数相同,主要子离子的相对丰度比接近(满足下表1规定值)的要求,则确定样品中没有添加n-丁基-3-(三氟甲基)-α-甲基苯乙胺,计算其检出浓度。表1定性确证时相对离子丰度的最大允许偏差相对离子丰度(%)k>50%50%≥k>20%20%≥k>10%k≤10%允许的最大偏差(%)±20±25±30±50检出浓度:按下表2中检出限,当称样量为1g(ml),稀释倍数为100时,检出浓度为:0.4μg/kg(l)。含量测定:线性范围:移取上述对照品溶液一,加甲醇稀释配制成最终浓度分别为0.1、0.5、1.0、5.0、10.0、50.0ng/ml的系列标准溶液,进样,采集质谱数据,以mrm定量离子对峰面积(y)对浓度(x)进行线性拟合,计算线性方程和相关系数(见表2)。结果显示在0.1-50ng/ml范围内,线性关系良好(r>0.999)。检出限:取浓度为0.1ng/ml对照品溶液用阴性样品提取液稀释10倍后进样测定,计算3倍信噪比时对应的浓度作为检出限,结果见表1。表2n-丁基-3-(三氟甲基)-α-甲基苯乙胺的线性范围、线性方程、相关系数、检出限准确度和精密度:以检测结果阴性的样品为基质,进行加标回收率测定。称取某阴性样品一次服用剂量置于100ml容量瓶中,分别加入n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照溶液(将对照品溶液一稀释成100ng/ml)1、5、10ml,各平行3份,加甲醇70ml,余下按步骤(3)中供试品溶液的制备,进样,测定,与相应浓度的对照品溶液比较,计算回收率(见表3)。精密度测定以浓度为10ng/ml的对照品溶液,连续进样6次,测定,计算待测物的色谱保留时间和定量离子对峰面积,计算其均值和相对标准偏差(rsd),结果可见精密度良好(见表4)。表3n-丁基-3-(三氟甲基)-α-甲基苯乙胺的回收率(n=3)浓度(ng/ml)平均回收率(%)rsd(%)1116.23.95104.11.910108.72.3表4n-丁基-3-(三氟甲基)-α-甲基苯乙胺的精密度(n=6)稳定性:取浓度为10ng/ml的对照品溶液置于自动进样器中(15℃),分别于0、2、4、8、12、24小时进样测定,计算组分的响应值,结果显示稳定性良好。进一步的,所述色谱柱为watersacquityhsst3,100mm×2.1mm,1.8μm。进一步的,所述步骤(3)中供试品为固体或液体剂型的中成药及食品。进一步的,所述供试品为固体型的中成药或食品的,取用时研至粒径≤180μm,所述供试品为中成药胶囊剂的,取用时倾取内容物。有益效果:1.本发明方法可准确鉴定减肥类中成药和食品中添加的n-丁基-3-(三氟甲基)-α-甲基苯乙胺;2.本发明方法主要适用于固体和液体剂型的中成药及食品中n-丁基-3-(三氟甲基)-α-甲基苯乙胺的测定;3.n-丁基-3-(三氟甲基)-α-甲基苯乙胺为制作减肥类中成药及食品中可能添加的化学物质,这种物质尚没有检测手段,通过本方法可以准确筛查,确证,为监管提供有力技术支撑。附图说明:图1为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为100μg/ml)的215nm色谱图(a:n-丁基-3-(三氟甲基)-α-甲基苯乙胺,下同)。图2为实施例中供试品溶液的215nm色谱图。图3为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为100μg/ml)的紫外吸收光谱图。图4为实施例1中供试品溶液的外吸收光谱图。图5为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的tic色谱图。图6为实施例1中供试品溶液的tic色谱图。图7为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的mrm(260.2/187.1)色谱图。图8为实施例中供试品溶液的mrm(260.2/187.1)色谱图。图9为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的mrm(260.2/159.1)色谱图。图10为实施例中供试品溶液的mrm(260.2/159.1)色谱图。图11为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的ms2质谱图(ce:20v)。图12为实施例1中供试品溶液的ms2质谱图(ce:20v)。图13为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的ms2质谱图(ce:25v)。图14为实施例1中供试品溶液的ms2质谱图(ce:25v)。图15为实施例中n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品溶液(浓度为10ng/ml)的ms2质谱图(ce:30v)。图16为实施例1中供试品溶液的ms2质谱图(ce:30v)。具体实施方式下面结合具体实施例对本发明做进一步的说明,下述具体实施例仅作为对本发明的解释性说明。仪器:shimadzulc-30a超高效液相色谱仪(shimadzu,japan);absciex6500+质谱仪(absciex,america);kq-300da型数据超声波清洗器(昆山超声仪器公司生产);milli-q纯水系统(millipore公司);metler-toledo电子天平(感量:0.01mg)。试剂:超纯水;甲醇和甲酸均为质谱纯;n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品(来源:trc)。实施例1一种减肥类中成药及食品中n-丁基-3-(三氟甲基)-α-甲基苯乙胺的检测方法,包括以下步骤:(1)检测条件:色谱柱:watersacquityhsst3,100mm×2.1mm,1.8μm;检测器:二极管阵列检测器、线性离子阱;流动相:a-0.1%甲酸溶液、b-0.1%甲酸-甲醇;流速:0.3ml/min;柱温:30℃;进样量:1μl;洗脱梯度程序:0-1min,30%b;10-10.2min,75%-95%b;12-12.2min,95%-30%b;紫外检测波长:200-400nm;质谱条件:离子源:esi+;脱溶剂温度(℃):550;离子化电压(v):5500;喷雾气(psi):55;辅助加热气(psi):55;采集模式:mrm,ms2;气帘气:25;碰撞气:medium;化合物离子对参数:注:*定量离子对(2)精密称量n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品约10mg,置于100ml容量瓶中,用甲醇溶解稀释至刻度,作为对照品溶液一;再移取适量,用甲醇逐级稀释,配成浓度约为10ng/ml的对照品溶液二。(3)将某批号的纤之素胶囊(黄色胶囊)20粒倾取内容物,混匀,精密称取一次服用量(约0.5g),置于100ml容量瓶中,加甲醇70ml,涡旋1min,室温水浴超声提取30min,静置,加甲醇定容至刻度,混匀,13000r/min离心5min,移取上清液,进样,测定。(4)采用超高效液相色谱-二极管阵列检测器-线性离子阱质谱法进行定性筛查,分别取空白溶液、供试品溶液和对照品溶液一,注入液质联用仪,采集色谱图及紫外吸收光谱;将供试品溶液适当稀释,与空白溶液和对照品溶液二,注入液质联用仪,采集质谱图,比对一、二级质谱特征。采集数据:比较步骤(2)和(3)采集的对照品溶液一和供试品溶液的液相色谱图,发现(3)在保留时间8.2min处显示有色谱峰,与n-丁基-3-(三氟甲基)-α-甲基苯乙胺对照品的保留时间及紫外光谱特征一致(见附图1-4)。将供试品溶液的稀释液与对照品溶液二比较发现:供试品溶液中n-丁基-3-(三氟甲基)-α-甲基苯乙胺保留时间一致处色谱峰对应的tic图、mrm图、ms2碎片均与对照品一致,且二级主要碎片的丰度比满足表1规定值(见附图5-16)。判断某批号的纤之素胶囊(黄色胶囊)中含有n-丁基-3-(三氟甲基)-α-甲基苯乙胺。按照步骤(3)中制备2份样品提取溶液,并根据其质谱响应适当稀释直至化合物浓度位于定量线性范围内,进样,采集数据,将响应信号代入拟合方程,计算出供试品中检出化合物的含量。结果:n-丁基-3-(三氟甲基)-α-甲基苯乙胺含量为41.6mg/g。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1