一种适于生物分子多重检测的成像系统的制作方法
1.本发明专利涉及生物检测领域,特别是涉及一种适于生物分子多重检测的成像系统。
背景技术:
2.目前光激化学发光的检测仪器,例如西门子的dimension exl analyzer、perkinelmer的multimode plate reader和北京科美的lica500全自动化学发光分析仪都只能检测整个均相溶液中的统一信号,无法对单个检测颗粒的信号进行检测,因此无法实现多重检测的功能。
技术实现要素:
3.鉴于以上所述现有技术的缺点,本发明的目的在于提供一种适于生物分子多重检测的成像系统。
4.本发明第一方面提供适于生物分子多重检测的成像系统,所述成像系统能够同时实现荧光和光激化学发光成像。
5.本发明第二方面提供适于生物分子多重检测的成像系统,所述成像系统至少包括第一光学路径和第二光学路径;所述第一光学路径为从激发光源至物镜,且所述激发光源和所述物镜之间设置有滤光片组,所述滤光片组被配置和布置为将从所述激发光源发出的激发光引导至所述物镜;所述第二光学路径为从所述物镜至图像采集装置,且所述物镜和所述图像采集装置之间设置有反光镜,所述反光镜被配置和布置为将由所述物镜接收到的荧光投射到所述图像采集装置;所述激发光源至少包括第一激发光源和第二激发光源,所述第一激发光源用于荧光信号的激发,所述第二激发光源用于光激化学发光信号的激发。
6.本发明第三方面提供前述适于生物分子多重检测的成像系统,在生物分子多重检测领域的应用。
7.本发明第四方面提供一种生物分子多重检测的成像方法,采用前述的适于生物分子多重检测的成像系统进行,至少包括如下步骤:
8.1)打开所述成像系统的第一激发光源,使激发光源的发出的光线通过滤光片组后,通过物镜到达样本并成像,获得样本的荧光图像;
9.2)切换至第二激发光源,使激发光源的发出的光线通过滤光片组后,通过物镜到达样本并成像,获得样本的光激化学发光图像。
10.本发明第五方面提供一种生物分子多重检测的图像分析方法,包括如下步骤:
11.s1根据光斑位置将检测液的荧光图像和光激化学发光图像进行匹配,以获得各光斑对应的荧光信号及光激化学发光信号,所述检测液的荧光图像和光激化学发光图像采用前述的生物分子多重检测的成像方法获得;
12.s2对荧光信号进行聚类分类,并获得各荧光信号对应的平均光激化学发光强度;
13.s3根据荧光信号的分类不同和平均光激化学发光强度,确定检测液中各待测分子
的含量。
14.本发明第六方面提供一种计算机可读存储介质,其上存储有计算机程序,该程序被处理器执行时实现前述的生物分子多重检测的图像分析方法的步骤。
15.如上所述,本发明的适于生物分子多重检测的成像系统,具有以下有益效果:
16.本发明首次将荧光成像和光激化学发光成像结合,可同时对荧光信号和光激化学发光信号进行检测,适用于多重光激化学发光检测。
附图说明
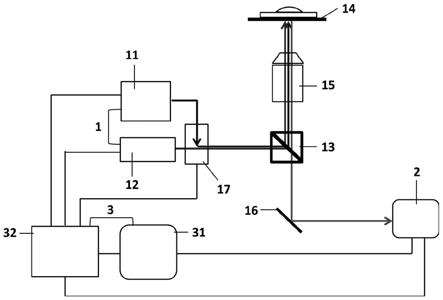
17.图1显示为本发明的适于生物分子多重检测的成像系统的示意图,图中箭头表示光线的传播方向。
18.图2显示为本发明的适于生物分子多重检测的成像系统用于多重光激化学发光得到图像。
19.图3显示为本发明的适于生物分子多重检测的成像系统用于多重光激化学发光图像分析的流程图。
20.图4显示为本发明的适于生物分子多重检测的成像系统图像分析软件用于多重光激化学发光图像的聚类分析结果,该结果显示了四种检测颗粒的荧光分类和相应的光激化学发光强度。
21.图5显示为本发明的成像系统的通讯关系图。
22.元件标号说明
[0023]1ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
激发光源
[0024]
11
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
第一激发光源
[0025]
12
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
第二激发光源
[0026]
13
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
滤光片组
[0027]
14
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
样本台
[0028]
15
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
物镜
[0029]
16
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
反光镜
[0030]
17
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
光源切换开关
[0031]2ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
图像采集装置
[0032]3ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
工作站
[0033]
31
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
控制中心
[0034]
32
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
触发控制盒
具体实施方式
[0035]
以下由特定的具体实施例说明本发明的实施方式,熟悉此技术的人士可由本说明书所揭露的内容轻易地了解本发明的其他优点及功效。
[0036]
请参阅图1至图5。须知,本说明书所附图式所绘示的结构、比例、大小等,均仅用以配合说明书所揭示的内容,以供熟悉此技术的人士了解与阅读,并非用以限定本发明可实施的限定条件,故不具技术上的实质意义,任何结构的修饰、比例关系的改变或大小的调整,在不影响本发明所能产生的功效及所能达成的目的下,均应仍落在本发明所揭示的技
术内容得能涵盖的范围内。同时,本说明书中所引用的如“上”、“下”、“左”、“右”、“中间”及“一”等的用语,亦仅为便于叙述的明了,而非用以限定本发明可实施的范围,其相对关系的改变或调整,在无实质变更技术内容下,当亦视为本发明可实施的范畴。
[0037]
本发明一实施例的适于生物分子多重检测的成像系统,所述成像系统能够同时实现荧光和光激化学发光成像。
[0038]
如图1所示,本发明的一实施例中的一种适于生物分子多重检测的成像系统,所述成像系统至少包括第一光学路径和第二光学路径;所述第一光学路径为从激发光源1至物镜15,且所述激发光源和所述物镜之间设置有滤光片组13,所述滤光片组13被配置和布置为将从所述激发光源发出的激发光引导至所述物镜;所述第二光学路径为从所述物镜15至图像采集装置2,且所述物镜15和所述图像采集装置2之间设置有反光镜16,所述反光镜16被配置和布置为将由所述物镜15接收到的荧光投射到所述图像采集装置2;所述激发光源1至少包括第一激发光源11和第二激发光源12,所述第一激发光源11用于荧光信号的激发,所述第二激发光源12用于光激化学发光信号的激发。
[0039]
所述成像系统能够同时实现荧光和光激化学发光成像。
[0040]
所述成像系统还包括样本台14所述样本台设于物镜上方,用于放置被观察对象。
[0041]
如图5所示,所述成像系统还包括工作站3和光源切换开关17,所述工作站与所述图像采集装置2通讯连接,所述光源切换开关17与所述激发光源1和所述工作站3通讯连接。
[0042]
所述通讯连接是指通过信号的传输交互,在连接的设备之间构成通讯。所述通讯连接包括有线连接和无线连接,例如可以为电讯号传输连接,数字讯号传输连接等。
[0043]
所述光源切换开关17能够切换激发光源1。
[0044]
如图5所示,所述工作站包括相互通讯连接的控制中心31和触发控制盒32,所述触发控制盒32与所述光源切换开关17、激发光源1以及图像采集装置2通讯连接,所述控制中心31与所述图像采集装置2通讯连接。
[0045]
所述控制中心31可以为计算机,所述计算机可用于搭载图像处理的程序,用于将带有编码功能的微载体信号激发后获得的图像与检测微粒信号激发后获得的图像进行匹配和信号分析。所述触发控制盒还可以搭载触发控制盒控制程序,用于控制触发控制盒。
[0046]
所述控制中心用于控制触发控制盒32,所述触发控制盒用于控制光源切换开关17、激发光源1的开闭以及图像采集装置2。
[0047]
控制中心31可以通过触发控制盒32直接控制激发光源1的开闭,也可以通过触发控制盒32,控制图像采集装置,从而实现激发光源的开闭。具体的,可以启动图像采集装置2,使图像采集装置产生ttl(晶体管-晶体管逻辑集成电路)信号并发送至触发控制盒,触发控制盒收到信号后立即发送ttl控制信号给激发光源1,进而能够控制激发光源1的开启。所述控制中心可通过控制光源切换开关的开闭实现第一激发光源11和第二激发光源12的切换。
[0048]
可选的,所述成像系统包括普通荧光成像模式和时间分辨荧光模式,所述普通荧光成像模式是指,激发光源发光与图像采集装置曝光同步;所述时间分辨荧光模式是指,所述激发光源与发光与图像采集装置曝光不同步。
[0049]
在一种实施方式中,可通过控制中心控制触发控制盒来实现两种荧光模式的切换。
[0050]
具体的,普通荧光成像模式为图像采集装置2开始曝光的同时激发光源打开,此时,可以设置激发光源的激发时间和相机曝光时间相同,启动图像采集装置2,使图像采集装置产生ttl(晶体管-晶体管逻辑集成电路)信号并发送至触发控制盒,触发控制盒收到信号后立即发送ttl控制信号给激发光源1,启动激发光源1,此时相机开始同步曝光,实现光源发光与图像采集装置曝光同步。
[0051]
时间分辨荧光成像模式为,控制中心通过触发控制盒控制激发光源打开,此时图像采集装置2曝光关闭。一段时间后激发光源关闭,此时图像采集装置2曝光再打开。此时,启动图像采集装置2,使图像采集装置产生ttl(晶体管-晶体管逻辑集成电路)信号并发送至触发控制盒,触发控制盒收到信号后,立即发送ttl控制信号给激发光源1,启动激发光源1,此时相机还未开始曝光;当设定的时间到达,激发光源关闭,此时相机再开始曝光,获得图像。这样可以进一步降低由激发光产生的背景噪音。时间分辨荧光功能可通过控制中心31上搭载的程序控制触发控制盒,进而实现时间分辨功能的打开或关闭。
[0052]
所述触发控制盒可以是常规的触发控制盒,例如fluoca的vv-trgbox触发控制盒。
[0053]
所述第一激发光源11可以是激光器、氙灯、汞灯、卤素灯或发光二极管中的一种或多种。
[0054]
所述第二激发光源12可以是激光器、氙灯、汞灯、卤素灯或发光二极管中的一种或多种。
[0055]
所述图像采集装置2可以为相机。
[0056]
所述图像采集装置2选自ccd、emccd、cmos或scmos中的一种或多种。
[0057]
所述滤光片组(13)至少包括第一滤光片组、第二滤光片组和第三滤光片组,各滤光片组均包括激发滤光片、发射滤光片和二向色镜。
[0058]
所述滤光片组13可拆卸。可根据不同激发和发射波长的荧光物质进行更换,或者根据不同光激化学发光微粒中填充的光敏剂种类和化学发光剂种类进行更换。
[0059]
所述滤光片组的数量可根据荧光物质的种类数量进行调整。
[0060]
在一种实施方式中,第一滤光片组为:激发滤光片488/15nm,二向色镜495nm长通,发射滤光片535/23nm.。
[0061]
在一种实施方式中,第二滤光片组为:激发滤光片488/15nm,二向色镜495nm长通,发射滤光片600/40nm。
[0062]
在一种实施方式中,第三滤光片组为:激发滤光片680/13nm,二向色镜653nm短通,发射滤光片615/20nm。
[0063]
所述滤光片组中,激发滤光片、二向色镜、发射滤光片依次排列。
[0064]
在一种实施方式中,所述二象色镜与激发光源产生的激发光的传播方向的夹角为45
°
。
[0065]
所述滤光片组中激发光源产生的激发光首先透过激发滤光片,再到达二向色镜表面,根据二向色镜本身的性质,在495nm以下波长的光被反射,495nm以上的光透射,故入射的激发光到达二向色镜后反射至物镜,而后传播至样本。样本被激发出的光信号经物镜后返回二向色镜,并透过二向色镜,而后透过发射滤光片,到达反光镜,被反光镜反射至图像采集装置。
[0066]
所述成像系统可实现荧光成像功能和光激化学发光成像功能。
①
荧光成像功能:
通过荧光照明光源经过第一滤光片组(激发滤光片488/15nm,二向色镜495nm长通,发射滤光片535/23nm)或第二滤光片组(激发滤光片488/15nm,二向色镜495nm长通,发射滤光片600/40nm)和物镜激发样本,样本产生的荧光信号再次通过物镜和第一滤光片组或第二滤光片组,最终被相机采集,产生两张荧光图像。
②
光激化学发光成像功能:由光激化学发光光源经过第三滤光片组(激发滤光片680/13nm,二向色镜653nm短通,发射滤光片615/20nm)和物镜激发样本,产生的光激化学发光信号再次经过物镜和第三滤光片组,最终被相机采集,产生光激化学发光图像。
[0067]
本发明所述工作台的控制中心可以根据需要安装不同的图像处理程序、触发控制盒控制程序。所述触发控制盒的控制程序只要知晓本发明的两种模式,本领域技术人员很容易即可实现。
[0068]
所述成像系统可通过的滤光片转盘切换三个滤光片组中的任意一个进入至成像光路。
[0069]
所述成像系统有两种成像模式,第一种为光激化学发光信号激发采用普通荧光模式,具体包括以下工作流程:
[0070]
步骤1:将样本置于样本台,对样本中的待测物进行对焦。
[0071]
步骤2:切换第一滤光片组进入成像光路,通过光源切换模块切换至荧光激发光源。关闭时间分辨荧光功能,设置相机曝光时间为200ms进行拍照,得到荧光图像1,如图2所示。
[0072]
步骤3:切换第二滤光片组进入成像光路,其他条件与步骤2相同,拍照得到荧光图像2,如图2所示。
[0073]
步骤4:切换第三滤光片组进入成像光路,通过光源切换模块切换至光激化学发光激发光源,关闭时间分辨荧光功能,设置光源激发时间为1000ms,相机曝光时间为1000ms。通过相机控制触发光源开关打开,此时相机同步开始曝光,1000ms后曝光结束,光源关闭,得到光激化学发光图像,如图2所示。
[0074]
第二种为光激化学发光信号激发采用时间分辨荧光模式具体包括以下工作流程:
[0075]
步骤1:将样本置于样本台,通过调节物镜和样本台间的距离的调焦旋钮对样本中的待测物进行对焦。
[0076]
步骤2:切换第一滤光片组进入成像光路,通过光源切换模块切换至荧光激发光源。关闭时间分辨荧光功能,设置相机曝光时间为200ms进行拍照,得到荧光图像1。
[0077]
步骤3:切换第二滤光片组进入成像光路,其他条件与步骤2相同,拍照得到荧光图像2。
[0078]
步骤4:切换第三滤光片组进入成像光路,通过光源切换模块切换至光激化学发光激发光源,打开时间分辨荧光功能,设置光源激发时间为500ms,相机曝光时间为1000ms。通过相机控制触发光源开关打开,此时相机曝光关闭;500ms后光源关闭,此时相机开始曝光,1000ms后曝光结束,得到光激化学发光图像。
[0079]
本发明一实施例的生物分子多重检测的成像方法,采用前述的适于生物分子多重检测的成像系统进行,至少包括如下步骤:
[0080]
1)打开所述成像系统的第一激发光源,使激发光源的发出的光线通过滤光片组后,通过物镜到达样本并成像,获得样本的荧光图像;
[0081]
2)切换至第二激发光源,使激发光源的发出的光线通过滤光片组后,通过物镜到达样本并成像,获得样本的光激化学发光图像。
[0082]
进一步的,所述成像方法还包括以下步骤:改变滤光片组的参数,重复步骤1),获得样本的多种荧光图像。
[0083]
所述样本的荧光图像和光激化学发光图像通过图像采集装置采集。
[0084]
在一种实施方式中,所述成像方法可以采用普通荧光模式或时间分辨荧光模式,其中,当采用时间分辨荧光模式时,步骤2)中,将成像系统至光激化学发光激发光源后,打开时间分辨荧光模式,获得样本的光激化学发光图像。具体的,可以参照前述的两种模式的工作流程。
[0085]
采用以上方法获得的图像可以在本发明所述成像系统的控制中心31进行分析处理。
[0086]
本发明一实施例的生物分子多重检测的图像分析方法,包括如下步骤:
[0087]
s1根据光斑位置将检测液的荧光图像和光激化学发光图像进行匹配,以获得各光斑对应的荧光信号及光激化学发光信号,所述检测液的荧光图像和光激化学发光图像采用前述的生物分子多重检测的成像方法获得;
[0088]
s2对荧光信号进行聚类分类,并获得各荧光信号对应的平均光激化学发光强度;
[0089]
s3根据荧光信号的分类不同和平均光激化学发光强度,确定检测液中各待测分子的含量。
[0090]
适用于上述分析方法的检测液为多重光激化学检测反应液。
[0091]
多重光激化学检测反应液为均相反应液,其反应物一般包括适于生物分子多重检测的检测颗粒、待测分子、和匹配微粒。待测分子与对应的检测颗粒及匹配微粒能形成复合物,复合物在激光照射下可发出光信号。
[0092]
多重光激化学检测反应液可在单个均相反应液中同时检测多个待测分子。
[0093]
待测分子可以是蛋白、小分子抗原或核酸。
[0094]
适于生物分子多重检测的检测颗粒,包括带有编码功能的微载体,微载体连接有检测微粒。
[0095]
所述带有编码功能的微载体可选自荧光编码微载体、拉曼信号编码微载体、光子晶体编码微载体或图案编码微载体中的一种或多种。
[0096]
检测微粒应适用于进行光激化学发光检测。检测微粒应当包括适用于光激化学发光检测的供体微粒(db)或受体微粒(ab)。其中,受体微粒能够发出荧光,供体微粒用于激发受体微粒发光。db内掺杂光敏剂,受光激发后能产生单线态氧。ab内掺杂化学发光剂和荧光剂,化学发光剂将单线态氧的能量转换成360nm发射光,激发荧光剂产生荧光。其中化学发光剂选自二氧杂环乙烯或二甲基噻吩中的一种或多种。
[0097]
检测微粒一般还应包括特异性的生物捕获物质,生物捕获物质包括但不限于生物捕获探针、抗原、抗体、protina、proting或链霉亲和素中的一种或多种。生物捕获物质可与供体微粒或受体微粒偶联。生物捕获物质可特异结合待测分子。
[0098]
匹配微粒为与检测颗粒中的检测微粒匹配的光激化学发光微粒。一般情况下,当检测微粒包括供体微粒时,匹配微粒应包括受体微粒;当检测微粒包括受体微粒时,匹配微粒应包供体微粒。
[0099]
匹配微粒一般还应包括检测物质,检测物质包括但不限于探针、抗原、抗体、protina、proting或链霉亲和素中的一种或多种。检测物质可与供体微粒或受体微粒偶联。检测物质不应直接结合检测颗粒,但可经待测分子与检测颗粒形成复合物。因此,检测物质应可特异结合待测分子,或者检测物质可经一中间结合物特异结合待测分子。
[0100]
当待测分子存在时,待测分子与对应的检测颗粒及匹配微粒形成复合物,在受到激光照射后,复合物中的db能激活周围环境中的氧转化为单线态氧,其生存时间仅为4微秒,短暂的生存时间决定了离子氧的传播直径很小(约为200nm),由于复合物中ab与db间距小于200nm,ab接受db产生的单线态氧而被激发出光信号。而当没有待测分子存在时,ab与db间距较远而无法激发出ab的光信号。
[0101]
多重光激化学检测反应液中应包括多种适于生物分子多重检测的检测颗粒,基于检测颗粒的编码不同,可发出不同荧光以区分不同的待测分子检测结果。和/或,也可基于待测分子与对应的检测颗粒及匹配微粒形成复合物的光激化学荧光差异以区分不同的待测分子检测结果。
[0102]
由于检测液中,各检测颗粒的位置相对静止,荧光图像的光斑来源于检测颗粒的编码物质和/或检测颗粒反应复合物,光激化学发光图像的光斑则来源于检测颗粒反应复合物,因此可以将荧光图像与光激化学发光图像中相同位置的光斑进行匹配,从而获得该位置检测颗粒或检测颗粒反应复合物对应的荧光信号和光激化学发光信号。进一步地通过对荧光信号聚类分类,获得各类荧光信号对应的平均光激化学发光强度。由于不同待测分子对应不同的荧光信号,因此可依据待测分子、荧光信号类别、与荧光信号对应地平均光激化学发光强度获知各待测分子对应的平均光激化学发光强度,进一步根据光激化学发光强度与浓度的对应关系获得各待测分子的含量。
[0103]
步骤s1中,可通过全局阈值化识别出光斑在图像中的位置,并根据光斑位置将检测液的荧光图像和光激化学发光图像进行匹配。
[0104]
可采集各种光信号参数表征荧光信号及光激化学发光信号,例如光斑的灰度值或者rgb值等。
[0105]
在一优选的实施方式中,在荧光图像和光激化学发光图像进行匹配前进行降噪,将荧光信号或光激化学发光信号和背景信号区分开。
[0106]
步骤s2中,可依据光信号表征值的不同对荧光信号进行聚类分类。可采用常规统计方法计算获得各荧光信号对应的平均光激化学发光强度。
[0107]
步骤s3中,具体的可包括下列步骤:
[0108]
依据待测分子与荧光信号类别的对应关系获得各待测分子对应的平均光激化学发光强度;
[0109]
依据各待测分子光激化学发光标准曲线及平均光激化学发光强度获得各待测分子的浓度。
[0110]
进一步的,本发明实施例还提供一种计算机可读存储介质,其上存储有计算机程序,该程序被处理器执行时实现前述方法的步骤。
[0111]
本领域普通技术人员可以理解:实现上述各方法实施例的全部或部分步骤可以通过计算机程序相关的硬件来完成。前述的计算机程序可以存储于一计算机可读存储介质中。该程序在执行时,执行包括上述各方法实施例的步骤;所述计算机可读存储介质可包
括,但不限于,软盘、光盘、cd-rom(只读光盘存储器)、磁光盘、rom(只读存储器)、ram(随机存取存储器)、eprom(可擦除可编程只读存储器)、eeprom(电可擦除可编程只读存储器)、磁卡或光卡、闪存、或适于存储机器可执行指令的其他类型的介质/机器可读介质。所述计算机可读存储介质可以是未接入计算机设备的产品,也可以是已接入计算机设备使用的部件。
[0112]
进一步的,本发明实施例中的控制中心31可以搭载图像分析软件以实现上述分析方法。
[0113]
在一个具体实施方式中,软件分析图像的流程包含图像预处理、共定位、灰度分析、聚类分析四个步骤。
①
图像预处理:对得到的荧光图像和光激化学发光图像进行降噪,将荧光信号或光激化学发光信号和背景信号区分开,并通过全局阈值化识别出信号在图像中的位置。
②
共定位:对荧光信号和光激化学发光信号在图像中的位置进行统一。
③
灰度分析:分别读取荧光信号和光激化学发光信号的灰度值。
④
聚类分析:对图像中不同位置的荧光信号依据灰度值的强弱进行聚类,得出不同分类,以此作为不同待测分子的类别。然后对不同荧光分类所在的光激化学发光信号的灰度值进行统计,以此得出不同类别待测分子的含量(浓度)水平。
[0114]
如图3所示,多重光激化学发光图像分析的流程:
[0115]
步骤1:图像输入。软件读取前述中得到的荧光图像和光激化学发光图像。
[0116]
步骤2:图像预处理。对得到的进行降噪,将荧光信号或光激化学发光信号和背景信号区分开,并通过全局阈值化识别出信号在图像中的位置。
[0117]
步骤3:共定位:对荧光信号和光激化学发光信号在图像中的位置进行统一。
[0118]
步骤4:灰度分析:分别读取荧光信号和光激化学发光信号的灰度值。
[0119]
步骤5:聚类分析:对图像中不同位置的荧光信号依据灰度值的强弱进行聚类,得出不同分类。然后对不同荧光分类所在的光激化学发光信号的灰度值进行统计,得出平均光激化学发光强度。
[0120]
步骤6:数据输出:将步骤5中得到的不同荧光分类与不同待测物的种类一一对应。再将不同荧光分类所在的平均光激化学发光强度代入相应待测物的标准曲线中,得到该待测物的实际含量(浓度)。
[0121]
图像分析软件用于多重光激化学发光图像的聚类分析结果如图4所示,该结果显示了四种检测颗粒的荧光分类和相应的光激化学发光强度。
[0122]
前述适于生物分子多重检测的系统可以用于在生物分子多重检测领域的应用。
[0123]
上述实施例仅例示性说明本发明的原理及其功效,而非用于限制本发明。任何熟悉此技术的人士皆可在不违背本发明的精神及范畴下,对上述实施例进行修饰或改变。因此,举凡所属技术领域中具有通常知识者在未脱离本发明所揭示的精神与技术思想下所完成的一切等效修饰或改变,仍应由本发明的权利要求所涵盖。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1