一种HPLC检测复方三维右旋泛酸钙糖浆B族维生素的方法与流程
本案是以申请日为2017-11-20,申请号为201711155001.3,名称为“一种检测复方三维右旋泛酸钙糖浆4种b族维生素的方法”的发明专利为母案而进行的分案申请。
本发明涉及复方三维右旋泛酸钙糖浆质量检测方法领域,具体涉及一种hplc检测复方三维右旋泛酸钙糖浆b族维生素的方法及其应用。
背景技术:
b族维生素是维护人体健康、促进生长发育和调节生理功能所必需的一类有机化合物,它在人体内无法自行合成,食物中含量也较低,必须额外补充。现代药理研究表明,维生素b1可用于脚气病、周围神经炎、消化不良等症状;维生素b2可促进肠道组织发育和细胞的再生,提高肠道吸收能力。维生素b6用于全胃肠道外营养及摄入不足所致营养不良,进行性体重下降时维生素b6的补充;烟酰胺与蛋白质的代谢及儿童智力发育关系密切,并在维持皮肤和消化器官正常功能中起着重要作用。另外,药理研究也表明配方中所含多种b族维生素能提高儿童味觉功能及提高胃黏膜消化功能,增进食欲,可有效治疗儿童厌食症。复方三维右旋泛酸钙糖浆,原名维他肥儿膏或维力膏,是一种临床上用于健脾胃的重要中西复方制剂,其主要成分包括维生素b1、维生素b2、维生素b6、烟酰胺等b族维生素和十味中药提取物混合的其主治功能为“补中益气,健脾止泻,消食导滞”;尤其适用于小儿营养不良及维生素缺乏症。复方三维右旋泛酸钙糖浆,在药品标准中的分类属于维生素类药品,其中4种b族维生素分别为维生素b1、维生素b2、维生素b6、烟酰胺添加量较高,也是其质量标准的检测指标。尽管现有技术中,关于复方三维右旋泛酸钙糖浆中b族维生素质量控制方法已有报道或者已有标准,但是这些方法均仅能测定1~2种维生素的含量,或者需用针对每种维生素采用多种不同方法来分别检测,难以全面反映复方三维右旋泛酸钙的b族质量,无法实现多种维生素的同时测定。
技术实现要素:
本发明所要解决的技术问题是:本发明提供一种高效液相色谱法(highperformanceliquidchromatography,hplc)法,可以实现以复方三维右旋泛酸钙糖浆及其中间体为背景的维生素b1、维生素b2、维生素b6、烟酰胺4种维生素同时测定的方法,为复方三维右旋泛酸钙糖浆的质量评价提供了新的技术手段。
为了解决上述技术问题,本发明采用的技术方案为:
一种hplc检测复方三维右旋泛酸钙糖浆b族维生素的方法,以乙腈为流动相a相,以含十二烷基硫酸钠的甲酸水溶液为流动相b相;取待测溶液进行hplc检测后,根据色谱图对维生素b1、维生素b2、维生素b6、烟酰胺4种维生素进行定性和/或定量分析;
所述hplc检测过程中采用梯度洗脱,洗脱程序为:
0~5min,流动相a相的体积分数为10%;
5~20min,流动相a相的体积分数由10%升至20%;
20~30min,流动相a相的体积分数由20%升至35%;
30~40min,流动相a相的体积分数由35%升至45%;
40~50min,流动相a相的体积分数由45%升至60%;
50~60min,流动相a相的体积分数由60%升至75%;
60~65min,流动相a相的体积分数为75%;
65~70min,流动相a相的体积分数由75%降至10%;
70~80min,流动相a相的体积分数为10%。
本发明的有益效果在于:本发明检测方法可同时实现维生素b1、维生素b2、维生素b6和烟酰胺的检测,采用本发明方法检测,操作简单,测定结果准确可靠。本发明检测方法不仅具有较高的精密度,还具有良好的重现性。采用本发明的洗脱梯度,可将四种维生素完全分开,分离度高,分离效果好。检测过程中,无需使用三乙胺,更加安全。本发明方法应用前景广泛,可以为复方三维右旋泛酸钙糖浆的开发和质量检测提供可靠的实验依据。
附图说明
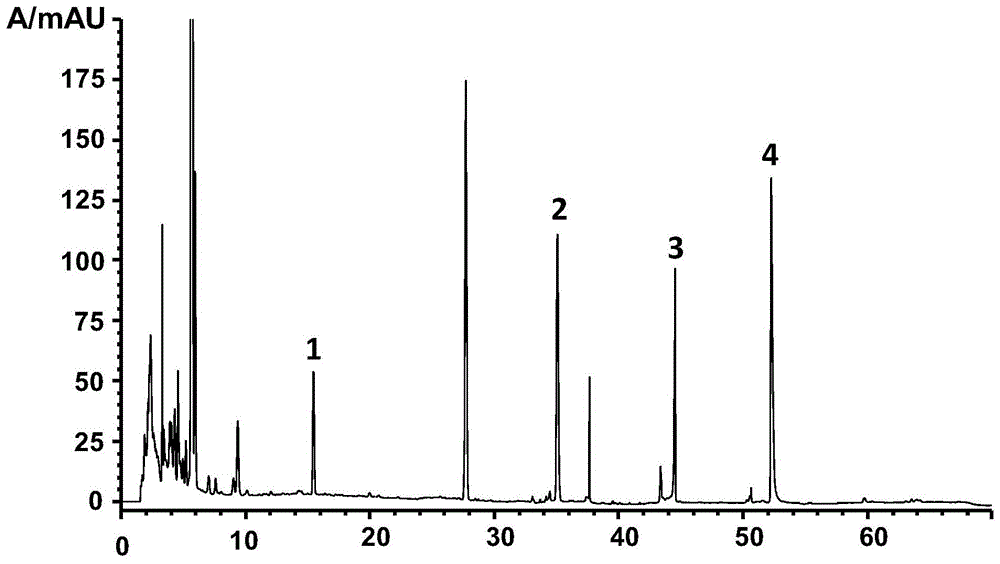
图1为本发明实施例1的hplc检测色谱图。
图2为本发明实施例2采用phenomenexlunac18色谱柱进行hplc检测的色谱图;
图3为本发明实施例2采用zorbaxbonus-rp色谱柱进行hplc检测的色谱图;
图4为本发明实施例2采用ultimatepolar-rp色谱柱进行hplc检测的色谱图;
图5为本发明实施例2采用zorbaxeclipsexdb-c18色谱柱进行hplc检测的色谱图;
图6为本发明实施例2采用watersx-selectcshc18色谱柱进行hplc检测的色谱图;
图7为本发明实施例2采用thermobetasilc18色谱柱进行hplc检测的色谱图;
图8为本发明实施例2采用甲醇作为流动相a相进行hplc检测的色谱图;
图9为本发明实施例2采用乙腈作为流动相a相进行hplc检测的色谱图;
图10为本发明实施例2采用5%乙腈作为起始流动相进行hplc检测的色谱图;
图11为本发明实施例2采用15%乙腈作为起始流动相进行hplc检测的色谱图;
图12为本发明实施例2采用10%乙腈作为起始流动相进行hplc检测的色谱图;
图13为本发明实施例2采用乙腈-乙酸乙酸铵水溶液作为流动相b相进行hplc检测的色谱图;
图14为本发明实施例2采用添加5mm己烷磺酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图15为本发明实施例2采用添加5mm庚烷磺酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图16为本发明实施例2采用添加5mm十二烷基硫酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图17为本发明实施例2采用添加1mm十二烷基硫酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图18为本发明实施例2采用添加2.5mm十二烷基硫酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图19为本发明实施例2采用添加5mm十二烷基硫酸钠的甲酸水溶液作为流动相b相进行hplc检测的色谱图;
图20为本发明实施例2采用添加5mm十二烷基硫酸钠的水溶液作为流动相b相进行hplc检测的色谱图;
图21为本发明实施例2采用添加5mm十二烷基硫酸钠的甲酸(0.01%)水溶液作为流动相b相进行hplc检测的色谱图;
图22为本发明实施例2采用添加5mm十二烷基硫酸钠的甲酸(0.03%)水溶液作为流动相b相进行hplc检测的色谱图;
图23为本发明实施例2采用添加5mm十二烷基硫酸钠的甲酸(0.05%)水溶液作为流动相b相进行hplc检测的色谱图;
图24为本发明实施例2为0.1%甲酸水溶液(ph=2)作为溶剂制备的样品进行hplc检测的色谱图;
图25为本发明实施例2为0.1%三乙胺(ph=6.5)水溶液作为溶剂制备的样品进行hplc检测的色谱图;
图26为本发明实施例2为10%甲醇(含0.05%甲酸)(ph=4)水溶液作为溶剂制备的样品进行hplc检测的色谱图;
图27为本发明实施例2在210nm波长下进行hplc检测的色谱图;
图28为本发明实施例2在230nm波长下进行hplc检测的色谱图;
图29为本发明实施例2在290nm波长下进行hplc检测的色谱图;
图30为本发明实施例2在320nm波长下进行hplc检测的色谱图;
图31为本发明实施例2在360nm波长下进行hplc检测的色谱图;
图32为本发明实施例2在260nm波长下进行hplc检测的色谱图。
标号说明:
1、维生素b2;2、烟酰胺;3、维生素b6;4、维生素b1。
具体实施方式
为详细说明本发明的技术内容、所实现目的及效果,以下结合实施方式并配合附图予以说明。
本发明最关键的构思在于:通过本发明hplc梯度洗脱程序将维生素b1、维生素b2、维生素b6和烟酰胺完全分离开来,进而实现对复方三维右旋泛酸钙糖浆中的维生素b14、维生素b2、维生素b63和烟酰胺进行定性和/或定量分析。
一种hplc检测复方三维右旋泛酸钙糖浆b族维生素的方法,以乙腈为流动相a相,以含十二烷基硫酸钠的甲酸水溶液为流动相b相;取待测溶液进行hplc检测后,根据色谱图对维生素b1、维生素b2、维生素b6、烟酰胺4种维生素进行定性和/或定量分析;
所述hplc检测过程中采用梯度洗脱,洗脱程序为:
0~5min,流动相a相的体积分数为10%;
5~20min,流动相a相的体积分数由10%升至20%;
20~30min,流动相a相的体积分数由20%升至35%;
30~40min,流动相a相的体积分数由35%升至45%;
40~50min,流动相a相的体积分数由45%升至60%;
50~60min,流动相a相的体积分数由60%升至75%;
60~65min,流动相a相的体积分数为75%;
65~70min,流动相a相的体积分数由75%降至10%;
70~80min,流动相a相的体积分数为10%。
从上述描述可知,本发明的有益效果在于:本发明检测方法可同时实现维生素b1、维生素b2、维生素b6和烟酰胺的检测,采用本发明方法检测,操作简单,测定结果准确可靠。本发明检测方法不仅具有较高的精密度,还具有良好的重现性。采用本发明的洗脱梯度,可将四种维生素完全分开,分离度高,分离效果好。检测过程中,无需使用三乙胺,更加安全。本发明方法应用前景广泛,可以为复方三维右旋泛酸钙糖浆的开发和质量检测提供可靠的实验依据。
所述维生素b1的结构式为:
进一步地,所述流动相b相中,甲酸的体积分数为0.5%。
进一步地,所述流动相b相中,十二烷基硫酸钠的浓度为1~5mmol/l,优选为5mmol/l。
从上述描述可知,本发明的有益效果在于:添加不同浓度的十二烷基硫酸钠均可将四种b族维生素分离开来,添加5mm的十二烷基硫酸钠时效果最佳。
优选地,所述hplc检测过程中,采用的流速为0.8~1.0ml·min-1。
进一步地,所述hplc检测过程中,采用的色谱柱为c18色谱柱,尺寸为4.6mm×250mm,5μm,优选地,所述c18色谱柱为betasilc18色谱柱,更优选地,所述c18色谱柱为thermobetasilc18色谱柱。
从上述描述可知,本发明的有益效果在于:thermobetasilc18(250*4.6mm,5μm)测定的结果中色谱峰容量多,分离度最好。
优选地,所述hplc检测过程中,采用的色谱柱柱温为25~35℃,优选为30℃。
进一步地,所述hplc检测过程中,采用的检测波长为230~290nm,优选为250~270nm,更优选为260nm。
优选地,所述hplc检测过程中,进样量为1~20μl,优选为20μl。
进一步地,所述检测方法还包括保留时间测定及标准曲线绘制步骤:以维生素b1、维生素b2、维生素b6和烟酰胺四种维生素对照品标准溶液,利用所述洗脱程序测定保留时间,并绘制维生素浓度与峰面积对应的标准曲线。
进一步地,所述待测溶液经过以下步骤制得:取待测样品,精密称定后,加入含体积分数为0.01~0.05%甲酸的10%甲醇水溶液溶解,配制成溶液后,过0.45μm滤膜,取续滤液。优选地,所述甲酸体积分数为0.05%。进一步地,所述待测样品为复方三维泛酸钙糖浆。
优选地,所述待测溶液经过以下步骤制得:取复方三维泛酸钙糖浆,精密称定后,加入含体积分数为0.01~0.05%甲酸的10%甲醇水溶液溶解,配制成0.18~0.22g/ml的溶液后,过0.45μm滤膜,取续滤液。优选地,所述甲酸体积分数为0.05%。
从上述描述可知,本发明的有益效果在于:添加甲酸的溶剂更利于将样品中的四种b族维生素分离开来,而添加体积分数为0.5%甲酸(ph=4)溶剂的样品分离效果则远优于添加体积分数为0.1%甲酸(ph=2)的溶剂。
优选地,所述待测溶液经过以下步骤制得:取复方三维泛酸钙糖浆5g,精密称定后,加入含0.05%甲酸的10%甲醇水溶液10ml,振摇20min,移入25ml容量瓶,润洗定容后,摇匀后过0.45μm滤膜,取续滤液。
本发明的实施例一为:一种hplc检测复方三维右旋泛酸钙糖浆b族维生素的方法具体操作过程及实验条件如下:
1、仪器与试药
1260型高效液相色谱仪(美国安捷伦公司);cpa225d型十万分之一分析天平(德国sartorius公司);kq-500e台式超声波清洗器(昆山市超声仪器有限公司);乙腈、甲酸为色谱纯(德国merck公司);milli-q超纯水仪(美国millipore公司)。
对照品维生素b1(批号:100390-201505,含量为97.0%)、维生素b2(批号:100369-201504,含量为98.2%)、维生素b6(批号:100116-201404,含量为100%)和烟酰胺(批号:100115-201604,含量为99.9%)均购自中国食品药品检定研究院。10个批次复方三维右旋泛酸钙糖浆均来源于国药控股星鲨制药(厦门)有限公司,测定过程中随意从其中选取了一支糖浆进行实验。
2、方法与结果
2.1溶液的制备
2.1.1对照品溶液
精密称取维生素b1、维生素b2、维生素b6和烟酰胺的对照品适量,共同置于同一量瓶中,用10%甲醇水(含0.05%甲酸)溶解并稀释到刻度,摇匀,分别得到质量浓度为28.8、5.8、8.6、28.8μg·ml-1的混合对照品溶液。
2.1.2待测溶液制备
取复方三维右旋泛酸钙糖浆5g,精密称定为5.0011g,置于具塞锥形瓶中,加10%甲醇水(含0.05%甲酸)10ml,超声或振荡溶解20分钟,移入25ml量瓶,锥形瓶用10%甲醇水(含0.05%甲酸)润洗3次,洗液并入量瓶中,加水稀释至刻度,摇匀,过0.45μm滤膜,取续滤液,即得。
2.2待测溶液及对照品溶液的检测
色谱条件:色谱柱:thermobetasilc18analytical(4.6mm×250mm,5μm);流动相:乙腈(a)-5mm十二烷基硫酸钠(含0.05%甲酸)水(b)溶液,梯度洗脱(0~5min,10%a→10%a;5~20min,10%a→20%a;20~30min,20%a→35%a;30~40min,35%a→45%a;40~50min,45%a→60%a;50~60min,60%a→75%a;60~65min,75%a→75%a;65~70min,75%a→10%a;70~80min,10%a→10%a);流速:1.0ml·min-1;检测波长:260nm;柱温:30℃;进样量:20μl,测定结果如图1所示,从图1中可以看出,采用本发明方案方法可将维生素b1、维生素b2、维生素b6和烟酰胺彻底分离开来,各物质的色谱峰峰型尖锐且对称,几乎无拖尾,半峰宽小于0.2,基线稳定基本无漂移且噪音小,分离度可达1.8以上。
本发明实施例2为不同检测条件下的实验分析:
1色谱条件实验分析
(1)不同型号色谱柱实验
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:色谱柱的型号不同,分别为phenomenexlunac18(250*4.6mm,5μm),zorbaxbonus-rp(250*4.6mm,5μm)、ultimatepolar-rp(250*4.6mm,5μm)、zorbaxeclipsexdb-c18(4.6*250mm,5μm)、watersxselectcshc18(4.6*250mm,5μm)、测定结果如图2~6所示。其中,phenomenexlunac18(250*4.6mm,5μm)的测定结果如图2所示,zorbaxbonus-rp(250*4.6mm,5μm)的测定结果如图3所示、ultimatepolar-rp(250*4.6mm,5μm)的测定结果如图4所示、zorbaxeclipsexdb-c18(4.6*250mm,5μm)的测定结果如图5所示、watersxselectcshc18(4.6*250mm,5μm)的测定结果如图6所示。
实验组部分,则完全与实施例1相同,测定结果如图7所示,对比图2~7可知,thermobetasilc18(250*4.6mm,5μm)测定的结果图1中峰容量多,分离度最好。
(2)不同有机相体系的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:流动相a相为甲醇,其他条件均与实施例1相同,测定结果如图8所示。
实验组部分,则完全与实施例1相同,测定结果如图9所示,对照图8和9可知,使用乙腈体系峰容量最佳,色谱分离度和峰型均远优于甲醇体系。
(3)不同起始流动相中乙腈浓度的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:流动相a相的起始浓度不同,分别为5%和15%,测定结果分别如图10和11所示。
实验组部分,则完全与实施例1相同,测定结果如图12所示,对照图10~12可知,10%乙腈作为起始比例色谱分离度较好,优于其他浓度。
(4)不同类型流动相b相的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:将水中分别添加有0.05%乙酸-5mm乙酸铵、5mm己烷磺酸钠(含0.05%甲酸)和5mm庚烷磺酸钠(含0.05%甲酸)作为流动相b相,测定结果分别如图13、14和15所示。
实验组部分,则完全与实施例1相同,测定结果如图16所示。对照图13~16可知,说明十二烷基硫酸钠优于其他类型酸水盐溶液,其中,从图13中可以看出,添加有己烷磺酸钠的溶液中烟酰胺的保留时间大大提前到溶剂峰范围内,难以分离开来,且维生素b6的信号极弱,因此,己烷磺酸钠完全不能满足本样品的分析。此外,添加乙酸的实验中,则只能检测到维生素b2及烟酰胺的信号,而添加庚烷磺酸钠的实验中,虽能检测到四种信号,但维生素b2与维生素b6则无法分离。
(5)添加有不同浓度十二烷基硫酸钠的流动相b相的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:流动相b相中十二烷基硫酸钠的浓度为1mm或2.5mm,其中,1mm十二烷基硫酸钠的实验测定结果如图17所示,1mm十二烷基硫酸钠的实验测定结果如图18所示。
实验组部分,则完全与实施例1相同,测定结果如图19所示。对照图17~19可知,添加不同浓度的十二烷基硫酸钠基本可将四种b族维生素分离开来,但添加1mm十二烷基硫酸钠时,维生素b1会出现轻微拖尾现象,而添加2.5mm十二烷基硫酸钠时,维生素b1会出现分叉的现象,因此,添加5mm的十二烷基硫酸钠时效果最佳。
(6)添加有不同浓度甲酸的流动相b相的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:流动相b相中添加有体积分数为0%、0.01%和0.03%的甲酸,其中,添加体积分数为0%的甲酸的流动相b相的测定结果如图20所示,添加体积分数为0.01%的甲酸的流动相b相的测定结果如图21所示,添加体积分数为0.03%的甲酸的流动相b相的测定结果如图22所示。
实验组部分,则完全与实施例1相同,测定结果如图23所示。对比图20~23发现,未添加甲酸的流动相b相测定时,维生素b2会的保留时间也同样提前到了溶剂峰的出峰时间,维生素b6则完全无法检测出来;添加有甲酸的流动相b相检测时,均能将4种维生素同时检测出来,且基本能分离开来,其中添加体积分数为0.05%的甲酸的流动相b相的分离效果最佳。
2、供测样品溶液溶剂实验分析:
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:在10%甲醇水溶液中添加体积分数为0.1%甲酸(ph=2)或在10%甲醇水溶液中添加体积分数为0.1%三乙胺(ph=6.5),其测定结果分别如图24和25所示。
实验组部分,则完全与实施例1相同,测定结果如图26所示。对比图24~26发现,虽然添加三乙胺时4种维生素也均能有信号,但维生素b6几乎无法分离出来。而添加甲酸的则可使四种b族维生素分离开来,而添加体积分数为0.5%甲酸(ph=4)的溶剂分离效果则远优于添加体积分数为0.1%甲酸(ph=2)的溶剂。
3、不同检测波长的实验分析
本组实验包括对照组部分和实验组部分,对照组和实验组采用由同一份待测样品进行进样测定。其中,对照组部分与实施例1的区别在于:检测波长分别为210nm、230nm、290nm、320nm或360nm,其测定结果依次如图27~31所示。
实验组部分,则完全与实施例1相同,测定结果如图32所示。对比图27~32发现,采用210nm或230nm作为检测波长时,基线漂移严重,其中210nm波长下,维生素b2的响应极低。290nm波长下,则信号较弱,而320nm或360nm时,则会出现烟酰胺和维生素b1信号极弱,而采用260nm的波长检测,则基线平稳。
本发明实施例3为方法精密度及准确性实验分析:
1、精密度试验:操作步骤与实施例一完全相同,精密吸取对照品溶液20μl,连续进样6次,测定检测方法的精密度,检测结果如表1所示。
表1精密度试验结果表
从表1中可以看出,采用本方法进行测定时,测定的4种维生素的rsd均小于0.5%,表明本发明方法精密度良好。
2、准确度试验:操作步骤与实施例一完全相同,进行进样分析,根据对照品浓度和峰面积的外标一点法计算其含量,并按照样品测定结果进行低、中、高三个水平的对照品添加,计算回收率表示准确度,结果如表2所示,表2为低、中、高三个水平的加样回收率结果表。
表2低、中、高三个水平的加样回收率结果
从表2可以看出,采用本发明检测方法,b族维生素标准品的加标回率在96~101%之间,说明本发明检测方法准确度高。
综上所述,本发明提供一种hplc检测复方三维右旋泛酸钙糖浆b族维生素的方法,通过hplc法实现快速定性鉴定和/或定量检测复方三维右旋泛酸钙糖浆中4种维生素(维生素b21、烟酰胺2、维生素b6和维生素b1),为复方三维右旋泛酸钙糖浆开发利用和质量评价提供了可靠的实验依据。
以上所述仅为本发明的实施例,并非因此限制本发明的专利范围,凡是利用本发明说明书及附图内容所作的等同变换,或直接或间接运用在相关的技术领域,均同理包括在本发明的专利保护范围内。
- 还没有人留言评论。精彩留言会获得点赞!