用于诊断髓母细胞瘤的尿液蛋白标记物及其用途
1.本发明涉及临床诊断的技术领域。具体地,本发明涉及用于诊断髓母细胞瘤的尿液蛋白标记物。具体而言,本发明涉及利用质谱分析蛋白组学技术获得的与人,特别是儿童髓母细胞瘤相关的尿液蛋白标志物及其用途。
背景技术:
2.髓母细胞瘤(medulloblastoma,mb)是一种多发于儿童的恶性脑肿瘤,约占儿童恶性脑肿瘤的30%。该肿瘤临床进展较快,且极易复发,约75%的患儿在术后2年内出现肿瘤的复发[参见,a.y.minn,b.h.pollock,l.garzarella,g.v.dahl,l.e.kun,j.m.ducore,a.shibata,j.kepner,p.g.fisher,surveillance neuroimaging to detect relapse in childhood brain tumors:a pediatric oncology group study,j.clin.oncol.19(2001)4135
–
4140.https://doi.org/10.1200/jco.2001.19.21.4135]。头痛、恶心呕吐是其最常见的首发症状[参见,s.wilne,j.collier,c.kennedy,a.jenkins,j.grout,s.mackie,k.koller,r.grundy,d.walker,progression from first symptom to diagnosis in childhood brain tumours,eur.j.pediatr.171(2012)87
–
93.https://doi.org/10.1007/s00431-011-1485-7],但是这些症状对于儿童来说并不具备特征性,早期常被基层医院误诊为“感冒,肠炎”。
[0003]
核磁共振成像(magnetic resonance imaging,mri)是诊断该肿瘤的主要方法,并且用于术后的影像学监测。为取得质量较高的成像,年龄较小的患儿常需要服用镇定剂,这样就使患儿面临着气道阻塞、误吸、缺氧甚至死亡的风险,因此mri对于患儿来说不易实施。基于以上原因,该疾病在儿童中常出现漏诊及误诊。
[0004]
目前并没有可靠的生物标志物(biomarker)来用于临床上筛查及术后的监测。因此,对于儿童来说,通过无创性方法取得的样本,从中探寻可用于临床上早期筛查及术后监测的生物标志物具有很高的研究价值。
[0005]
为快速探寻肿瘤的特异性生物标志物,基于质谱检测的蛋白组学分析是一种非常有效的方法。该方法已成功的用于检测多种体液的蛋白质组构型[参见,c.zhang,w.leng,c.sun,t.lu,z.chen,x.men,y.wang,g.wang,b.zhen,j.qin,urine proteome profiling predicts lung cancer from control cases and other tumors,ebiomedicine.30(2018)120
–
128.https://doi.org/10.1016/j.ebiom.2018.03.009;和m.frantzi,j.metzger,r.e.banks,h.husi,j.klein,m.dakna,w.mullen,j.j.cartledge,j.p.schanstra,k.brand,m.a.kuczyk,h.mischak,a.vlahou,d.theodorescu,a.s.merseburger,discovery and validation of urinary biomarkers for detection of renal cell carcinoma,j proteomics.98(2014)44
–
58.https://doi.org/10.1016/j.jprot.2013.12.010]。脑脊液、血液及尿液是常用于进行蛋白组学分析的重要体液。对于患儿来说腰穿难以实施,患者及家属的依从性较差。因此,通过这种有创的方式获取患儿的脑脊液难度大,可能会限制该体液检测的临床应用。而血液中蛋白质的异质性、浓度的较大
动态波动及蛋白质组构型的快速变化,使血液用于蛋白质组学分析成为一项艰巨的任务。相比较而言,尿液可以通过无创的方式多次、大量的获取,非常有利于通过质谱检测分析疾病的特异性生物标志物。已有研究表明尿液中含有与肿瘤相关的生物标志物,并可对疗效进行长期监测[参见,m.an,y.gao,urinary biomarkers of brain diseases,genomics proteomics bioinformatics.13(2015)345
–
354.https://doi.org/10.1016/j.gpb.2015.08.005]。此外,尿液中成分的较大波动可能更能反应人体的变化[参见,m.li,m.zhao,y.gao,changes of proteins induced by anticoagulants can be more sensitively detected in urine than in plasma,sci china life sci.57(2014)649
–
656.https://doi.org/10.1007/s11427-014-4661-y]。因此,有学者认为,相较于血浆而言,尿液是一种更好的、更为敏感的、可用于检测生物标志物的体液样本[参见,e.r.smith,d.zurakowski,a.saad,r.m.scott,m.a.moses,urinary biomarkers predict brain tumor presence and response to therapy,clin.cancer res.14(2008)2378
–
2386.https://doi.org/10.1158/1078-0432.ccr-07-1253]。尽管,目前有很多关于尿液的蛋白组学研究,但尚没有关于与儿童髓母细胞瘤相关的尿液蛋白质组或生物标志物的报道。
[0006]
为了寻找能够快速、方便、可靠地诊断儿童髓母细胞瘤特异性的生物标志物,本发明人使用正常儿童尿液、髓母细胞瘤患者术前及术后尿液来进行质谱分析,进而找到与该肿瘤相关的尿液蛋白组学标记物。
技术实现要素:
[0007]
一方面,本发明提供了检测受试者尿液中蛋白质含量的试剂在制备用于诊断和/或预后所述受试者中髓母细胞瘤的试剂中的用途,其中所述尿液中蛋白质选自以下一种或多种:cadh1、fibb、fgfr4、a1bg、1433b、vsig4、lyve1、kvd28、gels、pgrp1、lv321、sap3、iglc2、pcoc2、ggt6、ogfd3和lirb4;优选地,其中所述受试者为人受试者;更优选地,其中所述受试者为年龄为0-16岁的儿童受试者。
[0008]
在本发明的一个优选的实施方案中,所述cadh1具有如seq id no:10-13中任一项所示的氨基酸序列,或者由seq id no:10-13中任一项所示的氨基酸序列组成;
[0009]
在进一步优选的实施方案中,所述fibb具有如seq id no:4所示的氨基酸序列,或者由seq id no:4所示的氨基酸序列组成;
[0010]
进一步优选地,所述fgfr4具有如seq id no:15所示的氨基酸序列,或者由seq id no:15所示的氨基酸序列组成;
[0011]
优选地,所述a1bg具有如seq id no:5-6中任一项所示的氨基酸序列,或者由seq id no:5-6中任一项所示的氨基酸序列组成;所述1433b具有如seq id no:16所示的氨基酸序列,或者由seq id no:16所示的氨基酸序列组成;所述vsig4具有如seq id no:22-23中任一项所示的氨基酸序列,或者由seq id no:22-23中任一项所示的氨基酸序列组成;所述lyve1具有如seq id no:24-25中任一项所示的氨基酸序列,或者由seq id no:24-25中任一项所示的氨基酸序列组成;所述kvd28具有如seq id no:3所示的氨基酸序列,或者由seq id no:3所示的氨基酸序列组成;所述gels具有如seq id no:7-8中任一项所示的氨基酸序列,或者由seq id no:7-8中任一项所示的氨基酸序列组成;所述pgrp1具有如seq id no:
1-2中任一项所示的氨基酸序列,或者由seq id no:1-2中任一项所示的氨基酸序列组成;所述lv321具有如seq id no:17所示的氨基酸序列,或者由seq id no:17所示的氨基酸序列组成;所述sap3具有如seq id no:14所示的氨基酸序列,或者由seq id no:14所示的氨基酸序列组成;所述iglc2具有如seq id no:9所示的氨基酸序列,或者由seq id no:9所示的氨基酸序列组成;所述pcoc2具有如seq id no:21所示的氨基酸序列,或者由seq id no:21所示的氨基酸序列组成;所述ggt6具有如seq id no:18所示的氨基酸序列,或者由seq id no:18所示的氨基酸序列组成;所述ogfd3具有如seq id no:19所示的氨基酸序列,或者由seq id no:19所示的氨基酸序列组成;所述lirb4具有如seq id no:20所示的氨基酸序列,或者由seq id no:20所示的氨基酸序列组成。
[0012]
另一方面,本发明提供了诊断和/或预后受试者中髓母细胞瘤的方法,所述方法包括检测受试者尿液中选自以下一种或多种尿蛋白的含量:1433b、a1bg、vsig4、lyve1、kvd28、gels、pgrp1、lv321、sap3、iglc2、fgfr4、pcoc2、cadh1、ggt6、ogfd3、lirb4和fibb;
[0013]
其中与健康对照组或非肿瘤神经系统疾病对照组相比,所述受试者治疗前尿液中蛋白的含量增加或降低,优选地,大于或等于1.3倍;指示所述受试者患有髓母细胞瘤;和/或
[0014]
诊断患有髓母细胞瘤的受试者在治疗(包括但不限于手术、放疗和/或化疗)后,所述受试者尿液中尿蛋白的含量恢复,则所述受试者的预后良好;优选地,所述受试者尿液中蛋白含量的恢复是指治疗后与治疗前相比,尿蛋白含量的增加或降低大于或等于1.2倍;优先地,所述非肿瘤神经系统疾病包括但不限于癫痫、先天性畸形和其他神经疾病,肿瘤或神经系统感染除外。
[0015]
另一方面,本发明提供了检测受试者尿液中蛋白质含量的试剂在制备用于诊断和/或预后所述受试者中髓母细胞瘤的试剂中的用途,其中所述尿液中蛋白质为cadh1和fibb的组合;优选地,其中所述尿液中蛋白质进一步包括fgfr4;更优选地,所述尿液中蛋白质进一步包括1433b、a1bg、vsig4、lyve1、kvd28、gels、pgrp1、lv321、sap3、iglc2、pcoc2、ggt6、ogfd3和lirb4中的一种或多种。
[0016]
根据以上所述的本发明的方法或用途,其中所述检测受试者尿液中蛋白质含量的试剂是质谱鉴定试剂、抗体或其抗原结合片段;优选地,所述检测受试者尿液中蛋白质含量的试剂是单克隆抗体。
[0017]
另一方面,本发明提供了一种用于诊断和/或预后髓母细胞瘤的试剂盒或芯片,其包含检测受试者尿液中蛋白质含量的试剂,其中所述尿液中蛋白质为以下蛋白质的组合:1433b、a1bg、vsig4、lyve1、kvd28、gels、pgrp1、lv321、sap3、iglc2、fgfr4、pcoc2、cadh1、ggt6、ogfd3、lirb4和fibb。
[0018]
虽然可使用与本文所述类似或相同的任何方法和材料来实施或测试本发明,但是以下描述优选的方法和材料。通过说明书和权利要求书,本发明的其他特点、目的和优点将是显而易见的。在说明书和权利要求书中,除非上下文中有清楚的另外指明,单数形式包括复数指代物的情况。除非另有定义,本文使用的所有技术和科学术语都具有本发明所属领域普通技术人员所理解的一般含义。说明书中引用的所有专利和出版物都通过引用纳入。提出以下实施例是为了更全面地说明本发明的优选实施方式。这些实施例不应以任何方式理解为限制本发明的范围,本发明的范围由权利要求书限定。
[0019]
术语
[0020]
如本文所用,术语“髓母细胞瘤(medulloblastoma,mb)”是儿童最常见的恶性脑肿瘤(who iv级)。其诊断的高峰年龄约为6-8岁,但仍有些患者可能在出生后第一年或成年期出现髓母细胞瘤。组织形态学上,髓母细胞瘤是位于小脑的一种胚胎性肿瘤,其可能起源于生命早期不同的神经干细胞或前体细胞。
[0021]
髓母细胞瘤许多关键的基因事件已被确定。高水平myc基因扩增是第一个被报道的基因水平上的改变。myc现被认为是髓母细胞瘤中最常见的突变和最具特征的肿瘤基因。当前的治疗方式对伴随myc扩增髓母细胞瘤的患儿普遍效果不佳。从易患髓母细胞瘤的家族性肿瘤综合征(即gorlin综合征和家族性腺瘤性息肉病(fap))中获得的信息,为涉及髓母细胞瘤发病机制的基因和通路提供了早期线索。如,ptch1或sufu(shh信号通路的负调节因子)中的胚系突变易患gorlin综合征,并且这两种基因在胚系和体细胞中均存在突变,证实了shh信号在某些髓母细胞瘤患者中的重要作用。此外,约1%的患者存在apc胚系突变(易患fap),约7%的患者存在ctnnb1体细胞突变,因此wnt信号传导缺陷与髓母细胞瘤发病有关1。
[0022]
如本文所用,术语“蛋白质组学(proteomics)”是继“基因组”后发展迅速的“组学”技术,其与代谢组学、基因组学构成了系统生物学的主体,从而可以帮助人类从基因、蛋白质和代谢产物等方面综合、多维地认识疾病。
[0023]
蛋白质组学是对生物体、器官、组织、细胞或细胞器在某一特定时期内所含的全部蛋白质组分表达情况进行研究和描述。比较蛋白质组学是研究生物体不同状态下蛋白质表达水平的动态变化,以期发现关键的调控分子及与疾病相关的蛋白质标志物,最终可为疾病的防诊治等提供理论依据。因此需要对蛋白质进行定量分析,这样定量蛋白组学技术便逐渐发展起来。目前,最常用的技术包括lc-ms/ms、ce-ms以及2de maldi-tof。
[0024]
lc-ms/ms是一种高分辨率技术,在ms分析之前,应用预分离,可以获得更加细化蛋白质组特征。虽然通过该技术可以鉴定出数千种蛋白质,但分析时间较长,数据分析的复杂性较高,且存在误报的风险。非标记定量和稳定同位素标记定量是两种常用的定量技术,后者的使用更为广泛。因为运行一次ms可以同时分析多个样本,同位素标记定量分析的测定误差显著降低,但是一次分析的样本数量却受到标签数量的限制。相反的,使用非标记定量的方法,每个样本逐次进行分析,这样每次运行ms时产生的变化,可能会影响结果。但是,该方法对于样品数量没有限制。
[0025]
ce-ms作为一种补充的高分辨率技术,被用于鉴定体液(主要是尿液)中原有的肽段和小分子蛋白。与lc-ms/ms相比,分析的可重复性更高,且分析运行时间更短(约60分钟)。此外,ce-ms具有良好的技术特性,可用于生物标志物的发现、验证和临床应用。但是,后续的肽段测序则需要更为灵敏的质谱检测器。基于ms的技术的进步,将有助于克服经典的基于凝胶的蛋白质组学技术(如2de/dige)的一些局限性,即低吞吐能力和低分辨率。为进行验证,通常使用能对所选的蛋白质进行靶向分析的技术。虽然基于ms的靶向技术已取得进展,但免疫法(如elisa、wb)仍是最常用的方法。免疫法监测速度快,且普遍与临床实验室的设备兼容,但其分离性取决于抗体的质量,另外一次对多种蛋白同步分析也较为困难。当需要开发由多个生物标志物组成的组时,无法对多种蛋白同步分析将会成为该技术应用最大的阻碍。因此,一些基于ms的平台被应用于生物标志物验证,包括靶向(srm/mrm/prm)
kumar,a.neve,a.s.guerreiro stucklin,c.m.kuzan-fischer,e.j.rushing,m.d.taylor,d.tripolitsioti,l.behrmann,d.kirschenbaum,m.a.grotzer,m.baumgartner,tgf-βdetermines the pro-migratory potential of bfgf signaling in medulloblastoma,cell rep.23(2018)3798-3812.e8.https://doi.org/10.1016/j.celrep.2018.05.083]。
[0030]
如本文所用,术语“fibb”是纤维蛋白原的亚基,被确定为尿液生物标志物,可用于检测膀胱癌,前列腺癌,胰腺癌和肺癌以及肾细胞癌[参见,c.zhang,w.leng,c.sun,t.lu,z.chen,x.men,y.wang,g.wang,b.zhen,j.qin,urine proteome profiling predicts lung cancer from control cases and other tumors,ebiomedicine.30(2018)120
–
128.https://doi.org/10.1016/j.ebiom.2018.03.009;m.frantzi,j.metzger,r.e.banks,h.husi,j.klein,m.dakna,w.mullen,j.j.cartledge,j.p.schanstra,k.brand,m.a.kuczyk,h.mischak,a.vlahou,d.theodorescu,a.s.merseburger,discovery and validation of urinary biomarkers for detection of renal cell carcinoma,j proteomics.98(2014)44
–
58.https://doi.org/10.1016/j.jprot.2013.12.010;m.frantzi,k.e.van kessel,e.c.zwarthoff,m.marquez,m.rava,n.malats,a.s.merseburger,i.katafigiotis,k.stravodimos,w.mullen,j.zoidakis,m.makridakis,m.pejchinovski,e.critselis,r.lichtinghagen,k.brand,m.dakna,m.g.roubelakis,d.theodorescu,a.vlahou,h.mischak,n.p.anagnou,development and validation of urine-based peptide biomarker panels for detecting bladder cancer in a multi-center study,clin.cancer res.22(2016)4077
–
4086.https://doi.org/10.1158/1078-0432.ccr-15-2715;和i.belczacka,a.latosinska,j.siwy,j.metzger,a.s.merseburger,h.mischak,a.vlahou,m.frantzi,v.jankowski,urinary ce-ms peptide marker pattern for detection of solid tumors,sci rep.8(2018)5227.https://doi.org/10.1038/s41598-018-23585-y]。纤维蛋白原是将肿瘤细胞连接到细胞外基质的主要成分之一。纤维蛋白原还促进肿瘤血管生成和肿瘤进展[参见,m.w.mosesson,introduction:fibrinogen as a determinant of the metastatic potential of tumor cells,blood.96(2000)3301]。
[0031]
如本文所用,术语“a1bg”又称为α-1-b糖蛋白,是一种功能未知的血浆糖蛋白。该蛋白质显示出与某些免疫球蛋白超基因家族成员蛋白质的可变区的序列相似性。
[0032]
如本文所用,术语“vsig4”(v-set and ig domain-containing 4)vsig4属于b7超级家族的成员,是c3b/ic3b的补体受体,可以抑制细胞毒性t淋巴细胞的活化,可能在胶质瘤的发生发展中起重要作用[参见,xu,tao et al.“vsig4 is highly expressed and correlated with poor prognosis of high-grade glioma patients.”american journal of translational research vol.7,6 1172-80.15 jun.2015]。
[0033]
如本文所用,术语“1433b”(14-3-3protein beta/alpha),由ywhab基因编码,可阻断磷酸化srpk2(akt1)的核移位,拮抗其对细胞周期蛋白d1表达的刺激作用,从而阻断srpk2诱导的神经元凋亡。
[0034]
如本文所用,术语“lyve1”(lymphatic vessel endothelial hyaluronic acid receptor 1),是细胞内细胞器(tgn)与质膜间的配体特异性转运蛋白。可作为透明质酸(ha)转运体,介导其在淋巴管内皮细胞内的分解代谢吸收,或将其转运到传入淋巴管的管
腔,以便随后在淋巴结内重新吸收和降解。
[0035]
如本文所用,术语“kvd28”(immunoglobulin kappa variable 2d-28),参与抗原识别的免疫球蛋白轻链可变区v区.免疫球蛋白,又称抗体,是由b淋巴细胞产生的膜结合或分泌的糖蛋白。在体液免疫的识别阶段,膜结合免疫球蛋白作为受体,与特定抗原结合后,触发b淋巴细胞克隆性扩增、分化为分泌免疫球蛋白的浆细胞。抗原结合位点由一个重链的可变结构域及其相关轻链的可变结构域构成。因此,每个免疫球蛋白有两个抗原结合位点,对特定抗原具有显著的亲和力。在接触抗原和选择后,可变结构域通过一个称为v-(d)-j重排的过程组装,通过此过程允许特定抗原的亲和力成熟。
[0036]
如本文所用,术语“gels”(gelsolin),钙调节、肌动蛋白调节蛋白,与肌动蛋白单体或细丝的正(或倒钩)末端结合,防止单体交换。它可以促进单体组装成细丝以及已形成的多条细丝。
[0037]
如本文所用,术语“pgrp1”(peptidoglycan recognition protein 1),其对革兰氏阳性菌有杀菌作用。可能通过干扰肽聚糖生物合成杀死革兰氏阳性菌。与革兰氏阴性菌结合,对革兰氏阴性菌有抑菌作用。
[0038]
如本文所用,术语“lv321”(immunoglobulin lambda variable 3-21),参与抗原识别的免疫球蛋白轻链可变区v区。
[0039]
如本文所用,术语“sap3”(ganglioside gm2 activator),可结合神经节苷脂并刺激神经节苷脂gm2降解。刺激β-己糖胺酶a分解神经节苷脂gm2和糖脂ga2。
[0040]
如本文所用,术语“iglc2”(immunoglobulin lambda constant 2),为免疫球蛋白轻链恒定区。
[0041]
如本文所用,术语“pcoc2”(procollagen c-endopeptidase enhancer2),其与i型和ii型前胶原的c端前肽结合,并可能通过bmp1促进该前肽的裂解。
[0042]
如本文所用,术语“ggt6”(glutathione hydrolase 6),可分解谷胱甘肽结合物。
[0043]
如本文所用,术语“lirb4”(leukocyte immunoglobulin-like receptor subfamily b member 4),i类mhc抗原受体。可广泛识别hla-a、hla-b、hla-c、hla-g的等位基因。参与免疫反应的下调和耐受的产生,抑制受体介导的细胞蛋白磷酸化和细胞内钙离子的动员。
附图说明
[0044]
图1显示本发明髓母细胞瘤相关生物标记物筛选的流程图。在生物标记物的发现中,对9例髓母细胞瘤患者术前、术后及9例健康儿童的尿液进行串联质谱(tmt)定量分析,确定其蛋白组学特征;在生物标记物的验证中,对112个样本(来自29名髓母细胞瘤患儿术前及术后尿液样本58份,来自健康儿童的尿液样本26份,来自非肿瘤神经系统疾病患者的尿液样本28份),进行prm(平行反应监测)验证。
[0045]
图2表示无监督的pca分析的得分图,其显示健康对照组可以与两个疾病组分开,而髓母细胞瘤前组可以与髓母细胞瘤术后组部分分开。
[0046]
图3显示114种差异蛋白的热图,这些蛋白在髓母细胞瘤术前组和健康对照组之间发生了明显变化,但在髓母细胞瘤术后组中恢复了正常,表明尿液蛋白质组可以反映髓母细胞瘤的特征。
[0047]
图4显示17种差异蛋白(25种多肽)在术前、术后、健康对照与疾病对照组中的prm验证的结果。
[0048]
图5a显示cadh1、fibb、fgfr4的组合用于区分髓母细胞瘤术前与健康对照的roc曲线;图5b显示cadh1和fibb的组合用于区分髓母细胞瘤术前与疾病对照的roc曲线。
具体实施方式
[0049]
本发明人使用正常儿童尿液、髓母细胞瘤(mb)患者术前及术后尿液来进行质谱分析,进而描绘出该肿瘤患儿尿液的蛋白组学特征。并对三组样本中的尿蛋白水平进行了量化。平行反应监测(parallel reaction monitoring,prm)用于验证所得到的结果,该阶段使用了新的样本,包括:对照组、术前组、术后组、非肿瘤神经系统疾病组(图1)。本研究可为确定髓母细胞瘤患者尿液蛋白标志物提供有用的线索。
[0050]
实施例1.用于质谱检测的尿液样本的收集以及制备
[0051]
1.入组患者及样本收集
[0052]
在生物标志物发现阶段,分别采集了9名髓母细胞瘤患儿肿瘤切除前后的尿液。这些患者均在首都医科大学附属北京天坛医院确诊,并在该院实施了手术。患儿入组标准为:年龄≤16岁,术后病理证实为髓母细胞瘤,术前及样品采集期间未接受任何治疗(放疗及化疗)。术前尿液采集于手术前,术后尿液采集于术后1-2周。在此阶段,同时采集了9例健康儿童的尿液作为对照组。为验证结果,采用同样的标准采集了29例髓母细胞瘤患儿的术前术后尿液、26例与之相匹配的健康儿童尿液,28例非肿瘤神经系统疾病患儿的尿液(包括癫痫、先天性畸形和其他神经疾病,但肿瘤或神经系统感染除外)。每次收集尿液的总量为40ml。清晨7:00-9:00,患者空腹时留取晨尿(取中段尿)。对每份样本进行尿常规检查以排除潜在的疾病。离心3000g
×
15min取上清液,储存在-80℃冰箱中备用。本研究得到了伦理委员会的批准,且患者及法定监护人签署知情同意书。
[0053]
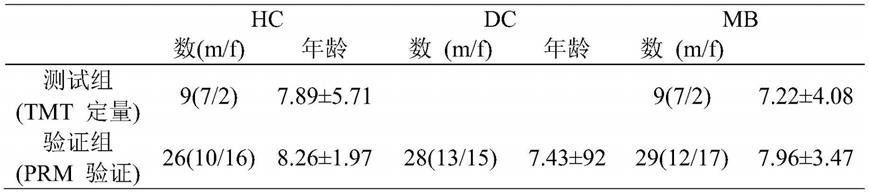
表1参与本发明研究的临床样本概况
[0054][0055]
2.样本制备
[0056]
2.1蛋白质富集
[0057]
取尿液样本10ml,加入-20℃的丙酮沉淀其中的蛋白质,离心14000g
×
15min,去上清液,将沉淀物溶解于含有8mol/l尿素的裂解液中复溶蛋白,离心14000g
×
15min,保留上清液。
[0058]
2.2蛋白质浓度测定
[0059]
bradford法测定样品的蛋白质浓度
[0060]
将1mg/ml的bsa(牛血清蛋白)标准蛋白稀释为不同浓度,加bradford工作液定量试剂,使用酶标仪测定波长在595nm处的吸光光度值,之后绘制出标准曲线。使用同样的测
定方法,测定待测样本蛋白质的吸光光度值,并根据之前所得的标准曲线算出待测样本的蛋白质浓度。
[0061]
2.3蛋白还原烷基化、酶切
[0062]
1)使用fasp法分解蛋白
[0063]
根据j.r.a.zougman,n.nagaraj,m.mann,universal sample preparation method for proteome analysis,nat.methods.6(2009)359
–
362.https://doi.org/10.1038/nmeth.1322所述的方法,首先,在尿蛋白样品中添加20mm dtt(dithiothreitol,二硫苏糖醇),95℃水浴5分钟(还原)。之后,加50mm iaa(iodoacetamide,碘乙酰胺),室温避光放置45分钟(烷基化)。然后,将还原烷基化后的尿蛋白样品上到30kd滤膜上,用ua溶液(含8mol尿素)和25mmol/l碳酸氢铵溶液清洗两次。最后,按胰蛋白酶与蛋白质质量比1:50的比例加入胰蛋白酶,37℃过夜酶切。
[0064]
2)多肽的收集
[0065]
将超滤管置入离心机,离心14000g
×
30min,温度设置18℃,至液体完全离下,留取超滤管中多肽溶液。在滤膜上加500mm nacl溶液10μl,用枪头反复吹打30次,涡旋振荡60s,使膜上粘附的残余多肽清洗干净。再次放入超速离心机,离心14000g
×
30min,温度设置18℃、约30min,至液体完全离下,保留管中含有多肽的溶液与第一次离心所得的多肽容易混合。
[0066]
3)oasis c18固相萃取柱提取肽样
[0067]
将3ml c18固相萃取柱,置入固相萃取装置。在c18固相萃取柱中加入500μl 100%乙腈,等待萃取柱的上层液体自然滴净后,再次重复上述步骤,以使c18固相萃取柱活化。之后,在c18固相萃取柱中加入500μl 1%三氟乙酸,将萃取柱上的残留乙睛溶液清洗干净,待液体自然滴净后,再次重复,以使c18固态萃取柱平衡。随后,将收集好的多肽溶液加入c18固态萃取柱,使溶液自然滴净。使用500μl 1%三氟乙酸,清洗脱盐,重复七次。加入500μl 100%乙腈,将洗脱液收集于微型离心管(ep管)中,完成多肽的洗脱。最后,将收集的洗脱液置入旋转真空干燥仪中,设置为不加热,真空抽干后,将其置于-20℃冰箱保存备用。
[0068]
4)bca法(二喹啉甲酸法)测定多肽浓度。
[0069]
称取血管紧张素ⅱ,用1%甲酸配成0μg/μl、0.1μg/μl、0.2μg/μl、0.5μg/μl、1μg/μl的蛋白质标准溶液。将多肽样品用1%的甲酸溶解,配成浓度为0.3μg/μl的溶液。在96孔板上每个孔中加入200μl配制好的bca工作液。将10μl不同浓度蛋白质标准液或多肽样品分别加入各个孔中,相同的样品做3个平行复孔,置于摇床摇匀后,将孔板放置于恒温水浴锅中37℃水浴30min。使用酶标仪测定波长在562nm处标准品的吸光光度值,之后绘制出浓度/吸光度标准曲线。使用同样的测定方法,测定待测样本的吸光光度值,并根据之前所得的标准曲线算出待测样本的多肽浓度。
[0070]
实施例2.尿液蛋白质谱分析
[0071]
1.tmt(tandem mass tag,串联质谱标签)标记定量蛋白组学分析
[0072]
1.1 tmt标记和离线液相分离
[0073]
1)tmt定量标记
[0074]
将3个术前及对应的术后样本、3个健康对照组样本,共计9个多肽样本,分别随机标记为127n、127c、128n、128c、129n、129c、130n、130c、131。10-plex tandem mass tags
(tmt)试剂的使用参照厂商的使用说明(thermo fisher scientific)。将术前、术后、健康对照三组混合后的样品用126tmt标记。
[0075]
2)离线高ph反相高效液相色谱分离tmt标记多肽
[0076]
利用反相高效液相色谱柱(waters,4.6mm
×
250mm,xbridge c18,3μm)对tmt标记样品进行了混合和分馏。将样品置于色谱柱上放入缓冲液a1(99.9%去离子水,0.1%氨水,ph=10)。缓冲液b1的分离梯度为5-25%(90%乙腈,ph=10),流速为0.8ml/min,持续60min。每分钟洗脱下来的肽段作为一个组分,洗脱的肽段以一管组分/min的速度收集,共计60个组分。真空抽干后的这60个组分用千分之一fa复溶,然后按照编号1,21,51合并为一个组分,2,22,52合并为一个组分,以此类推,共得到20个组分。将收集的20个组分置入旋转真空干燥仪中,真空抽干,-20℃冻存。
[0077]
1.2 lc-ms/ms分析
[0078]
利用自填充反相c18毛细管液相色谱柱(75μm
×
100mm,1.9μm)对tmt标记的样品混合物进行分析。缓冲液b2的洗脱梯度为5-30%(0.1%甲酸,99.9%乙腈),流速为0.3μl/min,持续时间为45分钟。使用ltq orbitrap fusion lumos(thermo scientific)质谱仪分析鉴定多肽混合物。仪器参数设置为:全扫描使用最高速度数据相关模式(3s);使用orbitrap进行全扫描,分辨率为60,00;hcd碰撞池设为32%标准化碰撞能量,分辨率为15,000;电荷状态筛选(不包括未知电荷态的前体或+1的电荷态);动态消除(dynamic exclusion)(消除持续时间为30s)。
[0079]
1.3数据分析
[0080]
所得质谱数据proteome discoverer software suite(v2.1,thermo fisher scientific)软件进行分析,数据库为uniprot(www.uniprot.org)的swissprot人类数据库。检索参数为:胰蛋白酶选择裂解特异性,2个误切位点;氨基甲基化半胱氨酸和tmt 10-plex标签设定为固定修饰,氧化蛋氨酸、脱酰胺天冬氨酸、脱酰胺谷氨酰胺、氨基甲酰赖氨酸和肽段的n端设定为动态修饰。搜索时采用的肽宽容度为20ppm,质量误差容忍度为0.05da。筛选标准设为:蛋白质水平上假阳性率小于1%,同时每个蛋白质至少含有1个特异性的肽段。筛选后,不同指示器离子通道的肽段丰度被标准化。基于特异性的肽段结果推算蛋白质丰度比。被认定为蛋白质组差异蛋白:术前组和健康对照组相比,差化倍数≥1.3,且术后组与术前组相比有恢复,差化倍数≥1.2。
[0081]
1.4使用tmt质谱分析鉴定出差异表达的尿蛋白的结果
[0082]
随机挑选9个健康儿童的尿液样本及9对髓母细胞瘤患儿的术前、术后尿液样本,分别使用tmt试剂进行标记。在tmt标记的定量蛋白质组学分析中,我们在术前组中鉴定出2041种蛋白,在术后组鉴定出2041种蛋白,在健康对照组鉴定出1908种蛋白,这些蛋白至少包含一个特异性的肽段。髓母细胞瘤术前组有2015种蛋白可被定量,术后组有2018种蛋白可被定量,健康对照组有1893种蛋白可被定量。术前、术后、健康对照组的中位cv分别为22.9%、24.5%、23.7%。1470种蛋白是髓母细胞瘤术前组、术后组及健康对照组所共有。
[0083]
首先,为了探讨三组样本蛋白质组学分析的差异,进行了无监督的pca分析。得分图显示健康对照组可以与两个疾病组分开,而髓母细胞瘤前组可以与髓母细胞瘤术后组部分分开(图2)。其次,进行opls-da来进一步确定三组之间的蛋白质组差异。在opls-da模型中,健康对照组,髓母细胞瘤术前和髓母细胞瘤术后组可以彼此分开。一百次置换检验表
明,这些模型没有过度拟合的情况。
[0084]
在先前的体液蛋白质组学研究中,差异蛋白质通常占总定量蛋白质的10%至20%[参见,l.pang,q.li,y.li,y.liu,n.duan,h.li,urine proteomics of primary membranous nephropathy using nanoscale liquid chromatography tandem mass spectrometry analysis,clin proteomics.15(2018)5.https://doi.org/10.1186/s12014-018-9183-3;j.-y.cao,y.-p.xu,x.-z.cai,tmt-based quantitative proteomics analyses reveal novel defense mechanisms of brassica napus against the devastating necrotrophic pathogen sclerotinia sclerotiorum,j proteomics.143(2016)265
–
277.https://doi.org/10.1016/j.jprot.2016.03.006;以及h.xiao,y.zhang,y.kim,s.kim,j.j.kim,k.m.kim,j.yoshizawa,l.-y.fan,c.-x.cao,d.t.w.wong,differential proteomic analysis of human saliva using tandem mass tags quantification for gastric cancer detection,sci rep.6(2016)22165.https://doi.org/10.1038/srep22165;以及l.zou,x.wang,z.guo,h.sun,c.shao,y.yang,w.sun,differential urinary proteomics analysis of myocardial infarction using itraq quantification,mol med rep.19(2019)3972
–
3988.https://doi.org/10.3892/mmr.2019.10088]。为了发现所有潜在的髓母细胞瘤标记物,将标准定为倍数变化≥1.3,在髓母细胞瘤和健康对照组之间共鉴定出300种(约20%)差异蛋白。在髓母细胞瘤术前样品中改变,但在髓母细胞瘤术后样品中恢复到与健康对照组样本相对水平的尿蛋白被认为是与髓母细胞瘤相关的差异蛋白。考虑到髓母细胞瘤相关蛋白可能无法在术后完全恢复到正常水平,因此将同时符合以下标准的蛋白定义为髓母细胞瘤相关的差异蛋白:髓母细胞瘤和健康对照组之间的倍数变化≥1.3;术后出现反向倍数变化≥1.2。因此,总共鉴定出114种髓母细胞瘤相关的差异蛋白(髓母细胞瘤组中51种上调而63种下调)。114种差异蛋白的热图(图3)表明,这些蛋白在髓母细胞瘤术前组和健康对照组之间发生了明显变化,但在髓母细胞瘤术后组中恢复了正常,表明尿液蛋白质组可以反映髓母细胞瘤的特征。
[0085]
实施例3.差异蛋白的通路分析(ingenuity pathway analysis,ipa)
[0086]
利用ipa软件(ingenuity systems,mountain view,ca)对所有差异表达蛋白进行分析。这些蛋白质被分为与疾病相关和与功能相关两类,并被描绘在ingenuity和其他数据库的生物学通路中。分别按z评分和p值进行排序。
[0087]
差异表达蛋白的功能分析
[0088]
通过ipa分析这114种差异蛋白,这些差异蛋白可被分为与疾病相关和功能相关两类,如肿瘤细胞的迁移、细胞凋亡、中枢神经系统转移、iii期的肿瘤、复发性肿瘤、头颈部肿瘤、转移,提示这些蛋白可能与神经系统肿瘤相关。富集在生物通路上的蛋白与以下通路相关:相关与网格蛋白介导的内吞信号、糖酵解i、组织因子在癌症中的作用、pparα/rxrα激活、神经炎症信号通路和hif1α信号,证实了这些尿蛋白在功能上的作用。从尿液中检测到的这些差异蛋白质都符合其来源和功能。
[0089]
实施例4.平行反应监测(parallel reaction monitoring,prm)分析
[0090]
从lc-ms/ms分析所得的114个差异蛋白中挑选了17个与肿瘤相关、并在功能上有关联的蛋白进行了prm验证。每个样本都使用调度模式(schedule mode)进行分析。为了保证数据的质量,对混合样本进行了质控分析,以确保仪器信号在整个过程中的稳定性。在每
个样品同时也增加了irt标准肽分析,并在分析过程中对色谱保留时间的稳定性进行评估。每个样本进行两次技术重复。为了减少系统偏差,对不同组的样品进行随机顺序的质谱分析。
[0091]
为验证结果,采用同样的标准采集了29例髓母细胞瘤患儿的术前术后尿液、26例与之相匹配的健康儿童尿液(hc),28例非肿瘤神经系统疾病患儿的尿液(dc)(包括癫痫、先天性畸形和其他神经疾病,但肿瘤或神经系统感染除外)。
[0092]
prm分析时,蛋白质提取与分解的方法与之前所述相同。用triple tof 5600质谱仪对液相色谱法洗脱出的肽段进行了分析。使用高灵敏度模式(high-sensitivity mode)获得ms数据,设置参数如下:prm模式、分辨率为40000的全扫描、分辨率为20000的ms/ms扫描、滚动碰撞能量、电荷态筛选(包括+2至+4电荷态的前体)、动态消除(排除消除时间15s)、ms/ms扫描范围100-1800m/z,扫描时间为100ms。每个样本重复两次。
[0093]
prm数据分析
[0094]
用skyline 3.6软件进行prm数据分析。将所有数据导入skyline 3.6,人工挑选正确的峰,之后输出在所有样本中所得的多肽。用progenesis软件提取出每个样品中+2-+5电荷的总离子强度。每个样品中每个肽段的质谱使用样品总离子强度标准化,以修正样品大小和质量信号强度的误差。对每个肽段进行定量分析,筛选不同组间的差异蛋白,并与tmt结果进行比较。
[0095]
统计分析
[0096]
使用simca 14.0(umetrics,瑞典)软件进行模式识别分析(主成分分析,pca;正交偏最小二乘判别分析,opls-da)。
[0097]
通过配对或不配对t检验分析比较各组之间监测到的肽段。p值小于0.05被认为具有统计学意义。利用metaboanalyst软件,建立各待选生物标志物的受者作用特征曲线(receiver operating characteristic curves,roc)。采用线性svm算法进行组合roc分析。以髓母细胞瘤为因变量,计算roc曲线下面积(auc),确定待选诊断标志物。
[0098]
差异蛋白prm验证的结果
[0099]
为了确定与肿瘤相关的生物标记物,从lc-ms/ms分析所得的差异蛋白中挑选了17种与肿瘤相关、并在功能上有关联的蛋白,并进行了prm验证,以确定这些蛋白是否具有诊断髓母细胞瘤的特异性。为了确保分析过程中的系统稳定性和限制系统性偏倚,将所有尿液样本的混合物作为质量控制(qc)。
[0100]
每个样品之前,之后和期间注入qc样品。通过对qc样品和单个尿液样品进行pca分析,qc样品是紧密聚集的。qc样本的相关图还显示,qc样本高度正相关,平均皮尔逊相关系数为0.926。以上结果表明了qc的可重复性。这些结果表明在分析过程中ms平台的稳定性。
[0101]
术前组与健康对照组(hc)相比,这17种蛋白(25种多肽)的prm验证结果与tmt的结果具有完全相同的变化趋势,其中1种蛋白上调、16种蛋白下调(图4,表2)。利用roc分析,进一步对这17种蛋白的诊断价值进行评估。其中13种蛋白在单独用于诊断评估时,表现出较好的区分度(auc>0.75),这些具有良好区分度的蛋白为a1bg、vsig4、kvd28、gels、pgrp1、lv321、sap3、iglc2、fgfr4、pcoc2、cadh1、ggt6、和fibb,其中cadh1、fibb、fgfr4的组合可显著提高诊断准确性,auc值为0.973(95%ci,0.923-1,图5a)。这些生物标记物可以用于髓母
细胞瘤的诊断。
[0102]
与疾病对照组(dc)相比,发现13种多肽有显著变化,对应9种下调蛋白(图4,表2),所述下调的9种蛋白为pgrp1,fibb,a1bg,iglc2,cadh1,fgfr4,lv321,lirb4,vsig4。roc分析显示pgrp1、cadh1、fibb这三种蛋白单独用于评估时,表现出很好的区分度(auc>0.75,数据未显示)。cadh1和fibb组合显示出更高的敏感性和特异性,auc值为0.884(95%ci,0.75-0.978,图5b)。这些生物标记物可以用于区分髓母细胞瘤与良性的神经系统疾病。
[0103]
[0104]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1