一种组织芯片制芯的方法与流程
1.本技术属于组织芯片技术领域,具体涉及一种组织芯片制芯的方法。
背景技术:
2.组织芯片(tissue chip,tc)又称组织微阵列(tissue microarray,tma),与基因芯片、蛋白质芯片及细胞芯片等一样,为生物芯片技术中的一个组成部分,属于生物高科技技术。组织芯片是将几十、几百例不同个体的组织标本按预定序列排列在载体上,进行形态学或分子生物学方面实验的一种新型的高通量、多样本的研究工具。组织芯片技术具有信息量大,实验误差小、可比性强、省时、省力、可大量节约经费等优点,与传统的病理学技术、组织化学技术、免疫组化技术(ihc)、原位杂交技术(ish)、荧光核酸原位杂交技术(fish)和原位pcr技术等相结合,可实现对正常或病变组织标本进行形态学观察和特定基因及其所表达的蛋白质等不同分子水平上研究,其逐渐应用于涉及医学、生物学及动植物学等领域的科研、临床、教学、生物试剂测试、质量监控及标准化等领域。
3.微阵列组织芯片技术的核心之一在于每个位点内的信息的准确性和靶组织的量,近年来随着生物制药不断发展,对组织芯片的要求越来越高,尤其是中高密度大样本组织芯片需求增加。而制作密度越大、信息量越多的组织芯片,就必须减小每一位点直径,比如点样直径从80点组织芯片的1.5mm直径,到100点以上甚至240点以上组织芯片的1.0mm-0.6mm直径。每一位点直径随着点数增加而减小,在点样直径缩小的同时要保证足够的靶细胞量及靶组织有效性,势必增加了每一位点组织芯片核心质量的难度。
4.tma构建过程中,病理组织学标记始终贯穿于中,而目前病理标记主要还是通过手工光镜下定位,标记范围大,定位精确性不高,对于靶组织的新鲜度、靶组织量把握不准,导致免疫组化等实验结果不稳定,假阴性、假阳性时有发生;同时现有病理标记存在水平层次不齐、以及组织分层出现靶组织量过少,坏死、出血及纤维组织过多,甚至掉片脱失而出现较多无效点的问题,导致制芯后的芯片核心质量不高,从而会导致实验效果不理想,浪费人力、物力和财力。
5.上述内容仅用于辅助理解本发明的技术方案,并不代表承认上述内容是现有技术。
技术实现要素:
6.为至少在一定程度上克服相关技术中存在的问题,本技术提供一种组织芯片制芯的方法,基于数字化智能扫描切片进行精准靶组织标记,有助于较好实现高密度组织芯片的制作标记。
7.为实现以上目的,本技术采用如下技术方案:
8.本技术提供一种组织芯片制芯的方法,该方法包括:
9.利用数字化扫描仪扫描石蜡切片,获取扫描放大的扫描图像;
10.基于所述扫描图像进行镜下标记,并根据标记结果从切片对应的蜡块中获取有效
靶组织作为组织芯片柱芯。
11.可选地,所述基于所述扫描图像进行镜下标记,包括:
12.根据所述扫描图像对切片进行观察评估,
13.针对切片中有效靶组织少而无效组织多的情况,采用病理组织学局域标记法进行镜像下标记,
14.而针对切片中有效靶组织多而无效组织少的情况,采用精准涂鸦法进行镜像下标记。
15.可选地,所述采用病理组织学局域标记法进行镜像下标记,具体为:
16.在所述扫描图像上确定无效组织区域并采用第一标识进行标记,在显微镜下对照切片,避开切片内的无效组织、以及靶组织间质的无效区域,对有效靶组织集中区域采用第二标识标记。
17.可选地,
18.所述切片内的无效组织包括,炎症反应干扰的组织、出血坏死的组织、以及这两类组织周围退变的组织;
19.所述靶组织间质的无效区域包括,靶组织间质内胶原纤维所对应的区域。
20.可选地,
21.所述采用第一标识进行标记具体为,采用画叉进行标记;
22.所述采用第二标识进行标记具体为,采用油性笔画圈进行标记。
23.可选地,所述采用精准涂鸦法进行镜像下标记,具体为:
24.在所述扫描图像上确定无效区域并采用第三标识进行标记,在显微镜下对照切片,对切片内的初筛无效区域进行涂色标记,之后针对切片未涂色区域配合所述扫描图像在高倍率视野下对细微无效区域进行涂色标记。
25.可选地,所述切片内的初筛无效区域包括,切片内出血坏死区域、厚壁血管区域及纤维组织区域;
26.所述细微无效区域包括,组织退变区,细胞变性区和炎症干扰区。
27.可选地,所述采用第三标识进行标记具体为,采用油性笔画叉进行标记;所述涂色标记具体为,用油性笔进行涂黑标记。
28.可选地,所述利用数字化扫描仪扫描石蜡切片,获取扫描放大后的扫描图像,具体为:
29.用无水酒精将石蜡切片擦拭干净并将其按顺序放入扫描仪的载物盘内;
30.配置数字化扫描仪分辨切片靶组织颜色,采用精准方式进行对焦扫描,以获取扫描放大后的扫描图像。
31.可选地,所述根据标记结果从切片对应的蜡块中获取有效靶组织作为组织芯片柱芯,具体为:
32.基于切片的标号和形状,确认切片所对应的蜡块,按照标记结果中标记区域在蜡块对应部位运用阵列仪取样针垂直钻取有效靶组织作为组织芯片柱芯。
33.本技术采用以上技术方案,至少具备以下有益效果:
34.基于数字化智能扫描切片进行精准靶组织标记,大大减少了构建的中高密度组织芯片的无效点,明显提升了组织芯片的核心质量及精准度,减少了恶性肿瘤组织芯片每个
点异质性差异,靶组织内细胞的新鲜度得到了有效保证,进而提高了免疫组化和基因研究的准确性。且能降低病理医生标记工作强度,缩短组织芯片制作时间并减少了废品率,从而节约了人力、物力和财力。
35.本发明的其他优点、目标,和特征在某种程度上将在随后的说明书中进行阐述,并且在某种程度上,基于对下文的考察研究对本领域技术人员而言将是显而易见的,或者可以从本发明的实践中得到教导。本发明的目标和其他优点可以通过下面的说明书,权利要求书,以及附图中所特别指出的结构来实现和获得。
附图说明
36.附图用来提供对本技术的技术方案或现有技术的进一步理解,并且构成说明书的一部分。其中,表达本技术实施例的附图与本技术的实施例一起用于解释本技术的技术方案,但并不构成对本技术技术方案的限制。
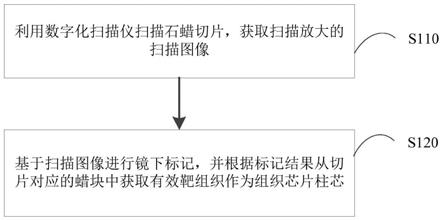
37.图1为本技术一个实施例提供的组织芯片制芯的方法的流程示意图。
具体实施方式
38.为使本技术的目的、技术方案和优点更加清楚,下面将对本技术的技术方案进行详细的描述。显然,所描述的实施例仅仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本技术所保护的范围。
39.基于背景技术中所述,本发明的目的在于提供一种组织芯片制芯的方法,在制作中高密度石蜡组织芯片柱芯中采用精准标记方法,从而使石蜡组织芯片柱芯内有效靶组织含量和精确度得到很大提高。
40.如图1所示,在一实施例中,本技术提出的组织芯片制芯的方法,包括:
41.步骤s110,利用数字化扫描仪扫描石蜡切片,获取扫描放大的扫描图像;
42.具体的,该步骤中,用无水酒精将石蜡切片擦拭干净并将其按顺序放入扫描仪的载物盘内;配置数字化扫描仪分辨切片靶组织颜色(基于切片的he染色技术),采用精准方式进行对焦扫描,以获取扫描放大后的扫描图像。举例而言,数字化扫描仪的型号为precice 500b,扫描倍率按照40倍物镜自动对焦扫描病理切片靶组织,以获取的扫描放大后的扫描图像。
43.之后进行步骤s120,基于获取到的扫描图像进行镜下标记,并根据标记结果从切片对应的蜡块中获取有效靶组织作为组织芯片柱芯,容易理解的是,这里进行标记操作的为具有病理学知识的专业人员。
44.该步骤中,首先根据扫描图像对切片进行观察评估,评估判断切片中有效靶组织与无效组织的含量对比情况,基于不同情况采用不同的方法进行处理;
45.本技术中,针对切片中有效靶组织少而无效组织多的情况,采用病理组织学局域标记法进行镜像下标记,而针对切片中有效靶组织多而无效组织少的情况,采用精准涂鸦法进行镜像下标记,下面对这两种标记方法分别进行介绍:
46.a、采用病理组织学局域标记法进行镜像下标记的过程为:
47.在扫描图像上确定无效组织区域并采用第一标识进行标记,例如采用画叉进行标
记,之后在显微镜下对照切片,避开切片内的无效组织(举例而言,切片内的无效组织指,炎症反应干扰的组织、出血坏死的组织、以及这两类组织周围退变的组织等)、以及避开靶组织间质的无效区域(举例而言,无效区域包括靶组织间质内胶原纤维所对应的区域),对有效靶组织集中区域采用第二标识标记,如采用油性marker笔精确画圈进行标记。
48.b、采用精准涂鸦法进行镜像下标记的过程为:
49.在扫描图像上确定无效区域并采用第三标识进行标记,举例而言,这里用油性笔画叉进行标记,之后在显微镜下对照切片,对切片内的初筛无效区域进行涂色标记(举例而言,切片内的初筛无效区域包括,切片内出血坏死区域、厚壁血管区域及纤维组织区域等),之后针对切片未涂色区域配合扫描图像在高倍率视野下对细微无效区域(举例而言,细微无效区域包括,组织退变区,细胞变性区和炎症干扰区等)进行涂色标记。这里两次进行的涂色标记,都可为用油性笔进行涂黑标记。
50.步骤s120中,在完成上述a或b的标记过程后,继续根据标记结果从切片对应的蜡块中获取有效靶组织作为组织芯片柱芯,基于获取的柱芯完成组织芯片制芯。
51.具体的,基于切片的标号和形状,确认切片所对应的蜡块(即需将标记后靶组织切片和同一蜡块对比编号和形状无误),之后按照切片标记结果中标记区域在蜡块对应部位运用阵列仪取样针垂直钻取有效靶组织作为组织芯片柱芯,基于该柱芯完成组织芯片制芯。
52.本技术采用以上技术方案,至少具备以下有益效果:
53.基于数字化智能扫描切片进行精准靶组织标记,大大减少了构建的中高密度组织芯片的无效点,明显提升了组织芯片的核心质量及精准度,减少了恶性肿瘤组织芯片每个点异质性差异,靶组织内细胞的新鲜度得到了有效保证,进而提高了免疫组化和基因研究的准确性。且能降低病理医生标记工作强度,缩短组织芯片制作时间并减少了废品率,从而节约了人力、物力和财力。
54.以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉该技术的人员在本发明所揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应该以权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1