CST-Cathepsin复合物作为肿瘤诊断标志物的应用的制作方法
cst-cathepsin复合物作为肿瘤诊断标志物的应用
技术领域
[0001]
本发明涉及医学诊断学领域,具体而言,涉及一种cst-cathepsin复合物作为肿瘤诊断标志物的应用。
背景技术:
[0002]
肿瘤发生是多因素、多阶段的过程,肿瘤侵袭转移包括粘附、降解和穿透,肿瘤的侵袭和转移是恶性肿瘤的重要特征。研究认为,蛋白水解酶在肿瘤侵袭过程中有关键作用。组织蛋白酶(cathepsin)是半胱氨酸蛋白酶家族的主要成员,它们与人类肿瘤密切相关,是近年来备受关注的一类靶标蛋白酶。其中半胱氨酸组织蛋白酶包括组织蛋白酶b、l、h、s、k、f、v、x、w、o和c,其中组织蛋白酶b、l、h和s已有相关报道与多种癌症的发生和发展相关。
[0003]
半胱氨酸蛋白酶抑制剂(cystatin,cst)是对半胱氨酸蛋白酶具有抑制作用的一类蛋白质,广泛分布于人体体液和分泌液中。血液中cystatin含量的变化与癌症的进展相关,因此cystatin也是常作为多种癌症筛查的标志物。半胱氨酸蛋白酶抑制剂家族主要包括cystatin a、b、c、d、e、f、s、sn、sa,每一个家族成员均包含至少一个cystatins结构域,该结构域为cystatin的活性区域,典型的cystatins结构域是由约100个氨基酸残基所构成一个楔形结构,该结构能够与半胱氨酸蛋白酶的活性部位相结合,从而抑制半胱氨酸蛋白酶的水解酶活性。基于其抑制作用,cst超家族蛋白与半胱氨酸蛋白酶可结合cathepsin-cst复合物形式。
[0004]
研究发现,作为与癌症筛查和癌症进展的标志物,不论是cathepsin还是cystatin家族蛋白的特异性均不太好,一方面是因为cathepsin家族蛋白在体内分布较为广泛,另一方面是cystatin家族蛋白之间的序列保守性较高。
技术实现要素:
[0005]
本发明涉及半胱氨酸蛋白酶抑制剂与cathepsin复合物(cst-cathepsin复合物)的定量检测剂在制备用于肿瘤的诊断、辅助诊断或预后分析的试剂盒中的应用;
[0006]
所述半胱氨酸蛋白酶抑制剂选自cystatin a、cystatin b、cystatin c、cystatin d、cystatin e、cystatin f、cystatin s、cystatin sa以及cystatin sn(cst1)中的任一种;
[0007]
所述cathepsin复合物选自cathepsin b、cathepsin h、cathepsin k、cathepsin l以及cathepsin s中的任一种。
[0008]
可选的,所述cst-cathepsin复合物选自所述cst-cathepsin复合物选自cst1-cathepsin l以及cst1-cathepsin b。
[0009]
可选的,所述肿瘤选自肺癌、肝癌、胃癌、食管癌、肠癌、前列腺癌、宫颈癌、乳腺癌和甲状腺癌中的一种。
[0010]
可选的,所述定量检测剂为所述半胱氨酸蛋白酶抑制剂以及所述cathepsin的特异性抗体,所述抗体可用于执行免疫共沉淀或酶联免疫吸附试验以对所述cst-cathepsin
d、cystatin e、cystatin f、cystatin s、cystatin sa以及cystatin sn(cst1)中的任一种;
[0029]
所述cathepsin复合物选自cathepsin b、cathepsin h、cathepsin k、cathepsin l以及cathepsin s中的任一种。
[0030]
本发明提供了一种用于诊断的新标志物:cst-cathepsin复合物。通过cst-cathepsin复合物的检测能够有效的提高标志物的组织特异性,还能够有效提高对肿瘤的检测率。
[0031]
在一些实施方式中,所述cst-cathepsin复合物选自cst1-cathepsin l以及cst1-cathepsin b。
[0032]
在一些实施方式中,所述肿瘤为实体瘤,肿瘤也可以为术语“癌”所替换,所述实体瘤/癌选自胰腺癌、膀胱癌、结肠直肠癌、乳腺癌、前列腺癌、肾癌、肝细胞癌、肺癌、卵巢癌、宫颈癌、胃癌、食管癌、头颈部癌、黑素瘤、神经内分泌癌、cns癌、脑肿瘤、骨癌和软组织肉瘤。
[0033]
优选的,所述肿瘤选自肺癌、肝癌、胃癌、食管癌、肠癌、前列腺癌、宫颈癌、乳腺癌和甲状腺癌中的一种。
[0034]
在一些实施方式中,所述实体瘤是良性的。
[0035]
在一些实施方式中,所述实体瘤选自晚期或转移性恶性实体瘤。
[0036]
术语“晚期或转移性恶性实体瘤”是指组织学或细胞学上所证实诊断的晚期、不可切除和/或转移性复发或难治性恶性实体瘤,其对标准疗法无效或不存在经证明对其有效的疗法。
[0037]
本文使用的术语“标志物”指要用作分析患者实验样品的靶标的分子。这样的分子靶标的实例是蛋白或多肽。在本发明中用作标志物的蛋白或多肽预期包括所述蛋白的天然存在的变体以及所述蛋白或所述变体的片段,特别是免疫学上可检测的片段。免疫学上可检测的片段优选地包含所述标志物多肽的至少5、6、7、8、9、10、11、12、15或20个连续氨基酸。本领域的技术人员可认识到,由细胞释放的蛋白或存在于胞外基质中的蛋白可能受到损害(例如,在炎症过程中),且可被降解或切割成这样的片段。某些标志物以无活性形式合成,其可以随后通过蛋白酶解来激活。如熟练的技术人员将明白的,蛋白或其片段也可以作为复合物的部分而存在。这样的复合物也可以用作本发明意义上的标志物。另外,或在替代方案中,标志物多肽或其变体可以携带翻译后修饰。翻译后修饰的非限制性实例是糖基化、酰化和/或磷酸化。特别地,所述标志物应当位于cst-cathepsin复合物中cst和cathepsin结合部位,这种“结合”是指cst和cathepsin相互作用时氨基酸序列互相接触的部位,可以是线性表位或空间表位。
[0038]
在一些实施方式中,所述定量检测试剂为所述半胱氨酸蛋白酶抑制剂以及所述cathepsin的特异性抗体,所述抗体可用于执行免疫共沉淀或酶联免疫吸附试验以对所述cst-cathepsin复合物进行检测。
[0039]
定量检测试剂对cst-cathepsin复合物的检测可采用本领域公知的方法;可尝试的方法例如生物质谱法、非变性聚丙烯酰胺凝胶电泳、色谱法、酶联免疫吸附试验、免疫荧光法、免疫化学发光法、免疫比浊法、免疫印迹法以及斑点印迹。常见的优选方法为免疫共沉淀以及酶联免疫吸附试验,可通过a抗体捕获cst,并洗去未结合的组分,再通过带有信号
物质的b抗体检测cathepsin;当然也可以捕获cathepsin再检测cst,这对本领域技术人员说容易的。
[0040]
定量检测剂通常是特异性地检测cst-cathepsin复合物的试剂,例如,特异性结合cst-cathepsin复合物的凝集素、特异性结合cst-cathepsin复合物的适配体或特异性结合cst-cathepsin复合物的抗体及抗体片段。特异性的结合剂对其相应的靶分子具有至少107l/mol的亲和力。特异性的结合剂优选对其靶分子具有108l/mol、或更优选109l/mol的亲和力。技术人员将理解,使用术语“特异性的”表示,样品中存在的其它生物分子不与cst-cathepsin复合物的定量检测剂发生显著的结合,这样的生物分子特别为单独游离的cst和cathepsin。
[0041]
在一些实施方式中,所述定量检测剂为cst-cathepsin复合物的特异性抗体。
[0042]
在一些实施方式中,所述特异性抗体为单克隆抗体或多克隆抗体。
[0043]
抗体免疫后可经过筛选过程,如本领域技术人员所容易想到的,可通过cst-cathepsin重组蛋白筛选特异性结合cst-cathepsin复合物的抗体,任选的还包括挑选抗体效价高的抗体。
[0044]
在一些实施方式中,所述特异性抗体具有用于指示信号强度的标记。
[0045]
在一些实施方式中,所述用于指示信号强度的标记选自发色团、地高辛标记探针、电子致密物质、胶体金或酶中的任一种或多种。
[0046]
下面非限定部分列出这些标记:
[0047]
·
产生可检测信号的酶,如通过比色法、荧光和发光来检测,如辣根过氧化物酶,碱性磷酸酶,β-半乳糖苷酶和葡萄糖-6-磷酸脱氢酶。
[0048]
·
发色团,如荧光、量子点、荧光微球、发光化合物(如吖啶酯或其衍生物)和染料。
[0049]
·
具有能被电子显微镜或通过其电特性,如传导性、电流分析、电压测量和电阻等检测的电子密度的基团。
[0050]
·
可检测基团,如其分子大小足以诱导在其物理和/或化学特性上可检测的修饰;这种检测可通过光学方法(如衍射、表面胞质团共振,表面变异和接触变异角度)或物理方法(如原子力谱学和隧道效应)实现。
[0051]
·
电子致密物质,如放射性分子(如
32
p,
35
s或
125
i)。
[0052]
根据本发明的再一方面,本发明还涉及肿瘤诊断、辅助诊断或预后分析试剂盒,其包含如上所述定义的特异性抗体。
[0053]
在一些实施方式中,所述的试剂盒还包含固相载体、封闭液、显色剂、cst-cathepsin融合抗原的校准品以及洗涤缓冲液中的至少一种。
[0054]
封闭液可以为bsa、牛血清、脱脂牛奶、tbst等成分中的一种或多种。
[0055]
显色液可根据抗体上标记的物质进行确定,例如当标记的物质为辣根过氧化物酶时,显色剂可以为鲁米诺。
[0056]
洗涤缓冲液可为pbs、tbs等成分。
[0057]
其中,封闭液、显色液、洗涤缓冲液可以工作浓度的形式包装于试剂盒中,也可以它们的浓缩母液的形式被包装(例如2、3、4、5、6、7、8、9、10、20、30、40、50倍浓缩的母液)。
[0058]
固相载体通常用于包被抗体,用于包被抗体的固相载体物质可为聚苯乙烯、纤维素、聚丙烯酰胺、聚乙烯聚丙烯、交联葡聚糖、玻璃、硅橡胶、琼脂糖凝胶等材质,载体的形式
可以是试管、ep管、多孔板(特别是化学发光板)、微量反应板凹孔、小珠(特别是磁珠)、小圆片等。
[0059]
优选的固相载体为化学发光板。其含有的孔位可以为16、32、48、64、96或更多。
[0060]
根据本发明的再一方面,本发明还提供了一种用于肿瘤的诊断、辅助诊断或预后分析的方法,所述方法包括:使用如上所述的定量检测剂/试剂盒测量cst-cathepsin复合物的含量。
[0061]
检测的样本可以为受试者的血液、血清、脑脊髓液、组织或组织裂解液、精液以及唾液样品中的至少一种。
[0062]
受试者通常为哺乳动物,优选为灵长类动物,再优选为人。
[0063]
下面将结合实施例对本发明的实施方案进行详细描述。
[0064]
实施例1、cst1-cathepsin l/cst1-cathepsin b重组蛋白的活性验证和抗体配对
[0065]
活性分析:以1ug/ml的重组cst1-cathepsin l/cst1-cathepsin b蛋白的碳酸盐缓冲液(ph9.5),100ul体积4℃过夜包被化学发光板,梯度稀释捕获抗体和酶标抗体(浓度为0~1ug/ml),加入羊抗鼠igg-hrp(100ng/ml)。检测发现捕获抗体和检测抗体在100ng/ml时的发光值均不低于20万,蛋白与抗体的反应曲线r2>0.99,蛋白的反应活性满足要求。
[0066]
抗体配对:以1ug/ml捕获抗体包被化学发光板,加入100ul不同浓度(5~1000pg/ml)的cst1-cathepsin l/cst1-cathepsin b校准品,37℃孵育60min,洗涤后加入100ul浓度为100ng/ml的hpr标记的检测抗体,并于37℃孵育60min,洗涤后加入化学发光底物并测定各孔发光强度。从结果上看,捕获抗体和检测抗体配对良好,可用于双抗夹心体系构建。
[0067]
实施例2、cst1-cathepsin l/cst1-cathepsin b校准曲线绘制
[0068]
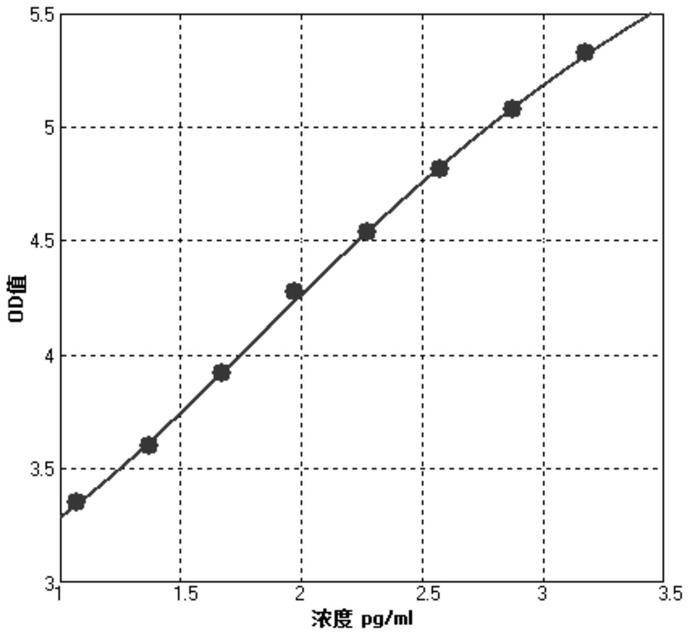
校准曲线绘制:首先在化学发光板上4℃过夜包被捕获抗体,浓度为1μg/ml,将重组人cst1-cathepsin l/cst1-cathepsin b校准品蛋白用蛋白质稳定剂稀释为0pg/ml、10pg/ml、50pg/ml、100pg/ml、200pg/ml、500pg/ml、1500pg/ml,每孔100μl,再加入辣根过氧化物标记的检测抗体,浓度5ng/ml,每孔100μl,37℃孵育1小时。用pbst清洗3次,加入化学发光底物并测定各孔发光强度。从校准曲线计算出被测样品的cst1-cathepsin l/cst1-cathepsin b含量。校准曲线线性范围10~1500pg/ml,附图1和2为cst1-cathepsin l/cst1-cathepsin b检测试剂盒校准曲线,其中,y轴代表发光值对数值,x轴代表cst1-cathepsin l/cst1-cathepsin b校准品的浓度对数值。
[0069]
实施例3、cst1-cathepsin l/cst1-cathepsin b试剂盒临床性能验证
[0070]
cst1-cathepsin l/cst1-cathepsin b检测试剂盒用于癌症诊断:从医院收集肺癌、肝癌、胃癌、食管癌、肠癌、前列腺癌、宫颈癌、乳腺癌和甲状腺癌患者术前血清各20例;同时从血站收集50例健康献血人员血清。使用cst1-cathepsin l/cst1-cathepsin b检测试剂盒检测胃癌、正常人血清中cst1-cathepsin l/cst1-cathepsin b浓度。样本浓度散点图显示,cst1-cathepsin l/cst1-cathepsin b对胃癌/肠癌和正常人检测结果的区分具有统计学意义,见附图3和4。以正常人样本为参照,通过roc分析计算cst1-cathepsin l和cst1-cathepsin b在特异性100%时不同癌症和正常人检测中的灵敏度,并绘制成柱状图,见附图5和6。其中,特异性100%时的cst1-cathepsin l对胃癌的检测灵敏度高达85%,cst1-cathepsin b对肠癌的检测灵敏度达80%,
[0071]
以上所述实施例的各技术特征可以进行任意的组合,为使描述简洁,未对上述实
施例中的各个技术特征所有可能的组合都进行描述,然而,只要这些技术特征的组合不存在矛盾,都应当认为是本说明书记载的范围。
[0072]
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对发明专利范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。因此,本发明专利的保护范围应以所附权利要求为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1