一种注射液中维生素C的检测方法与流程
一种注射液中维生素c的检测方法
技术领域
1.本发明涉及医药质量检测领域,特别涉及一种注射液中维生素c的检测方法。
背景技术:
2.长春西汀(vinpocetine,简称vin),化学名为:乙基(13as,13bs)
‑
13a
‑ꢀ
乙基
‑
2,3,5,6,13a,13b
‑
六氢
‑
1h
‑
吲哚[3,2,1
‑
de]吡啶并[3,2,1
‑
ij][1,5]二氮杂萘
‑
12
‑
羧酸。
[0003]
本品最早由匈牙利药物公司cedeon richter于1978年研发上市,主要用于治疗心脑血管疾病、缺血性高血压脑病、脑动脉硬化、脑局部缺血、间歇式脑血流供应不足、脑血管痉挛、脑血栓、衰老所致的脑部疾病等病症。
[0004]
本品化学结构为:
[0005][0006]
本品为长春西汀注射液,处方中用到的辅料有“酒石酸、维生素c、焦亚硫酸钠、山梨醇”,其中“维生素c”为抗氧剂,为注射液中存在变量的一个辅料,从处方研究的抗氧剂的选择试验可知,维生素c含量的多少会对成品的质量有一定的影响,故需对维生素c进行定量分析,以确保产品质量稳定性。
技术实现要素:
[0007]
鉴于此,本发明提出一种注射液中维生素c的检测方法,解决上述技术问题。
[0008]
本发明的技术方案是这样实现的:
[0009]
一种注射液中维生素c的检测方法,采用高效液相色谱法对长春西汀注射液中维生素c进行定量鉴别;所述高效液相色谱条件为:采用synergi hydro
‑
rp 色谱柱,采用流动相a和流动相b进行梯度洗脱,流动相a为含 0.018~0.020mol/l磷酸钾水溶液,流动相b为乙醇,梯度洗脱程序为:
[0010]
时间/min流动相a/%流动相b/%0.01
‑
1.0085151.01
‑
2.5045552.51
‑
3.5030703.51
‑
4.5090104.51
‑
7.001585
[0011]
。
[0012]
进一步的,对照品溶液配制如下:称取维生素c对照品,以0.008
‑
0.012mol/l 枸橼酸溶液为稀释剂,配制维生素c浓度为8
‑
12μg/ml的对照品溶液。优选地,对照品溶液配制如下:称取维生素c对照品,以0.01mol/l枸橼酸溶液为稀释剂,配制维生素c浓度为10μg/ml的对照品溶液。
[0013]
进一步的,供试品溶液配制如下:取长春西汀注射液,以0.008
‑
0.012mol/l 枸橼酸溶液为稀释剂,稀释70
‑
90倍,制得供试品溶液。优选地,供试品溶液配制如下:取长春西汀注射液,以0.01mol/l枸橼酸溶液为稀释剂,稀释80倍,制得供试品溶液。
[0014]
进一步的,检测波长为254nm。
[0015]
进一步的,柱温28~30℃。
[0016]
进一步的,进样量15~25μl。
[0017]
进一步的,流速0.8~1ml
·
min
‑
1。
[0018]
与现有技术相比,本发明的有益效果是:(1)本发明以一定浓度的枸橼酸溶液为稀释剂配制一定浓度的对照品溶液和供试品溶液,利用高效液相色谱法,设定特定的梯度洗脱程序,在一定色谱条件下,测定长春西汀注射液中维生素c 的含量,检测方法具有分离效果好、灵敏、准确等优点,保证了本品的质量稳定均一性及疗效。
[0019]
(2)本发明的质量控制方法简单、专属性强、重现性好,有效的保障了长春西汀注射液的质量和疗效,具有很强的实用性。
附图说明
[0020]
图1为本发明实施例1长春西汀注射液含量测定中维生素c对照品的 hplc图谱(扫描图);
[0021]
图2为本发明实施例1长春西汀注射液含量测定中维生素c供试品的hplc 图谱(扫描图)。
具体实施方式
[0022]
为了更好理解本发明技术内容,下面提供具体实施例,对本发明做进一步的说明。
[0023]
本发明实施例所用的实验方法如无特殊说明,均为常规方法。
[0024]
本发明实施例所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
[0025]
本发明所采用的长春西汀注射液由海南葫芦娃药业集团有限公司生产。
[0026]
实施例1
[0027]
(一)维生素c含量测定
[0028]
(1)对照品溶液配制:称取维生素c工作对照品适量,加0.01mol/l枸橼酸溶液溶解并稀释制成每1ml中含10μg维生素c的溶液作为对照品溶液;
[0029]
(2)供试品溶液配制:精密量取长春西汀注射液5ml,置于20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,即得供试品母液;再精密量取供试品母液1ml,置20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,取续滤液,即得供试品溶液;
[0030]
(3)吸取上述对照品溶液与供试品溶液,注入液相色谱仪进行测定,如下按外标法以峰面积计算,即得。其中色谱条件:采用synergi hydro
‑
rp色谱柱,检测波长为254nm;柱温28℃;进样量20μl;流速1ml
·
min
‑
1;采用流动相a 和流动相b进行梯度洗脱,流动相a为
含0.018mol/l磷酸钾水溶液,流动相b 为乙醇,梯度洗脱程序为表1:
[0031]
时间/min流动相a/%流动相b/%0.01
‑
1.0085151.01
‑
2.5045552.51
‑
3.5030703.51
‑
4.5090104.51
‑
7.001585
[0032]
。
[0033]
上述步骤(一)中,对hplc进行方法学考察,具体分析如下:
[0034]
(1)辅料干扰试验
[0035]
辅料空白溶液:精密量取空白辅料溶液5ml(除维生素c外),置20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,摇匀,即得。
[0036]
维生素c对照品溶液:取维生素c对照品适量,精密称定,加0.01mol/l 枸橼酸溶液溶解并稀释制成每1ml中含10μg的溶液,摇匀,即得。
[0037]
供试品溶液:精密量取长春西汀注射液5ml置20ml量瓶中,用0.01mol/l 枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,即得。
[0038]
测定法:精密量取上述3种溶液及溶剂空白各20μl,分别注入液相色谱仪,记录色谱图。
[0039]
从试验结果可知,溶剂没有吸收峰,空白辅料峰的保留时间为2.308分钟,供试品溶液中维生素c峰的保留时间为2.247分钟,空白辅料峰与维生素c峰重叠,干扰维生素c含量测定,但辅料峰峰面积较小,计算含量时可作相应扣除。
[0040]
(2)重复性试验
[0041]
精密量取长春西汀注射液6份,每份5ml,各置20ml量瓶中,用0.1mol/l 枸橼酸溶液稀释至刻度,摇匀,精密量取1ml,置20ml量瓶中,用0.1mol/l枸橼酸溶液稀释至刻度,摇匀,作为供试品溶液;另取维生素c工作对照品适量,精密称定,加0.01mol/l枸橼酸溶液溶解并稀释制成每1ml中含10μg的溶液,摇匀,作为对照品溶液;精密量取空白辅料溶液5ml(除维生素c外),置20ml 量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,摇匀,作为辅料空白溶液。精密量取辅料空白溶液、对照品溶液和各供试品溶液各20μl注入液相色谱仪,记录色谱图,并计算含量,其结果见表2:
[0042]
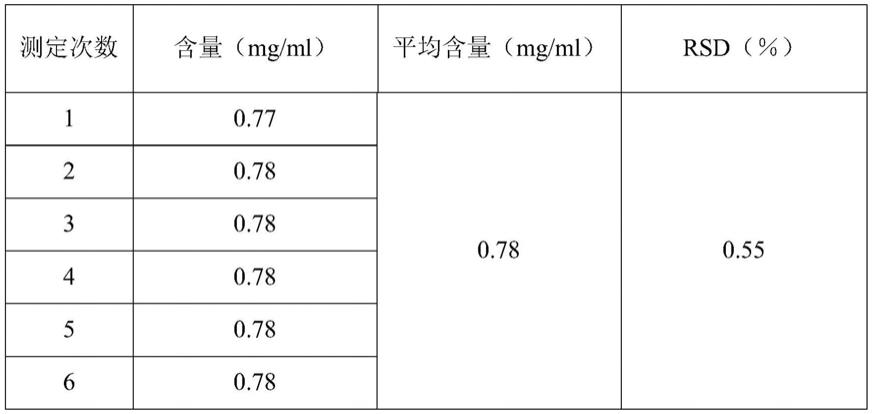
表2重复性试验结果
[0043][0044]
试验结果表明:连续测定6次含量平均值为0.78mg/ml,rsd值为0.55%,表明含量测定重复性试验良好。
[0045]
(3)精密度试验
[0046]
取维生素c工作对照品适量,精密称定,加0.01mol/l枸橼酸溶液溶解并稀释制成每1ml中含10μg的溶液,摇匀,作为对照品溶液。精密量取对照品溶液与溶剂空白溶液各20μl注入液相色谱仪,记录色谱图,并连续测定6次,考察其进样精密度,结果见以下表3:
[0047]
表3精密度试验结果
[0048][0049]
试验结果表明:连续进样6次,主峰峰面积rsd值为0.98%,表明进样精密度良好。
[0050]
(4)稳定性试验
[0051]
精密量取长春西汀注射液5ml,置20ml量瓶中,加0.01mol/l枸橼酸溶液稀释至刻度,摇匀,再精密量取1ml到20ml量瓶中,加0.01mol/l枸橼酸溶液稀释至刻度,摇匀,作为供试品溶液。同法制备2份。再精密量取空白辅料溶液5ml(除维生素c外),置20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,摇匀,作为辅料空白溶液。取供试品溶液在避光与不避光条件下于室温放置8小时,分别于0、2、4、6、8小时,各精密量取辅料空白溶液与供试品溶液20μl注入液相色谱仪,记录色谱图。考察主峰峰面积变化情况,试验结果详见表4
‑
5。
[0052]
表4溶液稳定性试验(避光)
[0053][0054][0055]
表5溶液稳定性试验(未避光)
[0056][0057]
试验结果表明:供试品溶液在避光与不避光条件下室温放置8小时,维生素c主峰面积的rsd均大于2%,说明溶液在室温下放置不稳定,应临用现配。
[0058]
(5)回收率试验
[0059]
供试品溶液:取维生素c工作对照品9份(其中每3份约含维生素c16.0mg、 20.0mg、24.0mg),精密称定,各置100ml量瓶中,再分别加入空白辅料溶液 5ml,加0.01mol/l枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,用0.01mol/l枸橼酸溶液稀释至刻度,摇匀,即得供试品溶液。
[0060]
对照品溶液:取维生素c工作对照品适量,精密称定,加0.01mol/l枸橼酸溶液溶解并定量稀释制成每1ml中含10μg的溶液,摇匀,即得对照品溶液。
[0061]
精密量取空白辅料溶液5ml(除维生素c外),置20ml量瓶中,用0.01mol/l 枸橼酸溶液稀释至刻度,摇匀,精密量取1ml置20ml量瓶中,摇匀,作为辅料空白溶液。
[0062]
测定:精密量取辅料空白溶液、对照品溶液和各供试品溶液各20μl注入液相色谱仪,记录色谱图,按外表法以峰面积计算含量,并计算回收率。试验结果见表6。
[0063]
表6回收率试验结果
[0064][0065]
试验结果表明:三个浓度的样品回收率在99.53%~101.74%,平均回收率为100.5%,rsd值为0.60%(n=9),回收率良好。
[0066]
实施例2
‑
本实施例与实施例1区别在于,流动相a磷酸钾水溶液浓度为 0.020mol/l。结果显示维生素c与长春西汀的峰形良好,没有相互干扰。
[0067]
实施例3
‑
本实施例与实施例1区别在于,柱温30℃。结果显示维生素c与长春西汀的峰形良好,没有相互干扰。
[0068]
实施例4
‑
本实施例与实施例1区别在于,进样量15μl。结果显示维生素c 与长春西汀的峰形良好,没有相互干扰。
[0069]
实施例5
‑
本实施例与实施例1区别在于,流速0.8ml
·
min
‑
1。结果显示维生素c与长春西汀的峰形良好,没有相互干扰。
[0070]
对比例1
‑
本实施例与实施例1区别在于,色谱柱替换为exformma c18柱。结果显示维生素c峰与长春西汀峰相互干扰。
[0071]
对比例2
‑
本实施例与实施例1区别在于,采用流动相a和流动相b进行梯度洗脱,以甲醇
‑
0.015mol/l醋酸钠(体积比5:95)为流动相。经检测,结果显示维生素c峰与长春西汀峰有明显干扰。
[0072]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1