一种用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用与流程
1.本发明属于分析化学技术领域,具体涉及一种用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用,尤其涉及一种专属性强、准确度高、精密度好、定量限低、检测限低的用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用。
背景技术:
2.现有技术例如cn105744940a和cn111670038a两篇专利公开报道了糖胺聚糖羧酸化衍生物作为药物具有抗肿瘤及抗肿瘤转移活性,具有广泛的应用前景。糖胺聚糖羧酸化衍生物为未分级肝素(ufh)经过两步氧化反应后得到的含有糖醛酸邻二醇结构氧化开环的双羧酸衍生物,其属于肝素衍生物,是一种链状、结构不均一的粘多糖物质。在药物代谢研究中,需要测定生物样品中药物的含量以评价该药物的药物代谢动力学性质。在生物样品中直接检测完整的结构不容易实现,而且由于生物样品中存在多种内源性物质,例如蛋白、磷脂等,常规的多糖测试方法易受到内源性物质的干扰而无法对糖胺聚糖羧酸化衍生物进行定量测定。因此,如何提供一种准确的糖胺聚糖羧酸化衍生物的检测方法,成为了亟待解决的问题。
技术实现要素:
3.针对现有技术的不足,本发明的目的在于提供一种用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用,尤其提供一种专属性强、准确度高、精密度好、定量限低、检测限低的用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用。
4.为达到此发明目的,本发明采用以下技术方案:
5.第一方面,本发明提供一种用于检测样品中糖胺聚糖羧酸化衍生物含量的方法,所述方法包括如下步骤:
6.(1)将含糖胺聚糖羧酸化衍生物的样品进行水解,得到含有式(i)所示化合物的水解液:
[0007][0008]
其中,各ra独立地为-so3h或-h,各rb独立地为h、-so3h或-c(o)ch3,各rc独立地为-so3h或-h,n为0、1、2、3、4或5;
[0009]
(2)采用液相色谱串联质谱对步骤(1)得到的水解液进行检测;
[0010]
(3)根据质谱信号峰面积对糖胺聚糖羧酸化衍生物标准品的量做的标准曲线计算
样品中糖胺聚糖羧酸化衍生物的含量;
[0011]
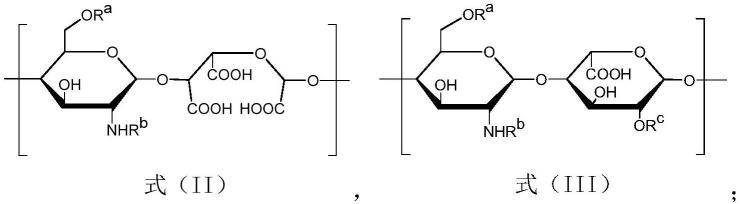
所述糖胺聚糖羧酸化衍生物包含式(ii)所示的结构单元和任选的式(iii)所示的结构单元:
[0012][0013]
其中,各ra独立地为-so3h或-h,rb独立地为h、-so3h或-c(o)ch3,rc独立地为-so3h或-h。
[0014]
优选地,所述式(i)所示化合物具有以下结构式中至少一种的结构:
[0015][0016]
其中,化合物(a)的质谱信号为ms(esi,neg.ion)m/z:432.0[m-h]-;
[0017]
化合物(b)的质谱信号为ms(esi,neg.ion)m/z:390.0[m-h]-;
[0018]
化合物(c)的质谱信号为ms(esi,neg.ion)m/z:522.98[m-2h]
2-。
[0019]
本发明所涉及的糖胺聚糖羧酸化衍生物包含如上所述式(ii)所示的结构单元和任选的式(iii)所示的结构单元,即糖胺聚糖化合物中己糖醛酸结构部分或全部开环。
[0020]
本发明所涉及的糖胺聚糖羧酸化衍生物经过水解后可以得到式(i)所示化合物,反应机理如方案1和2所示,其中,各ra独立地为-so3h或-h,各rb独立地为h、-so3h或-c(o)ch3,各rc独立地为-so3h或-h,n为0、1、2、3、4或5:
[0021]
方案1:
[0022][0023]
方案2:
[0024][0025]
在本发明所涉及的糖胺聚糖羧酸化衍生物的每条多糖链中,各双糖结构单元以任意顺序排列。
[0026]
由于糖胺聚糖羧酸化衍生物为非均一物质,在生物样品中直接检测完整的结构不容易实现,因此本发明所涉及的检测方法通过水解,可以稳定得到如上所述特定结构的水解产物化合物(a)、化合物(b)或化合物(c),该结构可以通过ms检测到并选择具有较高质谱丰度的水解产物,通过测定该水解产物的含量可以间接计算糖胺聚糖羧酸化衍生物的量。且该检测方法的专属性强、准确度高、精密度好、定量限低、检测限低。
[0027]
优选地,所述糖胺聚糖羧酸化衍生物的重均分子量为3000-20000da,例如3000da、5000da、7000da、8000da、9000da、10000da、11000da、12000da、13000da、13500da、14000da、16000da、18000da或20000da等,该数值范围内的其他具体点值均可选择,在此便不再一一
25min,例如15min、18min、20min、22min、25min等,上述各项数值范围内的其他具体点值均可选择,在此便不再一一赘述。
[0041]
优选地,所述液相色谱为反相色谱、尺寸排阻色谱或亲水色谱。
[0042]
优选地,所述液相色谱的流动相为流动相a和流动相b;所述流动相a为六氟异丙醇和戊胺的水溶液;所述流动相b为六氟异丙醇和戊胺的乙腈-水溶液;
[0043]
所述流动相a为含有45-55mm(例如45mm、48mm、50mm、52mm、55mm等)六氟异丙醇和13-17mm(例如13mm、15mm、17mm等)戊胺的水溶液;所述流动相b为含有45-55mm(例如45mm、48mm、50mm、52mm、55mm等)六氟异丙醇和13-17mm(例如13mm、15mm、17mm等)戊胺的乙腈-水溶液;所述流动相b中乙腈与水的体积比为70:30-80:20(例如70:30、75:25、80:20等)。上述各项数值范围内的其他具体点值均可选择,在此便不再一一赘述。
[0044]
进一步优选地,所述液相色谱的流动相为流动相a和流动相b,具体如下表所示。
[0045]
流动相a50mm六氟异丙醇,15mm戊胺,h2o流动相b50mm六氟异丙醇,15mm戊胺,乙腈/h2o(75/25,v/v)
[0046]
优选地,所述液相色谱的洗脱流程如下表所示:
[0047][0048][0049]
在本发明中,所述质谱条件示例性地可以选择如下条件内容:
[0050]
条件内容名称/指标质谱仪waters xevo g2-s qtof模式negative resolution mode[负离子分辨率模式]设定质量432.0da毛细管电压1.5kv取样椎25v源补偿电压80v源温度120℃脱溶剂温度500℃锥孔气流50l/hr
脱溶剂气流800l/hr采集起始分子量200采集终止分子量2000采集起始时间1.20mins采集终止时间6.0mins
[0051]
基于第一方面的内容,本发明还提供了一种全新的化合物,具体内容如下:
[0052]
第二方面,本发明提供一种化合物,所述化合物的结构如式(i)所示:
[0053][0054]
其中,各ra独立地为-so3h或-h,各rb独立地为h、-so3h或-c(o)ch3,各rc独立地为-so3h或-h,n为0、1、2、3、4或5。
[0055]
优选地,所述化合物具有以下其中之一的结构:
[0056][0057]
第三方面,本发明提供一种如第一方面所述的糖胺聚糖羧酸化衍生物的检测方法在糖胺聚糖羧酸化衍生物的药代动力学研究中的应用。
[0058]
第四方面,本发明提供一种如第一方面所述的糖胺聚糖羧酸化衍生物的检测方法在糖胺聚糖羧酸化衍生物药物制剂质量检测中的应用。
[0059]
相对于现有技术,本发明具有以下有益效果:
[0060]
由于糖胺聚糖羧酸化衍生物为非均一物质,在生物样品中直接检测完整的结构不容易实现,因此本发明所涉及的检测方法通过水解处理,可以稳定得到如上所述特定结构的水解产物化合物(a)、化合物(b)或化合物(c),该结构可以通过ms检测到并选择具有较高质谱丰度的水解产物,通过测定该水解产物的含量可以间接计算糖胺聚糖羧酸化衍生物的量。且该检测方法的专属性强、准确度高、精密度好、定量限低、检测限低。
附图说明
[0061]
图1是化合物(a)的质谱图;
[0062]
图2是化合物(a)的二级质谱图;
[0063]
图3是化合物(a)的氢谱图;
[0064]
图4是化合物(a)的碳谱图;
[0065]
图5是化合物(a)的13c dept 135
°
谱图;
[0066]
图6是化合物(a)的1h-1h cosy谱图;
[0067]
图7是化合物(a)的tocsy谱图;
[0068]
图8是化合物(a)的hsqc谱图;
[0069]
图9是化合物(a)的hmbc谱图;
[0070]
图10是化合物(c)的质谱图;
[0071]
图11是化合物(c)的二级质谱图;
[0072]
图12是化合物(c)的氢谱图;
[0073]
图13是化合物(c)的碳谱图;
[0074]
图14是化合物(c)的13c dept 135
°
谱图;
[0075]
图15是化合物(c)的1h-1h cosy谱图;
[0076]
图16是化合物(c)的tocsy谱图;
[0077]
图17是化合物(c)的roesy谱图;
[0078]
图18是化合物(c)的hsqc谱图;
[0079]
图19是化合物(c)的hmbc谱图。
具体实施方式
[0080]
下面通过具体实施方式来进一步说明本发明的技术方案。本领域技术人员应该明了,所述实施例仅仅是帮助理解本发明,不应视为对本发明的具体限制。
[0081]
下述实施例所涉及的sd大鼠购自北京维通利华实验动物技术有限公司。
[0082]
下述实施例所涉及的糖胺聚糖羧酸化衍生物h1011由专利cn111670038a中实施例3公开的制备方法制备得到,其重均分子量为9161da,开环度为43.1%。
[0083]
实施例1
[0084]
化合物(a)、化合物(b)和化合物(c)的制备:
[0085]
称取h1011(400mg)溶于水(4.0ml)中,将h1011水溶液加热至85℃反应72h,然后冷却至25℃;反应产物通过色谱技术分离纯化(色谱柱为dionex ionpac as11-hc,洗脱液m和n(具体组分见表1)),然后脱盐冻干得到化合物(a)、化合物(b)和化合物(c)。
[0086][0087]
表1
[0088][0089]
富集得到的化合物(a)、化合物(b)和化合物(c)通过质谱和核磁共振波谱法(一维1h-nmr、一维
13
cnmr、
13
c dept 135
°
、1h-1
h cosy、二维tocsy、hsqc、hmbc、二维dosy)鉴定结构。
[0090]
其中化合物(a)的表征数据如下:
[0091]
ms(esi,neg.ion)m/z:432.0[m-h]-;
[0092]1h nmr(600mhz,d2o):δ4.87(d,j=3.5hz,1h),4.34(dd,j=11.2,3.7hz,1h),4.29(d,j=4.6hz,1h),4.27(dd,j=11.0,2.1hz,1h),4.20(d,j=4.6hz,1h),4.05(ddd,j=10.1,3.7,2.2hz,1h),3.96(dd,j=10.6,3.5hz,1h),3.81(dd,j=10.5,9.2hz,1h),3.59(dd,j=10.1,9.2hz,1h),2.07(s,3h).
[0093]
13
c nmr(151mhz,d2o):δ24.79,56.23,69.39,71.95,73.04,74.14,76.51,83.25,99.56,177.34,178.79,179.99.
[0094]
化合物(a)的表征图谱如图1-图9所示。
[0095]
其中化合物(b)的表征数据如下:
[0096]
ms(esi,neg.ion)m/z:390.0[m-h]-;
[0097]
其中化合物(c)的表征数据如下:
[0098]
ms(esi,neg.ion)m/z:522.98[m-2h]
2-;
[0099]1h nmr(600mhz,d2o):δ5.37(d,j=3.5hz,1h),5.25
–
5.23(m,1h),5.16(d,j=
3.6hz,1h),5.15
–
5.12(m,1h),4.38
–
4.28(m,5h),4.23(dd,j=11.4,2.1hz,1h),4.19(dd,j=11.1,2.1hz,1h),4.13(dd,j=2.9hz,1h),3.87(dt,j=9.7,2.7hz,1h),3.84(dt,j=9.9,2.6hz,1h),3.78
–
3.70(m,2h),3.64(q,j=7.1hz,1h),3.60(dd,j=9.9hz,1h),3.56(dd,j=9.5hz,1h),3.25(dd,j=10.1,3.5hz,3h).
[0100]
13
c nmr(151mhz,d2o):δ60.45,60.63,68.92,69.10,70.44,70.60,71.82,72.44,72.80,73.05,73.50,74.54,77.54,78.74,79.51,81.24,100.90,101.38,101.69,175.69,176.18,177.23.
[0101]
化合物(c)的表征图谱如图10-图19所示。
[0102]
实施例2
[0103]
本实施例将本发明所涉及的糖胺聚糖羧酸化衍生物的检测方法应用于药代动力学研究(以化合物(a)作为检测对象),具体内容如下:
[0104]
(1)试验方法
[0105]
(1.1)实验动物:健康成年雄性sd大鼠6只,其中3只用于取空白血浆制作标准曲线,3只用于进行大鼠单次给药后血药浓度检测。
[0106]
(1.2)药物配制:称取糖胺聚糖羧酸化衍生物h1011用水配置60mg/kg的药物溶液。
[0107]
(1.3)给药和样品采集:皮下注射给药60mg/kg后,分别在时间点0、0.25、0.5、1、2、4、6、8、24h采血,采集全血后置于k2edta抗凝试管中,随后离心15min,分离得到血浆样品。
[0108]
(1.4)标准曲线的绘制:
[0109]
(1.4.1)称取糖胺聚糖羧酸化衍生物h1011并将其配成1mg/ml的水溶液,以上述空白血浆作为稀释液逐级稀释糖胺聚糖羧酸化衍生物水溶液,配置2μg/ml、4μg/ml、8μg/ml、16μg/ml、32μg/ml、64μg/ml、128μg/ml、256μg/ml的标准溶液,在85℃条件下水解72h;
[0110]
(1.4.2)水解后的标准溶液进行检测前处理,向水解后的标准溶液中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0111]
(1.4.3)进行液相色谱串联质谱检测,测得谱图,色谱条件如表2所示,质谱条件如表3所示:
[0112]
表2
[0113]
[0114][0115]
表3
[0116][0117]
[0118]
(1.4.4)以糖胺聚糖羧酸化衍生物标准溶液与化合物(a)峰面积线性关系作标准曲线,化合物(a)质谱信号为ms(esi,neg.ion)m/z:432.0[m-h]-;线性方程为:y=36.2154x-0.3216;相关系数为:r2=0.9987,其中,y为峰面积,x为标准溶液浓度。
[0119]
(1.5)检测血浆样品中糖胺聚糖羧酸化衍生物的含量:
[0120]
(1.5.1)将步骤(1.3)获得的血浆样品在85℃条件下水解72h,然后向其中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0121]
(1.5.2)进行液相色谱串联质谱检测,测得化合物(a)质谱峰面积,色谱条件如上表2所示,质谱条件如上表3所示;
[0122]
(1.5.3)根据化合物(a)质谱峰面积结合步骤(1.4)中绘制的标准曲线,计算得到各时间点血浆样品中糖胺聚糖羧酸化衍生物的浓度,并根据药物浓度-时间曲线计算药代动力学参数。
[0123]
(2)试验结果如表4所示:
[0124]
表4
[0125]
给药途径剂量auc
0-24
(h*μg/ml)t
1/2
(h)cl(ml/min/kg)i.h.60mg/kg537.473.750.110
[0126]
(3)方法学验证
[0127]
(3.1)专属性
[0128]
配制超纯水对照溶液和空白血浆对照溶液,经过与上述相同的高温水解、前处理过程,然后经过上述相同条件的液相色谱串联质谱检测,在超纯水对照和血浆对照溶液中未检测到432.0da的信号峰,即化合物(a)的质谱信号峰,表明超纯水和空白血浆对检测无干扰,本检测方法专属性强。
[0129]
(3.2)定量限和检测限
[0130]
经计算,本方法的定量限为0.8μg/ml,检测限为0.2μg/ml。
[0131]
(3.3)准确度
[0132]
设置1μg/ml、50μg/ml、120μg/ml三个浓度,测试糖胺聚糖羧酸化衍生物血浆样品,经计算回收率为82.6%-110.8%,且各个浓度6次实验结果的rsd值依次为4.2%、2.2%和1.3%。
[0133]
(3.4)精密度
[0134]
选取50μg/ml糖胺聚糖羧酸化衍生物血浆溶液,由两名不同检测员各检测6次,第一名检验员6次实验结果的rsd为2.0%,第二名检验员6次实验结果的rsd为1.8%,两名检验员12次实验结果的rsd为2.1%,均满足≤10.0%的可接受标准。方法精密度良好。
[0135]
(3.5)溶液稳定性
[0136]
选取50μg/ml糖胺聚糖羧酸化衍生物血浆溶液,水解并进行前处理,样品溶液第5天的检测结果为0时间的97.2%,符合标准。
[0137]
实施例3
[0138]
本实施例将本发明所涉及的糖胺聚糖羧酸化衍生物的检测方法应用于药代动力学研究(以化合物(b)作为检测对象),具体内容如下:
[0139]
(1)试验方法
[0140]
(1.1)实验动物:健康成年雄性sd大鼠6只,其中3只用于取空白血浆制作标准曲线,3只用于进行大鼠单次给药后血药浓度检测。
[0141]
(1.2)药物配制:称取糖胺聚糖羧酸化衍生物h1011用水配置60mg/kg的药物溶液。
[0142]
(1.3)给药和样品采集:皮下注射给药60mg/kg后,分别在时间点0、0.25、0.5、1、2、4、6、8、24h采血,采集全血后置于k2edta抗凝试管中,随后离心15min,分离得到血浆样品。
[0143]
(1.4)标准曲线的绘制:
[0144]
(1.4.1)称取糖胺聚糖羧酸化衍生物h1011并将其配成1mg/ml的水溶液,以上述空白血浆作为稀释液逐级稀释糖胺聚糖羧酸化衍生物水溶液,配置2μg/ml、4μg/ml、8μg/ml、16μg/ml、32μg/ml、64μg/ml、128μg/ml、256μg/ml的标准溶液,在90℃条件下水解48h;
[0145]
(1.4.2)水解后的标准溶液进行检测前处理,向水解后的标准溶液中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0146]
(1.4.3)进行液相色谱串联质谱检测,测得谱图,色谱条件如上表2所示,质谱条件如上表3所示,设置分子量为390.0da;
[0147]
(1.4.4)以糖胺聚糖羧酸化衍生物标准溶液与化合物(b)质谱峰面积线性关系作标准曲线,化合物(b)质谱信号为ms(esi,neg.ion)m/z:390.0[m-h]-;做出线性方程为:y=26.0235x;相关系数为0.9981,其中,y为峰面积,x为标准溶液浓度。
[0148]
(1.5)检测血浆样品中糖胺聚糖羧酸化衍生物的含量:
[0149]
(1.5.1)将步骤(1.3)获得的血浆样品在90℃条件下水解48h,然后向其中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0150]
(1.5.2)进行液相色谱串联质谱检测,测得化合物(b)峰面积,色谱条件如上表2所示,质谱条件如上表3所示,设置分子量为390.0da;
[0151]
(1.5.3)根据化合物(b)质谱峰面积结合步骤(1.4)中绘制的标准曲线,计算得到各时间点血浆样品中糖胺聚糖羧酸化衍生物的浓度,并根据药物浓度-时间曲线计算药代动力学参数。
[0152]
(3)方法学验证
[0153]
(3.1)专属性
[0154]
配制超纯水对照溶液和空白血浆对照溶液,经过与上述相同的高温水解、前处理过程,然后经过上述相同条件的液相色谱串联质谱检测,在超纯水对照和血浆对照溶液中未检测到390.0da的信号峰,即化合物(b)的质谱信号峰,表明超纯水和空白血浆对检测无干扰,本检测方法专属性强。
[0155]
(3.2)定量限和检测限
[0156]
经计算,本方法的定量限为1.1μg/ml,检测限为0.55μg/ml。
[0157]
(3.3)准确度
[0158]
设置1μg/ml、50μg/ml、120μg/ml三个浓度,测试糖胺聚糖羧酸化衍生物血浆样品,经计算回收率为81.2%-115.8%,且各个浓度6次实验结果的rsd值依次为5.4%、1.8%和2.0%。
[0159]
(3.4)精密度
[0160]
选取50μg/ml糖胺聚糖羧酸化衍生物血浆溶液,由两名不同检测员各检测6次,第一名检验员6次实验结果的rsd为1.6%,第二名检验员6次实验结果的rsd为2.6%,两名检验员12次实验结果的rsd为2.2%,均满足≤10.0%的可接受标准。方法精密度良好。
[0161]
(3.5)溶液稳定性
[0162]
选取50μg/ml糖胺聚糖羧酸化衍生物血浆溶液,水解并进行前处理,样品溶液第5天的检测结果为0时间的97.8%,符合标准。
[0163]
实施例4
[0164]
本实施例将本发明所涉及的糖胺聚糖羧酸化衍生物的检测方法应用于药代动力学研究(以化合物(c)作为检测对象),具体内容如下:
[0165]
(1)试验方法
[0166]
(1.1)实验动物:健康成年雄性sd大鼠6只,其中3只用于取空白血浆制作标准曲线,3只用于进行大鼠单次给药后血药浓度检测。
[0167]
(1.2)药物配制:称取糖胺聚糖羧酸化衍生物h1011用水配置60mg/kg的药物溶液。
[0168]
(1.3)给药和样品采集:皮下注射给药60mg/kg后,分别在时间点0、0.25、0.5、1、2、4、6、8、24h采血,采集全血后置于k2edta抗凝试管中,随后离心15min,分离得到血浆样品。
[0169]
(1.4)标准曲线的绘制:
[0170]
(1.4.1)称取糖胺聚糖羧酸化衍生物h1011并将其配成1mg/ml的水溶液,以上述空白血浆作为稀释液逐级稀释糖胺聚糖羧酸化衍生物水溶液,配置2μg/ml、4μg/ml、8μg/ml、16μg/ml、32μg/ml、64μg/ml、128μg/ml、256μg/ml的标准溶液,在90℃条件下水解36h;
[0171]
(1.4.2)水解后的标准溶液进行检测前处理,向水解后的标准溶液中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0172]
(1.4.3)进行液相色谱串联质谱检测,测得谱图,色谱条件如上表2所示,质谱条件如上表3所示,设置分子量为522.98da;
[0173]
(1.4.4)以糖胺聚糖羧酸化衍生物标准溶液与化合物(c)质谱峰面积线性关系作标准曲线,化合物(c)质谱信号为ms(esi,neg.ion)m/z:522.98[m-2h]
2-;做出线性方程。
[0174]
(1.5)检测血浆样品中糖胺聚糖羧酸化衍生物的含量:
[0175]
(1.5.1)将步骤(1.3)获得的血浆样品在90℃条件下水解36h,然后向其中加入百分之一体积比的三氟乙酸(5%,v/v)和两倍体积的乙腈/甲醇(v/v,50/50),混匀,然后置于-20℃静置20min,离心;取上清液干燥后再用超纯水复溶;
[0176]
(1.5.2)进行液相色谱串联质谱检测,测得化合物(c)质谱峰面积,色谱条件如上表2所示,质谱条件如上表3所示;
[0177]
(1.5.3)根据化合物(c)质谱峰面积结合步骤(1.4)中绘制的标准曲线,计算得到各时间点血浆样品中糖胺聚糖羧酸化衍生物的浓度,并根据药物浓度-时间曲线计算药代动力学参数。
[0178]
申请人声明,本发明通过上述实施例来说明本发明的一种用于检测样品中糖胺聚糖羧酸化衍生物含量的方法及其应用,但本发明并不局限于上述实施例,即不意味着本发明必须依赖上述实施例才能实施。所属技术领域的技术人员应该明了,对本发明的任何改进,对本发明产品各原料的等效替换及辅助成分的添加、具体方式的选择等,均落在本发明
的保护范围和公开范围之内。
[0179]
以上详细描述了本发明的优选实施方式,但是,本发明并不限于上述实施方式中的具体细节,在本发明的技术构思范围内,可以对本发明的技术方案进行多种简单变型,这些简单变型均属于本发明的保护范围。
[0180]
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合,为了避免不必要的重复,本发明对各种可能的组合方式不再另行说明。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1