牛病原体阵列的制作方法
牛病原体阵列
背景技术:
1.兽医体外诊断试验是确定动物健康状态和识别疾病爆发的必要工具。准确和及时的诊断将带来无数益处,包括:最大限度地减少经济损失、最大限度地提高生产力、显著改善动物福利、减少抗生素/驱虫药抗性、在贸易方面提供竞争优势/保证、以及支持全球同一健康倡议。
2.牛感染性疾病的血清学检测通常使用耗时、昂贵且需要大量样品的单重elisa进行。
3.牛传染性鼻气管炎(ibr)是由牛疱疹病毒1型(bohv-1)引起的高传染性、感染性呼吸道疾病。它影响所有年龄的牛并且特征在于上呼吸道的急性炎症。该病毒还可引起结膜炎、流产、脑炎和全身性感染。一旦动物从初次感染中恢复,它们会发展出终生潜伏期,这意味着受感染的动物具有持续感染畜群的风险。
4.ibr没有可用的直接的治疗方法。一旦识别,将受感染的动物与畜群的其余部分隔离,并在必要时用抗炎药和抗生素治疗继发性感染。还需要识别载体牛并将其从畜群中移除。
5.ibr的控制主要依赖于疫苗的使用。目前可用的疫苗包括改良活病毒(mlv)疫苗和灭活或灭活病毒(kv)疫苗。优选使用标记疫苗,因为它们具有缺失的特异性抗原,因此它们刺激的抗体可以与天然获得性感染产生的抗体区分开。
6.牛病毒性腹泻(bvd)是牛和其他反刍动物的另一种经济上重要的疾病,并由牛病毒性腹泻病毒(bvdv)引起。它是畜群中呼吸问题和生殖问题的常见原因。胎畜的先天性感染可导致吸收、流产或死产,即使受bvdv感染的犊牛在子宫内感染后存活,它们也可能虚弱且异常小。感染也将持续其一生,并且它们可以不断地将bvdv流出到农场环境中。
7.bvd的治疗主要受限于支持疗法。一旦识别,受感染的动物应被宰杀,诊断试验对于识别持续感染的动物是重要的。与ibr一样,活疫苗和灭活病毒疫苗都可用于bvd。灭活的(killed/inactivated)和改良的活bvd病毒疫苗都可以使用。使用灭活疫苗接种后,体液抗体应答主要针对bvd结构蛋白,如erns和e2,而针对非结构蛋白(如ns3)的反应大量减少或不存在(ridpath 2013)。此外,改良的活疫苗可以通过缺失病毒蛋白(如erns)而减弱,因此检测针对该蛋白的抗体可能仅作为天然感染的结果而发生。
8.新孢子虫病(neosporosis)是由原生动物犬新孢子虫(neospora caninum)引起的感染,其是导致牛流产的主要原因,从而导致重大经济损失和产量下降。发生不同阶段的感染,包括速殖子(急性感染)和缓殖子(慢性感染)。目前还没有任何对牛新孢子虫病的治疗证实有效,因此控制是基于生物安全和管理实践。受感染的牛需要通过诊断试验来识别,并从畜群中移除。所有具有新孢子虫抗体的牛都是其犊牛的传染源,流产的风险显著增加,而且平均而言,与抗体阴性的奶牛相比,产奶量更少。在诊断新孢子虫病之前,重要的是要消除畜群中的其他流产原因,特别是bvd或钩端螺旋体病(leptospirosis)。
9.约内氏病(johne's disease),或称副结核,是由鸟结核分枝杆菌副结核亚种(mycobacterium avium subspecies paratuberculosis)(map)引起的反刍动物慢性肠炎。
据认为,超过一半的欧洲奶牛群可能被感染(nielson&toft,2009),而且人们越来越关心这种细菌在人类食物链中的存在是克罗恩病(crohn's disease)的一个致病因素(chiodini等人,2012)。
10.由于感染的缓慢、渐进性,约内氏病的体征可能直到初次感染后数年才出现。当它们最终确实出现时,体征是长期腹泻和尽管食欲良好但重量减轻。一旦出现临床体征,动物将不会恢复并将继续恶化。与上述病理情况一样,目前没有治疗约内氏病的方法。可获得疫苗,但预防性方法可能更有效。
11.只有一小部分动物会出现明显的很容易被识别的临床体征,从而使得它们被从畜群中去除。动物中亚临床疾病的识别是疾病控制的关键,所述亚临床疾病可使生物体长期流出并因此成为畜群其它成员的感染源。动物通常在年轻时被感染,可能需要几年时间才能出现临床体征。pcr和血清学试验可用于副结核分枝杆菌(m.paratuberculosis)。
12.钩端螺旋体病是一种人畜共患病,由钩端螺旋体属(leptospira)的细菌引起。在牛中发现了许多血清型,其患病率根据地理位置而变化。这些血清型包括哈德焦型(hardjo)、波摩那型(pomona),犬型(canicola)、黄疸出血型(icterohaemorrhagiae)和感冒伤寒型(grippotyphosa)。牛哈德焦型钩端螺旋体(leptospira hardjo-bovis)是牛中唯一宿主适应性(host-adapted)的钩端螺旋体属血清型,并且可以感染任何年龄的动物,包括小犊牛。由于牛是牛哈德焦型(hardjo-bovis)的维持宿主(maintenance host),感染这种血清型后经常会在肾脏中产生与长期尿流出(urinary shedding)相关的带菌状态。
13.此外,牛哈德焦型的感染可持续存在于生殖道中。可由持续性生殖道感染引起的不孕也许是钩端螺旋体病的最具经济破坏性的方面。低抗体滴度通常与牛哈德焦型感染相关,使得检测和诊断困难。
14.由非宿主适应性钩端螺旋体属血清型引起的钩端螺旋体病可能很严重,特别是在犊牛中,其症状包括高热、贫血、血尿、黄疸,有时在3-5天内死亡。在年长的牛中,初始症状如发烧和昏睡往往比较轻微,而且经常不被注意。此外,钩端螺旋体病对老年动物通常不会致命。被感染的泌乳牛产奶量较少,而且在一周或更长时间内,它们产的奶是浓稠和黄色的。妊娠牛的感染可导致胚胎死亡、流产、死产、胎盘滞留和虚弱犊牛的出生。流产通常发生在感染后的3-10周。采用抗生素疗法可用于患有钩端螺旋体病的动物,也可以用于消除持续性感染。
15.蠕虫寄生虫(helminth parasite)肝片吸虫(fasciola hepatica)在牛和其它反刍动物中引起肝吸虫病(肝片吸虫病(fascioliasis)),并且也是重要的人病原体。牛感染导致死亡损失、增重减少、产奶量减少和屠体(carcass)品质降低。除了寄生虫感染的直接影响外,肝片吸虫和其它蠕虫损害其宿主的免疫应答,使其更易受其它感染并影响血清学试验的敏感度。实际上,肝片吸虫感染与未能在奶牛中检测到牛结核病相关(claridge等人,2012)。
16.牛感染性疾病的快速和准确诊断对于疾病控制和从畜群中根除以及治疗受影响的个体至关重要。商购获得的elisa被设计为检测单一生物标记,并因此允许在单一测定中对样品进行多种病原体筛查的多重试验,将为常规试验提供多种优势。本文提供了解决该需求的方法、基质和试剂盒。
17.参考文献
18.ridpath 2013.biologicals.2013jan;41(1):14-9.pmid:22883306nielson&toft 2009.prev vet med.2009jan 1;88(1):1-14.pmid:18817995
19.chiodini等人2012.crit rev microbiol.2012feb;38(1):52-93.pmid:22242906
20.claridge等人2012.nat commun.2012may 22;3:853.pmid:22617293
附图说明
21.图1说明了当前阵列的间接elisa格式。将来自病原体的抗原固定在与牛样品接触的基质上。如果样品含有抗原的任何抗体,则它们将结合,并且可以使用标记的检测抗体检测这些抗体。
22.图2在evidence investigator(randox laboratories ltd,crumlin,northern ireland)上进行的牛病原体阵列的测定方案实例。总测定时间为2.5小时。
23.图3多重阵列的基本阳性或阴性输出的实例
24.图4多重阵列的阳性百分率输出的实例
技术实现要素:
25.本发明的第一方面是一种筛查牛样品中针对多种重要病原体的抗体的多重方法(multiplex method)。这些病原体包括牛病毒性腹泻病毒(bvdv)、牛疱疹病毒1型(bohv-1)、副结核分枝杆菌(map)、钩端螺旋体属种、犬新孢子虫和肝片吸虫。
26.本发明的第二方面是一种能够进行这种多重检测的基质。所述基质具有两种或更多种的抗原,这些抗原选自bvdv ns3、bvdv erns、bvdv e2、bohv-1糖蛋白b、bohv-1糖蛋白e、map ppa、哈德焦型钩端螺旋体lipl32、犬新孢子虫srs2、犬新孢子虫sag1和肝片吸虫组织蛋白酶l1。
27.本发明的第三方面是一种筛查牛样品中针对副结核分枝杆菌的抗体的方法,包括使样品与其上固定有副结核分枝杆菌的抗原的基质和含有草分枝杆菌(mycobacterium phlei)的分析缓冲液接触。
28.本发明的第四方面是一种使用带有固定化靶抗原糖蛋白b和糖蛋白e的基质区别受bohv-1感染动物与免疫动物(diva)以及使用带有固定化靶抗原ns3和erns的基质区别受bvdv感染动物与免疫动物(diva)的方法。
29.本发明的第五方面是一种用于多重阵列的归一化方法,其能使结果易于解释并消除批次间差异。与对照相比,每个样品的阳性百分率或阴性百分率的附加信息有指示感染阶段,影响治疗途径,并能识别需要后续试验或监测的动物的可能性。
具体实施方式
30.除非另有说明,根据本领域技术人员已知的常规用法使用技术术语。
31.在第一个实施方案中,本发明包含一种筛查牛样品中针对多种病原体的抗体的方法,所述方法包括:(a)将牛样品与固定有两种或更多种病原体的两种或更多种抗原的基质接触(b)洗去未结合的样品(c)使用标记的检测抗体检测样品中与基质上的固定化抗原结合的任何抗体。
32.在一个优选的实施方案中,两种或更多种病原体选自bvdv、bohv-1、副结核分枝杆
菌、钩端螺旋体属种、犬新孢子虫和肝片吸虫。本文公开了任意两种、三种、四种或五种病原体的组合,或者实际上是所有六种病原体的组合。该方法包括将牛样品与固定有两种或更多种病原体靶标的两种或更多种抗原的基质接触,优选地,当病原体靶标之一是bvdv时,固定化抗原是ns3、erns和e2中的一种或多种。这取决于样品类型,例如,当样品是乳时,优选的bvdv抗原是ns3和erns。然而,当样品是血清时,优选的抗原是ns3和e2。当病原体靶标之一是bohv-1时,固定化抗原优选gb和ge。当病原体靶标之一是副结核分枝杆菌时,固定化抗原优选map ppa。当病原体靶标之一是钩端螺旋体属种时,固定化抗原优选lipl32。当病原体靶标之一是犬新孢子虫时,固定化抗原优选srs2和sag1中的一种或两种。当病原体靶标之一是肝片吸虫时,固定化抗原优选组织蛋白酶l1。
33.在一个优选的实施方案中,靶病原体至少包括bvdv、bohv-1和副结核分枝杆菌。在另一个优选的实施方案中,靶病原体至少包括bvdv、bohv-1和犬新孢子虫。在另一个优选的实施方案中,靶病原体至少包括bvdv、犬新孢子虫和钩端螺旋体属血清型。
34.本文所用的术语“筛查”是指测定样品中是否存在针对病原体的抗体。这些抗体可以是针对某种病原体的疫苗接种的结果或来自某种病原体的天然获得性感染的结果。
35.本文所用的术语“牛”是指牛亚科生物亚科(biological subfamily bovinae)内的物种。更具体地,它是指牛属(bos)中的物种,甚至更具体地是指家牛、普通牛(bos taurus)。
36.本文中所指的“样品”包括从牛受试者获得的任何合适的样品,其中可以检测病原体的抗体,这样的样品包括乳、全血、血浆、血清、尿、唾液、精液、脑脊液和组织提取物。当样品是全脂乳时,可将样品离心或静置以使乳脂与抗乳血清(lactoserum)分离。然后可以将抗乳血清用作试验样品。优选样品是乳和血清。
37.术语“抗体”是指特异性识别靶标上表位的免疫球蛋白,如通过重链和轻链的免疫球蛋白可变结构域(vh和vl)(更具体地是互补决定区(cdr))的结合特征所确定的。许多可能的抗体形式是本领域已知的,并被包括在上述定义中。这些可包括但不限于多种完整的单克隆抗体或包含完整的单克隆抗体的多克隆混合物、抗体片段(例如fab、fab'、f(ab')2和fv片段、包含抗体片段的线性抗体、单链抗体和多特异性抗体)、单链可变片段(scfv)、多特异性抗体、嵌合抗体、人源化抗体以及包含识别靶标上给定表位所必需的结构域的融合蛋白。抗体可包含γ、δ、α、μ和ε型重链恒定结构域,其中包含所述结构域的抗体分别被指定为igg、igd、iga、igm或ige类。根据重链恒定结构域序列的变化,类别可进一步划分为亚类(例如igg1-4)。根据恒定区的特性,轻链被指定为κ或λ类。抗体还可以与各种可检测标记缀合,包括但不限于放射性标记物、dna、rna、荧光分子、或转换基质的酶,从而可以检测其吸光度或化学发光。抗体还可以被修饰以使其以特定或非特定的方向固定在基质中。
38.检测抗体可以包含可检测的标记,一旦发生了结合事件,就可以使其可视化。可检测标记的非限制性实例包括放射性核苷酸、荧光团、染料或能转换基质的酶,从而可以检测其吸光度或化学发光信号。一个优选的可检测标记是辣根过氧化物酶(hrp)。检测抗体可以是任何对牛抗体具有足够交叉反应性的抗体,这些抗体在当前的测定中靶向牛抗体。例如,合适的检测抗体可以是源于绵羊、山羊、兔子或小鼠的抗igg或抗igm抗体。检测抗体也可以是具有足够交叉反应性以检测在另一物种中产生的对照中的抗体的任何抗体。优选地同一检测抗体被用于多重格式的所有阵列。在优选的实施方案中,检测抗体是抗牛igg或抗牛
igm。
39.本文所用的术语“ns3”是指牛病毒性腹泻病毒的非结构蛋白ns3(uniprot登录号p19711)。
40.本文所用的术语“erns”是指在病毒粒子表面发现的bvdv糖蛋白erns(uniprot登录号p19711)。
41.本文所用的术语“e2”是指bvdv糖蛋白e2(uniprot登录号p19711)。
42.本文所用的术语“gb”是指牛疱疹病毒1型的包膜糖蛋白b(uniprot登录号p12640)。本文所用的术语“ge”是指牛疱疹病毒1型的包膜糖蛋白e(uniprot登录号q08101)。
43.本文所用的术语“ppa”是指鸟结核分枝杆菌的原生质抗原,其是用于ptb血清学检测的最常见的抗原。
44.本文所用的术语“lipl32”是指钩端螺旋体属主要外膜蛋白lipl32(uniprot登录号q04sb6)。本文所用的术语“钩端螺旋体属种”是指钩端螺旋体属中能够感染牛的任何细菌。这些包括但不限于哈德焦血清型型博氏钩端螺旋体(leptospira borgpetersenii serovar hardjo)、哈德焦血清型问号钩端螺旋体(leptospira interrogans serovar hardjo)和波摩那血清型问号钩端螺旋体(leptospira interrogans serovar pomona)。
45.本文所用的术语“srs2”是指犬新孢子虫表面抗原相关序列2(uniprot登录号q9tvp5),也被称为p35。
46.本文所用的术语“sag1”是指犬新孢子虫表面抗原1(uniprot登录号q9tvv8),也被称为p29。
47.本文所用的术语“组织蛋白酶l1”是指肝片吸虫组织蛋白酶l1(uniprot登录号q7jnq9)。
48.本发明还提供了一种能够多重筛查牛样品中病原体抗体的基质。在所述基质的表面上固定两种或更多种抗原,优选来自两种或更多种病原体,其选自bvdv ns3、bvdv erns、bohv-1糖蛋白b、bohv-1糖蛋白e、map ppa、哈德焦型钩端螺旋体lipl32、犬新孢子虫srs2、犬新孢子虫sag1和肝片吸虫组织蛋白酶l1。具有任何两、三、四、五、六、七、八或九种这些抗原组合的基质是合适的。本发明优选的基质包括其上已经固定有抗原的那些基质,抗原为:
49.a)ns3和erns
50.b)gb和ge
51.c)srs2和sag1
52.d)ppa和组织蛋白酶l1
53.e)ns3、erns和lipl32
54.f)gb、ge和lipl32
55.g)srs2、sag1和lipl32
56.h)srs2、sag1和组织蛋白酶l1
57.i)ns3、erns、gb和ge
58.j)ns3、erns、srs2和sag1
59.k)gb、ge、srs2和sag1
60.l)ns3、erns、gb、ge和ppa
61.m)ns3、erns、gb、ge和srs2和sag1
62.n)ns3、erns、srs2、sag1和lipl32
63.o)ns3、erns、gb、ge、ppa、lipl32、srs2、sag1和组织蛋白酶l1。
64.在进一步的实施方案中,本发明的基质还可以包括,除了erns或作为erns的取代物的固定化的bvdv e2抗原。此外,本发明的基质可以包括针对沙门氏菌属(salmonella)种的另外的固定化抗原,例如都柏林沙门氏菌(salmonella dublin)或鼠伤寒沙门氏菌(salmonella typhimurium)中的至少一种。
65.本发明的基质可以针对特定的病原体群进行调整。例如,牛生殖病原体阵列可包括具有bvdv、bohv-1、钩端螺旋体属种、犬新孢子虫的固定化抗原以及引起生殖病症的其它病原体(如伯纳特立克次氏体(coxiella burnetti)和布鲁氏菌病(brucellosis))的固定化抗原的基质。牛呼吸病原体阵列可包括具有bvdv、bohv-1固定化抗原以及引起呼吸失调的其它病原体如牛呼吸道合胞病毒(brsv)、3型副流感病毒(pi3v)和牛支原体(mycoplasma bovis)的固定化抗原的基质。牛肠病原体阵列可包括具有副结核和肝片吸虫的固定化抗原以及引起肠道病症的其它病原体如沙门氏菌属种或冠状病毒(coronavirus)种的固定化抗原的基质。牛寄生虫阵列可包括具有犬新孢子虫和肝片吸虫的固定化抗原以及其它寄生虫例如奥斯特线虫(ostertagia ostertagi)和胎生网尾线虫(dictyocaulus viviparous)的固定化抗原的基质。
66.本发明的“抗原”可以是来自靶病原体的任何蛋白质或其片段,其可以在受感染的动物中诱导免疫应答。本领域技术人员将理解这些蛋白质的重组或突变形式作为elisa格式的捕获抗原可以是合适的,并且在某些情况下是有利的。本技术中显示的数据是使用重组蛋白捕获抗原产生的,除了用于map的抗原,其是来自分枝杆菌属种(mycobacterium spp.)的无菌、过滤和冻干的原生质细胞提取物。用于肝片吸虫的捕获抗原是灭活的重组组织蛋白酶l1变体gly
26
。
67.优选将抗原固定在基质的表面上,优选共价固定。基质可以是能够支持一种或多种抗原的任何物质,但优选是固态装置,如生物芯片。生物芯片是平面基质,其可以是例如基于矿物或聚合物基的,但优选陶瓷。
68.优选地,在本发明的方法中使用固态装置,优选生物芯片阵列技术系统(bat)(可从randox laboratories limited获得)。更优选地,可使用evidence evolution、evidence、evidence investigator和multistat仪器(可从randox laboratories获得)来确定样品中是否存在抗体。
69.本发明的抗原或其片段被固定在包含一个或多个支持基质的多重系统上。支持基质可包括固态装置,如平面、珠(bead)或微粒(microparticle),其上固定有抗原或其片段。这样的抗原可以固定在支持基质的活化表面的离散区域。或者,抗原可以被固定在离散的支持基质上,其中离散的支持基质被联合形成一个多重系统。固态装置可以进行多分析物分析(multi-analyte assay),从而平行地确定从受试者分离出来的样品中是否存在多种靶抗体。在本文中,支持基质可以是在多分析物微阵列技术中常规使用的一种。例如,它可以是生物芯片、载玻片或其他常规的平面支持材料、或珠或微粒。支持基质可以被定义为离散测试区(dta),其定义了整个基质,例如单一生物芯片是dta。dta是物理上不同的区域,液体或样品不可能在它们之间流动。在每个dta内,可能有多个离散测试区(dtr,本文指离散
反应区)存在。这些区域定义了基质上的离散位置并支持抗原或其片段。每个dtr在空间上与其他dtr分开,并且每个dtr可用于相同或不同的反应,这取决于反应如何进行。dtr通常存在于“生物芯片”内,装置上可以存在多个生物芯片,每个生物芯片与其他生物芯片在物理上分开。在这个实施方案中,固态装置有多个dtr,每个dtr都携带与基质共价结合的所需结合分子(捕获抗原),在固态装置内的dtr之间的基质的表面关于所研究的靶抗体是惰性的。因此,该固态多分析物装置可能表现出很少或无非特异性结合。不同的结合分子或抗原可以位于空间上分开的位置,即dta或生物芯片上的dtr内。在一个特定实例中,dta为约1cm2,并且在每个dta内可存在4
×
4个dtr,优选地在每个dta内存在5
×
5个dtr,7
×
7个dtr,8
×
8个dtr,9
×
9个dtr,10
×
10个dtr,12
×
12个dtr,15
×
15个dtr,20
×
20个dtr,30
×
30个dtr或更多。或者,多重系统可以包括两个或更多个离散的支持基质,每个支持基质支持单一病原体的抗原,或其中每个离散的支持基质支持单个抗原或其肽片段。支持基质可以是任何可以支持病原体抗原的固体物质。此类非限制性实例是珠、微粒等。因此,在目前多病原体检测发明的背景下的多重系统包括任何能够并行(concurrent)或同时结合和/或检测针对两、三、四、五、六、七、八或九种或更多种病原体的抗体的系统。
‘
并行’是指在类似的时间范围内发生,这个时间范围通常是在30分钟内,优选在15分钟内,更优选在5分钟内。并行或同时结合和检测分析物是多重分析系统的主要优势之一。
70.在一个实施方案中,dta中的每个dtr可以包含固定在其上的不同抗原或其片段。因此,可以采用间接测定来确定生物样品中是否存在多种抗体。在该实施方案中,待分析的牛样品可与结合的抗原一起孵育。该测定的原理是,牛样品中存在的抗体将与固定在离散dtr上的抗原结合,所述抗原抗体有交叉反应性。经过足够的时间让结合事件发生,未结合的牛样品可以通过洗涤从dta中去除,然后加入含有标记的检测抗体的缀合物。经过进一步的孵育和洗涤步骤,可以将标记的检测抗体和任何与固定化抗原结合的牛抗体在离散的dtr上的结合可视化。结合的程度可以报告关于牛样品中病原体特异性抗体的存在或浓度。样品中含有的病原体的抗体越多,在固定了病原体抗原的离散的dtr上的可视化结合就越多。
71.本发明的多重基质可以通过活化合适的基质表面,并将结合分子(捕获抗原)或其片段的阵列应用于表面上的离散位点来制备。如果需要,其他活性区域可以被阻断。结合分子或其片段以及阻断剂可以通过接头与基质结合。特别是,在与黏结剂反应之前,优选使用有机硅烷或聚合物涂层对活化的表面进行活化。本发明的方法中使用的固态装置可根据公开的方法制造(例如gb-a-2324866,该方法的内容已全部纳入本文)。优选地,本发明方法中使用的固态装置是生物芯片阵列技术系统(bat)(可从randox laboratories limited获得)。更优选地,可使用evidence
tm
、evidence evolution
tm
、evidence investigator
tm
和multistat仪器(可从randox laboratories公司获得)来确定样品中的抗体水平。
72.本发明的多重系统可以进一步提供关于样品中的抗体浓度与对照相比的差异的半定量的信息。例如,牛样品中的抗体水平可以与对照中的抗体水平进行对比。对照可以是不含靶抗体的阴性对照,也可以是含有已知量的特定病原体的靶抗体的阳性对照。在一个实例中,样品基于其与阳性对照的比例被解释为阳性或阴性。转化起源于探针与靶的结合的化学、荧光或放射性信号的方法是本领域技术人员熟知的。作为实例但不限于,样品中的抗体浓度可以由一系列已知浓度的抗体标准品绘制的校准曲线计算。优选地,使用与抗牛
抗体检测探针上存在的可检测标记相同的可检测标记检测标准品。优选地,在相同的dta上同时绘制校准曲线。作为实例但不限于,校准曲线可以由一系列已知浓度的抗体标准品绘制,校准曲线可以通过向被分析的生物样品中掺入抗体标准品绘制。
73.上述的一些方法和基质的优势是与某些疫苗一起使用时区分受感染的动物和接种的动物(diva)。例如,本文提供了一种用于diva的方法,包括将牛样品与包含固定化靶抗原ns3和erns或糖蛋白b和糖蛋白e,或所有四种抗原的基质接触,洗去未结合的样品,并用标记的检测抗体检测样品中与基质上固定化抗原结合的任何抗体。最常见的ibr疫苗是ge阴性疫苗,因此在接种的畜群中检测到这种抗体表明存在天然获得性感染。当前测定需要使用2个单独的单重elisa试验,例如ibr gb和ibr ge。
74.还提供了一种筛查牛样品中副结核分枝杆菌抗体的方法,包括(a)使牛样品与其上固定有副结核分枝杆菌的抗原的基质和含有草分枝杆菌的分析缓冲液接触(b)洗去未结合的样品(c)使用标记的检测抗体检测样品中与基质上的固定化抗原结合的任何抗体,其中所述方法在进行该方法之前不需要样品草分枝杆菌预吸收步骤。
75.还提供了一种检测牛样品中副结核分枝杆菌和至少一种其他病原体的抗体的方法,所述方法包括(a)使牛样品与其上固定有副结核分枝杆菌的抗原和至少一种其他病原体的抗原的基质和含有草分枝杆菌的分析缓冲液接触,(b)洗去未结合的样品(c)使用标记的检测抗体检测样品中与基质上的固定化抗原结合的任何抗体,其中所述方法在进行该方法之前不需要样品草分枝杆菌预吸收步骤。优选地,所述至少一种其他病原体选自牛病毒性腹泻病毒(bvdv)、牛疱疹病毒1型(bohv-1)、钩端螺旋体属种、犬新孢子虫和肝片吸虫。
76.这些新方法的优点是不需要样品草分枝杆菌预吸收步骤,从而使当前测定比现有测定更有效。所有可商购获得的elisa试剂盒都有含草分枝杆菌抗原的样品预吸收步骤,以通过限制与鸟结核分枝杆菌副结核亚种以外的分枝杆菌(mycobacteria)的交叉反应性来增强测定特异性。草分枝杆菌是牛病原体阵列分析缓冲液的一个复杂成分,因此不需要单独的样品预吸收步骤。该样品预吸收步骤可花费最高达2小时。除了需要预吸收步骤外,没有商业化的elisa是多重格式。本文缓冲液中包含草分枝杆菌没有对测定性能产生任何负面影响,并且与新的多重格式兼容。本技术方法的第一孵育步骤中含有草分枝杆菌的分析缓冲液与样品一起加入(步骤1,图2)。可以使用技术人员已知的任何合适的分析缓冲液。
77.本技术还提供了一种试剂盒,其包括其上固定有副结核分枝杆菌的抗原的基质和任选的至少一种其他病原体的抗原;和含有草分枝杆菌的分析缓冲液。优选地,所述至少一种其他病原体选自牛病毒性腹泻病毒(bvdv)、牛疱疹病毒1型(bohv-1)、钩端螺旋体属种、犬新孢子虫和肝片吸虫,并且优选地,抗原选自bvdv ns3、bvdv erns、bohv-1糖蛋白b、bohv-1糖蛋白e、map ppa、哈德焦型钩端螺旋体lipl32、犬新孢子虫srs2、犬新孢子虫sag1和肝片吸虫组织蛋白酶l1。
78.本发明的最后一个方面是一种使最终用户易于解释结果的多重测定归一化方法。所述方法包括将阵列中所有分析物的结果归一化为每个试验的》50%的测定截止值。可以使用各种不同的截止值,从》15%、25%、》30%、》35%、》50%、》60%等,只要对多重测定中的所有结果应用相同的截止值。这通过使用预先确定的特定于每批阳性对照的倍增因子来实现。倍增因子可以基于与测定截止值阈值相比母体阳性对照批次的测定输出(表4)。例如,测定输出可以是相对光单位(rlu)。这可以在随测定提供的结果工作文件(例如
microsoft excel电子表格)中自动进行,该工作文件不仅可以将结果显示为每种分析物的简单阳性和阴性,还可以显示阳性或阴性样品与对照的对比。基于elisa的试验的结果通常基于为该特定测定建立的截止值来报告。当用不同的截止值运行多个试验时,可能难以确定样品的阳性或阴性程度,并且当前的方法为最终用户简化了这一点。这种归一化方法的另外的优势是,由于结果是按照阳性对照的母体批次进行归一化的,因此它消除了批次间的差异问题。如果使用标准截止值,可能是一个问题的分析器间的差异也可以消除。本领域技术人员会理解,这种方法可以应用于所有的多重测定。在牛病原体阵列的实例中,这种多重测定归一化方法有许多优势。除了易于解释多种病原体的结果外,与对照相比,每个样品的阳性百分率或阴性百分率的附加信息有指示感染阶段,影响治疗途径,并能识别需要后续试验或监测的动物的可能性。
79.一种病原体的高阳性百分率与另一种病原体的高阳性百分率可以有不同的解释。例如,sp%可以指示感染的阶段(因为这些病原体中的一些的潜伏期可能不同)以及不同病原体的疾病程度/严重性。
80.sp%在确定疾病结果中也是非常重要的,因为对于这些病原体动物中的一些,如果它们受到及时和适当的治疗(例如肝片吸虫)将会恢复,然而对于其它病原体(例如map)治疗很大程度上是不成功的,并且在大多数情况下,如果识别出阳性动物,它将被安乐死以防止疾病在畜群中任何进一步地传播。
81.与竞争者的单重抗体检测试验一样,设想牛病原体阵列将主要用于乳牛群的监测,以监测个体和散装乳样品中随时间的抗体水平。散装乳样品是指从整个畜群中收集的混合乳样品。
82.在牛病原体阵列中,任何分析物的值≤50%都报告为阴性。这一结果可表明,动物/畜群从未暴露于该传染性病原体,或者也许以前发生的任何暴露都不是最近发生的,并且抗体水平已经下降到截止值水平以下。这样的阴性结果并不令人担忧,并且个别动物或畜群不需要由农民/兽医进行治疗。
83.许多国家已经建立了一些乳牛群健康方案,这些方案涉及每3个月对从畜群收集的散装乳样品进行试验(每年收集4个样品)。监管机构牛健康认证标准(cattle health certification standard)已经在英国和爱尔兰授权了许多这样的方案,包括国家乳实验室(the national milk laboratories)的bvd畜群检查方案(bvd herdcheck scheme)。
84.将获得的散装乳结果与以前的结果进行对比,如果在两个时间点之间出现针对特定病原体的抗体水平的显著增加,这将指示最近的暴露,即如果在1月收集的散装乳样品的bvd ns3 sp%值为12%,而在5月从相同畜群收集的另一散装乳样品的bvd ns3 sp%值为595%,这将表明畜群内的最近的暴露。负责畜群健康的农民/兽医然后可以从畜群内的所有奶牛中收集个体样品以识别哪些被感染。然后将感染的动物隔离并相应地治疗以防止在整个畜群中广泛传播疾病。
85.同样,如果1月份收集的散装乳样品的bvd ns3 sp%值为12%,而5月份从同一畜群收集的另一散装乳样品的bvd ns3 sp%值为75%,可以表明最近的暴露和检测到畜群中少数动物开始血清转化。因此,建议进行后续试验,但这将由负责畜群健康的农民/兽医决定。
86.确定个体或畜群样品的阳性程度也有助于划分治疗的优先次序,例如51%对
2000%的阳性结果可导致这些动物的不同治疗途径。
87.如果试验散装乳样品,即从整个畜群采集的混合样品,sp%的百分比越高,还可表明疾病的传播范围有多广,以及畜群中受影响的奶牛数量。
88.方法
89.选择出的特定于每种病原体的免疫显性抗原被固定在生物芯片表面定义的离散测试区域(dtr)上。将100微升乳样品加入含有200微升分析缓冲液的生物芯片孔中,在37℃下孵育1小时。接着用稀释的洗涤缓冲液进行两次快速洗涤和四次长洗涤(2分钟浸泡)后,将300μl辣根过氧化物酶(hrp)缀合的抗牛igg加入生物芯片孔中,在37℃下再次孵育1小时。在重复洗涤步骤(两次快速洗涤和四次长洗涤)之前,加入250μl信号试剂,其含有1:1的鲁米诺/过氧化物溶液混合物,生物芯片避光孵育2分钟。当hrp标记的抗牛igg与样品中的抗体(抗体与生物芯片表面含有dtr的抗原结合)结合时,就会产生化学发光信号。化学发光信号用数字成像技术(电荷耦合装置(ccd)摄像机,在本例中为randox laboratories ltd.的evidence investigator
tm
系统)检测,并将结果与内部测定的阳性和阴性对照进行对比。结果被报告为阳性或阴性。对于每个样品,提供相对于阳性对照的半定量阳性百分率值。
90.结果
91.表1-样品分类中牛病原体阵列(bpa)和商业化的上游elisa之间的一致性百分比(n=349)
92.试验一致性(%)bvd(ns3)100%ibr(gb)100%ibr(ge)100%map98%钩端螺旋体病100%犬新孢子虫100%肝片吸虫100%
93.表2-与使用全病毒抗原的上游elisa相比,牛传染性鼻气管炎的牛病原体阵列的增强的诊断性能。
94.样品idibr全阵列bpa ibr-gbbpa ibr-ge1阳性阳性阳性2阴性阴性阴性3阳性阴性阳性4阳性阳性阴性5阴性阴性阳性
95.bpa证实了与使用全病毒抗原时相比,样品3-5的diva能力。所有样品均为乳样品。
96.表3-与使用天然速殖子抗原的上游elisa相比,犬新孢子虫的牛病原体阵列的增强的诊断性能。
97.样品id速殖子抗原bpa nc-srs2bpa nc-p296阳性阳性阳性
7阴性阴性阴性8阴性阳性阴性9阴性阳性阳性
98.bpa证实了与仅使用天然速殖子抗原时相比,样品8和9在感染的速殖子和缓殖子阶段均有抗体检测。所有样品均为乳样品。
99.实施例1
100.在大型乳研究(每种分析物》300个乳样品)期间,使用多分析物阳性对照的母体批次确定每种分析物的样品/阳性对照的比例。由于每种分析物的样品/阳性对照的比例不同,决定将每种分析物的截止值归一化至》50%。这涉及分配》50%测定阈值所需的倍增因子。将所需的倍增因子插入上述结果公式中。
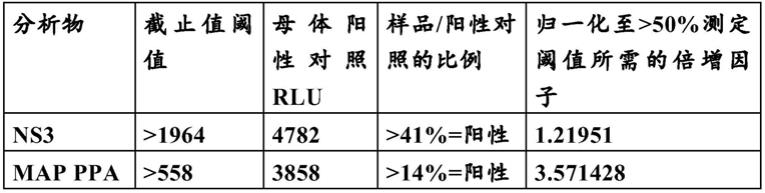
101.表4归一化至》50%测定阈值的实施例
[0102][0103]
牛病原体阵列的每种分析物/每批阳性对照的测定阈值将总是》50%。当制备新批次的多分析物对照时,这些对照与确定样品/阳性对照的比例和倍增因子的母体多分析物对照批次一起运行。多分析物对照批次中的任何差异将在分配给每个多分析物对照批次的倍增因子中考虑-参见以下实施例。
[0104]
用于计算样品阳性百分率(sp%)的公式如下:
[0105]
样品rlux100=sp%(x倍增因子)阳性对照rlu
[0106]
分析物:ns3
[0107]
母体批次阳性对照:2288rlu
[0108]
归一化至50%=倍增因子2.9[50/17.4=2.9]
[0109]
对照批次2:2500rlu(
↑
212rlu=
↑
9.27%)
[0110]
归一化至50%=2.9*1.0927%=倍增因子3.17
[0111]
样品a:2311rlu
[0112]
对照批次1=2311/2288*100*2.90=293%(阳性)
[0113]
对照批次2=2311/2500*100*3.17=293%(阳性)
[0114]
每种病原体的竞争者elisa通常采用各种不同的截止值,从》15%、25%、》30%、》35%、》50%、》60%等。为了最终用户易于解释结果,我们选择了》50%的截止值,并将其应用于牛病原体阵列中包含的所有测定,即如果对2个特定的样品获得以下结果,则更容易将结果分类为阳性或阴性,并应用了一系列不同的测定截止值解释样品1相对于样品2的阳性程度。
[0115]
表5使用》50%截止值的结果对比
[0116][0117]
表6使用多种不同截止值的结果对比
[0118][0119]
以上样品1和2所包括的sp%值仅是实施例值,并且彼此不相关。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1