定量检测末梢血样本中脂溶维生素含量的方法与流程
本发明涉及检测
技术领域:
,主要涉及一种定量检测末梢血样本中脂溶性维生素含量的方法。
背景技术:
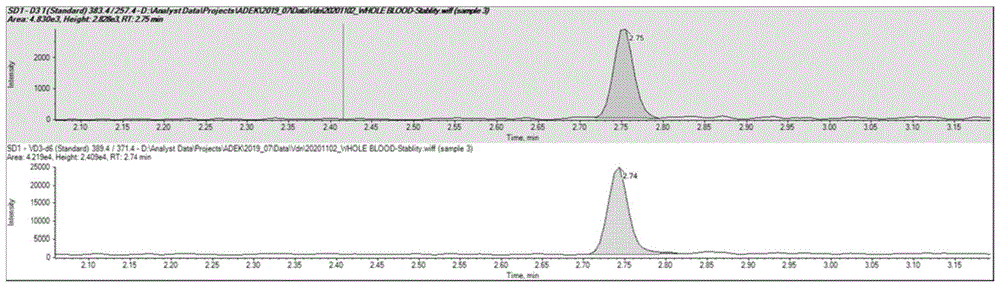
:脂溶性维生素是指易溶于有机溶剂而不溶于水的一类维生素,主要包括维生素a、维生素d和维生素e等。该类维生素能溶解于脂肪,不易被排泄,可储存于体内,对于人体的代谢和机能起着非常重要、不可或缺的作用。维生素a、d、e分别以酶和辅基激活剂的形式参与蛋白质、酶、激素和维生素的合成、分解与转化,影响人体生长发育、新陈代谢、免疫调节等生理活动。因此,将机体脂溶性维生素水平保持在适宜范围非常重要,a、d、e缺乏可引起多种疾病,而过量摄入又会导致中毒。目前,临床上检测多种脂溶性维生素(包括维生素a、维生素d3、维生素d2以及维生素e等)的方法主要包括免疫法、电化学法、色谱法以及液相色谱串联质谱法等,主流的脂溶性维生素检测样本类型为血清,检测所需血样量相对较多,但是由于婴幼儿特别是新生儿群体存在采血不便的情况,难以分离足量血清进行检测。但脂溶性维生素缺乏为小儿常见病,因此微量末梢血全血的脂溶性维生素检测项目具有非常重要的意义,但针对末梢血全血脂溶性维生素检测的文献及专利较少。cn110488008a及cn110488004a中分别公布了检测末梢血25-羟基维生素d3及末梢血25-羟基维生素d的试剂盒及其制备方法和应用,这两种试剂盒分别包括25羟基维生素d3免疫层析检测卡和释放剂以及25羟基维生素d免疫层析检测卡和释放剂,所述免疫层析检测卡包括试纸条,所述试纸条包括检测线及质控线,所述检测线上包被有25-羟基维生素d3或25-羟基维生素d完全抗原,所述质控线上包被有羊抗兔多克隆抗体。这两种方法的缺点在于仅能检测末梢血中的25-羟基维生素d3或25-羟基维生素d,未能对其它种类的脂溶性维生素进行检测。cn108802221a中公布了一种末梢血中维生素a和维生素e的微量检测方法,其检测步骤包括:1.末梢血样品加入含有内标及bht的甲醇溶液,完成蛋白沉淀;2.加入特丁基甲醚进行液液萃取,室温下氮气吹干萃取上清液,并加入80%甲醇复溶,涡旋震荡后离心得到待测样本;3.以超高效液相色谱串联质谱检测:通过超高效液相色谱串联质谱检测获得所述待测样本中待测物的峰面积和对应内标峰面积,完成微量末梢血样本中维生素a和维生素e的检测。cn110208435a中公布了同时检测人末梢血中25-羟基维生素d3和25-羟基维生素d2含量的方法,其步骤与cn108802221a中公布的样本前处理及检测步骤比较类似,但是所使用试剂的种类不同:1.末梢血样品加入含有内标的乙醇溶液,进行蛋白沉淀;2.加入正己烷进行液液萃取,室温下氮气吹干萃取上清液,并加入含甲酸的甲醇水复合溶液,涡旋震荡后离心得到待测样本;3.以高效液相色谱串联质谱检测完成微量末梢血样本中维生素d2和维生素d3的检测。这两种检测方法只能同批检测脂溶维生素d2和维生素d3,且前处理步骤非常复杂,耗时耗力并且难以实现高通量自动化操作。目前利用液相色谱串联质谱进行脂溶性维生素检测的常用样本类型为血清,样本量一般至少需要0.5ml血清,那么需要采集的静脉血量为1ml以上。对于婴幼儿特别是新生儿以及其他存在静脉穿刺的人群来说,难以采集到1ml以上的静脉血,那么末梢采血就显得尤为重要。与血清样本相比,在进行脂溶性维生素检测时,全血样本中的红细胞等组分会对脂溶性维生素的检测构成严重的基质效应,给全血脂溶性维生素检测方法的开发造成了很大困难。在目前已经公开的末梢血脂溶维生素检测现有技术中,各方案均只能对脂溶性维生素中的一项或者两项进行检测,无法对两种以上的脂溶性维生素实现同步检测。在利用液相色谱串联质谱进行末梢血全血脂溶维生素检测的前述现有技术中,所使用的样本前处理步骤复杂,包括蛋白沉淀、液液萃取、萃取液的吹干及待测物复溶等步骤,操作复杂,耗时耗力并且难以实现高通量自动化操作,且无法实现对两种以上脂溶维生素的同步检测。技术实现要素:本发明的目的是针对现有技术的不足,针对临床上对于末梢血脂溶性维生素的检测需求,提供一种前处理简便,检测效率高且成本低的液质联用检测方法,同时检测末梢血中维生素a、维生素d3、维生素d2以及维生素e。为了实现本发明的目的,本发明提供以下技术方案:本发明涉及定量检测末梢血样本中脂溶维生素含量的方法,所述脂溶维生素选自维生素a、维生素d3、维生素d2以及维生素e中的至少一种;所述方法包括如下步骤:将末梢血样本与含有内标的蛋白沉淀液混合,涡旋后离心,取上清液上机检测;采用高效液相色谱串联质谱系统对待检测液进行检测和分析;所述含有内标的蛋白沉降剂由有机溶剂和同位素内标配置而成,所述有机溶剂包括甲醇、乙醇以及丙醇等醇溶剂,所述同位素内标选自维生素a同位素内标、维生素d3同位素内标以及维生素e同位素内标中的至少一种,所述同位素内标任选含有维生素d2同位素内标。基于上述技术,本发明通过一种简单的前处理方法,即可准确、高效地检测出人末梢血样本中维生素a、维生素d2、维生素d3以及维生素e的浓度,为营养补充、临床诊断及治疗提供依据。在本发明的一个优选实施方式中,所选用的内标为维生素a同位素内标、维生素d3同位素内标以及维生素e同位素内标,其具体形式分别为维生素a-d6、维生素d3-d6和维生素e-d6。在本发明的一个优选实施方式中,所述末梢血待测样本的用量不超过50μl。在本发明的一个优选实施方式中,所述末梢血待测样本与所述含有内标的蛋白沉降剂的体积比为1:2-1:5,优选为1:3。本发明通过合理设置两者的比例,有助于提取脂溶维生素。在本发明的一个优选实施方式中,每个末梢血待测样本的液质分析时间不超过5分钟。在本发明的一个优选实施方式中,所述高效液相色谱条件为:高效液相色谱条件为:流动相a:含铵盐的水相流动相b:含铵盐的有机相色谱柱:经过修饰的c18色谱柱流动相梯度参数如表1所示。表1:高效液相色谱流动相梯度时间(min)流速(ml/min)流动相a(%)流动相b(%)00.790100.40.790101.20.7257530.729840.72984.050.790104.40.79010本发明通过采用上述液相色谱条件,既能够有效的分离所有脂溶维生素,又能够将液质分析时间控制在5分钟以内。在本发明的一个优选实施方式中,所述质谱的质谱条件为:离子源:大气压化学电离源模式:正、负离子分段模式,其中维生素e的检测方式为负离子,维生素d2、维生素d3以及维生素a的检测方式为正离子。本发明的质谱条件可以有效减低复杂基质的基质效应,保证检测结果的准确性。在本发明的一个优选实施方式中,本发明的方法为诊断目的或者是非诊断目的的。与现有技术相比,本发明具有以下优点中的一种或者多种或者是全部:(1)所需样本量少,50ul末梢血样本即可检测维生素a、维生素d2、维生素d3以及维生素e的浓度,因此对采集样本量的要求较低;(2)本发明将内标成分与蛋白沉淀剂配制到一起,因此一步操作即可达到蛋白沉降和内标校正的目的,前处理流程更简化;(3)本发明中前处理过程只需将样本与蛋白沉降剂混合涡旋后离心即可,因此检测成本较低,前处理时间短,易于实现自动化高通量样本前处理,对操作人员的技术要求低;(4)本发明通过合理设置色谱条件,每个样本的液质分析时间只有4.4min,检测效率高;(5)本发明的质谱条件中,维生素e的检测采用负离子模式,可以有效减低末梢血样本中复杂的基质效应,有效减低了红细胞中脂类物质可能产生的基质干扰,保证检测结果的准确性。附图说明图1.维生素d3(上图)和其内标(下图)的离子提取色谱图;图2.维生素d2(上图)和其内标(下图)的离子提取色谱图;图3:维生素a(上图)和其内标(下图)的离子提取色谱图;图4:维生素e(上图)和其内标(下图)的离子提取色谱图。具体实施方式:下面结合实例对本发明作进一步说明,以下实施例用来解释说明本发明,而不是对本发明进行限制,在本发明的精神和权利要求的保护范围内,对本发明做出的任何修改和改变,都落入本发明的保护范围。实施例1:(1)标准曲线的配置:用乙醇溶解准确称量的维生素a、维生素d2、维生素d3以及维生素e的标准品得到对应的标准品储备液,然后用pbs将上述储备液稀释成下表2所示浓度的标准曲线。表2:标准曲线浓度分析物线性范围(ng/ml)sd1sd2sd3sd4sd5sd6维生素d35~2505102550100250维生素d22~10024102040100维生素a40~2000408020040010002000维生素e500~250005001000250050001000025000(2)蛋白沉降剂的配置:用乙醇溶解准确称量的维生素a-d6、维生素d3-d6和维生素e-d6得到对应的同位素内标储备液,然后用乙醇将上述同位素内标储备液混合、稀释成一定浓度的蛋白沉降剂溶液,如表3所示。表3:内标浓度同位素内标同位素内标浓度(ng/ml)维生素d3-d6(vd3-d6)10维生素a-d6(va-d6)80维生素e-d6(ve-d6)1,000(3)加标质控样本的配置:取若干末梢血全血样本混合均匀,作为末梢血脂溶维生素检测的低质控,再分别准确添加中浓度和高浓度的标准品储备液得到中值质控和高值质控。(4)样本的处理:分别取50μl的标准曲线溶液、质控样本和待测样本至1.2ml的96孔板中,然后向每个孔中加入150μl的蛋白沉降剂,充分涡旋后离心。取100ul上清,上机检测。(5)上机检测高效液相色谱条件为:流动相a:含乙酸铵的水溶液流动相b:含乙酸铵的甲酸溶液色谱柱:经过修饰的c18色谱柱流动相梯度参数如表4所示。表4:高效液相色谱流动相梯度时间(min)流速(ml/min)流动相a(%)流动相b(%)00.790100.40.790101.20.7257530.729840.72984.050.790104.40.79010质谱条件为:离子源:apci(apci为大气压化学电离源,样品先形成雾,然后电晕放电针对其放电,在高压电弧中,样品被电离,然后去溶剂化形成离子,最后检测。)模式:正、负离子分段模式(正、负离子检测分段时间:3.3分钟)质谱检测参数如表5所示。表5:质谱检测参数注:上述分析物-1为均为定量离子对,分析物-2为定性离子对。各化合物保留时间如表6所示。表6:脂溶维生素保留时间化合物名称保留时间(min)维生素d32.75维生素d22.81维生素a2.82维生素e3.86(6)数据处理数据采用sciexanalyst软件采集,multiquant软件处理。以分析物峰面积与内标峰面积比对标准曲线中的分析物的理论浓度进行线性最小二乘法回归计算,所得回归方程计算样品中分析物的实测浓度。样品中分析物的实测浓度由以下回归方程计算:y=ax+b其中y=分析物与内标的峰面积比b=截距a斜率x=分析物的浓度检测结果如表7所示。表7:检测结果维生素a(ng/ml)维生素d2(ng/ml)维生素vd3(ng/ml)维生素e(ng/ml)样本1456.122.187.055891.11样本2415.751.817.487234.35样本3370.632.015.425276.21样本4441.251.277.936936.17样本5640.141.1311.7710100.58样本6373.061.355.434398.84样本7433.191.498.775293.34样本8564.551.428.396224.19样本9493.691.178.25257.36样本10342.221.847.855333样本11588.982.877.748920.18样本12386.481.7614.326660.46样本13578.91.839.715226.35样本14361.621.527.657927.09样本15460.671.1421.867359.72样本16387.381.197.724695.4样本17474.811.796.64637.85样本18397.491.4921.517453.07样本19531.341.0912.977578.74样本20551.51.074.976165.21由上述实施例结果分析,本发明能够同时检测末梢血样本中维生素a、维生素d2、维生素d3及维生素e。该方法的样本前处理简单,易于进行自动化高通量样本处理;每次检测仅需要50ul末梢血样本,特别适用于存在营养检测需求及采血困难的婴幼儿人群;液质分析时间只有4.5min,检测效率高;维生素e的检测方式为负离子,可以有效减低复杂基质的基质效应,保证检测结果的准确性。因此,本发明提供了一种同时检测末梢血样本中维生素a、维生素d2、维生素d3及维生素e的方法,前处理简单,检测成本低,检测效率高。对实施例中的脂溶性维生素进行方法学验证试验。通过对临床样本进行加标回收率的实验测定本发明方法学的准确度,通过日间精密度实验测定本发明方法学的精密度,各分析物及其内标的谱图如图1-4所示,根据谱图的结果可知,本发明的方法能够很好的分离各脂溶维生素。各分析物准确度和精密度的验证结果如下表8-11所示。表8:维生素d3的准确度与精密度验证表9:维生素d2的准确度与精密度验证表10:维生素a的准确度与精密度验证表11:维生素e的准确度与精密度验证上述验证结果表明,本发明的技术方案可以同时检测末梢血中多种脂溶性维生素,包括维生素a、维生素d3、维生素d2以及维生素e。该方法的样本前处理简单,只需加入蛋白沉降剂后涡旋离心即可;结果准确度高,精密度好,各分析物的变异系数(cv%)<15%;加标样本中各分析物的回收率的偏差(bias)<15%,符合方法验证要求。以上描述了本发明优选实施方式,然其并非用以限定本发明。本领域技术人员对在此公开的实施方案可进行并不偏离本发明范畴和精神的改进和变化。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1