人参皂苷CK自胶束化固体分散体的代谢组学分析方法与流程
人参皂苷ck自胶束化固体分散体的代谢组学分析方法
技术领域
1.本发明属于代谢组学分析方法技术领域,具体涉及人参皂苷ck固体分散体的代谢组学分析方法。
背景技术:
2.代谢组学(metabonomics/metabolomics)是效仿基因组学和蛋白质组学的研究思想,对生物体内所有代谢物进行定量分析,并寻找代谢物与生理病理变化的相对关系的研究方式,是系统生物学的组成部分,广泛用于疾病及药物作用机理研究,揭示机体生命活动代谢本质,同时将这些物质与生理病理学生物信息相关联,从而获得相应的病理标志物,研究对象包括糖类、氨基酸、有机酸等代谢物。
3.代谢组学数据采集分析技术手段众多,主要用到的有核磁共振(nmr)、气质联用(gc-ms)和液质联用(lc-ms)。相对于核磁共振技术而言,近年来新兴的uplc-ms联用技术,具有很高的灵敏度和专属性,可显著提高色谱的分辨率和灵敏度,缩短检测时间,也可以用来测定挥发性和热稳定性样品,待检样品简单预处理后进样,即可获得差异代谢组信息,进而得到代谢组分的结构信息。其中,uplc-q-tof-ms是集快速、高效分离,高精度、高通量检测于一体的先进分析技术,其在非靶标代谢组学应用中有着突出的优势,质谱分析可以采用的样本有血清、血浆、脑脊液、尿液、唾液及心、肝、脾、肺、肾、脑等各种组织。
4.人参皂苷化合物k(ginsenoside compound k,人参皂苷ck,ck)于1972年在人参皂苷的土壤细菌水解产物中被发现,并进行结构鉴定,其结构式为:,分子式为c
36h62
o8,分子量为622.87da。人参皂苷ck是原人参二醇如人参皂苷rb1、rb2、rc等在肠道菌群中主要的代谢产物,它能进一步代谢成20(s)ppd。有报道称人参皂苷的抗癌活性和糖基的数目成反比,而ck只有一个葡萄糖基,被认为是人参中最重要的活性物质。人参皂苷ck是人参皂苷的主要代谢产物之一,具有多种药理活性,研究表明人参皂苷ck具有很好的抗细胞突变、抑制肿瘤细胞转移、诱导肿瘤细胞凋亡、逆转肿瘤细胞耐药性和抗肿瘤诱导的血管生成等活性,还可以增强放疗和化疗的效果。除此之外,人参皂苷ck还有具有抗过敏和抗炎活性,并且可以起到神经保护作用,抗糖尿病作用和抗皮肤衰老作用。人
参皂苷ck药理作用显著,但几乎不溶于水,ph在5.0-8.0范围内logp在1-3之间,提示ck是偏脂溶性药物,其水中溶解度仅为35.2μg/ml,大鼠口服生物利用度只有4.3%,严重限制了其临床应用。因此,提高人参皂苷ck的水中溶解性,增加口服吸收,进而提高其生物利用度,是人参皂苷ck临床应用中亟待解决的问题。
5.自胶束化固体分散体属于第五代固体分散体,是药物高度分散于固体载体中形成的一种以固体形式存在的分散系统,遇水相可以自组装形成胶束,能够提高难溶性药物的溶出速率和溶解度,延缓或控制药物释放,提高药物的稳定性,提高药物的生物利用度。
6.石家庄以岭药业股份有限公司于2020年7月17日申请了名称为“一种含有人参皂苷ck的制剂组合物及其制备方法”的发明专利,专利中公开了人参皂苷ck的自胶束化固体分散体制剂,但未提供自胶束化固体分散体中人参皂苷ck的代谢组学分析的内容。
技术实现要素:
7.本发明的目的是提供人参皂苷ck自胶束化固体分散体的代谢组学分析方法,为人参皂苷ck的代谢组学研究提供参考依据。
8.为了实现上述目的,发明人提供了以下技术方案。
9.人参皂苷ck自胶束化固体分散体的代谢组学分析方法,包括以下操作步骤:a. 对血浆样本进行预处理,制备待测样品;b. 采用超高效液相色谱与串联四级杆飞行时间质谱仪(uplc-q-tof-ms)对步骤a得到的待测样品进行分析;c. 利用小分子数据分析软件对步骤b得到的数据进行处理,再将获得的数据采用simca-p软件进行pca和opls-da数据分析。
10.上述代谢组学分析方法,步骤a所述预处理的过程包括:取血浆样本,加入色谱甲醇,依次进行第一次涡旋震荡,第一次超声,第一次离心,取上清液,加入超纯水,冷冻干燥,得到固体,然后向固体中加入50%甲醇复溶,依次进行第二次涡旋震荡,第二次超声,第二次离心,得到上清液,即待测样品,备用。
11.步骤a中,第一次超声和第二次超声优选在冰浴条件下进行。第一次离心和第二次离心优选在低温条件下进行。第一次离心和第二次离心的转速优选为12000r/min。
12.上述代谢组学分析方法,步骤b所述分析的色谱条件为:色谱柱为t3色谱柱,规格为2.1 mm
×
100 mm, 1.8 μm,流动相以0.1%甲酸水溶液为a相,0.1%甲酸甲醇为b相,流速为0.35ml/min,梯度洗脱过程如下表所示。
13.上述代谢组学分析方法,步骤b所述分析的质谱条件为:雾化和锥孔气为n2,gas1
为50,gas2为50,气帘气为35,温度500℃,正离子模式电压为5500v。
14.上述代谢组学分析方法,步骤c所述数据分析筛选出的是vip》1.0和p《0.05的代谢物,再去除同位素离子、加合离子与碎片离子,得到潜在化合物信息,最终确定潜在的差异代谢物。
15.优选地,上述代谢组学分析方法,操作步骤包括:a. 取血浆样本,加入色谱甲醇,先进行涡旋振荡,再冰浴超声5min,然后在低温、转速12000r/min条件下离心15min,取上清液,加入适量超纯水,冷冻干燥,得到固体,向固体中加入50%甲醇复溶,涡旋振荡30s,冰浴超声5min,然后在转速12000r/min条件下离心15min,取上清液,即为待测样品,备用;低温优选为4℃;b. 采用超高效液相色谱与串联四级杆飞行时间质谱仪对步骤a得到的待测样品进行分析,分析的色谱条件为:色谱柱为t3色谱柱,规格为2.1 mm
×
100 mm, 1.8 μm,流动相以0.1%甲酸水溶液为a相,0.1%甲酸甲醇为b相,流速为0.35ml/min,梯度洗脱过程如下表所示,进样量为10μl,进样器温度为4℃;分析的质谱条件为:雾化和锥孔气为n2,gas1为50 ,gas2为50,气帘气为35,温度500℃,正离子模式电压为5500v;c. 利用小分子数据分析软件对步骤b得到的数据进行峰提取、峰去噪、峰对齐的归一化处理,再将获得的数据采用simca-p软件进行pca和opls-da数据分析,筛选出vip》1.0和p《0.05的代谢物,再去除同位素离子、加合离子与碎片离子,得到潜在化合物信息,包括保留时间、精确mass值与m/z值,再结合人类代谢组学数据库最终确定潜在的差异代谢物,其分子式依次为c
48h82
no8p、c
48h80
no8p、c
46h80
no8p、c
46h82
no7p、c
44h84
no8p、c
27h56
no7p、c
43h78
no8p、c
41h74
no8p、c
38h77
n2o6p、c
17h28
o3、 c
30h52
no7p、c
28h54
no7p、c
26h52
no7p、c
24h48
no7p,名称依次为pc(18:1(9z)/22:6(4z,7z,10z,13z,16z,19z))、pc(22:6(4z,7z,10z,13z,16z,19z)/18:2(9z,12z))、pc(22:6(4z,7z,10z,13z,16z,19z)/16:0)、pc(o-16:0/22:6(4z,7z,10z,13z,16z,19z))、pc(18:2(9z,12z)/18:0)、pc(19:0/0:0)、pe(p-18:0/20:4(5z,8z,11z,13e)(15oh[s]))、pe(16:0/20:4(5z,8z,11z,14z))、sm(d16:1/17:0)、dihydropanaxacol、lysopc(22:5(4z,7z,10z,13z,16z)/0:0)、lysopc(20:2(11z,14z)/0:0)、lysopc(18:1(11z)/0:0)、lysopc(16:1(9z)/0:0)。
[0016]
本发明中,simca-p软件是一款用于主成分分析及偏最小二乘-判别分析的工具,它可以将结果用得分图的形式形象地展现出来,pca是指主成分分析。
[0017]
opls-da是指正交偏最小二乘法判别分析vip(variable importance in the projection),为变量对模型的重要性,描述
了每一个变量对模型的总体贡献。
[0018]
hmdb是指人类代谢组学数据库。
[0019]
metlin是指代谢组学数据库和谱库。
[0020]
本发明中所述自胶束化固体分散体是指石家庄以岭药业股份有限公司于2020年7月17日申请的名称为“一种含有人参皂苷ck的制剂组合物及其制备方法”的发明专利中公开的人参皂苷ck的自胶束化固体分散体制剂。
[0021]
本发明基于代谢组学的整体性分析优势,将人参皂苷ck自胶束化固体分散体在脑缺血小鼠中应用,并进行血样收集,采用uplc-q-tof-ms进行数据采集及分析鉴定,共筛选出14种差异代谢物,其中包括6种磷脂酰胆碱(pc(18:1/22:6)、pc(22:6/18:2)、pc(22:6/16:0)、pc(o-16:0/22:6)、pc(18:2/18:0)、pc(19:0/0:0))和4种溶血磷脂 (lysopc(22:5(4z,7z,10z,13z,16z)/0:0)、lysopc(20:2(11z,14z)/0:0)、lysopc(18:1(11z)/0:0)、lysopc(16:1(9z)/0:0))。本发明拟合的数据模型合理,方法重现性良好,为人参皂苷ck自胶束化固体分散体的差异代谢物研究提供了可靠的途径。
附图说明
[0022]
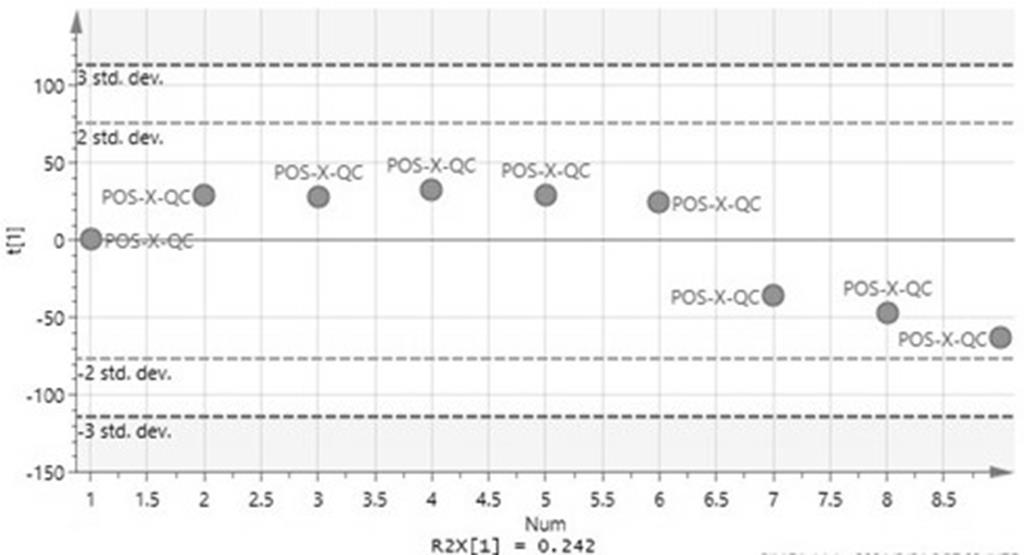
图1为qc样本正离子模式下pca分析图。
[0023]
图2为正离子模式下空白对照组的总离子流色谱图。
[0024]
图3为正离子模式下m组的总离子流色谱图。
[0025]
图4为正离子模式下人参皂苷ck组的总离子流色谱图。
[0026]
图5为正离子模式下ck-ssd组的总离子流色谱图。
[0027]
图6为在正离子模式下假手术组和m组的opls-da分析得分图。
[0028]
图7为正离子模式下假手术组和m组的permutation分析。
[0029]
图8为正离子模式下假手术组和m组的热图分析。
[0030]
图9为正离子模式下各组血浆样品的pca分析得分图。
[0031]
图10为正离子模式下各组血浆样品的opls-da分析得分图。
[0032]
图11为正离子模式下各组血浆样品的permutation分析。
具体实施方式
[0033]
下面结合具体实施例对本发明所述内容作进一步详细的说明。
[0034]
实施例1(一)实验动物c57bl/6n小鼠,雄性,20-24g,购于北京维通利华实验动物技术有限公司,许可证编号scxk(京)2016-0006,5只/笼,饲养于河北省中西医结合医药研究院新药评价中心动物屏障环境,进食大小鼠维持饲料,光照12h/天,温度20-23℃,相对湿度40-60%。
[0035]
(二)仪器uplc-q-tof-msabsciex公司genespeed1580r高速冷冻离心机基因有限公司as20500a超声波清洗器南京昕航科学仪器有限公司si-t256涡旋混合器scientificindustries公司
milli-q超纯水仪默克密理博公司precellysevolution高速研磨器法国bertin公司secura225d-1cn赛多利斯精密分析天平赛多利斯科学仪器(北京)有限公司heraeuspico21微量高速台式离心机美国赛默飞世尔公司(三)试剂乙腈、甲醇(色谱纯)德国默克merke公司色谱甲酸阿拉丁公司地高辛河南省标物生物科技有限公司ck上海源叶生物科技有限公司calibrationsolutionabsciex公司(四)人参皂苷ck自胶束化固体分散体的制备精密称取人参皂苷ck100.7mg、soluplus300.1mg置于圆底烧瓶中,加入10ml二氯甲烷使溶解后,采用30℃水浴旋转蒸发除去二氯甲烷;随后将圆底烧瓶置于真空干燥箱25-30℃干燥过夜;将圆底烧瓶中的固体取出,研磨后过180目筛,即得到人参皂苷ck的自胶束化固体分散体。
[0036]
(五)小鼠大脑中动脉栓塞(mcao)模型的建立方法采用线栓法:用异氟烷麻醉小鼠,待麻醉成功后颈部前正中脱毛,仰卧固定于手术板上;医用碘伏依次消毒小鼠颈前皮肤,颈部正中皮肤,之后眼科剪剪出长约1.5cm纵切口,钝性分离颈下皮肤肌肉,游离右侧颈总动脉(commoncarotid artery, cca)、颈外动脉(external carotid artery, eca)及颈内动脉(internal carotid artery, ica)。用缝合线6-0号手术线结扎cca近心端及eca,在cca适当位置用显微剪45
°
剪一小切口,将线栓插入cca,继续将线栓插入颈内动脉,当线栓插入深度距cca与ica分叉处约9-10mm时停止插线,固定线栓(sham组小鼠仅分离血管而不插线栓)。缺血1h后拔出线栓依次缝合皮肤与肌肉,碘伏消毒,然后将手术小鼠置于电热毯37℃保温,苏醒后单笼饲养。
[0037]
(六)动物分组及样本收集实验小鼠随机分为假手术组(sham)、模型组(model, m)、人参皂苷ck原料药组(ck)和人参皂苷ck自胶束化固体分散体制剂组(ck-ssd)。其中sham和m组给等体积生理盐水,ck和ck-ssd组给药50mg/kg(按ck计算)。预给药4次,每日一次,末次给药后1h进行造模手术,术后1h拔出线栓再灌注,逐层缝合肌肉和皮肤。术后24h,再给药,每日一次,连续 3次,末次给药后4h,脱臼处死,取小鼠血浆,即为血浆样本,-80℃保存备用。
[0038]
(七)代谢组学分析方法a. 待测样品的制备取-80℃保存的血浆样本,置于4℃冰箱解冻,取100μl血浆,加入300μl色谱甲醇,涡旋振荡,冰浴超声5min。将所有样本在4℃低温条件下12000r/min离心15min,取上清液,加入适量超纯水,冷冻干燥,得到的样品加入100μl 50%甲醇复溶,涡旋30s,冰浴超声5min,12000r/min离心15min,留取上清液,即待测样品,备用。
[0039]
qc样本:每个待测样品等量取20μl混合均匀,作为质控样本进行uplc-q-tof-ms检测分析。
[0040]
b. 待测样品的分析
本发明所采用的仪器分析平台是uplc-q-tof-ms (agilent 1200 uplc和ab5600-tof-ms/ms),色谱柱为waters acquity uplc hss t3 色谱柱 (2.1 mm
×
100 mm, 1.8μm),流动相以0.1%甲酸溶液为a相,0.1%甲酸甲醇为b相,流速0.35ml/min,梯度洗脱程序如表1所示,进样量10μl,进样器温度4℃。
[0041]
质谱检测中,雾化和锥孔气为n2,为确保质谱检测质量的准确性和重复性采用dbs实时矫正。gas1为50 psi,gas2为50 psi,curtain gas为35 psi,温度500℃,正离子模式电压为5500v。
[0042]
在仪器运行时,通过运行qc样本来确保实验的稳定性。
[0043]
c. 数据处理与分析利用小分子数据分析软件waters progenesis qi进行峰提取、峰去噪、峰对齐的归一化处理,将得到的数据采用simca-p软件进行pca和opls-da数据分析,筛选出vip》1.0和p《0.05的代谢物,再去除同位素离子、加合离子与碎片离子,得到潜在化合物信息(包括保留时间、精确mass值与m/z值)。结合代谢物数据库检索hmdb和metlin等,将二级碎片信息与massbank和chemspider数据库种的碎片信息及文献进行比对分析,根据网络数据库与文献中的精确ms质谱图来初步确定潜在的差异代谢物。
[0044]
(八)结果1、仪器稳定性分析仪器稳定性实验结果如附图1所示,qc样本的pca分析图显示仪器的稳定性较好,说明本发明建立的分析方法重现性良好。
[0045]
2. 小鼠血液代谢轮廓分析采用uplc-q-tof-ms对各组小鼠血浆样本进行分离和数据采集,得到正离子模式下各组总离子流色谱图(tic)。从图中可以看出,空白对照组、m组、ck组和ck-ssd组的代谢物具有明显差异。
[0046]
3. 各组间模式识别分析及筛选差异代谢物将所得样本数据经归一化处理后,进行pca分析。在正离子模式下,空白组和m组的样本点相分离,且各组样本在一定范围内聚集,说明mcao造模后,动物体内的正常生理代谢被干扰。进一步对样本进行opls-da分析,opls-da是一种有监督的预测模型,如附图6所示,正离子模式下,模型的q2为0.976,r2x=0.407,r2y=0.999。为防止过拟合,进行了permutation验证,经过200次置换检验后,如附图7所示,产生r2=0.881和q2=-0.229,说明模型具有良好的预测能力,并且真实可靠。
[0047]
通过统计学处理后,在sham组和m组中,结合p《0.05和vip》1.0,共查找到1049种代谢差异物,通过热图分析显示(附图8)m组和假手术组具有明显差异。
[0048]
4. 基于代谢组学分析ck-ssd对mcao模型的干预作用为探讨ck及新制剂对mcao模型的干预效果,对各组样本进行了pca分析,结果如附图9所示,sham组、m组、ck组和ck-ssd组的样本点相分离,且各组样本在一定范围内聚集。进一步对样本进行opls-da分析,结果显示(附图10),正离子模式下,模型的r2x=0.472,r2y=0.991,q
2 为0.961,r2x和r2y分别表示模型中相应主成分对x矩阵和y矩阵中整体变异的解释能力,q2表示主成分对模型变异的预测能力。表明99.1%的数据符合模型判别,并且该模型的预测能力达到96.1%。
[0049]
采用置换检验的方法,经过200次置换检验后,如附图11所示,产生r2=0.651和q2=-0.367,说明模型具有良好的预测能力,并且真实可靠。通过统计学处理后进行差异代谢物的鉴定,结合p《0.05和vip值大于1.0,确定差异代谢物,并结合数据库、网站并与文献进行比较后,确定14种差异代谢物结构(见表2)。本发明鉴定出六种磷脂酰胆碱分别是pc(18:1/22:6)、pc(22:6/18:2)、pc(22:6/16:0)、pc(o-16:0/22:6)、pc(18:2/18:0)和pc(19:0/0:0),与sham组比较,m组磷脂酰胆碱含量下降,采用ck和ck-ssd干预后磷脂酰胆碱有向正常组回调的趋势,回调趋势ck-ssd组优于ck组。除此之外,还鉴定出四种溶血磷脂,分别是lysopc(22:5(4z,7z,10z,13z,16z)/0:0)、lysopc(20:2(11z,14z)/0:0)、lysopc(18:1(11z)/0:0)、lysopc(16:1(9z)/0:0),与sham组比较,m组血浆中溶血磷脂浓度下降,ck和ck-ssd药物干预后溶血磷脂血浆暴露量上升。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1