13C美沙西汀颗粒剂及其制备方法和应用与流程
13c美沙西汀颗粒剂及其制备方法和应用
技术领域
1.本发明涉及药物制剂领域,特别涉及13c美沙西汀颗粒剂及其制备方法和应用。
背景技术:
2.肝脏是人体重要的代谢器官,目前用于临床的肝功能检查指标虽然很多,但能够在肝硬化早期定量反映肝脏储备和代偿能力的试验却较少。13c美沙西汀呼气试验是近来出现的一种检测肝储备功能的新方法,通过实验发现,13c美沙西汀呼气试验值能够区分肝硬化和非肝硬化,在临床中具有非常高的价值。
3.其中,13c美沙西汀,化学名为对乙酰氨基苯甲醚(甲氧基-13c),其结构式如式ⅰ所示:
[0004][0005]
在药物制剂研究中越来越关注产品的剂型,因为药物不同剂型在药物稳定性、服用及吸收过程等方面可能会有不同程度的影响,13c美沙西汀为诊断用,需在体内快速吸收,所以本产品在服用时需尽快溶解在水中服用,为确保13c美沙西汀制剂产品的质量稳定性,以及服用和吸收过程中的安全性和有效性,研发具有优异溶解性和稳定性的13c美沙西汀剂型具有重要意义。
技术实现要素:
[0006]
有鉴于此,本发明提供了13c美沙西汀颗粒剂及其制备方法和应用。本发明所述的13c美沙西汀颗粒剂相对于传统的13c美沙西汀,稳定性好,颗粒度均匀,有利于储存以及后续制剂的生产。本发明所述的13c美沙西汀颗粒剂的制备方法,操作简单,重复性好,收率高。
[0007]
为了实现上述发明目的,本发明提供以下技术方案:
[0008]
本发明提供了13c美沙西汀颗粒剂,包括13c美沙西汀、甘露醇、助溶剂和润湿剂;所述助溶剂包括吐温80、β环糊精、氢氧化钠、柠檬酸钠、磷酸氢二钠、磷酸二氢钠、聚乙二醇6000、聚乙二醇4000、聚乙二醇2000、聚乙二醇1500中的一种或多种;所述润湿剂包括水或乙醇的水溶液中的一种或两种。
[0009]
在本发明的一些具体实施方案中,所述13c美沙西汀与所述助溶剂的重量比为1:
(0.1~100)。
[0010]
在本发明的一些具体实施方案中,以g/ml计,所述13c美沙西汀、甘露醇和所述助溶剂的混合物,与所述润湿剂的重量比为100:(1~100)。
[0011]
在本发明的一些具体实施方案中,以g/ml计,所述13c美沙西汀和所述助溶剂的混合物,与所述润湿剂的重量比为100:(1~20);所述润湿剂为乙醇的水溶液,所述乙醇的水溶液中乙醇和水的体积比为1﹕5~5﹕1。
[0012]
在本发明的一些具体实施方案中,所述13c美沙西汀与所述甘露醇的重量比为1:(20~60)。
[0013]
本发明还提供了所述的13c美沙西汀颗粒剂的制备方法,取13c美沙西汀粉碎后与甘露醇、助溶剂混合制得混合物,将所述混合物与润湿剂混合后制粒、干燥,制得13c美沙西汀颗粒剂。
[0014]
在本发明的一些具体实施方案中,所述干燥的温度为30~100℃,所述干燥的时间为1~8h。
[0015]
在本发明的一些具体实施方案中,所述干燥的温度为45℃,所述干燥的时间为3h。
[0016]
本发明还提供了所述的13c美沙西汀颗粒剂或所述的制备方法制得的13c美沙西汀颗粒剂在制备用于疾病的诊断、肝脏储备功能评估、肝脏手术前后评估的药物、试剂或试剂盒中的应用。
[0017]
在本发明的一些具体实施方案中,所述疾病包括肝硬化、原发胆汁性肝硬化、单纯脂肪变性、慢性肝病分期、酒精性肝病、肝纤维化的程度或分期、非酒精脂肪肝、新生儿胆汁淤积、胆道闭锁、肝内炎症、急性肝衰竭、肝细胞癌中的一种或多种;
[0018]
所述肝脏储备功能评估包括相关疾病肝脏功能评价、化疗肝损伤的评估、预测慢性肝衰死亡、肝解毒能力的评估中的一种或多种;
[0019]
所述手术前后评估包括肝切除后再生的评估、肝移植紧迫性的评估、术后肝衰的评估、相关手术前后评估中的一种或多种。
[0020]
与现有技术相比,本发明的有益效果包括但不限于:
[0021]
(1)本发明所述的13c美沙西汀颗粒剂具有良好的稳定性,有利于储存和后续制剂的生产等;
[0022]
(2)本发明所述的13c美沙西汀颗粒剂的制备方法,条件温和,操作简单,便于生产控制;
[0023]
(3)本发明所述的13c美沙西汀颗粒剂水溶性好,在临床使用时能快速溶于水,便于服用。
[0024]
(4)本发明所述的13c美沙西汀颗粒剂可用于制备用于疾病的诊断、肝脏储备功能评估、肝脏手术前后评估的药物、试剂或试剂盒中的应用,其具有良好的稳定性。
[0025]
本发明所述的疾病包括肝硬化、原发胆汁性肝硬化、单纯脂肪变性、慢性肝病分期、酒精性肝病、肝纤维化的程度或分期、非酒精脂肪肝、新生儿胆汁淤积、胆道闭锁、肝内炎症、急性肝衰竭、肝细胞癌中的一种或多种;
[0026]
本发明中所述肝脏储备功能评估包括相关疾病肝脏功能评价、化疗肝损伤的评估、预测慢性肝衰死亡、肝解毒能力的评估中的一种或多种;
[0027]
本发明所述手术前后评估包括肝切除后再生的评估、肝移植紧迫性的评估、术后
肝衰的评估、相关手术前后评估中的一种或多种。
附图说明
[0028]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。
[0029]
图1示实施例1制得的13c美沙西汀颗粒的hplc谱图;
[0030]
图2示实施例2制得的13c美沙西汀颗粒的hplc谱图;
[0031]
图3示实施例3制得的13c美沙西汀颗粒的hplc谱图;
[0032]
图4示实施例4制得的13c美沙西汀颗粒的hplc谱图;
[0033]
图5示实施例5制得的13c美沙西汀颗粒的hplc谱图;
[0034]
图6示实施例6制得的13c美沙西汀颗粒的hplc谱图;
[0035]
图7示本发明提供的13c美沙西汀颗粒与散剂、其他颗粒剂的水溶性、稳定性的比较结果。
具体实施方式
[0036]
本发明公开了13c美沙西汀颗粒剂及其制备方法和应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
[0037]
本发明的第一目的在于提供13c美沙西汀颗粒剂。
[0038]
本发明的第二目的在于提供13c美沙西汀颗粒剂的制备方法,所述制备方法操作简便,收率高。
[0039]
本发明的第三目的在于提供13c美沙西汀颗粒剂在制备用于疾病的诊断、肝脏储备功能评估、肝脏手术前后评估的药物、试剂或试剂盒中的应用。
[0040]
本发明所述的疾病包括肝硬化、原发胆汁性肝硬化、单纯脂肪变性、慢性肝病分期、酒精性肝病、肝纤维化的程度或分期、非酒精脂肪肝、新生儿胆汁淤积、胆道闭锁、肝内炎症、急性肝衰竭、肝细胞癌中的一种或多种;
[0041]
本发明中所述肝脏储备功能评估包括相关疾病肝脏功能评价、化疗肝损伤的评估、预测慢性肝衰死亡、肝解毒能力的评估中的一种或多种;
[0042]
本发明所述手术前后评估包括肝切除后再生的评估、肝移植紧迫性的评估、术后肝衰的评估、相关手术前后评估中的一种或多种。
[0043]
其中,所述助溶剂选自吐温80、β环糊精、氢氧化钠、柠檬酸钠、磷酸氢二钠、磷酸二氢钠、聚乙二醇6000、聚乙二醇4000、聚乙二醇2000、聚乙二醇1500中的一种或两种,所述润湿剂为乙醇水溶液,体积比为1﹕5-5﹕1。
[0044]
在本发明一优选实施方式中,所述助溶剂的组合方式包括聚乙二醇4000,或聚乙二醇4000和磷酸二氢钠,或聚乙二醇4000和磷酸氢二钠。加入助溶剂的比例为1:0.1~100。
[0045]
在本发明一优选实施方式中,所述13c美沙西汀混合粉与所述润湿剂的比例为100g﹕(1~100)ml,优选为100g﹕(2~20)ml,更优选为100g﹕(5~10)ml。
[0046]
采用上述辅料用量比,能够在保证13c美沙西汀颗粒充分溶解的同时,配合加入助溶剂的量,促进13c美沙西汀颗粒剂的水溶性,提高颗粒的稳定性。
[0047]
本发明还提供了一种所述13c美沙西汀颗粒剂的制备方法,包括如下步骤:
[0048]
1原辅料粉碎:使用粉粹机分别对碳[13c]-美沙西汀、甘露醇、助溶剂进行粉碎过筛,并使用65目筛进行复筛复核。
[0049]
2配料混合:将原料药碳[13c]-美沙西汀、辅料按比例分别称重。原辅料加入至混合机混合。
[0050]
3制粒工序:
[0051]
配制乙醇水溶液:使用药用级95%乙醇加纯水配制。
[0052]
将混合粉投入湿法混合制粒机中,按比例将润湿剂加入混合物中,同时开启搅拌、制成软材。
[0053]
将软材置于摇摆式颗粒机中制粒,大小均匀的颗粒置入不锈钢容器中。
[0054]
4干燥工序:将湿颗粒放入减压干燥烘箱中,在45℃干燥3小时,将烘干后颗粒进行筛分得目标颗粒。
[0055]
5总混灌装:将颗粒在混合机中混至颗粒均匀一致,将总混后的颗粒灌装完成。
[0056]
在本发明一优选实施方式中,所述干燥的温度为30~100℃,优选为45℃。进一步的,所述干燥的方式包括鼓风干燥、真空干燥,优选为真空烘干。
[0057]
如在不同实施方式中,所述干燥的温度可根据实际需求进行调整选择,干燥的时间可根据溶剂种类和含量进行适当的缩短或延长。
[0058]
在本发明一优选实施方式中,所述干燥的时间为1~8h。
[0059]
本发明还提供了上述13c美沙西汀颗粒剂在制备用于疾病的诊断、肝脏储备功能评估、肝脏手术前后评估的药物、试剂或试剂盒中的应用。
[0060]
所述疾病包括肝硬化、原发胆汁性肝硬化、单纯脂肪变性、慢性肝病分期、酒精性肝病、肝纤维化的程度或分期、非酒精脂肪肝、新生儿胆汁淤积、胆道闭锁、肝内炎症、急性肝衰竭、肝细胞癌中的一种或多种;
[0061]
所述肝脏储备功能评估包括相关疾病肝脏功能评价、化疗肝损伤的评估、预测慢性肝衰死亡、肝解毒能力的评估中的一种或多种;
[0062]
所述手术前后评估包括肝切除后再生的评估、肝移植紧迫性的评估、术后肝衰的评估、相关手术前后评估中的一种或多种。
[0063]
在本发明一优选实施方式中,所述药物的颗粒剂包括冲服颗粒、胶囊颗粒等。
[0064]
本发明提供的13c美沙西汀颗粒剂及其制备方法和应用中,所用原料及试剂均可由市场购得。
[0065]
下面结合实施例,进一步阐述本发明:
[0066]
实施例1
[0067]
本实施例提供了13c美沙西汀颗粒剂的制备方法,步骤如下:
[0068]
称取13c美沙西汀粗品1g,20克甘露醇,5克聚乙二醇4000,按步骤粉碎,混合,制粒,干燥;得到25.1g的13c美沙西汀颗粒,收率为96.5%,含量为100.4%,纯度为99.9%。
[0069]
实施例2
[0070]
本实施例提供了13c美沙西汀颗粒剂的制备方法,包括如下步骤:
[0071]
称取13c美沙西汀粗品1g,50克甘露醇,5克聚乙二醇4000,磷酸二氢钠0.5克按步骤粉碎,混合,制粒,干燥;得到53.3g的13c美沙西汀颗粒,收率为94.3%,含量为99.8%,纯度为99.9%。
[0072]
实施例3
[0073]
本实施例提供了13c美沙西汀颗粒剂的制备方法,包括如下步骤:
[0074]
称取13c美沙西汀粗品1g,60克甘露醇,3克聚乙二醇4000,磷酸氢二钠1克按步骤粉碎,混合,制粒,干燥;得到62.5g的13c美沙西汀颗粒,收率为96.2%,含量为100.1%,纯度为100%。
[0075]
实施例4
[0076]
本实施例提供了13c美沙西汀颗粒剂的制备方法,包括如下步骤:
[0077]
称取13c美沙西汀粗品1g,50克甘露醇,3克聚乙二醇2000,磷酸氢二钠2克按步骤粉碎,混合,制粒,干燥;得到53.1g的13c美沙西汀颗粒,收率为96.2%,含量为99.8%,纯度为100%。
[0078]
实施例5
[0079]
本实施例提供了13c美沙西汀颗粒剂的制备方法,包括如下步骤:
[0080]
称取13c美沙西汀粗品1g,50克甘露醇,3克吐温80、1克柠檬酸钠按步骤粉碎,混合,制粒,干燥;得到52.8g的13c美沙西汀颗粒,收率为96.0%,含量为99.5%,纯度为99.9%。
[0081]
实施例6
[0082]
称取13c美沙西汀粗品1g,30克甘露醇,3克β环糊精、1克磷酸氢二钠按步骤粉碎,混合,制粒,干燥;得到32.7g的13c美沙西汀颗粒,收率为93.4%,含量为99.8%,纯度为100%。
[0083]
效果例1
[0084]
本发明实施例1~6制备得到的13c美沙西汀颗粒剂的长期稳定性试验(25
±
2℃/60%
±
5%rh),结果如表1~表6所示:
[0085]
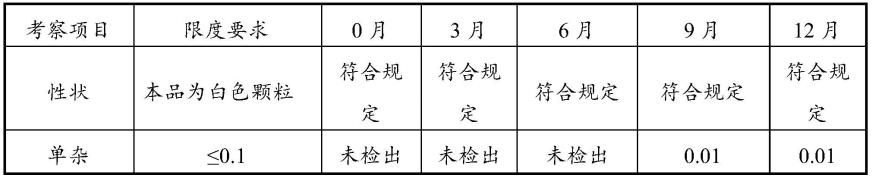
表1实施例1制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0086][0087][0088]
表2实施例2制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0089][0090]
表3实施例3制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0091][0092]
表4实施例4制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0093][0094][0095]
表5实施例5制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0096]
[0097]
表6实施例6制备得到的13c美沙西汀颗粒剂的稳定性检测结果
[0098][0099]
效果例2
[0100]
实验组1~6:本发明实施例1~6制得的13c美沙西汀颗粒剂;
[0101]
对照组1:散剂。将各辅料和原料药按照处方比例称重,在混合机混合3小时混合均匀后制得散剂粉。
[0102]
对照组2:其他颗粒剂。称取13c美沙西汀粗品1g,25g甘露醇按步骤粉碎,混合,制粒,干燥;得到25.1g的13c美沙西汀颗粒,收率为96.5%,含量为100.4%,纯度为99.9%。
[0103]
比较结果见表7。
[0104]
表7水溶性及稳定性对比
[0105][0106]
因13c美沙西汀在水中的溶解度较低,溶解速度较慢,50mg溶解到100ml水中需要搅拌较长时间,在服用时不方便。在储存过程中粉末易结块,且发生降解反应,影响产品质量;散剂为混合粉,添加辅料后对产品的水溶性有提高,但是还不能满足临床使用的要求,溶解速度也较慢,粉末在储存过程有结块,加入辅料有助于提高产品的稳定性,降解的杂质较原料药粉末减少;研制的颗粒经过处方改造及制剂工艺开发,水溶性达到临床要求,贮存时也没有结块,降解得到有效抑制,杂质很少,远低于标准限度。经对比研制的颗粒剂具有更好的稳定性和水溶性,质量稳定使用价值高。
[0107]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应
视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1