质谱技术检测尿液中PSM-E分子水平在制备用于早期诊断前列腺癌产品中的应用的制作方法
质谱技术检测尿液中psm
‑
e分子水平在制备用于早期诊断前列腺癌产品中的应用
技术领域
1.本发明涉及临床检验诊断技术领域,具体地,涉及质谱技术检测尿液中psm
‑
e分子水平在制备用于早期诊断前列腺癌产品中的应用。
背景技术:
2.根据《2020年全国癌症中心年度工作报告》报道,我国前列腺癌发病率位列第九(总人群),死亡率位列第八(总人群)。我国前列腺癌呈现发病率上升快,发病年龄逐渐年轻化。并且,60%~70%的前列腺癌患者在初诊时,已经为局部晚期或晚期。目前,国内外均缺乏准确方便的前列腺癌筛查技术。前列腺特异性膜抗原(prostate specific membrane antigen,psma)是具有水解叶酸和神经递质n
‑
乙酰天冬酰胺酶功能的跨膜糖蛋白,高表达于前列腺癌中,将其作为前列腺癌的诊断指标及潜在治疗靶点,近年来受到广泛关注。近期研究表明psma存在显著的肿瘤间及肿瘤内异质性,且关于psma对前列腺癌进程的生物学效应也出现了矛盾的数据,限制了其应用。
3.液相色谱串联质谱(lc
‑
ms/ms)由于其高灵敏度与选择性,被广泛应用于血液等生物基质中蛋白质或氨基酸的检测。中等复杂的、混合度较高的蛋白质样品需要进行lc
‑
ms/ms分析,一次可以鉴定几十到上百个蛋白质;除鉴定蛋白质之外,若需深度分析蛋白质序列信息,如位点氨基酸突变、翻译后修饰等,则需尽可能多的扫描到蛋白质的序列片断,得到很高的覆盖率。
4.lc
‑
ms/ms分析首先将蛋白溶液酶解成肽段混合物,通过液相色谱分离,如lc的c18反相柱,分离后肽段组分经离子源离子化后进入串联质谱分析,得到的质谱数据与相应的数据库进行检索匹配。特征肽是指在靶蛋白的胰蛋白酶消化产物中其氨基酸序列具有唯一专属性的多肽。
5.前列腺特异性膜抗原新型剪接变异体psm
‑
e作为psma的新型剪接变异体显示出与其不同的生物学功能及更好的肿瘤特异性,psm
‑
e在前列腺癌中特异性高表达并展现出抑制前列腺癌发展的生物学特性,为其成为新型前列腺癌诊断与治疗靶点提供了潜力。现有技术(瞿虎.前列腺特异性膜抗原新型剪接变异体psm
‑
e的外周血定量表达检测分析及其临床意义探讨[d].中山大学,2009.)具体地公开了外周血psm—e检测可用于诊断pca,并且psm—e在诊断pca的敏感性、特异性方面要优于psma,psm—e的检测灵敏度优于psma,可操作性更好。
技术实现要素:
[0006]
本发明的目的是为了克服现有技术的上述不足,提供质谱技术检测尿液中psm
‑
e分子水平在制备用于早期诊断前列腺癌产品中的应用。
[0007]
为了实现上述目的,本发明是通过以下方案予以实现的:
[0008]
本发明的第一个目的是提供检测尿液蛋白中前列腺特异性膜抗原剪接变异体
psm
‑
e水平的物质在制备用于诊断前列腺癌的产品中的应用。
[0009]
本发明的第二个目的是提供一种前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段。
[0010]
本发明的第三个目的是提供一种诊断前列腺癌的产品。
[0011]
本发明利用液相色谱串联质谱技术(lc
‑
ms/ms)结合蛋白质组学软件,确定了一个能够鉴别区分psm
‑
e的特征肽段。通过构建的特征肽段的质谱信息,对被测尿液样品蛋白酶解后的多肽混合物进行定向监测,实现对psm
‑
e在尿液中含量的定量检测。其原理为:质谱中特征肽段的响应峰面积与psm
‑
e总蛋白的含量呈线性关系,将质谱响应峰面积与psm
‑
e总蛋白含量建立标准曲线,以肽段的谱峰面积代表psm
‑
e总蛋白的实际量,通过标准曲线计算得到被测尿液标本中psm
‑
e含量。
[0012]
因此本发明要求保护检测尿液蛋白中前列腺特异性膜抗原剪接变异体psm
‑
e水平的物质在制备用于诊断前列腺癌的产品中的应用。
[0013]
优选地,所述物质是用于检测前列腺特异性膜抗原剪接变异体psm
‑
e蛋白质水平的物质。
[0014]
优选地,所述尿液蛋白中前列腺特异性膜抗原剪接变异体psm
‑
e水平是检测全长前列腺特异性膜抗原剪接变异体psm
‑
e、和/或前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段。
[0015]
更优选地,前列腺特异性膜抗原剪接变异体psm
‑
e的全长的氨基酸序列如seq id no:1所示。
[0016]
更优选地,前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段的氨基酸序列如seq id no:2所示。
[0017]
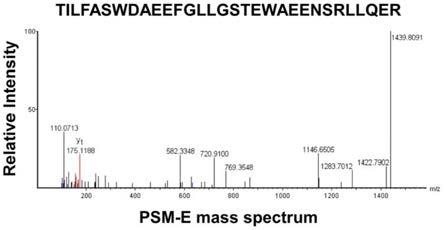
seq id no:2:tilfaswdaeefgllgstewaeensrllqer。
[0018]
优选地,其中,所述物质是用于通过如下方法中的一种或多种进行检测:多维液相色谱串联质谱(lc
‑
ms/ms)分析、免疫组化法、化学发光法、放射性同位素法、荧光发光法(如免疫荧光法)、酶标法、胶体金法、生物芯片检测法、蛋白质印迹法。
[0019]
本发明还要求保护一种前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段,所述前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段的氨基酸序列如seq id no:2所示。
[0020]
一种诊断前列腺癌的产品,能够检测尿液蛋白中前列腺特异性膜抗原剪接变异体psm
‑
e水平。
[0021]
优选地,所述尿液蛋白中前列腺特异性膜抗原剪接变异体psm
‑
e水平是检测全长前列腺特异性膜抗原剪接变异体psm
‑
e、和/或前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段。
[0022]
更优选地,所述产品包括氨基酸序列如seq id no:1所示前列腺特异性膜抗原剪接变异体psm
‑
e的全长、和/或氨基酸序列如seq id no:2所示前列腺特异性膜抗原剪接变异体psm
‑
e特征肽段。
[0023]
与现有技术相比,本发明具有以下有益效果:
[0024]
1、lc
‑
ms/ms不需要特定抗体试剂,具有高选择性、高特异性、灵敏度等优点,蛋白的转录后修饰以及突变形式。
[0025]
2、由于靶向质谱直接测定被测物的质荷比,使用同位素或其他标记物稀释校准系
统(包含内部标准化和外部校准),容易实现国际单位制(international system of units,si)溯源。而免疫方法存在非特异抗体结合、自身抗体干扰等问题,这使其溯源性存在较大的挑战。
[0026]
3、操作简单,结果稳定,整个过程只需要2h内。
[0027]
4、适用于前列腺癌的早期诊断,同时一管尿液标本可进行多种疾病早筛,通用性强。
[0028]
5、适用范围广,尿液采样方便,完全无创,可居家采样送样。尿液样品中dna、血红蛋白、白蛋白和脂质等的污染将不会对结果造成影响。
[0029]
本发明通过构建的特征肽段的质谱信息,对被测尿液样品蛋白酶解后的多肽混合物进行定向检测,实现对psm
‑
e在尿液中含量的定量检测。尿液蛋白样本经稀释后直接引入液相色谱
‑
电喷雾电离
‑
串联质谱仪进行测定,可快速、准确检测出尿液中psm
‑
e的含量水平。本发明为一种全新的尿液中psm
‑
e含量的测定方法,采用全合成的psm
‑
e特征肽标准品作为内标定量分析物,可以减少样品前处理过程中引起的误差。应用液相色谱串联质谱法更好的提高了方法的选择性与准确性。通过色谱柱以及洗脱条件的选择与优化,较好的提高了色谱分离过程,缩短了色谱分析的时间。本发明可以实现对尿液标本中psm
‑
e的定量检测,操作简单、应用方便,并证明了尿液中psm
‑
e的含量可作为前列腺癌检测的特异性生物标志物,为前列腺癌的早期筛查提供了高效、可行的技术方法。
附图说明
[0030]
图1为psm
‑
e特征肽的二级质谱图。
[0031]
图2为psm
‑
e特征肽在健康者与i
‑
iii期前列腺癌患者尿液中的含量。
[0032]
图3为psm
‑
e特征肽作为前列腺癌标志物的观测者操作特性曲线(receiver operating characteristic,roc)。
具体实施方式
[0033]
下面结合说明书附图及具体实施例对本发明作出进一步地详细阐述,所述实施例只用于解释本发明,并非用于限定本发明的范围。下述实施例中所使用的试验方法如无特殊说明,均为常规方法;所使用的材料、试剂等,如无特殊说明,为可从商业途径得到的试剂和材料。
[0034]
实施例1 psm
‑
e特征肽的标准品的合成与标准工作液的配制
[0035]
一、实验方法
[0036]
1、psm
‑
e特征肽标准品的合成
[0037]
psm
‑
e特征肽标准品经由杭州中肽生化有限公司合成,其氨基酸序列为:tilfaswdaeefgllgstewaeensrllqer(seq id no:2);5mg;纯度99.5%。
[0038]
2、psm
‑
e特征肽标准品的准备
[0039]
用ddh2o稀释bsa标准品至1ng/μl。设置8个浓度梯度的蛋白标注品:将标准品按0、1、2、4、8、10、12、14、16、18、和20μl加到96孔培养板的标准品孔中,不足20μl的孔用超纯水补足到20μl。
[0040]
表1标准品加样表
[0041][0042]
实施例2尿液中psm
‑
e特征肽含量的检测
[0043]
一、尿液标本中蛋白酶解
[0044]
方法具体如下:
[0045]
(1)将尿液样品转移至对应的10kda的超滤管中,12,000g离心20min;
[0046]
(2)每个超滤管各加200μl buffer1(8m urea/100mm tris
‑
hcl,ph 8.5),充分溶解变性蛋白;
[0047]
(3)加入20μl dtt(100mm)溶液,37℃反应2h还原二硫键;
[0048]
(4)加入20μl iaa(500mm)溶液,室温避光反应15min;
[0049]
(5)将还原烷基化后的蛋白溶液12,000g离心20min,弃掉收集管底部溶液。加入200ul buffer1离心,重复2次;
[0050]
(6)加200μl buffer2(8m urea/100mm tris
‑
hcl,ph 8.0),12,000g离心20min,弃掉收集管底部溶液,重复1次;
[0051]
(7)加200μl碳酸氢铵溶液(25mm),12,000g离心20min,弃掉收集管底部溶液,重复2次;
[0052]
(8)更换新收集管,加入100μl胰酶溶液(0.01μg/μl),37℃反应14h;
[0053]
(9)取出超滤管,12,000g离心20min,收集酶解后肽段;
[0054]
(10)超滤管中再加入100μl碳酸氢铵溶液(25mm),12,000g离心10min,收集管底溶液并与前次溶液合并;
[0055]
(11)离心干燥,待做上机。
[0056]
二、lc
‑
ms/ms分析
[0057]
将得到的酶切多肽样品经离心干燥后,重新溶解于nano
‑
lc流动相a(体积比:0.1%甲酸/水)中装瓶上样,以进行在线lcms分析。溶解后的样品以2μl的体积上样到nanoviper c18预柱上(3μm,),然后20μl流动相a冲洗脱盐。
[0058]
液相为easy nlc 1200纳升液相系统(thermofisher,usa),样品在预柱上脱盐保留后再经分析柱分离,分析柱规格是c18反相色谱柱(acclaim pepmap rslc,75μm
×
25cm c18
‑
2μm),梯度为60min内流动相b(体积比:80%乙腈,0.1%甲酸)体积比:由5%升高至38%。
[0059]
质谱采用thermofisher q exactive系统(thermofisher,usa)结合纳升喷雾nano flex离子源(thermofisher,usa),喷雾电压为1.9kv,离子传输管加热温度为275℃。
[0060]
质谱扫描方式为信息依赖的采集工作模式下(dda,data dependent analysis),一级质谱扫描分辨率为70000,扫描范围350~2000m/z,最大注入时间100ms。每次dda循环下最多采集20个电荷为2+到5+的二级图谱,二级质谱离子最大注入时间为50ms。碰撞室能量(高能碰撞诱导解离,hcd)设定为28ev,适用于所有前体离子,动态排除设置为25s。
[0061]
三、结果判读
[0062]
psm
‑
e特征肽段序列及其主要参考质谱参数见表2。psm
‑
e特征肽的二级质谱图见图1。
[0063]
表2:
[0064][0065]
实施例3尿液中psm
‑
e特征肽含量的检测
[0066]
一、实验方法
[0067]
共入选132名研究对象,各组间性别、年龄、血压、吸烟、药物使用等发面的差异均无统计学意义,具有可比性。采集70例健康者组(control)、30例i期前列腺癌组(pca
‑
i)、51例ii期前列腺癌组(pca
‑
ii)和65例iii期前列腺癌组(pca
‑
iii)病人的血清,使用实施例3的方法,检测各组尿液标本中psm
‑
e特征肽的含量。
[0068]
二、实验结果
[0069]
如图2和3所示,psm
‑
e特征肽(seq id no:2)在上述各组的尿液中浓度分别为0.9831
±
0.8322ng/ml,2.4430
±
1.3780ng/ml,5.5170
±
2.836ng/ml,6.8740
±
3.1350ng/ml。其中,与健康者组相比,在i
‑
iii期前列腺患者的尿液标本中psm
‑
e特征肽含量明显升高,且差别具有统计学意义。采用观测者操作特性曲线(receiver operating characteristic,roc)分析,在各组标本中,roc曲线下方的面积大小(areas under the curve,auc)为0.9424(95%ci,0.9082 to 0.9765),且差别具有统计学意义(p<0.0001)。并且可分析计算出psm
‑
e特征肽的cutoff值为2.249ng/ml(高于此值为前列腺癌患者,低于此值为健康人),敏感性为89.92%,特异性为90.14%。
[0070]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1