一种定量检测人体血液中新冠病毒抗体的检测试剂盒、其检测方法与流程
1.本发明属于生物技术领域,具体涉及一种定量检测人体血液中新冠病毒抗体的检测试剂盒、其检测方法。
背景技术:
2.新型冠状病毒肺炎是一种由新型冠状病毒(covid
‑
19)引起的传染较强的肺炎,部分重症患者可出现呼吸窘迫综合征或脓毒症休克,甚至死亡。感染新型冠状病毒(covid
‑
19)患者早起出现发热、乏力、干咳,逐渐呼吸困难等症状。具有较强的传染性。可引起较大的公共卫生安全事件。
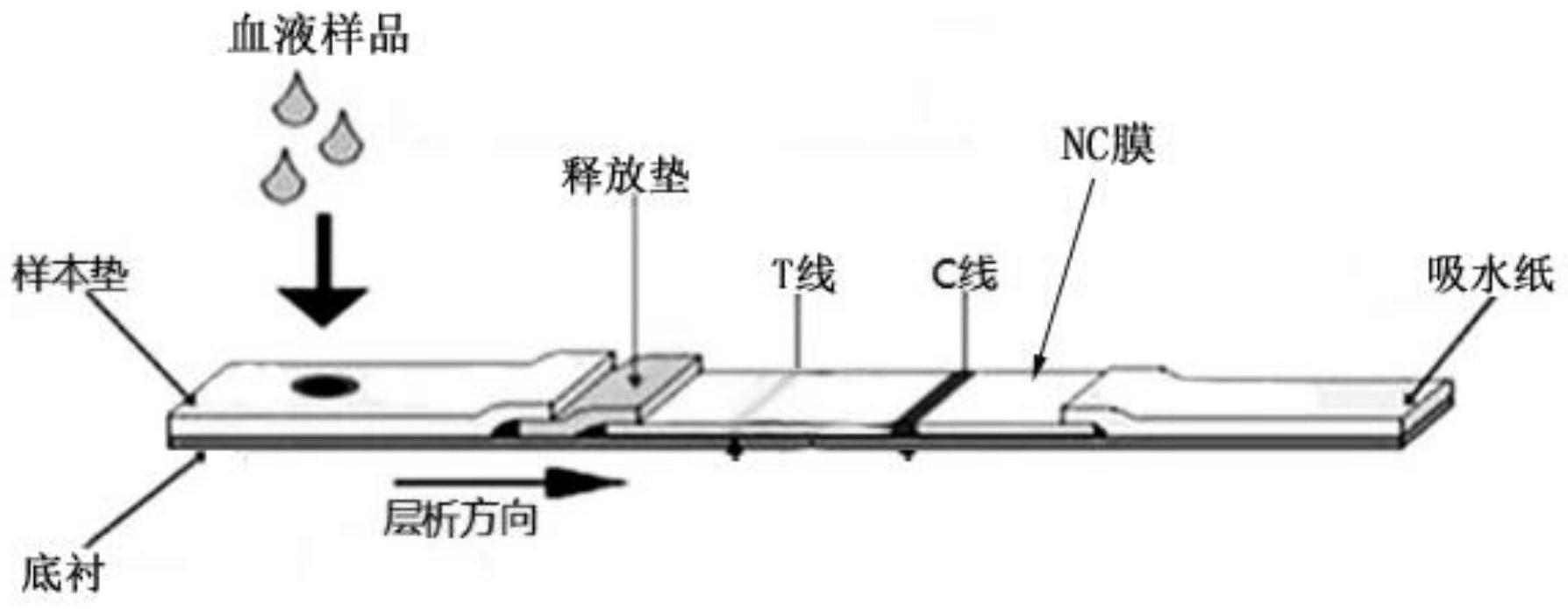
3.目前,在全球范围内已经有很多国家大范围接种新型冠状病毒疫苗,而接种疫苗后产生抗体情况的检测,对于人们预防新型冠状病毒感染具有重大的意义,对于注射了疫苗未能产生抗体的人群,应当补种疫苗,进一步有利于预防感染。但是现有常规检测试剂条的结构通常是如图1所示结构,它在释放垫的前侧通常是只有一个加样孔,释放垫上喷涂有荧光标记的抗体,nc膜的t线上包被相应的抗原,当加入血液样品进行层析检测时,荧光标记的抗体容易在层析的推动作用下提前接触到t线上的抗原,这种情况下即使血液样品中含有阳性抗体,也会容易在t线上显示淡淡的荧光条带,测试出现假阴的结果,这使得检测的正确率不高。
技术实现要素:
4.针对现有技术存在的上述技术问题,本发明的目的在于提供一种定量检测人体血液中新冠病毒抗体的检测试剂盒、其检测方法。
5.所述的一种定量检测人体血液中新冠病毒抗体的检测试剂盒,其特征在于所述检测试剂盒包括免疫层析试剂条,免疫层析试剂条包括底衬、nc膜、样品垫一、样品垫二、释放垫和吸水纸;样品垫二、释放垫、样品垫一、nc膜和吸水纸从左至右依次搭接并组装在底衬上,样品垫一和吸水纸分别叠压在nc膜的左右两端,并在nc膜的表面形成检测区,在nc膜上设置靠近样品垫一的检测线t线和靠近吸水纸的控制线c线;释放垫右端再叠压在样品垫一的左端上,样品垫二再叠压在释放垫左端上;将兔igg偶联于羧基量子点微球,获得qm
‑
兔igg;将rbd抗体偶联于羧基量子点微球,获得qm
‑
rbd抗体;将所述qm
‑
rbd抗体和所述qm
‑
兔igg混合后喷涂在免疫层析试剂条的释放垫上,并在t线区的nc膜上包被重组rbd抗原,c线区的nc膜上包被羊抗兔二抗gar。
6.所述的检测试剂盒定量检测人体血液中新冠病毒抗体的方法,其特征在于包括以下操作步骤:1)制作标准曲线:以重组新冠病毒rbd的单克隆抗体为标准品,用ph缓冲液配制成一系列不同浓度的标准工作液,空白对照液为ph缓冲液;分别点样所述检测试剂盒的免疫
层析试剂条,标准工作液或空白对照液滴入到免疫层析试剂条的样品垫一上,随后在样品垫二上滴入ph缓冲液作为层析推动液,层析一段时间后用干式荧光层析分析仪测定t线荧光值,以平均荧光值为纵坐标,标准品的浓度为横坐标绘制标准曲线,线性回归获得线性方程;2)检测血液样品:将血液样品滴入到免疫层析试剂条的样品垫一上,随后在样品垫二上滴入ph缓冲液作为层析推动液,层析一段时间后用干式荧光层析分析仪测定t线荧光值,将测得的t线荧光值代入步骤1)的线性方程中,即可推算出血液样品中新冠病毒抗体的含量。
7.所述的定量检测人体血液中新冠病毒抗体的方法,其特征在于步骤1)或步骤2)中,所述ph缓冲液为ph=7.4的pbs缓冲液或者ph=6的mes 缓冲液。
8.所述的定量检测人体血液中新冠病毒抗体的方法,其特征在于步骤1)中,标准工作液或空白对照液取20~40ul,优选为30ul滴入到免疫层析试剂条的样品垫一上;在样品垫二上滴入ph缓冲液的体积为80~100ul,优选为90ul;层析时间为12~20min,优选层析时间为15min后用干式荧光层析分析仪测定t线荧光值。
9.所述的定量检测人体血液中新冠病毒抗体的方法,其特征在于步骤2)中,血液样品的测样体积为20~40ul,优选为30ul;在样品垫二上滴入ph缓冲液的体积为80~100ul,优选为90ul;层析时间为12~20min,优选层析时间为15min后用干式荧光层析分析仪测定t线荧光值。
10.所述的定量检测人体血液中新冠病毒抗体的方法,其特征在于步骤2)中,所述血液样品为全血、血浆或血清;当血液样品为全血或血浆时,血液样品用ph缓冲液稀释至原来体积的3
‑
5倍,然后用于测样。
11.所述的一种定量检测人体血液中新冠病毒抗体的检测试剂盒,其特征在于所述羧基量子点微球为表面具有羧基功能团的量子点荧光微球,所述qm
‑
兔igg或qm
‑
rbd抗体的制备过程为:用edc/nhs交联剂活化,将兔igg或rbd抗体共价交联于量子点荧光微球,多余的火花基团用bsa和甘氨酸封闭获得量子点荧光标记的兔igg或rbd抗体。
12.所述的一种定量检测人体血液中新冠病毒抗体的检测试剂盒,其特征在于所述qm
‑
兔igg或qm
‑
rbd抗体的具体制备步骤如下:s1微球缓冲体系调整:将浓度为 20mmol/l、ph=6的mes缓冲液与浓度为1μmol/l的羧基量子点微球溶液按照1:1的体积比混合稀释,获得微球缓冲体系;s2微球活化:将浓度为20mg/ml edc
‑
hcl溶液和浓度为20mg/ml nhs溶液按照1:1的体积比快速混匀后,37℃反应15min,8000g离心20min,弃上清,沉淀用步骤s1制得的微球缓冲体系重悬;s3抗体偶联微球:步骤s2微球活化后,立即加入兔igg或rbd抗体,迅速混匀,37℃反应 1h;s4洗涤和封闭:加入20μl封闭剂,混匀,37℃反应0.5h,8000g离心15min,弃上清,沉淀用缓冲液重悬、分散,即偶联完成。
13.相对于现有技术,本发明取得的有益效果是:1、本发明通过量子点荧光标记提高检测灵敏度,在免疫层析试剂条的释放垫的左右两端分别叠加样品垫二和样品垫一,在样品垫一上先滴加血液样品,使得血液样品先层
析一定区域,随后马上在样品垫二上滴加pbs缓冲液作为层析推动液,血液样品中的阳性抗体能够赶在量子点荧光标记的rbd抗体之前,先与nc膜的t线上包被的重组rbd抗原结合,提高检测的准确性。
14.2、本发明的检测原理是基于竞争法原理,血液样品中的阳性抗体与释放垫上喷涂的量子点荧光标记的rbd抗体,竞争与nc膜的t线上包被的重组rbd抗原结合。当本发明的改进试剂条用于检测抗体阴性血液样品时,量子点荧光标记的rbd抗体与重组rbd抗原的结合作用最强,此时t线荧光值最高;当血样样品中的阳性抗体的量适当时,由于血液样品中的阳性抗体的竞争作用下,量子点荧光标记的rbd抗体与重组rbd抗原的结合作用减弱,t线荧光值一定程度上减弱,通过本发明绘制的标准曲线能够定量检测出血样样品中的阳性抗体的含量;而当血样样品中的阳性抗体的量较大时,血液样品中的阳性抗体赶在量子点荧光标记的rbd抗体之前与nc膜的t线上包被的重组rbd抗原结合,结合作用较强,将重组rbd抗原封闭起来,此时t线荧光消失,只可定性认定血样样品为阳性。
附图说明
15.图1为现有常规检测试剂条的结构示意图;图2为本发明改进试剂条的检测过程示意图;图3为本发明的改进试剂条用于检测抗体阴性血清时,检测结果示意图;图4为本发明的改进试剂条用于检测抗体阳性血清时,检测结果示意图。
具体实施方式
16.下面结合具体实施例对本发明作进一步说明,但本发明的保护范围并不限于此。
17.实施例1 qm
‑
rbd抗体和qm
‑
兔igg的制备s1微球缓冲体系调整:将0.2ml浓度为20mmol/l、ph=6的mes缓冲液与0.2ml浓度为1μmol/l的羧基量子点微球溶液混合稀释,得到微球缓冲体系。微球缓冲体系的体积是0.4ml,最终羧基量子点微球的浓度0.5μmol/l,最终缓冲体系为10mmol/l、ph=6 mes。
18.s2微球活化:将4ul 20mg/ml edc
‑
hcl(cas:25952
‑
53
‑
8)和4ul 20mg/ml nhss(cas:6066
‑
82
‑
6),快速混匀后37℃反应15min,8000g离心20min,弃上清,沉淀用步骤s1制得的0.4ml微球缓冲体系重悬至0.2ml体积(使微球浓度恢复为约1μmol/l),混匀;s3抗体偶联微球:步骤s2微球活化后,立即加入0.08mg待标记抗体,迅速混匀,37℃反应 1h;s4洗涤和封闭:加入20μl封闭剂,混匀,37℃反应0.5h,8000g离心15min,弃上清,沉淀用缓冲液重悬、分散,即偶联完成。
19.上述步骤s2中,edc:nhs:微球摩尔比约为2000:3000:1。
20.上述步骤s4中,封闭剂配方:10mg bsa溶解于1ml 100mm甘氨酸溶液中。步骤s4中的缓冲液可以是pb等简单缓冲液,也可以包含例如bsa等稳定剂,但离子强度宜低以利于胶体稳定。
21.按照上述制备过程,当步骤s3加入的待标记抗体为兔igg或rbd抗体时,制得量子点荧光标记的兔igg或量子点荧光标记的rbd抗体,分别标记为qm
‑
兔igg、qm
‑
rbd抗体。
22.实施例2:检测试剂盒的制备
1)将上述实施例1制备的量子点荧光标记rbd抗体和qm
‑
兔igg混合后喷涂在试剂盒的释放垫上,37
º
c烘干12h备用;2)用包被稀释液(150mm pb,ph 7.4)分别将重组rbd抗原和羊抗兔二抗gar稀释成0.2 mg/ml,以膜液量30
ꢀµ
l/30cm分别均匀喷涂划线于nc膜检测线区(标记为t线区)和控制线区(标记为c线区)上,37
º
c烘干处理12h,封袋备用。
23.采用上述制备的释放垫,以及t线区上包被重组rbd抗原、c线区上包被羊抗兔二抗gar的nc膜制备检测试剂条:1)常规试剂条的制备(结构如图1所示):试剂条包括底衬、nc膜、样品垫、释放垫和吸水纸。样品垫、释放垫、nc膜和吸水纸搭接组装在底衬上,释放垫和吸水纸分别叠压在nc膜的左右两端,样品垫叠加在释放垫的左端,组装后形成试纸板,切割成宽度3.78mm条状。对照图1中,t线与c线在nc膜上左右间隔设置,t线与释放垫相靠近,c线与吸水纸相靠近。
24.对照图1中,上述制备的常规试剂条组装在试剂盒中时,有一个加样孔,通过加样孔向样品垫滴加血液样品进行检测,且血液样品需用pbs缓冲液进行稀释。
25.2)本发明改进试剂条的制备:试剂条包括底衬、nc膜、样品垫一、样品垫二、释放垫和吸水纸。样品垫二、释放垫、样品垫一、nc膜和吸水纸从左至右依次搭接并组装在底衬上,样品垫一和吸水纸分别叠压在nc膜的左右两端,并在nc膜的表面形成检测区,在nc膜上设置靠近样品垫一的检测线t线和靠近吸水纸的控制线c线;释放垫右端再叠压在样品垫一的左端上,样品垫二再叠压在释放垫左端上。组装后形成试纸板,切割成宽度3.78mm条状。t线与c线在nc膜上左右间隔设置,t线与样品垫一相靠近,c线与吸水纸相靠近。
26.本发明改进试剂条组装在试剂盒中时,有两个加样孔,通过加样孔一向样品垫一滴加血液样品进行检测,通过加样孔二向样品垫二滴加pbs缓冲液作为层析推动液。本发明改进试剂条的结构示意图如图2所示。
27.本发明的改进试剂条用于检测抗体阴性血清时,检测结果示意图如图3所示。从图3可以看出,量子点荧光标记rbd抗体结合在试剂条的t线上,在t线上显现出荧光条带。
28.本发明的改进试剂条用于检测抗体阳性血清时,检测结果示意图如图4所示。血清中的阳性抗体结合在试剂条的t线上,量子点荧光标记rbd抗体最终层析到吸水纸上。
29.实施例3:基于实施例2制备的本发明改进试剂条组装在试剂盒中时,定量检测人体血液中新冠病毒抗体的方法1)标准曲线:以新冠病毒抗体rbd为标准品,用ph=7.4的pbs分别配制成50、100、200、400、800 ng/ml浓度的标准工作液,空白为ph=7.4的pbs缓冲液。分别点样本发明的试剂条,通过加样孔一向样品垫一滴加标准工作液30ul,随后马上通过加样孔二向样品垫二滴加90ul的pbs缓冲液作为层析推动液,层析约15min后在t线上显示荧光条带,用干式荧光层析分析仪测定t线荧光值;每个浓度设5个重复,以平均荧光值为纵坐标,浓度为横坐标绘制标准曲线,线性回归得到线性方程;2)检测血液样品:取人体血液用ph=7.4的pbs缓冲液稀释至原来体积的2.5倍后,取30ul通过加样孔一滴加至样品垫一上,随后马上通过加样孔二向样品垫二滴加90ul的
pbs缓冲液作为层析推动液,层析15min后用干式荧光层析分析仪测定t线荧光值,将测得的t线荧光值代入步骤1)的线性方程中,即可推算出血液样品中新冠病毒抗体的含量。我们在杭州地区进行检测,取20个没有注射过新型冠状病毒疫苗的健康人的血液,以及20个全程注射过三针安徽智飞科技有限公司生成的新型冠状病毒疫苗的健康人的血液,用本发明技术方案研发的试剂盒进行检测,20个未注射疫苗人的血液检测时,t线上的荧光值很强,结果均为阴性。20个注射疫苗人的血液检测时,基本都检出阳性抗体,当检测出阳性抗体时,t线上的荧光值明显减弱,按照本发明的方法绘制的标准曲线,也可推测出血液中抗体的含量,结果准确度高。
30.基于实施例2制备的常规试剂条组装在试剂盒中时,检测人体血液中新冠病毒抗体的方法:1)检测定性:以新冠病毒抗体rbd为标准品,用ph=7.4的pbs配制成100 ng/ml浓度的工作液,点样常规试剂条,将所述工作液90ul通过加样孔滴加至样品垫上,层析约3min后在t线上显示荧光条带;2)检测血液样品:取人体血液用ph=7.4的pbs缓冲液稀释至原来体积的5倍后,取90ul通过加样孔滴加至样品垫上,层析3min后用干式荧光层析分析仪测定t线荧光值。我们在杭州地区进行检测,取20个没有注射过新型冠状病毒疫苗的健康人的血液,以及20个全程注射过三针安徽智飞科技有限公司生成的新型冠状病毒疫苗的健康人的血液,用如图1所示的常规试剂条组装的试剂盒进行检测,20个未注射疫苗人的血液检测时,t线上的荧光值很强,结果均为阴性。20个注射疫苗人的血液检测时,基本只能检测出弱阳性的结果(这是因为采用现有常规方案进行检测时,即使在血液样品中含有相对较高浓度的抗体,也不能很好地使t线的荧光消失)。
31.根据检测结果,相对于常规试剂条的检测方法,本发明改进试剂条的检测方法的层析速度明显变慢,这是因为本发明的检测方法在样品垫一上先滴加血液样品,使得血液样品先层析一定区域,随后马上在样品垫二上滴加pbs缓冲液作为层析推动液时,层析推动液推动量子点荧光标记rbd抗体通过血液样品的层析区域向nc膜前进时,样品垫一上的血液样品对通过的层析推动液存在一定程度的层析阻力。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1