头孢哌酮钠或其制剂中杂质的分离检测方法与流程
1.本发明涉及药物质量控制技术领域,特别涉及一种头孢哌酮钠或其制剂中杂质的分离检测方法。
背景技术:
2.药品杂质谱控制是当前药物研发中的热点。杂质谱分析可以更好地反映产品中杂质的来源,进而针对性的提出控制策略,更好的控制产品质量。β-内酰胺类抗生素药物(如青霉素、头孢菌素等)是临床上最为常用的抗生素类药物,其生产工艺及自身结构的特点决定产品中有机杂质的种类复杂,其中不仅包括各种异构体和降解物,还包括药效成分聚合反应生成的聚合物杂质,使得杂质谱分析困难。
3.以头孢哌酮钠为例,其属于第三代头孢菌素类抗生素,主要用于由敏感菌引起的呼吸系统、泌尿生殖系统感染等的治疗。《中国药典》2020年版采用高效液相色谱(rp-hplc)法和凝胶色谱法分别对其小分子杂质和聚合物杂质分别进行控制,该控制方法需要两种检测手段,这无疑增加了设备投入成本,而且效率低。
技术实现要素:
4.本发明的至少一个主要目的在于提供一种头孢哌酮钠或其制剂中杂质的检测方法,该方法能够实现同时分离检测出头孢哌酮钠的小分子杂质和聚合物杂质,检测效率得到有效提高,且定量效果更准确,是控制原药或制剂中聚合物杂质的可靠方法。
5.为了实现以上目的,本发明提供了以下技术方案:
6.本发明的一个方面提供一种头孢哌酮钠或其制剂中杂质的分离检测方法,采用高效液相色谱分析方法,其中高效液相色谱条件如下:
7.色谱柱:十八烷基硅烷键合硅胶柱或辛烷基硅烷键合硅胶柱;
8.色谱柱温度:25℃~35℃,优选27℃~33℃;
9.流速:0.8ml/min~1.2ml/min;
10.检测波长:250nm~260nm;
11.流动相:由流动相a和流动相b组成,梯度洗脱;其中流动相a为ph值为2.0~3.0的溶液,流动相b选自乙腈、甲醇、四氢呋喃中的一种或多种;
12.其中,经分离检测方法分离后的杂质包括小分子杂质和聚合物杂质。
13.本发明的头孢哌酮钠制剂可以为单方制剂或复方制剂,复方制剂包括注射用头孢哌酮钠舒巴坦钠、注射用头孢哌酮钠他唑巴坦钠等典型制剂,单方制剂或复方制剂的剂型不受限,不限于典型的注射液等。
14.在一些实施方式中,流动相a选自三乙胺醋酸溶液、氨水水溶液、三氟乙酸水溶液、磷酸水溶液、枸橼酸水溶液、甲酸水溶液中的一种或多种,优选为三乙胺醋酸溶液或氨水水溶液,更优选为三乙胺醋酸溶液;流动相b为乙腈或甲醇或四氢呋喃,优选乙腈或甲醇,更优选为乙腈。
15.在一些实施方式中,流动相a的ph值可以是2.0~3.0范围内的任意值,例如2.0、2.1、2.2、2.3、2.4、2.5、2.6、2.7、2.8、2.9、3.0等,更优选ph2.4~2.6。
16.在一些实施方式中,所述流动相a是ph值为2.0~3.0的三乙胺醋酸溶液或氨水水溶液,优选ph值为2.4~2.6的三乙胺醋酸溶液。
17.在一些实施方式中,流动相是ph值为2.0~3.0的三乙胺醋酸溶液与乙腈的组合,或者ph值为2.0~3.0的三乙胺醋酸溶液与甲醇的组合,或者ph值为2.0~3.0 的三乙胺醋酸溶液与四氢呋喃的组合。
18.在一些实施方式中,流动相是ph值为2.4~2.6的三乙胺醋酸溶液与乙腈的组合,或者ph值为2.4~2.6的三乙胺醋酸溶液与甲醇的组合,或者ph值为2.4~2.6 的三乙胺醋酸溶液与四氢呋喃的组合。
19.在一些实施方式中,梯度洗脱的条件为:以体积比计,0min,a为90%~ 92%,b为10%~8%;2min,a为90%~92%,b为10%~8%;4min,a为 83%~93%,b为17%~7%;25min,a为83%~93%,b为17%~7%; 45min,a为60%~80%,b为40%~20%;55min,a为60%~80%,b为 40%~20%;56min,a为90%~92%,b为10%~8%;60min,a为90%~ 92%,b为10%~8%。
20.在一些实施方式中,梯度洗脱的条件为:以体积比计,0~2min,流动相a 为91%;2~4min,流动相a由91%降至88%;4~25min,流动相a为88%;25~45min,流动相a由88%降至70%;45~55min,流动相a为70%; 55~56min,流动相a由70%升至91%;56~60min,流动相a为91%。
21.在一些实施方式中,hplc检测的进样量为10~100μl,流速为 1.0~1.2ml/min,柱温25~35℃,优选为27~33℃,这样能够在分离度、分析时间、重现性等因素之间取得平衡,或者可以进一步将检测波长保持在254nm。
22.在一些实施方式中,配制供试品溶液的方法为:取头孢哌酮钠或其制制剂,先磷酸盐缓冲液用溶解,再用稀释剂稀释。其中,磷酸盐缓冲液和稀释剂的ph值优选接近流动相的ph值,以利于洗脱。为此,在一些实施方式中,稀释剂由流动相a和流动相b组成,流动相的体积占比为90~92%。在一些实施方式中,磷酸盐缓冲液的ph值为2.0~3.0。
23.在一些实施方式中,供试品溶液中头孢哌酮钠浓度为2mg/ml~5mg/ml。
24.在一些实施方式中,分离检测方法包括:设置所述高效液相色谱条件;配制头孢哌酮钠或其制剂的供试品溶液,以及对照溶液和/或对照品溶液;取上述配制的溶液进行高效液相色谱检测,记录色谱图;及采用主成分自身对照法和/或外标法对杂质含量进行计算。其中“对照溶液”是指通过对“供试品溶液”稀释后得到的溶液,“对照品溶液”是指采用外标法对杂质定量计算时需配制的溶液。
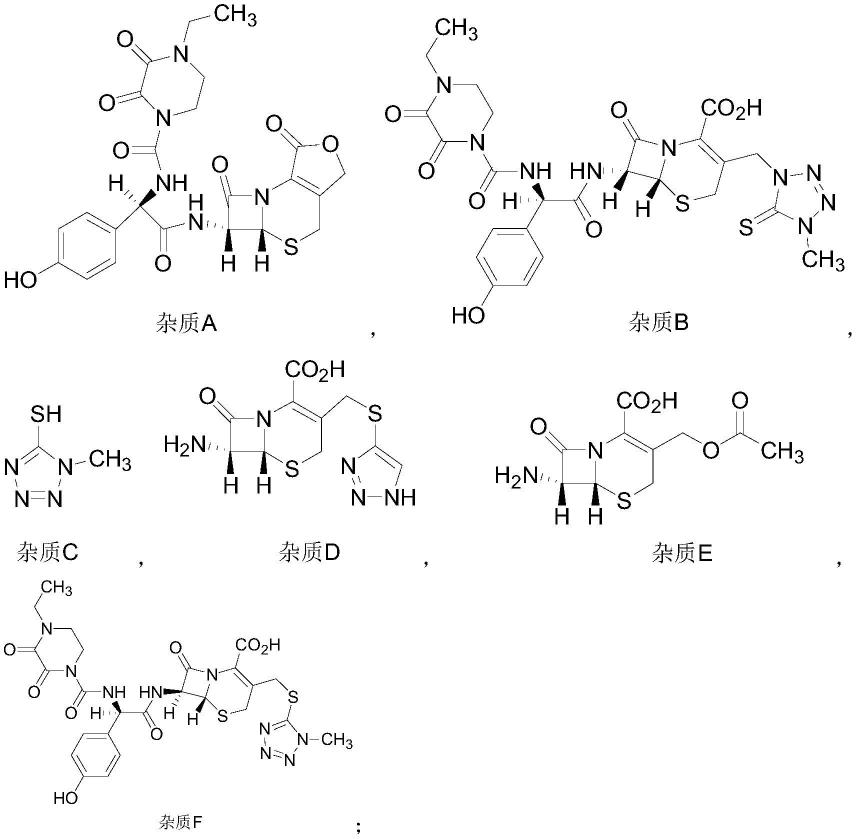
25.在一些实施方式中,杂质对照品溶液包括杂质a对照品溶液和杂质c对照品溶液,杂质a和杂质c的含量通过所述外标法定量计算;以及,杂质b、杂质d、杂质e、杂质f的含量通过主成分自身对照法定量计算。
26.本发明上述的多种技术方案主要能够分离出头孢哌酮钠制品中常见的小分子杂质(包括下文所示结构式的杂质a、杂质b、杂质c、杂质d、杂质e、杂质f中的一种或多种),还可以分离出聚合物杂质(包括头孢哌酮聚合物和聚合物杂质1和2)。对于这些种类繁多、结构差异大的分子,可能适用的定量分析方法有差异,主要从内标法、外标法、主成分自身对
照法、面积归一化法等中选择,针对不同的分析方法,在配制供试品溶液外还需要配制对照品溶液、对照溶液等与分析方法适配的溶液。经过多次试验发现,杂质a和杂质c更适宜外标法,杂质b、d、e、f更适宜主成分自身对照法。
27.在一些实施方式中,配制供试品溶液时,还配制对照溶液,以及杂质a对照品溶液和杂质c对照品溶液。
28.在一些实施方式中,供试品溶液中,每1ml中约含头孢哌酮钠0.2mg~5mg;对照溶液的制备方法包括:取部分供试品溶液,用稀释剂稀释成1ml中约含头孢哌酮钠1μg~25μg的对照溶液;杂质a和杂质c混合对照品溶液中,每1ml 中约含杂质a为3μg~75μg,每1ml中约含杂质c为1μg~25μg。
29.其中,本发明采用的主成分自身对照法为加校正因子的主成分自身对照法或者不加校正因子的主成分自身对照法,与凝胶色谱法相比,高效液相色谱法 (rp-hplc)方法专属性强,且采用主成分自身对照法进行杂质定量,聚合物杂质含量测定更准确。
30.另外,为了确认聚合物杂质是否为头孢哌酮钠或其制剂中的指针性杂质,本发明还对药品进行了强制降解处理,若相应的聚合物杂质含量增加,则基本可以认定为指针性杂质。
31.在一些实施方式中,强制降解处理包括将每1ml中约含头孢哌酮钠200mg 的水溶液置于室温下放置10天~60天,和/或进行强制氧化降解。通过进行强制降解处理,可以制备富含聚合物杂质的供试品溶液,从而更好的分离检测聚合物杂质1、聚合物杂质2。该些聚合物杂质可作为头孢哌酮钠聚合物的指针性杂质,进一步提高头孢哌酮钠或其制剂的质量可控性。
32.本发明基于以上特定的色谱条件至少可以达到以下技术效果:
33.(1)提供了一种能够同时控制头孢哌酮钠的小分子杂质和聚合物杂质的高效液相色谱法方法,能够有效提高检测效率。具体而言:
34.该方法不仅可以分离出头孢哌酮钠制品中常见的小分子杂质(包括以下结构式的杂质a、杂质b、杂质c、杂质d、杂质e、杂质f),还可以分离出聚合物杂质(包括头孢哌酮聚合物和聚合物杂质1和2)。对于头孢哌酮钠而言,现有已知可以单纯分离小分子杂质或单纯分离聚合物杂质的分离检测方法,而本发明可以实现一次性的同时分离小分子杂质和聚合物杂质,大大提高了检测效率,对于实际工业生产中的药品质量控制具有重要意义。
[0035][0036]
(2)通过改进检测方法,有效分离出了新的聚合物杂质,该些新的聚合物杂质可以作为头孢哌酮钠或其制剂的指针性杂质,以评价原药/制剂的稳定性。分离出的聚合物杂质至少包括聚合物杂质1和聚合物2,其中聚合物1为在杂质 b后出峰,相对头孢哌酮峰保留时间为1.5-2.5的第一个色谱峰,聚合物2为在杂质b后出峰,相对头孢哌酮峰保留时间为1.5-2.5的第二个色谱峰,聚合物杂质1的结构如下式(1)所示,聚合物杂质1的结构选自下式(2-a)、(2-b)中的一种或多种。实验发现头孢哌酮钠及其制剂经强制降解处理后,聚合物杂质1和2 的含量明显增加,证明二者可以作为头孢哌酮聚合物的指针性杂质,这相比现有检测方法仅需要一种检测手段,成本更低。
[0037][0038]
(3)该方法具有检测准确度高、检测精密度高、灵敏度高且专属性强等特点,是控制头孢哌酮钠原药或制剂中聚合物杂质的可靠方法。
附图说明
[0039]
通过阅读下文优选实施方式的详细描述,各种其他的优点和益处对于本领域普通技术人员将变得清楚明了。附图仅用于示出优选实施方式的目的,而并不认为是对本发明的限制。而且在整个附图中,用相同的参考符号表示相同的部件。在附图中:
[0040]
图1至图3分别为实施例1的空白溶液、供试品溶液、系统适用性溶液的色谱图;
[0041]
图4为聚合物杂质1的杂质的准分子离子峰;
[0042]
图5为聚合物杂质2的杂质的准分子离子峰;
[0043]
图6为实施例6的高效液相色谱图;
[0044]
图7为实施例7的高效液相色谱图;
[0045]
图8为对照例1的高效液相色谱图;
[0046]
图9为对照例2的高效液相色谱图;
[0047]
图10为对照例3的高效液相色谱图。
具体实施方式
[0048]
下面将结合实施例对本发明的实施方案进行详细描述,但是本领域技术人员将会理解,下列实施例仅用于说明本发明,而不应视为限制本发明的范围。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用原药、试剂或仪器未注明生产厂商
者,均为可以通过市售购买获得的常规产品或者可以根据现有技术制备得到。
[0049]
下文以头孢哌酮钠原料药为例,进行方法的建立和验证。
[0050]
其中,以下实施例所用的头孢哌酮对照品和各杂质对照品为:头孢哌酮对照品(含量:93.8%,中国食品药品检定研究院,批号:130420-201105);杂质 a(含量:98.1%,中国食品药品检定研究院,批号:130428-201605);杂质b (含量:95.8%,药渡,批号:pn5254-imp-b-180719);杂质c(含量:99.8%,药渡,批号:pn5254-imp-c-170922);杂质d(含量:95.0%,tlc,批号: 1530-014a4);杂质e(含量:98.6%,molcancorporation,批号:151203);杂质f(含量:100.0%,中国食品药品检定研究院,批号:130412-200902)。杂质a至f具有如上文所示的结构式。
[0051]
实施例1
[0052]
稀释剂:三乙胺醋酸溶液(ph值2.5)-乙腈(91∶9)。
[0053]
供试品溶液:取头孢哌酮钠适量,精密称定,加少量磷酸盐缓冲液(称取磷酸二氢钾1.0g和磷酸氢二钠1.8g,加水1000ml使溶解,即得)溶解,再用稀释剂[三乙胺醋酸溶液(ph值2.5)-乙腈(91∶9)]定量稀释制成每1ml中约含2mg的溶液,即得。
[0054]
对照溶液:精密量取上述供试品溶液1ml,置200ml量瓶中,用稀释剂稀释至刻度,摇匀,即得。
[0055]
杂质a和杂质c的混合杂质对照品溶液:精密称取头孢哌酮杂质a对照品和头孢哌酮杂质c对照品各适量,加少量乙腈溶解,超声3min,再用稀释剂定量稀释制成每1ml含头孢哌酮杂质a和头孢哌酮杂质c分别约为30μg、10μg 的溶液,即得。
[0056]
系统适用性溶液:分别取头孢哌酮对照品和各杂质对照品适量,用稀释剂溶解并稀释制成每1ml含杂质e、杂质d、杂质c、杂质a、头孢哌酮、杂质f、杂质b分别约为10μg、10μg、10μg、30μg、2mg、10μg、10μg的溶液,即得。
[0057]
取空白溶液(稀释剂)、供试品溶液、系统适用性溶液,分别注入色谱仪,检测。
[0058]
色谱条件:
[0059]
agilent eclipse xdb-c18,150
×
4.6mm,5μm,流动相a:三乙胺醋酸溶液(取三乙胺14ml与冰醋酸5.7ml,加水稀释至100ml,摇匀,取1.2ml与880ml 水混匀,并用冰醋酸调节ph值至2.5),流动相b:乙腈,流速:1.0ml
·
min-1
,紫外检测波长:254nm;柱温:30℃;进样量:30μl。洗脱梯度如表1。
[0060]
表1梯度洗脱程序
[0061][0062]
结果:
[0063]
如图1至3所示,分别为空白溶液、供试品溶液、系统适用性溶液的色谱图,可以看出:
①
不仅可以检出各国药典中所有收载的已知杂质(杂质a、b、 c、d、e、f),而且在杂质b后相对头孢哌酮峰保留时间为1.5-2.5的范围内发现两个新的未知聚合物类杂质(如图3);
②
空白溶液(稀释剂)不干扰测定,系统适用性溶液各色谱峰与相邻色谱峰分离度均大于1.5。
[0064]
实施例2对聚合物类杂质的结构分析
[0065]
供试品溶液:取头孢哌酮钠约20.0g,置100ml容量瓶中,加水溶解并稀释至刻度,配制成含头孢哌酮钠约200mg/ml的溶液,室温放置30天,得到富含聚合物杂质的母液。取母液1ml,置100ml量瓶中,加稀释剂定量稀释制成每 1ml中约含2mg的溶液,作为富含聚合物杂质的供试品溶液。采用lc-ms方法对上述富含聚合物杂质的供试品溶液进行质谱分析。
[0066]
结果:
[0067]
聚合物杂质1(图3)的+esi图中存在m/z 679.51130、m/z 717.46758的准分子离子峰(图4),分别为[m+h]+和[m+k]+峰,提示该杂质的分子量为678da;其结构见式i。
[0068][0069]
聚合物杂质2(图3)的+esi图中存在m/z 792.15286、m/z 130.86103的准分子离子峰(图5),分别为[m+h]+和[m+k]+峰,提示该杂质的分子量为791da;其结构见式2-a或2-b。
[0070][0071][0072]
实施例3各杂质线性及校正因子、检测限(lod)、定量限(loq)
[0073]
分别精密称取头孢哌酮、杂质a、b、c、d、e和f各适量,配制成loq、限度浓度40%、80%、100%、120%、200%和400%(其中,100%参照药物中允许的杂质最高限量,a、b、c、d、e和f的最高限分别为1.5%、0.5%、0.5%、 0.5%、0.5%和0.5%)的系列混合对照品溶液,进样测定,分别记录头孢哌酮及各杂质的色谱峰面积。其中,信噪比的10倍值作为各杂质的定量限,信噪比的 3倍值作为各杂质的检测限。将峰面积(a)与各自的质量浓度(c)作线性回归,计算头孢哌酮以及各杂质的线性方程。采用两套色谱仪检测:agilengt 1260 高效液相色谱仪(即仪器系统1),waters e2695高效液相色谱仪(即仪器系统 2),色谱条件实施例1。
[0074]
聚合物杂质1和聚合物杂质2在后续样品杂质含量计算时默认校正因子为 1(即不加校正因子的主成分自身对照法)。
[0075]
结果:
[0076]
①
头孢哌酮以及各杂质在各自的测定范围内线性关系良好(表2);
②
头孢哌酮、杂质a、杂质b、杂质c、杂质d、杂质e和杂质f的检测限(s/n=3) 分别为9.06、1.86、8.11、0.62、0.52、0.54和10.05ng;
③
定量限(s/n大于10) 分别为18.12、18.60、16.22、2.05、1.75、18.16和20.10ng,连续进样6针峰面积的rsd分别为1.5%、0.4%、2.1%、5.8%、0.8%、2.5%和4.3%;
④
见表2,部分杂质具有满足要求的校正因子(相对头孢哌酮的校正因子);校正因子不在 0.7~1.3范围内时,采用杂质对照品外标法定量是理想的方法。参考中国药
典2020年版,结合表2的数据,本发明选择对头孢哌酮杂质a(校正因子为0.86) 和杂质c(校正因子为0.40)采用外标法定量,对头孢哌酮杂质b、杂质d、杂质e、杂质f(校正因子分别为0.86,1.14,0.77,1.19)采用主成分自身对照法定量,建议引入校正因子提高检测的准确性。
[0077]
表2头孢哌酮及各杂质标准曲线及线性范围
[0078][0079]
实施例4专属性
[0080]
利用强制降解试验进一步验证方法的专属性:取头孢哌酮钠约100mg,共 6份,分别进行不破坏、固体光照(4500
±
500lx,7d)、固体高温(60℃,7d)、氧化(0.3%双氧水5ml,室温放置4h)、酸(0.01mol/l hcl,室温放置25h)、碱(0.01mol/l naoh,室温放置10min)破坏处理后,用稀释液溶解并稀释制成2mg
·
ml-1
的溶液;分别精密量取30μl注入色谱仪,检测,色谱条件同实验 (一)。
[0081]
结果:
[0082]
①
在酸、碱、氧化及高温强制降解条件下,头孢哌酮钠均有不同程度的降解(表3),对各降解样品进行分析,主峰与杂质峰的分离度均大于1.5,主峰纯度角均小于纯度阈值,
质量平衡均在90%~110%之间(表4)。
[0083]
②
聚合物杂质1和聚合物2在强制氧化降解反应中明显增加(表3),在实际样品中可以检出,提示该杂质可能是头孢哌酮二聚体的降解产物,可以作为头孢哌酮聚合物的指针性杂质。
[0084]
表3降解杂质汇总表
[0085][0086]
表4强制降解实验结果汇总表
[0087]
[0088][0089]
实施例5准确度
[0090]
精密称取已知杂质含量的供试品约22mg,分别置于9个10ml量瓶中,分别加入杂质a、b、c、d、e和f,制成含各杂质约为限度浓度40%、100% (分别指药物中各杂质被允许的最大限)和200%的溶液,测定其含量,计算回收率,色谱条件同实验(一)。
[0091]
结果:
[0092]
如表5所示,各浓度水平各杂质的回收率均在90%~108%之间,回收率rsd 均小于10.0%。
[0093]
表5头孢哌酮及各杂质回收率结果
[0094][0095][0096]
实施例6
[0097]
改变色谱条件,与实施例1的区别是流动相a的ph值为2.6,其余色谱条件同实施例
1。
[0098]
检测结果如图6,结果显示:杂质d与杂质e的分离度由3.2降低到2.9,说明流动相a的ph值对杂质分离度影响较大。
[0099]
实施例7
[0100]
改变色谱条件,与实施例1的区别是初始比例为流动相b的比例为10%,其余色谱条件同实施例1。
[0101]
检测结果如图7,结果显示:杂质a对初始比例的变化比较灵敏,当初始比例为流动相b的比例为10%,杂质a与相邻未知杂质分离度明显下降,分离度为1.26,小于1.5。
[0102]
对照例1
[0103]
与实施例1的区别是梯度洗脱的变化不同,参见下表6进行梯度洗脱,其余色谱条件同实施例1。
[0104]
表6
[0105]
洗脱时间流动相a体积比/%流动相b体积比/%0min881225min881245min752555min752556min881265min8812
[0106]
检测结果如图8,结果显示,当流动相b起始比例大于10%时,头孢哌酮杂质d和头孢哌酮杂质e无法达到基线分离,说明有机相起始比例过高,不利于杂质分离。
[0107]
对照例2
[0108]
与实施例1的区别是采用流动相a:流动相b=88:12的等度洗脱,其余色谱条件同实施例1。
[0109]
结果如图9,结果发现,当采用流动相a:流动相b=88:12的等度洗脱,而不提高有机相比例,可以洗脱出小分子杂质,但无法洗脱出聚合物杂质。可见,本发明采用特定的洗脱条件能达到意想不到的效果。
[0110]
对照例3
[0111]
与实施例1的区别是柱温不同,本实施例选择柱温为20℃,其余条件保持不变,考察柱温对杂质分离的影响。
[0112]
检测结果如图10,结果显示,当柱温为20℃时,头孢哌酮杂质f和头孢哌酮无法达到基线分离,说明柱温的不同,会影响杂质分离效果。
[0113]
以上所述,仅为本发明较佳的具体实施方式,但本发明的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,可轻易想到的变化或替换,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以所述权利要求的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1