基于NanoSPR的生物芯片在检测食品中小分子化合物上的应用的制作方法
基于nanospr的生物芯片在检测食品中小分子化合物上的应用
技术领域
1.本发明属于传感和免疫分析技术领域,特别是基于nanospr的生物芯片在检测食品中小分子化合物上的应用。
背景技术:
2.在近20年的发展中,出现了一种拥有spr与lspr两种模式的新型生物传感器——等离子体纳米孔阵列(nanospr)。nanospr由于其独特的三维结构,不同于平面模型的spr效应,也不同于金属纳米颗粒的lspr效应,可以同时支持spr与lspr两种模式。
3.纳米孔阵列生物传感器的等离子共振效应可以直接入射到纳米孔金属结构,表面光场立即激发,因此不需要复杂的光路和大型光学仪器的支持。nanospr纳米孔阵列生物传感器保留了传统spr传感器的实时、无需标记、无背景干扰、高分辨率等诸多优点。nanospr传感器也保留了lspr传感器在性能改造上的优势,通过对纳米孔阵列的孔径、深度、形状、周期以及表面金属的类型、厚度等参数的调节,选择出可以捕捉到存在lspr最强信号的高品质芯片,无需大型光谱仪也可以得到更强的信号。
4.基于上述优点,nanospr生物传感器的检测能力能够满足生物分子传感检测的实际需求,广泛应用于生物医药检测、药物分析、食品安全、环境检测和细胞生物学等领域。基于spr原理的传感器不需要任何标记试剂;经处理可以再次使用,节约成本;可以通过动力学研究,监控芯片界面上生物分子之间结合、解离与再活化的全过程,实时观测自己的实验对象,可应用于药物筛查与抗体活性测试;适用于小型化和高通量检测,对于便携式传感器的制造非常有益,自主研发小体积检测、功能相当的spr传感器用于原位检测临床物质和现场检测环境污染物等领域;与待测样品没有直接接触,无污染、无损失检测;灵敏度高,部分待测物被直接检测到的浓度可低于0.01ng/ml,利用分子间各种结合放大技术,还能够进一步降低检测极限;样品前处理简单,只需过滤和稀释即可满足要求。
5.现有技术中,例如中国专利申请cn106442427a提供了一种检测磺胺的表面等离子体共振免疫方法,该方法通过将固定等离子体共振芯片用edc和nhs混合液活化,再通入通入磺胺-ova溶液,使芯片完成磺胺-ova包被修饰,对四种磺胺类药物(磺胺喹恶啉、磺胺氯哒嗪、磺胺甲恶唑和磺胺甲氧嗪)的检测具有较高的灵敏度和准确度,检测过程简单、快速。
技术实现要素:
6.针对以上现有技术的不足,本发明提供了一种基于nanospr生物芯片,采用小分子化合物竞争法来进行食品小分子化合物检测的纳米表面等离子体共振免疫方法,可实现高通量、快速、超灵敏度的食品小分子化合物检测,具体通过以下技术实现。
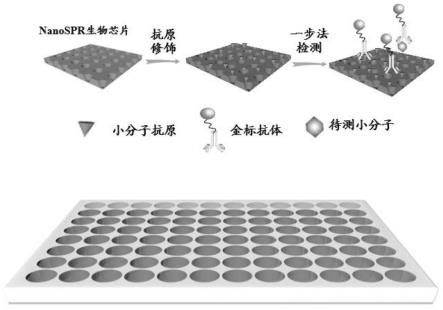
7.基于nanospr的生物芯片在检测食品中小分子化合物上的应用,包括以下步骤:
8.s1、在集成有纳米等离子共振生物芯片的芯片微孔板上进行小分子化合物的包被抗原修饰;
9.s2、用小分子化合物的抗体标记胶体金颗粒,并冻干或真空抽干在普通微孔板中;
10.s3、将待测样品加入到步骤s2所得的已冻干有小分子化合物抗体标记的金颗粒的普通微孔板中,混合均匀;然后加入到步骤s1所得的已修饰小分子化合物抗原的芯片微孔板中;
11.s4、采用酶标仪记录数据完成检测。
12.优选地,上述应用的检测方法中,所述食品小分子为抗生素类、毒素类和额外添加物类;所述抗生素类为磺胺类、氟喹诺酮、β-内酰胺类抗生素、头孢氨苄、林可霉素、替米考星-泰乐菌素、地塞米松、氯霉素、、四环素、庆大霉素、氟苯尼考、红霉素、链霉素、苯甲酸、新霉素、金霉素、土霉素、沙星类、孔雀石绿和结晶紫;所述毒素类为黄曲霉毒素m1、b1、玉米赤霉烯酮,所述额外添加物类为三聚氰胺、己烯雌酚、双酚a、β内酰胺酶。
13.本发明将免疫检测高特异性与纳米表面等离子共振技术的高灵敏、快速等特点有效结合,检测过程简单,采用先分别在芯片微孔板和普通微孔板中制备相应的产物,然后将普通微孔板中的产物加至芯片微孔板中,这种两步式高通量进行大量样本的快速检测。所构建的纳米表面等离子体共振生物芯片免疫传感检测微孔板具有检测准确度和灵敏度高、可重复使用且结果重现性好等优点,可用于牛奶、鸡蛋、鸡肉、牛肉、鱼肉等样品中的小分子药物化合物的分析检测,例如磺胺、喹诺酮、沙星类、氟虫腈等。
14.更优选地,所述食品小分子为磺胺时,磺胺的检测方法为:
15.p1、对集成有纳米等离子共振生物芯片的芯片微孔板的每个微孔先后用超纯水、无水乙醇进行清洗,氮气吹干;每个微孔中加入2-100μg/ml磺胺抗原进行第一次孵育,用pbst缓冲液清洗,氮气吹干;再加入0.5-8%的牛血清白蛋白封闭液第二次孵育,用pbst缓冲液清洗,氮气吹干后备用;
16.p2、取胶体金溶液,加入碳酸钾溶液,混匀;然后加入磺胺抗体混匀、静置;再加入peg 20000混匀,静置;冷冻离心,去上清后取沉淀加入复溶液,混匀;再加入到普通微孔板中,冻干后密封备用;
17.p3、取待测样品(一般为30-100μl)加入到步骤p2所得的已冻干有磺胺抗体标记的金颗粒的普通微孔板中,混合均匀反应5-10min;然后将普通微孔板的每个微孔中的混合液加入到步骤p1所得的已修饰磺胺抗原的芯片微孔板的每个微孔中;采用酶标仪记录数据完成检测。
18.进一步优选地,步骤p1中,第一次孵育的条件是4-37℃孵育2-24h,第二次孵育的条件是4-37℃孵育0.5-2h。
19.进一步优选地,步骤p2具体为:取1ml胶体金溶液,加入6-20μl 0.1m碳酸钾溶液,混匀;然后加入0.5-5μg磺胺抗体混匀、静置;再加入10μl 10%的peg20000混匀,静置;冷冻离心,去上清后取沉淀加入100μl复溶液,混匀;再取该胶体金复溶液加入到普通微孔板中,冻干或真空抽干后密封备用。
20.更进一步优选地,步骤p2中,冷冻离心的条件为4℃、7000-9000rpm离心20-30min。
21.更进一步优选地,步骤p2中,复溶液是含有1-5%的蔗糖、1-5%葡萄糖、0.5-4%甘露醇、0.1-5%bsa的pbst缓冲液。
22.基于上述nanospr生物芯片在检测食品中小分子化合物上的应用方法,本发明还提供了一种检测食品中小分子化合物的检测试剂盒,包括集成有纳米等离子共振生物芯片
的芯片微孔板、普通微孔板、小分子化合物抗体、小分子化合物包被抗原、复溶液。上述检测试剂盒利用间接竞争法,样品中的磺胺类药物与芯片微孔板上固定的抗原特异性竞争结合抗体,从而与纳米孔芯片产生等离子共振效应,在特定波长处引起吸光度的改变。读值大,含量少;读值小,含量多。
23.与现有技术相比,本发明的有益之处在于:本发明提供了一种基于nanospr生物芯片,采用小分子竞争法来进行食品小分子检测的纳米表面等离子体共振免疫方法,可实现高通量、快速、超灵敏度的食品小分子检测,相比于elisa方法的2h检测时间,本发明的整个检测阶段的耗时可以缩短至不超过30min。
附图说明
24.图1为光刻获得的硅晶圆芯片照片;
25.图2为集成纳米等离子共振生物芯片的96微孔板;
26.图3为nanospr生物芯片检测小分子化合物的原理示意图;
27.图4为实施例1的nanospr生物芯片检测不同浓度的磺胺小分子的全光谱图;
28.图5为实施例1的5min nanospr生物芯片检测不同浓度的磺胺小分子的柱状图;
29.图6为实施例1的5min nanospr生物芯片检测不同浓度的磺胺小分子的标准曲线图;
30.图7为实施例1的10min nanospr生物芯片检测不同浓度的磺胺小分子的柱状图;
31.图8为实施例1的10min nanospr生物芯片检测不同浓度的磺胺小分子的标准曲线图;
32.图9为实施例1的15minnanospr生物芯片检测不同浓度的磺胺小分子的柱状图;
33.图10为实施例1的15min nanospr生物芯片检测不同浓度的磺胺小分子的标准曲线图。
具体实施方式
34.下面将对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动条件下所获得的所有其它实施例,都属于本发明保护的范围。
35.实施例1
36.以磺胺类小分子化合物为例,针对采集到的待测样品,进行磺胺类小分子化合物的检测,
37.以下检测方法所使用的具体材料、试剂和仪器如下:
38.纳米等离子共振生物芯片的芯片微孔板的制备方法为:(1)在氧化硅片上进行光刻即可制作出纳米孔模具;(2)通过纳米压印方法将12寸硅晶圆纳米模具上的纳米结构转印到高分子柔性材料基底上形成反相的晶圆级纳米器件结构;(3)在其表面镀上贵金属膜层后(例如钛9nm,金70nm),即变为等离子体传感芯片;
39.磺胺抗原和磺胺抗体:采购自广州优抗多生物技术有限公司;
40.牛血清白蛋白:采购自武汉千泽穗生物科技有限公司;
41.胶体金溶液的制备方法为:
42.(1)加入400ml超纯水于洁净的三颈圆底烧瓶中,将三颈圆底烧瓶放置于油浴锅中,调节油浴锅温度至120℃,安装冷凝管,打开冷凝管水流开关。
43.(2)加热至沸腾后,加入1%柠檬酸三钠6ml,塞住瓶口。
44.(3)继续加热至再次沸腾后,加入1%氯金酸4ml,观察颜色的变化,待颜色保持在红色不再变化后倒计时10min。
45.(4)计时结束后,停止加热,关闭油浴,将三颈圆底烧瓶取出,倒出制备好的胶体金溶液于500ml洁净的玻璃瓶中自然冷却至室温后拧紧瓶盖,密封备用;
46.酶标仪:具有纳米等离子共振生物芯片特定波长(如580nm、590nm、600nm、610nm)波长的酶标仪,如xelement spr100,或使用全光谱酶标仪(如biotek epoch)或具有这些波长覆盖范围的光学检测设备。以下实施例采用的是xelement spr100。
47.超纯水:默克密理博纯水仪制备;
48.pbst缓冲液:十二水磷酸氢二钠29g,磷酸二氢钠2.72g,氯化钾2g,氯化钠20g,tween-20 5ml,防腐剂proclin300 5ml,双蒸水10l;
49.具体检测方法如下:
50.p1、对集成有纳米等离子共振生物芯片的芯片微孔板的每个微孔采用多通道移液枪加入200μl灭菌超纯水,清洗两次,再用200μl无水乙醇清洗两次,氮气吹干;每个微孔中加入10μg/ml磺胺抗原,进行第一次孵育,孵育条件为4-37℃孵育2h;用pbs缓冲液清洗两次后氮气吹干;再加入1%的牛血清白蛋白封闭液第二次孵育,37℃孵育0.5h,用pbs缓冲液清洗,氮气吹干后备用;
51.p2、取1ml胶体金溶液加至1.5ml离心管中,加入20μl 0.1m碳酸钾溶液,上下颠倒混匀;然后在离心管中加入4μg磺胺抗体,上下颠倒混匀,室温静置10min;再在离心管中加入10μl 10%的peg 20000,上下颠倒混匀,静置10min;4℃、7000rpm冷冻离心22min,取出离心管,轻柔去上清后,取沉淀(磺胺抗体标记的金颗粒沉淀)加入100μl复溶液,混匀;分别取2μl再加入到普通微孔板的每个微孔中,冻干后密封,再干燥环境中保存备用;复溶液是含有1-5%的蔗糖、1-5%葡萄糖、0.5-4%甘露醇、0.1-5%bsa的pbs缓冲液;
52.p3、将待测样品进行稀释预处理(稀释后的浓度分别为0.25、0.5、1.0、2.0、4.0、8.0、16.0ng/ml,同时设置0ng/ml的空白对照);分别取50μl加入到步骤p2所得的已冻干有磺胺抗体标记的金颗粒的普通微孔板的每个微孔中,混合均匀;然后加入到步骤p1所得的已修饰磺胺抗原的芯片微孔板中;采用酶标仪记录初始值,然后以300rpm转速振板反应5min,分别采用酶标仪记录终点值,完成检测。
53.p4、将待测样品进行稀释预处理(稀释后的浓度分别为0.25、0.5、1.0、2.0、4.0、8.0、16.0ng/ml,同时设置0ng/ml的空白对照);分别取50μl加入到步骤p2所得的已冻干有磺胺抗体标记的金颗粒的普通微孔板的每个微孔中,混合均匀;然后加入到步骤p1所得的已修饰磺胺抗原的芯片微孔板中;采用酶标仪记录初始值,然后以300rpm转速振板反应10min,分别采用酶标仪记录终点值,完成检测。
54.p5、将待测样品进行稀释预处理(稀释后的浓度分别为0.25、0.5、1.0、2.0、4.0、8.0、16.0ng/ml,同时设置0ng/ml的空白对照);分别取50μl加入到步骤p2所得的已冻干有磺胺抗体标记的金颗粒的普通微孔板的每个微孔中,混合均匀;然后加入到步骤p1所得的已修饰磺胺抗原的芯片微孔板中;采用酶标仪记录初始值,然后以300rpm转速振板反应
15min,分别采用酶标仪记录终点值,完成检测。
55.p3-p5的检测过程和具体检测结果如图1-图10所示。
56.图1中,(a)为完成纳米级光刻和刻蚀加工工艺的硅晶圆;(b)、(c)为nanospr芯片照片;(d)为芯片表面微观结构的电子显微镜照片;图2为集成纳米等离子共振生物芯片的96微孔板;
57.从图4-图10可以看到,本实施例的检测方式能够检测到0.25-16ng/ml的磺胺含量,具有非常高的检测灵敏度,且检测时间很短,检测通量很高。
58.实施例2
59.将待测样品进行稀释预处理(稀释后的浓度分别为0.25、0.5、1.0、2.0、4.0、8.0、16.0ng/ml,同时设置0ng/ml的空白对照,同时在样本中分别加入浓度为0.5、2.0、8.0ng/ml的磺胺标准品,每个浓度制备三个平行样本做样本回收率检测);分别取50μl加入到步骤p2所得的已冻干有磺胺抗体标记的金颗粒的普通微孔板的每个微孔中,混合均匀;然后加入到步骤p1所得的已修饰磺胺抗原的芯片微孔板中;采用酶标仪记录初始值,然后以300rpm转速振板反应15min,分别采用酶标仪记录终点值,完成检测。检测结果如下表1所示。
60.表1实施例2的15min nanospr生物芯片检测样本中磺胺小分子的回收率
[0061][0062]
从上表1可以看到,采用本发明的方法,对样品中磺胺类小分子的检测回收率符合要求(80-120%),是一种快速、灵敏、准确、可靠的检测方法。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1