一种原发性抑郁症的血清多肽诊断分子组合物及其应用的制作方法
1.本发明属于生物标志物技术领域,具体涉及一种原发性抑郁症的血清多肽分子组合物及其检测方法和应用。
背景技术:
2.抑郁症被科学家们描述为“21世纪的癌症”,它是目前全球疾病负担的主要原因之一,全球范围内患病率从3%到17%不等,对患者的身心健康及社会生活均产生了极大的影响。和其他精神类疾病一样,抑郁症的病因极其复杂,涉及心理社会、遗传、表观遗传、神经内分泌和神经免疫等因素。这种复杂性直接影响到我们诊断抑郁症及其亚型的准确性,影响我们对其病理生理学的理解,以及选择有效治疗策略的能力。目前临床上对于抑郁症的诊断包括病史评估及精神检查等,常用的标准化患者自评量表和临床量表可用于评估患者抑郁症状的严重性,包括phq-9、sds、bdi、qids-sr等精神量表,都缺少对抑郁症早期发病的诊断策略,而且现有的诊断方法对抑郁症早期的筛查诊断缺乏敏感性和特异性。因此,探讨抑郁症发生发展的精确分子机制,寻找新的特异性的诊断标志物对于抑郁症早期诊断和治疗,改善患者生存质量有着重要的临床意义。
3.任何疾病在出现病理变化之前,细胞内的蛋白质在成分和数量上都会有相应改变,并通过血清中的蛋白质模式反映出来。因此,通过比较不同疾病人群血清中差异蛋白质的表达,可能筛选出疾病相关的标志分子。血清蛋白质组学是指研究选定的目标人群血清中表达的全部蛋白质,在建立正常蛋白质表达图谱(protein expression map,pem)的基础上,寻找其差异蛋白质点,鉴定疾病相关蛋白质,进而研究其结构和功能,为研究重大疾病病理生理学机制、早期诊断的特异性标志物、药物作用靶点等开辟新的途径。人类血清中存在大量蛋白和多肽,其中部分蛋白和多肽的存在和缺失以及表达的高低与人类健康程度密切相关,成为疾病诊断的生物标志物。
4.血清诊断被认为是早期诊断癌症最新、最有效的方法。它是通过寻找血液中的肿瘤标志物特别是其中的蛋白标志来评判肿瘤的发生和发展情况,从而实现对肿瘤的早期诊断。人类血清中存在大量蛋白和多肽,其中部分蛋白和多肽的存在和缺失以及表达的高低与人类健康程度密切相关,成为疾病诊断的生物标志物。
技术实现要素:
5.为了克服上述现有技术的缺点,本发明的目的在于提供一种诊断原发性抑郁症的血清多肽分子组合物及其检测方法和应用,该分子多肽组合物包含
①
人α-胰蛋白酶抑制剂重链4(isoform 2of inter-alpha-trypsin inhibitor heavy chain h4precursor,itih4)
②
人β-管白微管蛋白(tubulin beta chain,tubb),该组合物是原发性抑郁症的血清标志物。
6.为了达到上述目的,本发明采用以下技术方案予以实现:
7.本发明公开了一种血清多肽诊断分子组合物,包括多肽itih4和多肽tubb,所述
itih4的氨基酸序列如seq.id.no.1所示,所述tubb的氨基酸序列如seq.id.no.2所示。
8.优选地,itih4的分子量为1062.35道尔顿,tubb的分子量为1868.21道尔顿。
9.本发明还公开了上述的血清多肽诊断分子组合物在制备原发性抑郁症血清诊断试剂中的应用,itih4在原发性抑郁症患者血清当中的检测参数为35.03-88pg/ml,在正常健康人群血清中的检测参数为18.705-56.255pg/ml;tubb在原发性抑郁症患者血清当中的检测参数为47.475-197.875pg/ml,在正常健康人群血清中检测参数为27.6-93.155pg/ml。
10.优选地,itih4与tubb在原发性抑郁症患者血清样本中显著高表达。
11.优选地,原发性抑郁症血清诊断标志物为elisa检测原发性抑郁症的血清多肽分子。
12.优选地,血清多肽分子组合物itih4与tubb是elisa检测标志物的新的靶点。
13.本发明还公开了与血清多肽诊断分子组合物相结合的分子在制备原发性抑郁症血清诊断试剂中的应用,所述血清多肽诊断分子组合物包括itih4和tubb,itih4的氨基酸序列如seq.id.no.1所示,tubb的氨基酸序列如seq.id.no.2所示。
14.本发明还公开了一种原发性抑郁症诊断试剂盒,所述原发性抑郁症诊断试剂盒包含血清多肽分子组合物itih4和tubb,所述itih4的氨基酸序列如seq.id.no.1所示,所述tubb的氨基酸序列如seq.id.no.2所示
15.与现有技术相比,本发明具有以下有益效果:
16.本发明公开了一种原发性抑郁症的血清多肽分子组合物,其氨基酸序列如s eq.id.no.1和seq.id.no.2所示,该分子组合物包括
①
itih4
②
tubb。itih4为人α-胰蛋白酶抑制剂重链4,其精确分子量为1062.35道尔顿;tubb为人β-管白微管蛋白,其精确分子量为1868.21。itih4和tubb在原发性抑郁症患者血清检测中呈现特异性的高表达:
①
itih4在原发性抑郁症患者血清中表达范围为:35.03-88pg/ml;正常健康人群中血清中表达范围为:18.705-56.255pg/ml,且两组间的表达具有极显著差异(p《0.001);
②
tubb在原发性抑郁症患者血清中表达范围为:47.475-197.875pg/ml;正常健康人群血清中表达范围为:27.6-93.155pg/ml,且两组间的表达具有显著差异(p《0.05)。
17.鉴于itih4和tubb在原发性抑郁症血清中特异性高表达,那么itih4和tubb的组合物就可以作为原发性抑郁症血清诊断标志物;用基质辅助激光解析电离飞行时间质谱仪(maldi-tof-ms)检测itih4和tubb的组合物或elisa方法检测itih4和tubb组合物的表达水平,可作为原发性抑郁症患者检测的方法。而针对elisa检测原发性抑郁症血清的诊断,itih4和tubb的组合物就可以作为elisa检测药物的新的靶点。
附图说明
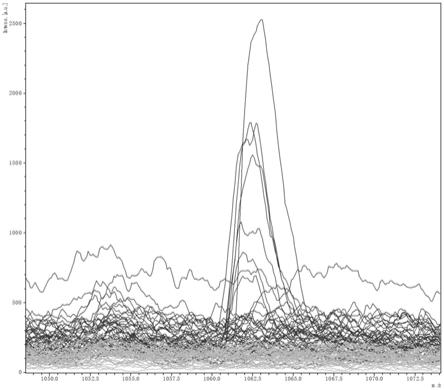
18.图1为本发明的蛋白多肽峰m/z:1062.35在原发性抑郁症患者(红色)和正常健康人群组(绿色)中的蛋白多肽表达差异图;
19.图2为本发明的蛋白多肽峰m/z:1868.21在原发性抑郁症患者(红色)和正常健康人群组(绿色)中的蛋白多肽表达差异图;
20.图3为本发明的原发性抑郁症患者血清蛋白多肽混合物的凝胶色谱分离图:其中,色谱图中横坐标表示样本流出时间,纵坐标代表多肽相对丰度;
21.图4为本发明的itih4的ms/ms质谱鉴定图谱;其中,m/z:1062.35,z=1;
22.图5为本发明的tubb的ms/ms质谱鉴定图谱;其中,m/z:1868.21,z=2;
23.图6为本发明的原发性抑郁症患者组和正常健康人群组血清中itih4蛋白的表达水平;其中,n=21;
24.图7为本发明的原发性抑郁症患者组和正常健康人群组血清中tubb蛋白的表达水平;其中,n=17。
具体实施方式
25.为了使本技术领域的人员更好地理解本发明方案,下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分的实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都应当属于本发明保护的范围。
26.需要说明的是,本发明的说明书和权利要求书及上述附图中的术语“第一”、“第二”等是用于区别类似的对象,而不必用于描述特定的顺序或先后次序。应该理解这样使用的数据在适当情况下可以互换,以便这里描述的本发明的实施例能够以除了在这里图示或描述的那些以外的顺序实施。此外,术语“包括”和“具有”以及他们的任何变形,意图在于覆盖不排他的包含,例如,包含了一系列步骤或单元的过程、方法、系统、产品或设备不必限于清楚地列出的那些步骤或单元,而是可包括没有清楚地列出的或对于这些过程、方法、产品或设备固有的其它步骤或单元。
27.下面结合附图对本发明做进一步详细描述:
28.具体的该原发性抑郁症血清诊断标志物的筛选方法为:
29.首先应用液体蛋白芯片技术分离提取原发性抑郁症患者和正常健康人群血清蛋白多肽,应用基质辅助激光解析电离飞行时间质谱技术捕获原发性抑郁症患者和正常健康人群血清蛋白多肽图谱,并且采用clinprotools2.1软件对比分析原发性抑郁症患者和正常健康人群血清蛋白多肽的血清蛋白多肽谱图差异,找出组间显著差异表达的蛋白多肽分子,在原发性抑郁症患者血清中显著低表达的蛋白多肽峰值中筛出原发性抑郁症血清标志物。
30.对于所筛选的原发性抑郁症多肽血清诊断标志物的验证为:
31.应用hplc(高效液相色谱)将原发性抑郁症患者血清分离的蛋白多肽混合物分为20~30个组分,再对其进行二级质谱的鉴定,并且对鉴定出的蛋白多肽采用酶联免疫法进行血清回归分析,结果血清回归验证证明其在原发性抑郁症患者血清中显著高表达,具有特异性,可以作为原发性抑郁症患者血清筛查的生物标志物。
32.1.样本的采集与处理
33.样本采集自延安大学咸阳医院精神科(2020年9月至2021年1月)的48例(男性15例;女性33例)原发性抑郁症患者,48例正常健康人群(男性18例;女性30例)。样本考虑年龄、性别、采集时间、储存条件是否一致以及有无基础疾病等因素。被采集者晨起空腹采血,用真空采血管(黄帽、有隔离胶)采集全血5ml,室温静置30min;室温离心5min(3000g),将上层血清分装成100μl/管,立即保存于-80℃,避免反复冻融。
34.试剂与仪器:
35.血清蛋白的提取采用德国布鲁克公司的磁珠试剂盒“弱阳离子型”(mb-wcx),以及光谱纯(hplc级)乙腈、三氟乙酸(德国merck公司)和α-氰基-4-羟基肉桂酸(hcca)(美国sigma公司)。
36.实验所用仪器包括磁珠分离器、600/384anchorchip靶板和autoflexiii基质辅助激光解析电离飞行时间质谱(matrix assisted laser desorption ionization time of flight mass spectrometry,maldi-tof-ms)(德国bruker daltonics公司)。
37.2.血清蛋白样本的制备
38.运用弱阳离子(mb-wcx)磁珠试剂盒捕获血清蛋白多肽,具体操作步骤如下:
39.①
用混匀器完全混匀磁珠悬浮液1min;
40.②
加10μl mb-wcx结合液以及10μl mb-wcx磁珠至pcr管,混匀后加5μl血清,混匀至少5次,静置5min;
41.③
将pcr管放入磁柱分离器,使磁珠贴壁1min,液体清澈后弃上清液;
42.④
加100μl mb-wcx冲洗液,在磁柱分离器上前后移动10次pcr管,磁珠贴壁后弃上清液,重复步骤
③
、
④
两次;
43.⑤
加5μl mb-wcx洗脱液洗涤贴壁的磁珠,并反复吹打10次,磁珠贴壁2min,将上清液移入干净的离心管;
44.⑥
加5μl mb-wcx稳定液至离心管并混匀,提取的蛋白多肽可以用于直接maldi-tof-ms检测或者冻存于-20℃冰箱24h之内质谱分析。
45.质谱分析:
46.将分离收集得到的蛋白样本1μl与10μl的基质α-氰基-4-羟基肉桂酸混匀,取1μl混匀物点在anchorchip靶板(德国bruker公司)上,每个样本分别点三个靶点以作三次重复。待室温干燥后将靶板放入质谱仪进行飞行时间质谱分析,采用flexcontrol 2.0软件进行标准品校正后开始样本检测,每个样本要经过总共300次激光打靶(5次点靶,每次打靶2
×
30次)之后生成质谱图,获得由不同质核比(m/z)组成的蛋白多肽谱图。采用clinprotools2.1软件结合遗传算法等生物统计学和生物信息学方法分析两组血清样本的蛋白多肽图谱。进行归一化平滑处理总离子流图,消除化学及电物理噪声;分析组间差异蛋白并计算差异大小,按差异大小由大到小排列,找出组间表达具有显著差异的蛋白多肽峰值(p《0.001)。
47.将原发性抑郁症患者和正常健康人群血清样本采用磁珠分离系统处理后,经过maldi-tof-ms分析后,对原发性抑郁症患者和正常健康人群的每个样本进行蛋白多肽图谱绘制,在分子量范围800da~10000da共检测到136个蛋白多肽峰图,且每个样本的三次重复稳定性较高。
48.采用clinprotools 2.1软件对质谱捕获的原发性抑郁症患者和正常健康人群的血清蛋白多肽图谱进行分析,将原发性抑郁症患者血清多肽谱图与正常健康人群进行比较分析,检测到具有极显著差异的蛋白多肽峰图(p《0.001),对在抑郁症患者中表达显著上调的蛋白多肽进行分析,具体如表1所示:
49.表1质谱捕获的原发性抑郁症患者和正常健康人群的血清蛋白多肽图谱分析结果
50.分子量(质荷比)p值原发性抑郁症平均表达正常健康人群平均表达1868.21
↑
《0.0000013.86
±
2.272.53
±
1.85
1062.35
↑
《0.0000019.09
±
15.232.8
±
0.60
51.对表1中的原发性抑郁症患者血清中特异高表达2个蛋白多肽进行flex analysis软件分析,结果如图1和图2所示,经过m/z:1062.35和1868.21在原发性抑郁症患者(红色)和正常健康人群(绿色)中的表达比较,发现m/z:1062.35和1868.21的蛋白多肽峰图在原发性抑郁症患者血清中均显著高表达,因此对其进行序列鉴定并作为标志物的首选进一步鉴定。
52.3.原发性抑郁症血清潜在标志物的序列鉴定
53.具体采用液相色谱分离与质谱联用的技术对原发性抑郁症患者血清多肽标志物m/z:1062.35和1868.21进行鉴定,采用thermo scientific公司的纳升流速hplc液相系统easy nlc 1200对经磁珠分离收集的质谱上样剩余的血清蛋白多肽进行二维凝胶色谱分离,再联用thermo sceientific的orbitrap fusion质谱仪对原发性抑郁症患者血清中表达上调的蛋白多肽m/z:1062.35和1868.21进行序列鉴定。
54.具体的操作步骤为:
55.3.1样本前处理
56.将100μl样本与800μl 5%乙腈0.5%甲酸溶液混合后加入1.5ml、小于10kda的超滤管中,在低温离心机中设置20℃,7000转离心40min,浓缩至500μl。脱盐,最后用70%甲醇0.5%甲酸洗脱多肽,收集浓缩至100μl,zip-tip柱处理浓缩。
57.3.2色谱分离
58.每份样品采用纳升流速hplc液相系统easy nlc 1200进行分离。缓冲液:a液为0.1%甲酸水溶液,b液为0.1%甲酸乙腈溶液。色谱柱以95%的a液平衡。样品由自动进样器上样到质谱预柱c18trap column(c18 3m 0.10
×
20mm),再经分析柱c18 column(c18 1.9m 0.15
×
120mm)分离,流速为600nl/min。相关液相梯度如表2所示,凝胶色谱分离结果如图3所示。
59.表2相关液相梯度
[0060][0061][0062]
3.3质谱鉴定
[0063]
每份样品经毛细管高效液相色谱分离后用orbitrap fusion质谱仪(thermo sceientific)进行质谱分析。主要参数设置如表3所示,质谱鉴定结果如图4、5所示:
[0064]
表3质谱分析的主要参数设置
[0065][0066]
3.4数据分析
[0067]
质谱分析原始数据为raw文件,用软件sequest和proteome discoverer 2.5.0(thermo scientific)在数据库“uniprot-human”中进行搜库鉴定,搜库时将raw文件通过proteome discoverer提交至sequest服务器,选择已经建立好的数据库,然后进行数据库搜索,相关参数如表4所示:
[0068]
表4进行数据库搜索的相关参数
[0069][0070]
结果过滤参数为:peptide fdr≤0.01。
[0071]
检索结果如表5所示:
[0072]
表5数据库搜索的检索结果
[0073][0074]
因此,用基质辅助激光解析电离飞行时间质谱仪(maldi-tof-ms)检测itih4和tubb组合物或elisa方法检测itih4和tubb组合物的表达水平,可作为原发性抑郁症患者检测的方法。提示itih4和tubb组合物是与原发性抑郁症特异性相关的蛋白,进一步通过elisa检测来进行验证。
[0075]
4.原发性抑郁症血清itih4表达的elisa血清验证分析
[0076]
4.1血清样本
[0077]
收集原发性抑郁症患者血清21例(男性8例;女性13例)、以及正常健康人群血清21例(男性10例;女性11例)进行elisa的血清验证分析。所有血清样本均来自延安大学咸阳医院,采集时间2020年9月~2021年1月。
[0078]
4.2检测方法
[0079]
采用酶联免疫法(elisa)检测原发性抑郁症患者和正常健康人群的血清itih4的表达水平,试剂盒购自中国恒远生物公司。本试剂盒应用双抗体夹心法测定标本中人α-胰蛋白酶抑制剂重链4(itih4)水平。用纯化的人α-胰蛋白酶抑制剂重链4(itih4)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入α-胰蛋白酶抑制剂重链4(itih4),再与hrp标记的α-胰蛋白酶抑制剂重链4(itih4)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物tmb显色。tmb在hrp酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的α-胰蛋白酶抑制剂重链4(itih4)呈正相关。用酶标仪在450nm波长下测定吸光度(od值),通过标准曲线计算样品中人α-胰蛋白酶抑制剂重链4(itih4)浓度。具体实验步骤参照试剂盒说明书,阳性判定标准按照试剂盒说明书界定。
[0080]
4.3统计方法
[0081]
采用spss20软件进行独立样本t检验。
[0082]
4.4结果分析
[0083]
酶联免疫法分析结果表明itih4在不同检测组中的表达水平为原发性抑郁症患者》正常健康人群,并且两组间具有极显著性差异,具体结果如表6、图6所示:
[0084]
表6不同组别血清中itih4蛋白的表达水平
[0085][0086]
对原发性抑郁症患者和正常健康人群血清中的itih4进行elisa检测,结果表明
itih4的表达具有特异性:在原发性抑郁症患者血清中表达范围为:35.03-88pg/ml;正常健康人群血清中表达范围为:18.705-56.255pg/ml,且两组间的表达具有极显著差异(p《0.001)。这表明:itih4是原发性抑郁症患者发生密切相关的蛋白,可以作为初步的原发性抑郁症病变的检测指标。
[0087]
因此可以通过elisa实验对待检血清样本的itih4表达初步判定其为原发性抑郁症患者(35.03-88pg/ml)或正常健康人群(18.705-56.255pg/ml)。
[0088]
5.原发性抑郁症血清tubb表达的elisa血清验证分析
[0089]
5.1血清样本
[0090]
收集原发性抑郁症患者血清17例(男性9例;女性8例)、以及正常健康人群血清17例(男性10例;女性7例)进行elisa的血清验证分析。所有血清样本均来自延安大学咸阳医院,采集时间2020年9月~2021年1月。
[0091]
5.2检测方法
[0092]
采用酶联免疫法(elisa)检测原发性抑郁症患者和正常健康人群的血清tubb的表达水平,试剂盒购自中国恒远生物公司。本试剂盒应用双抗体夹心法测定标本中人β-微管蛋白(tubb)水平。用纯化的人β-微管蛋白(tubb)抗体包被微孔板,制成固相抗体,往包被单抗的微孔中依次加入β-微管蛋白(tubb),再与hrp标记的β-微管蛋白(tubb)抗体结合,形成抗体-抗原-酶标抗体复合物,经过彻底洗涤后加底物tmb显色。tmb在hrp酶的催化下转化成蓝色,并在酸的作用下转化成最终的黄色。颜色的深浅和样品中的β-微管蛋白(tubb)呈正相关。用酶标仪在450nm波长下测定吸光度(od值),通过标准曲线计算样品中人β-微管蛋白(tubb)浓度。具体实验步骤参照试剂盒说明书,阳性判定标准按照试剂盒说明书界定。
[0093]
5.3统计方法
[0094]
采用spss20软件进行独立样本t检验。
[0095]
5.4结果分析
[0096]
酶联免疫法分析结果表明tubb在不同检测组中的表达水平为原发性抑郁症患者》正常健康人群,并且两组间具有显著性差异,具体结果如表7、图7所示:
[0097]
表7不同组别血清中tubb蛋白的表达水平
[0098][0099]
对原发性抑郁症患者和正常健康人群血清中的tubb进行elisa检测,结果表明tubb的表达具有特异性:在原发性抑郁症患者血清中表达范围为:47.475-197.875pg/ml;正常健康人群血清中表达范围为:27.6-93.155pg/ml,且两组间的表达具有显著差异(p《0.05)。这表明:tubb是原发性抑郁症患者发生密切相关的蛋白,可以作为初步的原发性抑郁症病变的检测指标。
[0100]
因此可以通过elisa实验对待检血清样本的tubb表达初步判定其为原发性抑郁症患者(47.475-197.875pg/ml)或正常健康人群(27.6-93.155pg/ml)。
[0101]
以上内容仅为说明本发明的技术思想,不能以此限定本发明的保护范围,凡是按
照本发明提出的技术思想,在技术方案基础上所做的任何改动,均落入本发明权利要求书的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1