外消旋苏木精的半合成和用途的制作方法
外消旋苏木精的半合成和用途
背景技术:
1.苏木精已经被描述为组织学、组织化学、组织病理学和细胞学中最重要和最常用的染料。若干组织化学染色方案(包括苏木精和曙红(h&e)染色和巴氏染色剂(pap)染色)依赖染料苏木精以对细胞学样品和组织样品进行染色。特别地,由病理学家使用细胞核的苏木精染色以检测肿瘤活检样品中恶性和/或转移性细胞的存在。
2.苏木精是一种天然存在的化合物,存在于采木(haematoxylum)属树木的红色心材中。苏木精本身在水溶液中是无色的,并且不是染色组织成分的活性成分。相反,苏木精的氧化产物氧化苏木精成为苏木精溶液的活性染色组分,特别是在与媒染剂络合时。例如,为了生产功能性染料,苏木精被氧化为氧化苏木精,并且随后与若干种金属离子中的一种金属离子结合,该金属离子包括铝(al
+3
)、铁(fe
+3
)和铬(cr
+3
)。氧化苏木精是通过暴露在空气和阳光下自然产生的。自然过程称为“熟成”,并且可能需要三个月或更长时间才能提供适用于细胞染色的溶液。
3.苏木精染色可以使用浸泡(dip-and-dunk)技术手动完成,或通过使用自动化系统(例如由ventana medical systems,inc.提供的自动化系统)完成。染色过程通常涉及:(a)从粘附至显微镜载玻片的样本中去除石蜡,并且通过在水中浸泡来使样本保湿;(b)在特定制剂中应用苏木精,以对细胞核进行染色;(c)通过用水冲洗来去除过量的苏木精;(d)将载玻片与ph值高于5.0的浓缩溶液接触,使苏木精变为蓝色(例如蓝化溶液);以及(e)通过用水冲洗来去除蓝化溶液。
技术实现要素:
4.本公开提供了包含外消旋苏木精的苏木精制剂。在一些实施例中,外消旋苏木精制剂适用于染色生物学样品中的细胞核。在一些实施例中,外消旋苏木精制剂适用于对粗面内质网、核糖体、胶原蛋白、髓鞘、弹性纤维和酸粘蛋白进行染色。在一些实施例中,外消旋苏木精制剂适合作为cish(显色原位杂交)中的复染剂,或适用于观察特定抗原-抗体复合物周围的形态(显色免疫组织化学)。申请人意外发现,用外消旋苏木精染色在功能上等同于用市售对映纯苏木精染色。
5.本公开的第一方面为苏木精制剂,该苏木精制剂包含外消旋苏木精和至少一种添加剂(例如,选自溶剂、化学氧化剂、媒染剂、稳定剂和抗氧化剂的至少一种添加剂)。在一些实施例中,苏木精制剂包含添加剂中的至少两种添加剂。在一些实施例中,苏木精制剂包含添加剂中的至少三种添加剂。在一些实施例中,苏木精制剂包含外消旋苏木精、溶剂、化学氧化剂、媒染剂、稳定剂和抗氧化剂。在一些实施例中,存在于苏木精制剂中的一定量的化学氧化剂足以将外消旋苏木精的至少一部分转化为氧化苏木精。在一些实施例中,溶剂为水性溶剂。在一些实施例中,抗氧化剂为水溶性抗氧化剂。在一些实施例中,水溶性抗氧化剂包括对苯二酚。
6.在一些实施例中,溶剂包括水、低级烷醇和多元醇中的一者或多者。在一些实施例中,溶剂包括水和多元醇。在一些实施例中,多元醇选自由以下项组成的组:丙二醇、聚(乙
二醇)和聚(丙二醇)。
7.在一些实施例中,苏木精制剂中介于1%与50%之间的外消旋苏木精由化学氧化剂氧化为氧化苏木精。在一些实施例中,化学氧化剂包括碘酸钠、氧化汞、高锰酸钾、高碘酸钾和过氧化氢中的一者或多者。在一些实施例中,化学氧化剂包括碘酸钠。在一些实施例中,组合物中苏木精与氧化剂的摩尔比在约6:1与约1:1之间的范围内。在一些实施例中,媒染剂包括铝媒染剂、铁媒染剂、铋媒染剂、铜媒染剂、钼媒染剂、钒媒染剂和锆媒染剂中的一者或多者。在一些实施例中,媒染剂包括硫酸铝。
8.在一些实施例中,稳定剂包括环糊精或环糊精衍生物。在一些实施例中,环糊精或环糊精衍生物为β-环糊精和β-环糊精衍生物中的一者或多者。
9.在一些实施例中,苏木精制剂进一步包括酸。在一些实施例中,不向苏木精制剂中添加酸。
10.本发明的另一个方面为一种用于对生物学样品进行染色的方法,该方法包括使生物学样品与外消旋苏木精制剂接触。在一些实施例中,外消旋苏木精制剂包含:溶剂;苏木精;足以将苏木精的至少一部分转化为氧化苏木精的量的化学氧化剂;媒染剂;抗氧化剂和稳定剂。在一些实施例中,稳定剂选自由以下项组成的组:多糖、穴醚、穴蕃、穴状配体、冠醚、树枝状聚合物、纳米管、杯芳烃、缬氨霉素和尼日利亚菌素。
11.在一些实施例中,该方法进一步包括使样品与复染剂接触。在一些实施例中,复染剂选自由以下项组成的组:曙红y、橙黄g、亮绿sf淡黄、俾斯麦棕和固绿fcf。在一些实施例中,样品与外消旋苏木精制剂的接触包括进行性苏木精染色方案。在一些实施例中,样品与外消旋苏木精制剂的接触包括退行性苏木精染色方案。在一些实施例中,该方法为自动化的。在一些实施例中,生物学样品被支持在基底上。在一些实施例中,基底包括显微镜载玻片。
12.在一些实施例中,在约25℃下,稳定剂的水溶性大于约100mg/ml。在一些实施例中,抗氧化剂选自由以下项组成的组:对苯二酚、没食子酸正烷基酯、还原性糖、苯甲酸、羟基苯甲酸、亚硫酸、焦亚硫酸、柠檬酸、酒石酸、乳酸、异抗坏血酸抗坏血酸、尿酸、单宁酸、一种或若干种螯合剂、水合氯醛、它们的衍生物以及盐。
13.本公开的另一个方面为ph降低的苏木精制剂,该苏木精制剂包含外消旋苏木精和酸,该酸的量在占ph降低的苏木精制剂的总体积的约0.2%至约4%的范围内,并且其中ph降低的苏木精制剂的ph值小于约2.4。在一些实施例中,酸选自由以下项组成的组:盐酸、硫酸、高氯酸和硝酸。在一些实施例中,ph值小于约2.3。在一些实施例中,ph值小于约2.2。在一些实施例中,ph值小于约2.1。在一些实施例中,ph值在约2.1至约2.2之间的范围内。
14.在一些实施例中,ph降低的苏木精制剂进一步包含媒染剂和氧化剂。在一些实施例中,ph降低的苏木精制剂进一步包含稳定剂。在一些实施例中,稳定剂包括多元醇。在一些实施例中,多元醇选自由以下项组成的组:丙二醇、乙二醇以及它们的混合物。
15.在一些实施例中,制剂基本上由外消旋苏木精、媒染剂、氧化剂和酸组成。在一些实施例中,氧化剂包括碘酸钠。在一些实施例中,媒染剂包括铝。
16.在本公开的另一个方面,为一种对生物学样品进行染色的方法,该方法包括:提高ph降低的苏木精制剂的等分试样的ph值以提供ph值在约2.4至约2.6的范围内的外消旋苏木精染色溶液,以及使生物学样品与ph值在约2.4至约2.6的范围内的苏木精染色溶液接
触。在一些实施例中,通过添加包含强碱或缓冲剂的重新调整溶液,提高ph降低的苏木精制剂的等分试样的ph值。
17.在一些实施例中,强碱选自由以下项组成的组:氢氧化钠、氢氧化钾、氢氧化锂和氨。
18.在一些实施例中,重新调整溶液进一步包含选自由以下项组成的组的添加剂:多元醇、氧化剂、媒染剂以及它们的任何组合。在一些实施例中,在使生物学样品与苏木精染色溶液接触之前,提高ph降低的苏木精制剂的ph值。在一些实施例中,生物学样品包括组织学样品或细胞学样品
19.在本公开的另一个方面,提供了一种包括第一组分和第二组分的试剂盒。在一些实施例中,第一组分包含ph降低的苏木精制剂,该苏木精制剂包含外消旋苏木精和酸,该酸的量在占ph降低的苏木精制剂的总体积的约0.1%至约10%的范围内,并且其中ph降低的苏木精制剂的ph值小于约2.4。第二组分包含强碱或缓冲剂,并且以相对于第一组分的量提供,使得当第一组分和第二组分合并时,ph降低的苏木精制剂的ph值提高至大于约2.4。
20.在一些实施例中,第二组分以相对于第一组分的量提供,使得当第一组分和第二组分混合时,ph降低的苏木精制剂的ph值提高至大于约2.5。在一些实施例中,第二组分以相对于第一组分的量提供,使得当第一组分和第二组分混合时,ph降低的苏木精制剂的ph值在约2.45至约2.54之间的范围内。在一些实施例中,第二组分以相对于第一组分的量提供,使得当第一组分和第二组分混合时,ph降低的苏木精制剂的ph值在约2.5至约2.6之间的范围内。
21.在一些实施例中,第一组分进一步包含媒染剂和氧化剂。在一些实施例中,第一组分进一步包含保质期延长剂。在一些实施例中,保质期延长剂为多元醇。在一些实施例中,多元醇选自由以下项组成的组:丙二醇、乙二醇以及它们的混合物。
22.在一些实施例中,ph降低的苏木精制剂基本上由苏木精、媒染剂、氧化剂和酸组成。在一些实施例中,第二组分包含选自由以下项组成的组的强碱:氢氧化钠、氢氧化钾和氢氧化锂。在一些实施例中,第二组分包含选自由以下项组成的组的缓冲剂:氰基乙酸盐、富马酸盐和硫酸盐。
23.在一些实施例中,试剂盒进一步包括第三组分,第三组分包含复染剂。在一些实施例中,复染剂选自由以下项组成的组:曙红y、橙黄g、亮绿sf淡黄、俾斯麦棕和固绿fcf。
24.在本公开的另一个方面,提供了一种用于对安装在基底上的生物学样品进行染色的系统,该系统包括第一容器和第二容器,该第一容器包含ph降低的苏木精制剂外消旋苏木精和酸,该酸的量在占ph降低的苏木精制剂的总体积的约0.1%至约10%的范围内,并且其中ph降低的苏木精制剂的ph值小于约2.4,该第二容器包含重新调整溶液。在一些实施例中,第一容器和第二容器流体耦合至混合容器,使得ph降低的苏木精制剂和重新调整溶液可以合并,以提供苏木精染色溶液。在一些实施例中,该系统进一步包括基底保持器,该基底保持器用于保持安装在基底上的生物学样品,基底保持器与混合容器流体连通,使得苏木精染色溶液可以施加到生物学样品。
附图说明
25.有关对本公开特征的一般理解,请参考附图。在附图中,整个附图使用相同的附图
标记来识别相同的元素。
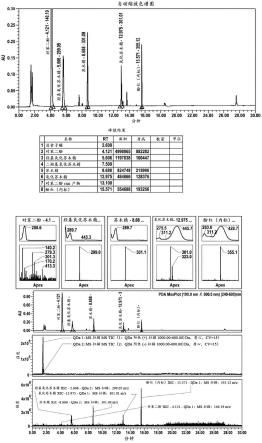
26.图1a示出了包含商业苏木精的溶液的自动缩放hplc色谱图,并且进一步示出了峰值结果。
27.图1b示出了对于溶液的各个组分,图1a的hplc色谱图的峰值结果的放大视图。
28.图2a示出了包含外消旋苏木精的溶液的自动缩放hplc色谱图,并且进一步示出了峰值结果。
29.图2b示出了对于溶液的各个组分,图2a的hplc色谱图的峰值结果的放大视图。
30.图3a示出了用商业苏木精染色的组织样品。
31.图3b示出了用商业苏木精染色的组织样品。
32.图4a示出了用外消旋苏木精染色的组织样品。
33.图4b示出了用外消旋苏木精染色的组织样品。
34.图5a和5b比较了肾小球组织上20倍下的商业苏木精与20倍下的合成苏木精(三色苏木精)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
35.图6a和6b比较了结肠组织上20倍下的商业苏木精与20倍下的合成苏木精(粘蛋白卡红铁苏木精)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
36.图7a和7b比较了结肠组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精ii)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
37.图8a和8b比较了肾小球组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精ii)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
38.图9a和9b比较了扁桃体组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精ii)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
39.图10a和10b比较了肾小球组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
40.图11a和11b比较了肌肉血管组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
41.图12a和12b比较了结肠组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
42.图13a和13b比较了皮脂腺毛囊组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
43.图14a和14b比较了皮肤组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
44.图15a和15b比较了扁桃体组织上20倍下的商业苏木精与20倍下的合成苏木精(苏木精和曙红)。用合成苏木精染色会提供相对更多的核细节并且使更清晰的图像重叠。
具体实施方式
45.还应该理解的是,除非指明是相反情况,否则在本文所要求保护的包括一个以上步骤或动作的任何方法中,所述方法的所述步骤或动作的顺序不必限于表述所述方法的所述步骤或动作的所述顺序。
46.说明书中提及“一个实施例”、“实施例”及“示例实施例”等意指描述的实施例可包括具体特征、结构或特性,但每一个实施例可以或并不必需包括具体特征、结构或特性。此外,这种短语并不必然指相同实施例。此外,当结合实施例描述具体特征、结构或特性时,需要注意的是,无论是否明确说明,本领域技术人员均知晓结合其他实施例来实现上述特征、结构或特性的效果。
47.如本文所用,除非上下文另有明确指示,否则单数形式“一(a/an)”和“该/所述”包括复数个指代物。同样,除非上下文另有明确指示,否则词语“或”旨在包括“和”。术语“包括”定义为包容性,如“包括a或b”是指包括a、b或a和b。
48.如本文在说明书和权利要求书中所用,“或”应理解为与上文定义的“和/或”具有相同的含义。例如,在分隔列表中的项目时,“或”或“和/或”应解释为具有包容性,例如,若干元素或元素列表中的至少一个元素,但也包含一个以上元素,以及任选地包含额外的未列出的项目。只有指明与之相反的术语,如“仅其中之一”或“恰好其中之一”,或者在权利要求中使用的“由
…
组成”,将指包含若干元素或元素列表中的恰好一个元素。一般来说,本文使用的术语“或者”只有在前面有“或”、“其中之一”、“只有一个”或“恰好一个”等排他性术语时,才应解释为表示排他性的替代选择(例如,“一个或另一个,但不是两个”)。在权利要求书中使用的“基本上由...组成”应具有在专利法领域使用的普通含义。
[0049]“包括”、“包含”、“具有”等术语可互换使用,且含义相同。类似地,“包括”、“包含”、“具有”等可互换使用并且具有相同的含义。具体而言,每个术语的定义都与普通美国专利法对“包括”的定义一致,因此每个术语都可理解为一个开放性术语,其含义为“至少以下”,并且也可理释为不排除额外的特征、限制、方面等。因此,例如“具有组件a、b和c的装置”是指所述装置至少包括组件a、b和c。同样,短语:“涉及步骤a、b和c的方法”是指所述方法至少包括步骤a、b和c。此外,尽管本文可以特定的顺序概述步骤和过程,但是本领域技术人员将认识到,所述顺序步骤和过程可能会有所不同。
[0050]
如本文在说明书和权利要求书中所用,就一个或多个元素的列表而言,短语“至少一个”应理解为选自元素列表中任何一个或多个元素的至少一个元素,但不一定包括元素列表中具体列出的每个元素中的至少一个,也不排除元素列表中的任何元素组合。除了在短语“至少一个”所涉及的元素列表中具体确定的元素之外,该定义还允许其他元素任选地存在,无论这些元素与具体确定的元素相关与否。因此,作为一个非限制性实例,“a和b中的至少一个”(或者等效地,“a或b中的至少一个”,或者等效地,“a和/或b中的至少一个”)在一个实施例中可以指至少一个任选地包括一个以上的a,但没有b(以及任选地包括b以外的元素);在另一个实施例中,指至少一个任选地包括一个以上的b,但没有a(以及任选地包括a以外的元素);在又一个实施例中,指至少一个任选地包括一个以上的a,以及至少一个任选地包括一个以上的b(以及任选地包括其他元素)等。
[0051]
术语“抗氧化剂”是指一种原子或分子,该原子或分子的氧化还原电位比第二原子或分子更大,使得抗氧化剂而非第二原子或分子优先地被氧化。例如,抗氧化剂的氧化电位可以比氧化苏木精更大,从而有助于防止氧化苏木精氧化为氧基氧化苏木精。此外,抗氧化剂还可以起还原剂(例如,可以将氧基氧化苏木精转化回氧化苏木精的还原剂)的作用。抗氧化剂可以以约1mm至约1m、例如约5mm至约500mm、诸如约50mm至约150mm的范围内的浓度存在于所公开的制剂中。
[0052]
术语“水性溶剂”是指具有水作为主要组分并且在室温下为液体的组合物。水和具有约50体积%或更高水含量的一种或多种低级烷醇或多元醇的混合物为水性溶剂的示例。
[0053]
术语“生物学样品”是指从生物实体(例如动物)获得或以其他方式衍生自该生物实体的任何样品,例如,从人类或兽医动物(诸如狗、猫、马或牛)获得的样品。生物学样品的示例包括细胞学样品、组织样品和生物流体。生物学样品的非限制性特定示例包括血液、尿液、预射精液、乳头抽吸物、精液、乳汁、痰、粘液、胸膜液、盆腔积液、滑液、腹水、体腔清洗液、眼刷、皮肤刮屑、口腔拭子、阴道拭子、子宫颈抹片、直肠拭子、抽吸物、穿刺活检、例如通过手术或尸检而获得的组织切片、血浆、血清、脊髓液、淋巴液、汗液、眼泪、唾液、肿瘤、器官以及从体外细胞或组织培养物中获得的样品。通常,样品将为已经被固定、处理以去除水分,并且包埋在石蜡中或其他合适的蜡状物质以用于切割成组织切片的活检样品。生物学样品可以被安装在基底(例如显微镜载玻片)上,以用于进行处理和/或检查。
[0054]
术语“媒染剂”是指一种离子金属物种,染料(例如氧化苏木精)可以与该离子金属物种形成复合物(例如阳离子复合物),该复合物用于将染料(例如氧化苏木精)与特定细胞组分(诸如核dna、髓鞘、弹性纤维和胶原纤维、肌肉条纹和线粒体)结合。媒染剂的示例包括铝(例如,呈明矾的形式,诸如硫酸铝、硫酸铝钾或硫酸铝铵)、铁、钨、锆、铋、钼(磷钼酸或钼酸)和钒(钒酸盐)。
[0055]
术语“氧化剂”是指一种原子或分子,该原子或分子的氧化还原电位比第二分子更大,例如,氧化还原电位比苏木精更大,使得该氧化剂将与苏木精反应并且将该苏木精氧化为氧化苏木精。氧化剂包括大气中天然存在的分子氧以及“化学氧化剂”,该分子氧可以扩散至苏木精并且将其氧化,该化学氧化剂与苏木精(通常在溶液中)主动结合,以将苏木精的至少一部分转化为氧化苏木精。有用的化学氧化剂的示例包括碘酸盐(诸如碘酸钠和碘酸钾)、氧化汞、高锰酸盐(例如高锰酸钾)、高碘酸盐(诸如高碘酸钠和高碘酸钾)和过氧化物(例如过氧化氢)中的一者或多者。在特定实施例中,化学氧化剂包括碘酸钠。
[0056]
术语“稳定剂”是指具有内腔部分或沟槽部分的有机或无机分子、复合物或材料,并且更具体地,是指具有内腔部分或沟槽部分的分子,该内腔部分或沟槽部分可以容纳氧化苏木精或其他染料分子的至少一部分或其他染料分子。
[0057]
概述
[0058]
本公开提供了包含外消旋苏木精的苏木精制剂。在一些实施例中,外消旋苏木精制剂适用于染色生物学样品中的细胞核。申请人意外发现,用外消旋苏木精染色在功能上等同于用市售对映纯苏木精染色。该结果令人惊讶,因为手性对于生物系统中几乎所有的化学过程均具有极其重要的意义。它也固有地存在于多核苷酸(如dna和rna)的结构中,两者在分子和超分子尺度上,已经被发现构成了基于苏木精的阴离子染色的主要靶标。[1,2]它们的不对称d-核糖和d-2-脱氧核糖单位含有具有手性环境的若干立体中心和位点,该手性环境适用于氢键结合、静电相互作用或化学试剂的协调结合。[12e]此外,它们的螺旋性给它们的三级结构带来了另一个层次的手性,如例如在b-dna中可以观察到该情况。
[0059]
手性在dna和rna的功能中起着至关重要的作用,因为它指导着它们与其他手性和非手性化学试剂的相互作用,诸如酶或甚至小分子(如染料)。[1,12e]因此,大量的药物、染料以及有机金属复合物与不同dna序列和构象之间的相互作用已经成为许多研究的主题。[2,3,4,5]可以证明,在如用手性染料来进行染色[2,5,6]或用对映纯药物治疗疾病[4]的
过程中,dna结合的对映选择性为决定性参数,并且甚至可以控制非期望的副作用(诸如毒性和致突变性)的发生。众所周知,多种天然产物的对映异构体与dna的结合和反应不同。
[0060]
在该背景下,杜卡霉素(duocarmycin)a(从链霉菌属分离的天然产物,以高效力对dna进行烷基化)的对映异构体为突出性示例。boger和其他人已经示出,(+)-杜卡霉素a比(-)-杜卡霉素a更有选择性地进行结合,并且其烷基化dna的效率优于(-)-杜卡霉素a 110倍。[9]道诺霉素为另一种突出的天然产物和高活性抗癌药物,以其柔红酮苷元单元插入dna,并且使用其d-六碳氨糖残基来与b-dna的小沟结合。[10]最近的研究可以确定,当与其(-)-对映异构体相比时,(+)-道诺霉素对b-dna中的某些序列如聚[(dgdc)]2的结合亲和力增加了21倍。[11]此外,各种单体的和连接的聚酰胺已经用于阐明手性对与多核苷酸结构的结合能力的影响。[12]对于该组分子,一般来说,r-对映异构体的与b-dna的结合亲和力强烈增强。
[0061]
对映纯染料对dna的手性识别已经得到最深入地研究,研究对象为螺烯和其他经取代的平面多环烃,如芘和蒽衍生物。[3,6]因此,由质子化的氨基基团修饰的螺烯的p-对映异构体在b-dna与z-dna之间的结合中显示出区别。[5]已经证明一组手性阳离子[4]螺烯对dsdna的结合亲和力存在差异,其因子介于1.2至2.3之间。[3]由于dna-金属相互作用的普遍重要性,因此也已经对手性无机物和有机金属复合物进行大量研究,研究对象为它们对dna样结构的结合特性。例如,在使用r,r-形式而非其s,s-异构体时,1,2-二氨基-环己烷的某些pt复合物表现出显著较低的毒性,并且甚至是更有效的抗癌药物。[7]与此类似,人们已经发现了许多其他手性金属复合物(其中心承载铁、铑、钌和锇)的结合中的对映选择性,并且该手性金属复合物用作探测不同dna构象的工具。[8]苏木精明矾本身作为基于苏木精的染色制剂的最好示例,是路易斯酸al3+和氧化苏木精的有机金属复合物(后者仍然拥有一个立体中心),从而使苏木精明矾在所有关闭其不同的、ph依赖性的组合物和配体球体中具有手性。[1]
[0062]
尽管j.a.kiernan最近的研究表明,红色苏木精明矾阳离子仅被静电吸引至dna的磷酸阴离子,使得当经染色的制剂在ph值高于5.5的情况下被蓝化时,红色阳离子反而原位沉淀为蓝色化合物,蓝化前和蓝化后的苏木精明矾-dna相互作用的性质仍然没有得到具体解决。[2]考虑到上述化学原理和科学发现,熟练的化学家将假设,在组织学染色中使用苏木精的任一纯对映异构体均将产生不同的着色强度,因为与dna的结合亲和力不同。基于前述,在组织学中采用外消旋苏木精而非纯的天然对映异构体应当产生较少或较强的染色,这取决于哪种异构体形成更多的dna-仿射al3+-复合物。由于组织诊断中的组织学分析仍然主要是由实验者进行主观视觉判断,因此任何与由纯(+)-苏木精制备的制剂不同的染色特性均将对组织学家的个人操作经验和其报告结果的正确性构成挑战。只有(+)-苏木精和(-)-苏木精对dna的行为大致相同,才能使它们的外消旋物在基于苏木精的组织诊断中具有使用价值。
[0063]
外消旋苏木精制剂
[0064]
本公开提供了包含外消旋苏木精的苏木精制剂(后文称为“外消旋苏木精制剂”)。一般来说,外消旋苏木精制剂包含外消旋苏木精和至少一种附加组分。在一些实施例中,附加组分选自稳定剂、溶剂、抗氧化剂、氧化剂、媒染剂和酸。在一些实施例中,外消旋苏木精制剂包含外消旋苏木精和至少两种附加组分。在一些实施例中,外消旋苏木精制剂包含外
消旋苏木精和至少三种附加组分。在一些实施例中,外消旋苏木精制剂包含外消旋苏木精和至少四种附加组分。
[0065]
例如,在一些实施例中,外消旋苏木精制剂包含外消旋苏木精、溶剂、化学氧化剂和媒染剂。再例如,在一些实施例中,外消旋苏木精制剂包含外消旋苏木精、溶剂和酸。又例如,在一些实施例中,外消旋苏木精制剂包含外消旋苏木精、溶剂、化学氧化剂、媒染剂,以及稳定剂和抗氧化剂中的一者或两者。又例如,在一些实施例中,外消旋苏木精制剂包含外消旋苏木精、溶剂、化学氧化剂、媒染剂、稳定剂和抗氧化剂。又例如,在一些实施例中,外消旋苏木精制剂包含两种或更多种不同的抗氧化剂,诸如两种或更多种水溶性抗氧化剂。又例如,在一些实施例中,外消旋苏木精制剂包含一种或多种稳定剂和一种或多种抗氧化剂。
[0066]
适用于在本公开的任何外消旋苏木精制剂内使用的附加组分由avwioro等人“histochemical uses ofhematoxylin-a review,”jpcs第(1)卷,2011年4月至6月,和bryan d.llewellyn,"hematoxylin formulae,"http://stainsfile.info,october 2013所示,其公开内容据此以引用方式整体并入本文。
[0067]
外消旋苏木精
[0068]
苏木精具有下述结构。外消旋苏木精(rac-苏木精)包括(+)-苏木精和(-)-苏木精的混合物。
[0069][0070]
在一些实施例中,(+)-苏木精与(-)-苏木精的比率在约1:10至约10:1之间的范围内。在其他实施例中,(+)-苏木精与(-)-苏木精的比率在约1:5至约5:1之间的范围内。在又一些实施例中,(+)-苏木精与(-)-苏木精的比率在约1:4至约4:1之间的范围内。在又一些实施例中,(+)-苏木精与(-)-苏木精的比率在约1:3至约3:1之间的范围内。在又一些实施例中,(+)-苏木精与(-)-苏木精的比率在约1:2.5至约2.5:1之间的范围内。在又一些实施例中,(+)-苏木精与(-)-苏木精的比率在约1:2至约2:1之间的范围内。
[0071]
在一些实施例中,外消旋苏木精包括介于约40重量%至约60重量%之间的(+)-苏木精。在其他实施例中,外消旋苏木精包括介于约45重量%至约55重量%之间的(+)-苏木精。在又一些实施例中,外消旋苏木精包括介于约48重量%至约52重量%之间的(+)-苏木精。在又一些实施例中,外消旋苏木精包括约50重量%的(+)-苏木精。
[0072]
在一些实施例中,外消旋苏木精可以根据本文实例2所述的程序而衍生。在其他实施例中,外消旋苏木精可以根据dann o,hofmann h(1965)chromane xvii.die synthesechem.ber.98:1498
–
1504,[german]所示的程序来合成,其公开内容据此以引用方式整体并入本文。
[0073]
稳定剂
[0074]
合适的稳定剂包括多糖,诸如直链淀粉、环糊精和含有多个醛糖环的其他环状或螺旋状化合物,例如通过单糖(诸如葡萄糖、果糖和半乳糖)和二糖(诸如蔗糖、麦芽糖和乳糖)的1,4和1,6键形成的化合物。其他稳定剂包括穴醚、穴蕃、穴状配体、冠醚、树枝状聚合物、纳米管、杯芳烃、缬氨霉素和尼日利亚菌素。
[0075]
在一些实施例中,稳定剂可以包括用一个或多个取代基修饰的环糊精衍生物、直链淀粉衍生物、穴醚衍生物、穴蕃衍生物、穴状配体衍生物、冠醚衍生物、树枝状聚合物衍生物、纳米管衍生物、杯芳烃衍生物、缬氨霉素衍生物和尼日利亚菌素衍生物。例如,稳定剂包括直链淀粉衍生物和环糊精衍生物,其中羟基基团或羟基基团的氢原子的组成醛糖环的该羟基基团或羟基基团的氢原子中的一者或多者被取代基取代。取代基的示例包括酰基基团(例如乙酰基基团)、烷基基团、芳基基团、对甲苯磺酰基基团、甲磺酰基基团、氨基基团(包括伯氨基基团、仲氨基基团、叔氨基基团和季氨基基团)、卤素基团(-f、-cl、-br和-i)、硝基基团、含磷基团(诸如磷酸酯基团和磷酸烷基酯基团)、含硫基团(诸如硫酸盐基团和硫酸酯基团)、桥连基团(例如,该桥连基团连接环糊精环上的两个或更多个羟基位置,或连接两个或更多种稳定剂)、醛基团、酮基团、肟基团、羧酸基团以及它们的衍生物、碳酸酯和氨基甲酸酯基团、含硅基团、含硼基团、含锡基团和羟基烷基基团(诸如羟基乙基基团和羟基丙基基团)。
[0076]
环糊精的特定示例包括α-环糊精、β-环糊精、γ-环糊精和δ-环糊精,以及这些类别的环糊精中的每种环糊精的衍生物。环糊精衍生物的特定示例包括羟丙基化α-环糊精、羟丙基化β-环糊精、羟丙基化γ-环糊精、羟乙基化α-环糊精、羟乙基化β-环糊精、羟乙基化γ-环糊精、羟异丙基化α-环糊精、羟异丙基化β-环糊精、羟异丙基化γ-环糊精、羧甲基化α-环糊精、羧甲基化β-环糊精、羧甲基化γ-环糊精、羧乙基化α-环糊精、羧乙基化β-环糊精、羧乙基化γ-环糊精、辛基琥珀酸化-α-环糊精、辛基琥珀酸化-β-环糊精、辛基琥珀酸化-γ-环糊精、乙酰化-α-环糊精、乙酰化-β-环糊精、乙酰化-γ-环糊精、硫酸化-α-环糊精、硫酸化-β-环糊精和硫酸化-γ-环糊精。环糊精衍生物的其他特定示例包括以下β-环糊精衍生物:2,3-二甲基-6-氨基甲基-α-环糊精、6-叠氮基-α-环糊精、6-溴-β-环糊精、6a,6b-二溴-β-环糊精、6a,6b-二碘-β-环糊精、6-o-麦芽糖基-β-环糊精、6-碘-α-环糊精、6-对甲苯磺酰基-β-环糊精、过乙酰基-麦芽糖基-β-环糊精、6-叔丁基二甲基甲硅烷基-β-环糊精、2,3-二乙酰基-6-丁基二甲基甲硅烷基-β-环糊精、2,6-二丁基-3-乙酰基-β-环糊精、2,6-二丁基-β-环糊精、2,6-叔丁基-二甲基甲硅烷基-β-环糊精和2,6-二-o-甲基-3-烯丙基-β-环糊精。各种环糊精和环糊精衍生物可以例如从ctd,inc.(high springs,fla.)商购获得,或者它们可以根据科学文献中,例如在"synthesis of chemically modified cyclodextrins,"croft and bartsch,tetrahedron,39:1417
–
1474,1983中概述的程序合成。
[0077]
在一些实施例中,稳定剂为环糊精或环糊精衍生物中的一者或多者。在其他实施例中,稳定剂为β-环糊精和β-环糊精衍生物中的一者或多者。在又一些实施例中,稳定剂可以为α-直链淀粉、β-直链淀粉或γ-直链淀粉。
[0078]
在一些实施例中,稳定剂可以包含在任何外消旋苏木精制剂中,其浓度在约1mm至约1m之间的范围内、约5mm至约500mm之间的范围内或约5mm至约25mm之间的范围内。
[0079]
在又一些实施例中,稳定剂可以为环糊精或环糊精衍生物,并且更具体地,稳定剂可以为环糊精或环糊精衍生物,其在约25℃下表现出大于约5mg/ml,诸如大于约20mg/ml、大于约100mg/ml或甚至大于约500mg/ml的水溶性。
[0080]
溶剂
[0081]
在本公开的外消旋苏木精制剂中可以利用各种溶剂。在一些实施例中,溶剂包括水、低级烷醇(例如乙醇)和多元醇中的一者或多者。在其他实施例中,溶剂包括水性溶剂,其中水性溶剂包括水和多元醇。
[0082]
多元醇的合适示例包括甘油、乙二醇、丙二醇、聚(乙二醇)和聚(丙二醇)。在一些实施例中,水性溶剂制剂包含介于约5体积%至约45体积%之间的乙二醇和丙二醇中的一者或多者。在其他实施例中,水性溶剂制剂包含介于约10体积%至约40体积%之间的乙二醇和丙二醇中的一者或多者。在又一些实施例中,水性溶剂制剂包含介于约15体积%至约30体积%之间的乙二醇和丙二醇中的一者或多者。
[0083]
抗氧化剂
[0084]
适用于任何外消旋苏木精制剂的抗氧化剂的示例包括对苯二酚;没食子酸;还原性糖,诸如如山梨醇和甘露醇;苯甲酸和羟基苯甲酸;亚硫酸和焦亚硫酸;某些酸,诸如柠檬酸、酒石酸、乳酸、异抗坏血酸抗坏血酸、尿酸、单宁酸和此类酸的盐(诸如mg
2+
、nh
4+
、na
+
、k
+
和ca
2+
盐);去除起氧化剂的作用的金属的螯合剂,例如edta;以及水合氯醛。在其他实施例中,水溶性抗氧化剂包括对苯二酚和没食子酸正丙酯中的一者或多者。
[0085]
氧化剂
[0086]
合适的化学氧化剂包括大气中天然存在的分子氧以及“化学氧化剂”,该分子氧可以扩散至外消旋苏木精并且将其氧化,该化学氧化剂与外消旋苏木精(通常在溶液中)主动结合,以将外消旋苏木精的至少一部分转化为氧化苏木精。半氧化苏木精溶液为其中所包含的氧化剂的量氧化大约一半的可用外消旋苏木精的溶液,如gill,acta cytologica,18(4):300
–
11(1974)所述,其公开内容以引用方式整体并入本文。有用的化学氧化剂的示例包括碘酸盐(诸如碘酸钠和碘酸钾)、氧化汞、高锰酸盐(例如高锰酸钾)、高碘酸盐(诸如高碘酸钠和高碘酸钾)和过氧化物(例如过氧化氢)中的一者或多者。在特定实施例中,化学氧化剂包括碘酸钠。
[0087]
氧化剂的存在量可以足以将外消旋苏木精完全(例如基本上定量地)氧化为氧化苏木精,或者仅足以将外消旋苏木精部分氧化为氧化苏木精。在特定实施例中,超过一半的外消旋苏木精由化学氧化剂氧化为氧化苏木精,并且在其他实施例中,小于一半的外消旋苏木精由化学氧化剂氧化为氧化苏木精。例如,介于1%与50%之间的外消旋苏木精可以由化学氧化剂氧化为氧化苏木精,但更通常地,介于约10%与约30%之间的外消旋苏木精由化学氧化剂氧化为氧化苏木精。在特定示例中,制剂中使用的外消旋苏木精与氧化剂的摩尔比在6:1与1:1之间。应当理解,尽管化学氧化剂被认为是制剂的一部分,但该化学氧化剂在与外消旋苏木精的反应后会转化为其还原产物。这些还原产物将保留在制剂中。
[0088]
媒染剂
[0089]
用于任何外消旋苏木精制剂的合适的媒染剂包括铝媒染剂、铁媒染剂、铋媒染剂、铜媒染剂、钼媒染剂、钒媒染剂和锆媒染剂。在一些实施例中,媒染剂包括明矾。在其他实施例中,媒染剂包括硫酸铝。在一些实施例中,制剂中媒染剂的浓度可以大于制剂中氧化苏木
精的浓度(可以通过折光法、薄层色谱法或光谱法来进行确定),或者制剂中该媒染剂的浓度可以小于制剂中氧化苏木精的浓度。替代地,在一些实施例中,制剂中外消旋苏木精与媒染剂的摩尔比在约2:1与约1:100之间的范围内。在其他实施例中,制剂中外消旋苏木精与媒染剂的摩尔比在约2:1与约1:50之间的范围内。在又一些实施例中,制剂中外消旋苏木精与媒染剂的摩尔比在约1:5与约1:20之间的范围内。
[0090]
酸
[0091]
在一些实施例中,外消旋苏木精制剂可以进一步包括酸和/或缓冲剂。任何酸均可以用于外消旋苏木精制剂。合适的酸的非限制性示例包括乙酸、氢碘酸、氢溴酸、盐酸、硝酸、氢氟酸、亚硝酸和甲酸。
[0092]
外消旋苏木精制剂的示例
[0093]
在一些实施例中,外消旋苏木精制剂中的外消旋苏木精的摩尔浓度在约0.01m与约0.05m之间。在其他实施例中,外消旋苏木精制剂中的外消旋苏木精的摩尔浓度在约0.02m与约0.04m之间。在又一些实施例中,外消旋苏木精制剂中的外消旋苏木精的摩尔浓度为约0.03m。
[0094]
在一些实施例中,外消旋苏木精制剂包含作为溶剂的水和乙二醇的混合物,作为氧化剂的碘酸钠,作为媒染剂的硫酸铝,以及作为稳定剂的β-环糊精或其衍生物。一种或多种水溶性抗氧化剂(诸如对苯二酚和没食子酸正丙酯)也可以包括在此类特定实施例中。在其他实施例中,水和乙二醇的混合物包含约10体积%至约40体积%的乙二醇和约60体积%至约90体积%的水。在一些实施例中,外消旋苏木精制剂包含水、乙二醇醚和外消旋苏木精的混合物。
[0095]
制备外消旋苏木精制剂的方法
[0096]
本公开还涉及制备外消旋苏木精制剂的方法,该方法例如用于生物学样品的组织化学染色。在一些实施例中,该方法包括:形成氧化苏木精溶液,向氧化苏木精溶液添加媒染剂以形成染色溶液,以及向染色溶液添加稳定剂和抗氧化剂中的一者或两者以形成外消旋苏木精制剂。在一些实施例中,氧化苏木精溶液的形成包括:将外消旋苏木精溶解在溶剂中,以及添加足以将外消旋苏木精的至少一部分转化为氧化苏木精的量的化学氧化剂。在一些实施例中,用于溶解外消旋苏木精的溶剂包括水性组合物,诸如包含水和多元醇的组合物。如本文所述,合适的多元醇的非限制性示例包括甘油、乙二醇和丙二醇。形成苏木精组合物的其他方法描述于美国公开号2017/0284908中,其公开内容以引用方式整体并入本文。
[0097]
ph降低的外消旋苏木精制剂
[0098]
本公开提供了ph降低的苏木精制剂。一般来说,ph降低的苏木精制剂包含外消旋苏木精、酸和至少一种添加剂,诸如本文所述添加剂中的任何添加剂。在一些实施例中,包括至少两种添加剂。在其他实施例中,包括至少三种添加剂。在一些实施例中,ph降低的苏木精制剂包含溶剂、外消旋苏木精和酸。在一些实施例中,酸为强酸。在一些实施例中,强酸选自氢碘酸、氢溴酸、盐酸和硝酸。在其他实施例中,酸为弱酸。在一些实施例中,弱酸选自氢氟酸和甲酸。在一些实施例中,ph降低的苏木精制剂包含外消旋苏木精、酸,以及媒染剂、氧化剂、保质期延长剂、抗氧化剂和稳定剂中的至少一者。
[0099]
在一些实施例中,ph降低的苏木精制剂的ph值小于约2.4。在一些实施例中,ph降
低的苏木精制剂的ph值小于约2.375。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.35。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.325。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.3。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.275。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.25。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.225。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.2。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.175。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.15。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.125。在其他实施例中,ph降低的苏木精制剂的ph值小于约2.1。
[0100]
在一些实施例中,ph降低的苏木精制剂的ph值为约1.5与约2.4之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约1.5与约2.3之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约1.6与约2.3之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约1.8与约2.3之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约2与约2.3之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约2与约2.3之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约2与约2.2之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约1.5与约2.2之间。在其他实施例中,ph降低的苏木精制剂的ph值介于约1.6与约2.2之间。
[0101]
本领域技术人员将理解,制剂中的酸的量可能有所变化,当然,该变化取决于所选择的特定酸、酸的摩尔浓度、酸的当量浓度和/或外消旋苏木精制剂中其他组分的存在。在一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.05%至约15%的范围内。在其他实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.05%至约12%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.1%至约10%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.1%至约7.5%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.1%至约6%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.1%至约5%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.1%至约4%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.2%至约4%的范围内。
[0102]
在其他实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约12%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约10%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约7.5%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约6%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约5%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约0.5%至约4%的范围内。在又一些实施例中,任何ph降低的外消旋苏木精制剂中的酸的量在占制剂的总体积的约1%至约4%的范围内。
[0103]
制备ph降低的外消旋苏木精制剂的方法
[0104]
本公开的一些方面涉及制备ph降低的外消旋苏木精制剂的方法。在一些实施例中,ph降低的外消旋苏木精制剂可以通过降低外消旋苏木精制剂(例如本文公开的外消旋苏木精制剂中的任何外消旋苏木精制剂;或包含外消旋苏木精和至少一种其他添加剂的任何苏木精制剂,该至少一种其他添加剂包括上述添加剂中的任何添加剂)的ph值来进行配制。
[0105]
一般来说,可以通过向外消旋苏木精制剂添加酸(例如强酸)来降低外消旋苏木精溶液的ph值。在一些实施例中,酸为强酸。在一些实施例中,强酸选自盐酸、硫酸、高氯酸、硝酸或它们的混合物。在其他实施例中,强酸为盐酸。在一些实施例中,强酸为1m盐酸。在其他实施例中,强酸为0.5m盐酸。在其他实施例中,强酸为0.5m硫酸。在又一些实施例中,强酸为0.25m硫酸。当然,本领域技术人员将能够选择任何酸,该酸允许外消旋苏木精制剂达到预定ph值。
[0106]
在一些实施例中,可以向外消旋苏木精或外消旋苏木精制剂添加酸化溶液,以提供ph降低的外消旋苏木精制剂。在一些实施例中,酸化溶液包含酸碱和一种或多种添加剂。在一些实施例中,酸化溶液的该一种或多种添加剂选自稳定剂、媒染剂、氧化剂、保质期延长剂和抗氧化剂中的一者或多者。酸化溶液的添加剂可以按照本文所述的外消旋苏木精制剂的如本文所述相同数量或比率来呈现。
[0107]
本领域技术人员将理解,添加至外消旋苏木精或外消旋苏木精制剂的酸和/或缓冲剂的量可能有所变化,当然,该变化取决于所选择的特定酸、酸的摩尔浓度、酸的当量浓度和/或起始外消旋苏木精制剂中其他组分的存在。
[0108]
在一些实施例中,添加一定量的酸(酸化溶液),使得外消旋苏木精溶液或外消旋苏木精制剂的ph值降低介于约2%至约20%之间,即,外消旋苏木精溶液或外消旋苏木精制剂的初始ph值降低介于约2%至约20%之间,以提供ph值相对较低的ph降低的外消旋苏木精溶液或ph降低的外消旋苏木精制剂。在其他实施例中,添加一定量的酸,使得外消旋苏木精溶液或外消旋苏木精制剂的ph值降低介于约2.5%至约15%之间。在又一些实施例中,添加一定量的酸,使得外消旋苏木精溶液或外消旋苏木精制剂的ph值降低介于约3%至约12.5%之间。在又一些实施例中,添加一定量的酸,使得外消旋苏木精溶液或外消旋苏木精制剂的ph值降低介于约4%至约12%之间。在又一些实施例中,添加一定量的酸,使得外消旋苏木精溶液或外消旋苏木精制剂的ph值降低介于约5%至约10%之间。
[0109]
在一些实施例中,在添加酸(或酸化溶液)后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化(即ph值的降低)为约0.25(即,降低约0.25个ph单位)。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.225。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.2。在一些实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.175。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.15。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.125。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.1。在其他实施例中,在添加酸后,外消旋苏木精溶液或外消旋苏木精制剂的ph值的变化为约0.075。
[0110]
在一些实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸(或
酸化溶液),使制剂的ph值降低至低于约2.4。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.35。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.3。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.25。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.2。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.15。在其他实施例中,向外消旋苏木精溶液或外消旋苏木精制剂添加一定量的酸,使制剂的ph值降低至低于约2.1。
[0111]
本领域技术人员将能够添加适量的酸(或酸化溶液)以降低外消旋苏木精溶液或外消旋苏木精制剂的ph值,无论所选择的起始苏木精溶液的性质如何。
[0112]
重新调整ph降低的外消旋苏木精制剂的ph值的方法
[0113]
本发明的一些方面涉及重新调整ph降低的外消旋苏木精制剂的ph值,以提供适用于染色的ph经调整的外消旋苏木精制剂。在一些实施例中,该方法包括向ph降低的外消旋苏木精制剂添加重新调整溶液。在一些实施例中,重新调整溶液包含溶剂以及强碱和/或缓冲剂中的一者。在一些实施例中,溶剂选自本文所述的溶剂。在一些实施例中,在ph降低的外消旋苏木精制剂和重新调整溶液中使用相同的溶剂。
[0114]
在一些实施例中,强碱选自由以下项组成的组:氢氧化钠、氢氧化钾、氢氧化锂。在其他实施例中,碱为氨。在一些实施例中,并且强碱为1m氢氧化钠。在其他实施例中,强碱为0.5m氢氧化钠。在又一些实施例中,强碱为0.1m氢氧化钠。
[0115]
在一些实施例中,缓冲剂选自马来酸盐、磷酸盐、甘氨酸、柠檬酸盐、甘氨酰甘氨酸、苹果酸盐、甲酸盐、氰基乙酸盐、琥珀酸盐、乙酸盐、丙酸盐、富马酸盐、硫酸盐、丙氨酸、精氨酸、异亮氨酸、亮氨酸、正亮氨酸、脯氨酸、丝氨酸、苏氨酸或它们的任何组合。在一些实施例中,缓冲剂的弱酸的pka在约1.5至约3.5的范围内。在其他实施例中,缓冲剂的弱酸的pka在约1.8至约3.2的范围内。在又一些实施例中,缓冲剂的弱酸的pka在约2至约3的范围内。
[0116]
在一些实施例中,重新调整溶液进一步包含选自由以下项组成的组的添加剂:媒染剂、氧化剂、保质期延长剂和抗氧化剂。
[0117]
在一些实施例中,向ph降低的外消旋苏木精制剂添加足量的强碱、缓冲溶液或重新调整溶液,使得ph降低的外消旋苏木精制剂的ph值提高至至少约2.4。在其他实施例中,向ph降低的外消旋苏木精制剂添加一定量的强碱、缓冲溶液或重新调整溶液,使得ph值提高至至少约2.45。在又一些实施例中,向ph降低的外消旋苏木精制剂添加一定量的强碱、缓冲溶液或重新调整溶液,使得ph值提高至至少约2.5。在又一些实施例中,向ph降低的外消旋苏木精制剂添加一定量的强碱、缓冲溶液或重新调整溶液,使得ph值提高至至少约2.55。
[0118]
在一些实施例中,该方法包括:测量ph降低的外消旋苏木精制剂的等分试样的初始ph值,以及添加一定量的强碱、缓冲溶液或重新调整溶液,直至等分试样的ph值提高至至少约2.4。在一些实施例中,该方法包括:测量ph降低的外消旋苏木精制剂的等分试样的初始ph值,以及添加一定量的强碱、缓冲溶液或重新调整溶液,直至等分试样的ph值提高至至少约2.45。在一些实施例中,该方法包括:测量ph降低的外消旋苏木精制剂的等分试样的初始ph值,以及添加一定量的强碱、缓冲溶液或重新调整溶液,直至等分试样的ph值提高至至
少约2.5。在一些实施例中,该方法包括:测量ph降低的外消旋苏木精制剂的等分试样的初始ph值,以及添加一定量的强碱、缓冲溶液或重新调整溶液,直至等分试样的ph值提高至至少约2.55。
[0119]
用于苏木精染色的系统
[0120]
在一些实施例中,本文所述的外消旋苏木精制剂被手动应用或引入生物学样品,或使用浸泡技术来进行应用。在其他实施例中,外消旋苏木精制剂例如通过自动化染色设备被应用或分配至生物学样品。本领域技术人员将理解,任何外消旋苏木精制剂的分配是指将该外消旋苏木精制剂施加到生物学样品或基底(例如载玻片)。
[0121]
本文所公开的方法和制剂可以适于与现有的自动化处理系统一起使用。例如,ventana medical systems,inc.是公开用于执行自动分析的系统和方法的多项美国专利的受让人,包括美国专利号:5,650,327、5,654,200、6,296,809、6,352,861、6,827,901和6,943,029,以及美国公开申请号:20030211630和20040052685,其各自以引用方式并入本文。这些系统可以适于与本发明兼容。简而言之,前述应用中描述的自动化载玻片处理系统为高容量载玻片处理系统,该系统在对载玻片执行各种载玻片处理操作的工作站之间,穿梭运输将多个载玻片保持在基本上水平的位置(以将交叉污染最小化)的托盘。在处理过程中,新鲜的试剂可以被施加到每个载玻片,并且载玻片与试剂的交叉污染可以基本上被消除,因为载玻片在托盘中以间隔的方式被分别进行处理。在一种配置中,系统包括辐射加热器、脱石蜡器/染色器/溶剂交换器组合工作站、对流烤箱和盖玻片器。承载石蜡包埋的组织样品的载玻片的托盘可以在系统的辐射加热器下加热,以使样品中的石蜡扩散以用于使其更容易地去除,并且也将样品粘附至载玻片。然后可以将托盘输送至多功能脱石蜡器/染色器/溶剂交换器工作站,在此处可以对载玻片进行脱石蜡、染色和溶剂交换。可以将准备好覆盖盖玻片的经染色的载玻片的托盘穿梭运输至系统的盖玻片器,在此处将盖玻片添加至载玻片。一旦载玻片被覆盖盖玻片,则可以将托盘输送至对流烤箱,以固化经染色的载玻片上的盖玻片。刚刚描述的高容量染色器可以从ventana medical systems,inc,tucson,ariz商购获得。
[0122]
其他市售样本处理系统(可以通过该市售样本处理系统来应用本文所述溶液和制剂)的示例包括:ventana symphony(单独载玻片染色器)和ventana he 600(单独载玻片染色器)系列,以及来自agilent technologies的dako coverstainer(批量染色器);来自leica biosystems nussloch gmbh的leica st4020小型线性染色器(批量染色器)、leica st5020多级染色器(批量染色器)和leica st5010自动化染色器xl系列(批量染色器)h&e染色器。
[0123]
在一些实施例中,虽然上述染色系统可以配置为执行任何组织学染色过程,但示例性苏木精和曙红染色方案包括:烘烤步骤,该烘烤步骤用于将样品粘附至载玻片;脱石蜡步骤,该脱石蜡步骤用于从石蜡包埋的样品中去除石蜡;苏木精染色步骤(可以利用所公开的苏木精制剂);蓝化步骤,该蓝化步骤提高ph值并且使苏木精变为蓝色,以提供更好的与下游添加的曙红的对比;曙红染色步骤;分化步骤,该分化步骤用于去除过量的曙红并且使曙红变为红色至粉色的各种色度;脱水步骤,该脱水步骤用于使用无水乙醇来从样品中去除水;将载玻片暴露于高温和气流以去除烃的步骤;覆盖盖玻片步骤,在该步骤中将d-柠檬烯分配至样品;以及固化步骤。
[0124]
在其他实施例中,虽然上述染色系统可以配置为执行任何组织学染色过程,但示例性苏木精和曙红染色方案包括:烘烤步骤,该烘烤步骤用于将样品粘附至载玻片;脱石蜡步骤,该脱石蜡步骤用于从石蜡包埋的样品中去除石蜡;苏木精染色步骤(可以利用所公开的苏木精制剂);蓝化步骤,该蓝化步骤提高ph值并且使苏木精变为蓝色,以提供更好的与下游添加的曙红的对比;曙红染色步骤;分化步骤,该分化步骤用于去除过量的曙红并且使曙红变为红色至粉色的各种色度;脱水步骤,该脱水步骤用于使用乙二醇醚(例如二丙二醇丙醚)来从样品中去除水分;将载玻片暴露于高温和气流以去除烃的步骤;覆盖盖玻片步骤,在该步骤中将d-柠檬烯分配至样品;以及固化步骤。
[0125]
在一些实施例中,和自动化染色系统包括包含外消旋苏木精制剂的一个或多个储存器、容器和/或分配器。在其他实施例中,自动化染色系统包括单独的储存器或容器,该存储器或容器含有单独的ph降低的苏木精制剂和重新调整溶液。在一些实施例中,系统进一步包括分配系统,该分配系统将外消旋苏木精制剂(在重新调整ph降低的外消旋苏木精制剂后)和任何其他溶液递送至生物学样品,例如安装在载玻片上的生物学样品。在一些实施例中,ph降低的外消旋苏木精制剂和/或其他溶液(例如重新调整溶液)在施加到生物学样品之前被合并。在一些实施例中,ph降低的外消旋苏木精制剂的容器和另一种溶液(例如重新调整溶液)的容器被加压并且流体地连接至混合容器。混合容器可以为能够容纳或输送混合溶液的任何容器,诸如刚性或柔性管。在一些实施例中,混合容器为流体地连接至分配器的管。在一些实施例中,ph降低的外消旋苏木精制剂和重新调整溶液经由管件来流体地连接至t型接头。来自t型接头的输出继而流体地连接至分配器。在这些实施例中,ph降低的外消旋苏木精制剂和重新调整溶液进料至t型接头,并且溶液的混合发生在从t型接头引出的管道中。在一些实施例中,将ph降低的外消旋苏木精制剂和重新调整溶液分别分配至生物学样品上。在这些实施例中,可以允许溶液通过在样品上扩散来进行混合,或该溶液可以例如通过用移液管搅拌来进行机械混合。
[0126]
在一些实施例中,自动化样本处理设备可以包括圆盘传送带,该圆盘传送带用于保持多个基底,例如显微镜载玻片,其中每个基底包括待染色的生物学样品。在一些实施例中,自动化染色设备还可以包括:用于以预定速度旋转圆盘传送带的装置;以及用于在圆盘传送带旋转过程中,引导并控制将试剂(包括本文所述的溶液和制剂)施加至基底和样品上的机构。在一些实施例中,一旦载玻片被装载至仪器,则测试方案将决定在特定时间哪些流体被分配至基底上。在适当的时间,在一些实施例中,分配器支架将旋转以在基底上方对齐正确的流体,并且仪器将预定量的流体分配至基底上。在一些实施例中,仪器将允许流体与生物学样品保持接触,持续预定量的时间。
[0127]
在一些实施例中,该系统为自动化载玻片处理系统,其包括:载玻片托盘,该载玻片托盘将多个载玻片保持在基本上水平的位置(例如呈两排,其中载玻片保持在与水平面介于约0.2度与约1.2度之间的角度);以及一个或多个工作站(例如,呈竖直堆叠排列),该一个或多个工作站接收载玻片托盘,并且对载玻片托盘中的载玻片执行一个或多个载玻片处理操作。在一些实施例中,工作站可以对载玻片托盘中的一个或多个单独的载玻片(例如,载玻片托盘中的至少两个或四个载玻片)执行载玻片处理操作,或者它可以同时对载玻片托盘中的所有载玻片执行载玻片处理操作。在一些实施例中,该一个或多个工作站将试剂分配至载玻片托盘中的载玻片,而与第一载玻片接触的大量试剂不会与第二载玻片接
触,从而使载玻片之间的交叉污染最小化。此类工作站可以包括一个或多个定向喷嘴,该一个或多个定向喷嘴将试剂分配至载玻片上,例如,该一个或多个定向喷嘴可以包括跨载玻片的表面在相反方向上分配试剂的一对定向喷嘴。在更特定的实施例中,该一个或多个定向喷嘴可以进一步包括定向喷嘴,该定向喷嘴朝向载玻片的底部表面分配试剂。在其他特定实施例中,该一个或多个工作站可以同时将试剂(例如,相同试剂)分配至保持在给定工作站内载玻片托盘中的至少两个载玻片,或者该一个或多个工作站可以同时将试剂(例如相同试剂)分配至保持在给定工作站内载玻片托盘中的所有载玻片。附加的系统部件和托盘配置(以及控制系统)在美国专利号8,663,991、7,468,161和9,528,918中有所描述,这些专利的公开内容据此以引用方式整体并入本文。
[0128]
在一些实施例中,本公开提供了一种用于自动处理生物样本的设备,该设备包括:至少一个载玻片托盘,该至少一个载玻片托盘将多个载玻片保持在基本上水平的位置,其中所述生物样本位于所述载玻片上;一个或多个工作站,该一个或多个工作站接收所述载玻片托盘,并且对保持在所述载玻片托盘中的所述多个载玻片执行一个或多个载玻片处理操作;运输器,该运输器将所述载玻片托盘移入和移出所述一个或多个工作站;流控模块,该流控模块与所述一个或多个工作站流体连通,该流控模块向所述一个或多个工作站供应试剂;气动模块,该气动模块与所述一个或多个工作站和所述流控模块流体连通;其中所述气动模块向所述一个或多个工作站和所述流控模块提供真空和/或加压气体;以及控制模块,该控制模块与所述运输器、所述一个或多个工作站、所述流控模块和所述气动模块电连通,其中所述控制模块在处理所述生物样本期间协调设备的部件的功能。该设备可以适于递送本文所述的溶液和/或制剂中的一者或多者。
[0129]
复染剂
[0130]
在一些实施例中,该系统和方法进一步包括用附加染色剂(例如复染剂)对生物学样品进行染色。在一些实施例中,样品与复染剂的接触包括使样品与以下项中的一者或多者接触:曙红y(cas号15086-94-9)、橙黄g(cas号1936-15-8)、亮绿sf淡黄(cas号5141-20-8)、俾斯麦棕(cas号:8005-77-4)、固绿fcf(cas号2353-45-9)、og-6(包括橙黄g)、ea25(包括亮绿sf、俾斯麦棕和曙红y)、ea36(包括亮绿sf、俾斯麦棕和曙红y)、ea50(包括亮绿sf、俾斯麦棕和曙红y)以及ea65(包括亮绿sf、俾斯麦棕和曙红y)。例如,可以在例如以下资料中找到制备此类复染剂的配方和方法:stainsfile(由bryan llewellyn维护的针对组织技术学家的互联网资源);kiernan,“histological and histochemical methods:theory andpractice,”第3版,butterworthheinemann,oxford,uk;以及horobin和kiernan,"conn's biological stains:a handbook of dyes,stains and fluorochromes for us in biology and medicine,"第10版,oxford:bios,isbn 1859960995,2002。在其他实施例中,样品与苏木精制剂的接触包括进行性苏木精染色方案。在其他实施例中,样品与苏木精制剂的接触包括退行性苏木精染色方案。该方法可以为自动化的,并且可以在支持在基底(例如显微镜载玻片)上的生物学样品上执行。在特定实施例中,该方法用于对组织切片或安装在显微镜载玻片上的细胞学样品进行染色。在进一步包括复染步骤的特定实施例中,该方法可以为苏木精和曙红染色法或pap染色法,并且更具体地,为自动化苏木精和曙红或pap染色法。
[0131]
可以与本发明的染色程序协同使用的其他组织学染色剂包括染料,诸如吖啶染
and practice,”第3版,butterworth heinemann,oxford,uk;以及horobin和kiernan,"conn's biological stains:a handbook of dyes,stains and fluorochromes for us in biology and medicine,"第10版,oxford:bios,isbn 1859960995,2002。上文紧接着引用的两份绑定参考文献的内容以引用方式并入本文。
[0132]
实例
[0133]
实例1
–
使用外消旋苏木精制剂来进行组织染色
[0134]
介绍
[0135]
制备了两个单独批次的ventana he 600苏木精溶液,并且通过hplc分析和功能性染色对其进行了评估。一批由市售苏木精制备;而另一批由外消旋苏木精制备(例如,根据本文实例2所述的半合成来进行制备)。通过功能性测试(h&e染色)和hplc分析对两种溶液进行评估,并且发现两种溶液基本上等同。
[0136]
试剂
[0137]
(1)edta/酚红稀释溶液
[0138]
向瓶子添加1l市售0.02m edta溶液。
[0139]
添加0.01g酚红,钠盐指示剂染料。
[0140]
进行混合直至染料溶解。
[0141]
(2)25mm甲酸铵流动相缓冲溶液(ph=4,水)
[0142]
向瓶子添加约1l去离子(di)水。
[0143]
添加1.0ml的99重量%的甲酸。
[0144]
添加1.3ml的约29重量%的氨水溶液,并且打旋以进行混合。
[0145]
(3)乙腈(hplc级)
[0146]
(4)ms检测器稀释剂
[0147]
向5l的瓶子添加500ml的hplc级乙腈。
[0148]
用di水使其体积达到5l。
[0149]
添加1ml的99重量%的甲酸。
[0150]
倒置若干次以进行混合。
[0151]
(5)苏木精(商业)
[0152]
(6)苏木精(外消旋)
[0153]
(7)乙二醇
[0154]
(8)碘酸钠
[0155]
(9)硫酸铝水合物
[0156]
(10)对苯二酚
[0157]
(11)β-环糊精水合物
[0158]
样品制备
[0159]
根据he 600苏木精显影配方方法制备ventana he 600苏木精溶液的两个样品,该方法如下:
[0160]
向容器添加65ml的di水。
[0161]
开始适度搅拌。
[0162]
添加28g乙二醇。
[0163]
添加0.61g苏木精。
[0164]
适度搅拌30至120分钟。
[0165]
添加0.065g的碘酸钠。
[0166]
在添加碘酸钠的10分钟内,添加2.7g硫酸铝水合物。
[0167]
适度搅拌30至120分钟。
[0168]
添加0.93g对苯二酚。
[0169]
添加1.1g的β-环糊精。
[0170]
用di水使其体积达到100ml。
[0171]
适度搅拌30至120分钟。
[0172]
最终溶液的ph值应当介于2.45与2.54之间。
[0173]
分析方法
[0174]
每种he 600苏木精溶液在以下条件下由hplc进行分析:
[0175]
样品制备:用edta/酚红稀释溶液将20μl样品稀释至1ml
[0176]
仪器:waters alliance e2695分离模块
[0177]
运行时间:30分钟
[0178]
注射体积:20μl
[0179]
流速:1ml/分钟
[0180]
柱id:waters xbridge c18
[0181]
柱长度:150mm
[0182]
柱直径:4.6mm
[0183]
粒径:3.5μm
[0184]
流动相a:25mm甲酸铵缓冲剂,ph=4
[0185]
流动相b:乙腈
[0186]
柱温:40℃
[0187]
uv-vis检测器:waters 2998光电二极管阵列
[0188]
ms检测器:waters qda质量检测器
[0189]
结果
[0190]
两种溶液的色谱图(图1a和2a)示出了类似的定性反应(也参见图1b和2b)。对苯二酚、羟基氧化苏木精、苏木精和氧化苏木精的主峰均出现在两张色谱图中。两张色谱图中均出现了相同的未识别的小峰。用每个样品分析了内标,从中获得了定量结果。除苏木精水平之外,两种溶液内的所有组分均示出了几乎相等的水平。与用商业苏木精制备的样品相比,外消旋苏木精制剂示出了约1.5倍的苏木精水平。两个色谱图的结果汇编在表1中。
[0191][0192][0193]
功能性染色
[0194]
使用由外消旋苏木精和商业苏木精制备的制剂,在ventana he 600仪器上对八对
5合1组织载玻片用苏木精和曙红(h&e)染色剂进行染色。观察到的染色结果的唯一显著差异是,由商业苏木精制备的溶液(参见例如图3a和3b)示出了比由外消旋苏木精制备的溶液(例如,参见图4a和4b)略强的粘蛋白染色。
[0195]
讨论
[0196]
外消旋苏木精溶液和商业苏木精溶液产生的hplc色谱图具有类似的定性结果,这表明在配制过程中两种苏木精来源由碘酸钠氧化,以形成氧化苏木精和羟基氧化苏木精。外消旋苏木精似乎在化学反应上等同于商业苏木精。
[0197]
外消旋苏木精色谱图中示出的苏木精浓度较高,这表明该苏木精来源可能比商业来源更纯。在两种不同的溶液中,苏木精的氧化产物(羟基氧化苏木精和氧化苏木精)为等同的。如果碘酸钠(氧化剂)为制剂中的限制试剂,并且外消旋苏木精的苏木精起始浓度较高(纯度较高),则在两种溶液的氧化完成后,它们的氧化产物的水平将相等,但外消旋苏木精溶液的未氧化苏木精的剩余水平将较高。
[0198]
关于在ventana he 600仪器上进行h&e染色,等同的苏木精溶液经常在染色中示出少量但显著的差异。这些差异是由于与ventana he 600仪器上的染色过程相关联的变化所导致的。因为外消旋苏木精和商业苏木精在染色方面仅示出轻微差异(粘蛋白染色),所以不能说这些溶液染色不同。
[0199]
该示例中描述的测试表明,通过分析和功能,外消旋苏木精和商业来源的苏木精表现相当。
[0200]
实例2-外消旋苏木精的半合成
[0201]
1.1一般方法
[0202]
所有反应采用标准schlenk技术在惰性气体(n2或氩气)的正压下磁力搅拌和进行。玻璃器皿在使用前在620℃真空下反复干燥。液体试剂和溶剂借助注射器或烘干的不锈钢套管通过橡胶隔片进行添加。固体在惰性气体逆流下进行添加或将其溶解在合适的溶剂中。低温反应在装有以下冷却剂的杜瓦瓶中进行:丙酮/干冰(-78℃)或h2o/冰(0℃)。高于室温的反应温度在加热的油浴中进行。如果遵循文献已知的程序,则将相应的参考添加到实验细节中。如果没有另外说明,则产率是指分离的均质和光谱纯材料。
[0203]
1.1.1溶剂和试剂:干溶剂,诸如丙酮、四氢呋喃(thf)、乙酸乙酯和甲苯均购自商业供应商,并且按原样使用。用于萃取和快速柱色谱的溶剂以hplc等级购买。6s,11r-苏木精(1)购自sigma-aldrich。所有其他试剂和溶剂均购自化学品供应商(sigma-aldrich(西格玛奥德里奇)、acros有机物、阿法埃莎、tci欧洲、abcr)并按原样使用。
[0204]
1.1.2色谱法:在来自merckkgaa的硅胶f254 tlc板上通过定性薄层色谱法(tlc)来监测反应和色谱级分。玻璃板上的分析物通过以下方式观察:用uv光照射和/或通过将tlc板浸泡在适当的染色溶液中然后用热风枪加热(350℃)。应用以下染色溶液:
[0205]
kmno4染色溶液(3.0g kmno4、20g k2co3、5.0ml的5.0重量%naoh水溶液、0.3lh2o)。
[0206]
在来自merck kgaa的si60(40μm至63μm)硅胶上执行快速柱色谱法。所有含有所需基底的级分被合并,并且在减压下去除溶剂,然后真空干燥(10-2
mbar)。
[0207]
1.1.3核磁共振光谱:nmr光谱是在配备了onenmr探针的安捷伦400-mr dd2400 mhz光谱仪上进行测量的,该探头在400mhz下运行,用于质子核(100mhz用于碳核)。dmso-d6和cdcl3购自西格玛奥德里奇。1h的nmr位移以ppm为单位进行报告,与tms的残余位移有关。
将1h的nmr位移校准到残余溶剂共振:dmso-d6(2.50ppm)以及cdcl3(7.26ppm)。将
13
c nmr位移校准到残余溶剂共振的多重信号的中心:dmso-d6(29.84ppm)以及cdcl3(77.16ppm)。1h的nmr光谱数据报告如下:以ppm为单位的化学位移(多重性、耦合常数j、积分强度)。多重性缩写为s(单峰)、br(宽信号)、d(双重峰)、t(三重峰)、q(四重峰)、m(多重峰)和mc(中心对称多重峰)。在组合多重性的情况下,首先表述具有较小耦合常数的多重性。除多重峰外,所有信号,以及除中心对称多重峰外的化学位移被报告为共振范围的中心。除了1h和
13
c nmr测量,2d nmr技术(如同核相关光谱法(cosy)、异核单量子相干(hsqc)和异核多键相干(hmbc))用于分配信号。耦合常数j以hz为单位进行报告。使用来自化学新技术开发公司的acd/spectrus处理器2015.2.7程序来分析所有nmr光谱。
[0208]
1.1.4质谱:低分辨率质谱(lrms)记录在来自waters gmbh(沃特斯股份有限公司)的hplc-ms系统(2695分离模块,996光电二极管阵列检测器,micromasszq,grace vydac 218tp c185u)上,该系统通过waters(沃特斯)masslynx v4.1进行计算机控制。每种分析物仅表明特征分子片段或分子离子峰。
[0209]
1.2合成路线
[0210][0211]
方案1:用于外消旋-苏木精(6)的合成路线,从市售的天然6s,11r-苏木精(1)开始。
[0212]
1.3合成程序
[0213][0214]
将苄基醚2:6s,11r-苏木精(1,1.00g,3.31mmol,1.00当量)和k2co3(2.05g,14.9mmol,4.50当量)于惰气气氛下在室温下溶解在无水丙酮(33ml)中。然后,一次性添加苄基溴(1.77ml,14.9mmol,4.50当量),并且剧烈搅拌所得混合物,并加热至56℃(油浴温
度)持续20小时。当tlc分析表明物质1完全转化时,将反应冷却到室温,并且经由添加乙酸乙酯(150ml)和盐水(100ml)的经搅拌的混合物来进行淬灭。分离各层,并用乙酸乙酯(75ml,2次)萃取水相。将合并的有机层经na2so4干燥,过滤,并且真空浓缩。经由快速柱色谱法(二氧化硅,n-hex:etoac=80:20梯度至60:40)来实现粗制苄基醚2的最终纯化,从而得到6s,11r-四苄基-苏木精(2,2.01g,3.03mmol,92%),其为淡黄色固体。
[0215]
rf(n-hex:etoac=2:3)=0.60。
[0216]1hnmr(cdcl3,400mhz):δ=7.46
–
7.27(m,20h),6.92(dd,j=1.00,8.66hz,1h),6.87(d,j=1.00,1h),6.80(s,1h),6.69(d,j=8.78hz,1h),5.15(s,2h),5.11(s,2h),5.08(s,2h),5.08(s,2h),4.04(s,1h),4.01(dd,j=1.38,11.29hz,1h),3.72(d,j=11.04hz,1h),3.17(d,j=16.19hz,1h),2.84(d,j=15.43hz,1h),2.31(s,1h)ppm。
[0217]
13
cnmr(cdcl3,100mhz):δ=151.6,149.1,148.5,148.0,137.8,137.5,137.4,137.4,137.2,137.0,132.0,128.9,128.7,128.6,128.6,128.2,128.0,127.9,127.7,127.5,127.4,125.0,116.9,112.5,112.4,108.4,77.52,75.3,72.2,71.8,71.5,70.4,50.7,41.2ppm。
[0218]
用于c
44h39o6+
[mh
+
]的esi-lrms:计算。663.3
[0219]
发现值663.4.
[0220][0221]
将一硫代碳酸酯3:6s,11r-四苄基-苏木精(2,0.50g,0.75mmol,1.00当量)于惰气气氛下在室温下溶解在无水thf(10.0ml)中,并且随后冷却至-78℃。然后,向经搅拌的溶液滴加甲基锂(0.59ml,0.94mmol,1.25当量)。在室温下搅拌30分钟后,再次将反应冷却至-78℃,并且滴加o-硫代氯甲酸苯酯(0.13ml,0.94mmol,1.25当量)。将所得混合物在室温下搅拌两小时,此后tlc分析表明醚2完全转化。该反应经由添加二氯甲烷(100ml)和饱和nahco3水溶液(75ml)的经搅拌的混合物来进行淬灭。分离各层,并用乙酸乙酯(75ml,2次)萃取水相。将合并的有机层经na2so4干燥,过滤,并且真空浓缩(最高30℃)。经由快速柱色谱法(二氧化硅,n-hex:etoac=95:5梯度至85:15)来实现粗制一硫代碳酸酯3的最终纯化,从而得到6s,11r-四苄基-苏木精-o-苯基-一硫代碳酸酯(3,0.53g,0.66mmol,87%),其为淡黄色泡沫。
[0222]
rf(n-hex:etoac=2:1)=0.75。
[0223]1hnmr(cdcl3,400mhz):δ=7.46
–
7.25(m,23h),7.10
–
7.08(m,2h),6.96(d,j=1.00,8.66hz,1h),6.89(s,1h),6.82(s,1h),6.71(d,j=8.66hz,1h),5.36(dd,j=1.76,12.92hz,1h),5.15(s,2h),5.13(s,2h),5.09(m,2h),4.60(s,1h),3.75
–
3.70(m,2h),3.59(d,j=16.94hz,1h)ppm。
[0224]
13
cnmr(cdcl3,100mhz):δ=192.2,153.1,151.7,149.3,148.9,148.0,137.8,
137.4,137.4,137.3,137.3,134.9,130.5,129.6,128.7,128.6,128.6,128.6,128.2,128.0,128.0,127.7,127.5,127.4,126.7,124.5,122.1,115.5,112.2,111.8,108.2,89.9,75.3,72.1,71.7,71.5,64.5,49.3,39.2ppm。
[0225]
用于c
51h43
o7s
+
[mh
+
]esi-lrms:计算。799.3
[0226]
发现值799.3.
[0227][0228]
将烯烃4:6s,11r-四苄基-苏木精-o-苯基-一硫代碳酸酯(3,470mg,0.59mmol)于惰气气氛下在室温下溶解在无水甲苯(15.0ml)中。剧烈搅拌反应混合物,并加热至115℃(油浴温度)持续三小时,此后tlc分析表明物质3完全转化。然后将反应冷却至室温并真空浓缩。由此获得的粗制烯烃4经由快速柱色谱法(二氧化硅,n-hex:etoac=95:5梯度至70:30)来进行纯化,从而得到3,4,9,10-四(苄基氧基)-6,7-二氢茚并[2,1-c]色烯(4,308mg,0.48mmol,81%),其为无色固体,其暴露于空气后变为微红色。
[0229]
rf(n-hex:etoac=3:1)=0.50。
[0230]1hnmr(cdcl3,400mhz):δ=7.52
–
7.25(m,22h),7.14(s,1h),6.61(d,j=8.28hz,1h),5.21(s,2h),5.19(s,2h),5.15(s,2h),5.11(s,4h),3.33(s,1h)ppm。
[0231]
13
cnmr(cdcl3,100mhz):δ=152.7,148.2,147.8,147.4,137.9,137.7,137.5,137.4,137.2,137.2,135.3,134.3,131.8,128.8,128.7,128.6,128.6,128.3,128.0,128.0,128.0,127.9,127.7,127.6,127.5,117.8,116.5,112.4,109.4,106.6,75.3,72.7,72.0,71.2,67.2,37.5ppm。
[0232]
用于c
44h37o5+
[mh
+
]的esi-lrms:计算。645.3
[0233]
发现值645.5.
[0234][0235]
外消旋-苄基醚5:烯烃4(200mg,0.31mmol,1.00当量)于惰气气氛下在室温下溶解在无水thf(5.0ml)中,并且随后冷却至0℃至4℃。然后,在搅拌下缓慢添加硼烷四氢呋喃复合物(0.62ml,1m在thf中,0.62mmol,2.00当量)。将所得混合物在室温下搅拌4小时,此后tlc分析表明物质4完全消耗。然后,缓慢添加无水乙醇(1.00ml)(注意:h2释放!)并且再继续搅拌10分钟。此后,添加氢氧化钠水溶液(3m,2.0ml)和过氧化氢(30重量%,0.8ml),并且将反应再剧烈搅拌90分钟。用二氯甲烷(75ml)和水(50ml)稀释后,分离各层,并且用二氯甲
烷(50ml,2次)萃取水相。将合并的有机层用盐水(50ml)洗涤,经na2so4干燥,过滤并且真空浓缩。经由快速柱色谱法(二氧化硅,n-hex:etoac=80:20梯度至60:40)来实现粗制外消旋-苄基醚5的最终纯化,从而得到外消旋-四苄基-苏木精(5,194mg,0.29mmol,94%),其为橙色泡沫。
[0236]
rf(n-hex:etoac=2:3)=0.60。
[0237]1hnmr(dmso-d6,400mhz):δ=7.46
–
7.27(m,20h),7.11
–
7.08(s,2h),6.93(s,1h),6.74(d,j=8.78hz,1h),5.14
–
5-04(m,6h),4.91(dd,j=1.13,11.67hz,2h),3.97(s,1h),3.90(d,j=11.29hz,1h),3.76(d,j=11.04hz,1h),2.90(s,2h)ppm。
[0238]1hnmr(cdcl3,400mhz),
13
cnmr(cdcl3,100mhz):δ=数据与用于化合物2的所记录的数据相匹配。
[0239]
用于c
44h39o6+
[mh
+
]的esi-lrms:计算。663.3
[0240]
发现值663.4.
[0241][0242]
外消旋-苏木精6
[1
–
3]
:外消旋-四苄基-苏木精(5,600mg,0.91mmol,1.00当量)于惰气气氛下在室温下溶解在无水、脱气的乙酸乙酯(5.0ml)中。向其中添加钯/碳(96.3mg,10重量%pd,0.09mmol,0.10当量pd),并且经由抽真空和回填来用氢气交换大气(循环3次)。将所得混合物剧烈搅拌两天,此后tlc分析表明完全转化为物质6。随后,将悬浮液经脱气硅藻土塞过滤(脱气乙酸乙酯洗涤),并且在惰气气氛下真空浓缩。将所得橙色玻璃状固体(250mg)从脱气的水中结晶,以产生外消旋-苏木精(6,187mg,0.62mmol,68%),其为淡黄色、棕色固体。
[0243]
rf(n-hex:etoac=2:3)=0.10。
[0244]1hnmr(dmso-d6,400mhz):δ=8.57(s,br,3h),8.21(s,br,1h),6.64
–
6.61(m,2h),6.53(s,1h),6.42(d,j=9.54hz,1h),5.27(s,br,1h),3.92
–
3.86(m,2h),3.59(d,j=10.29hz,1h),2.88(d,j=15.43hz,1h),2.72(d,j=15.31hz,1h)ppm。
[0245]
13
cnmr(dmso-d6,100mhz):δ=144.2,144.0,143.9,142.5,135.6,133.2,129.7,119.3,115.2,112.0,111.7,108.7,76.3,69.7,49.9,42.0ppm。用于c
16h13o6-[(m-h)
–
]的esi-lrms:计算。301.1
[0246]
发现值301.3.
[0247]
实例3
–
合成苏木精的等效性分析
[0248]
目前,由少数商业生产商从洋苏木树的心材中萃取苏木精。该产物在不同批次和不同制造之间的杂质水平以及苏木精与氧化苏木精的比率均有所不同。这些因素表明,合成苏木精可以提供更一致且更有潜力的优异替代品,以替代目前由商业生产商提供的天然产物。
[0249]
针对购自abbeycolor,inc.的商业苏木精(批号7740)评估了合成苏木精的染色性能。按照由ottodann和hanshofman,"diesynthesevon(+/-)-hamatoxylin,chromane(xvii),1965,第1498至1504页所述的程序来生产外消旋合成苏木精。评估了含有苏木精的整套ventana产物的染色性能。染色剂包括弹性nf苏木精、he600苏木精、三色苏木精、粘蛋白卡红铁苏木精、苏木精i和苏木精ii。对于每种所评估的染色剂,用合成苏木精和商业苏木精来制备制剂。使用16对分析(每对32个载玻片)来测量等效性。所有测试载玻片均由合格的读取器来进行分析。
[0250]
一般来说,合成苏木精性能相当于或优于天然产物。在hemii中使用合成制剂的所有载玻片均非常出色,其中核染色质细节通常优于使用天然产物的制剂。在其中测试了合成制剂的所有特殊染色剂均相当于或优于天然制剂。
[0251]
材料和方法
[0252]
根据ventanamf09186212001,revc制备弹性nf苏木精。根据ventanamf07283270001,revm制备he600苏木精。根据ventanamf06518168001,revf制备三色苏木精a。根据以下项制备铁苏木精a:ventanamf75001,revp。在所有情况下,每种制剂均生产了20ml,从而允许每种制剂染色100个载玻片。
[0253]
苏木精i的制备:0.3g
[0254]
材料:
[0255]
水,去离子化
[0256]
乙二醇,part#10547
[0257]
苏木精染料,material#06002960001或合成材料
[0258]
碘酸钠,beantownchemical,catalog#212330-100g
[0259]
硫酸铝,part#10357
[0260]
乙酸,glacial,vwr,product#0714-500ml
[0261]
tween20,sigma,catalog#p-7949
[0262]
程序:
[0263]
将56.25ml水和20.87g乙二醇混合
[0264]
添加0.30g苏木精和36.0mg碘酸钠
[0265]
在室温下搅拌20min
[0266]
添加5.28g硫酸铝和1.5ml乙酸
[0267]
在室温下搅拌1h
[0268]
过滤溶液
[0269]
添加75.0mg的tween20
[0270]
苏木精ii的制备:0.15g
[0271]
材料:
[0272]
水,去离子化
[0273]
乙二醇,part#10547
[0274]
苏木精染料,material#06002960001或合成材料
[0275]
碘酸钠,beantownchemical,catalog#212330-100g
[0276]
硫酸铝,part#10357
[0277]
乙酸,glacial,vwr,product#0714-500ml
[0278]
tween 20,sigma,catalog#p-7949
[0279]
程序:
[0280]
将56.5ml水和20.87g乙二醇混合
[0281]
添加0.15g苏木精和18.0mg碘酸钠
[0282]
在室温下搅拌20min
[0283]
添加1.32g硫酸铝和1.5ml乙酸
[0284]
在室温下搅拌1h
[0285]
过滤溶液
[0286]
添加75.0mg的tween 20
[0287]
备注:溶液在室温下储存,并且在使用前老化48小时。
[0288]
苏木精i稀释液制备和染色
[0289]
(1)使用11.6ml乙酸(p/n 10040)和62.4ml的peg 200(p/n 10068)来制备72ml乙酸/peg 200原液。通过倒置十次来进行混合。
[0290]
(2)用如下列出的量的所需材料来制备一系列的稀释液:
[0291]
向一系列适当大小的容器添加适量的水。
[0292]
添加peg/乙酸原液。
[0293]
添加适当体积的苏木精原材料。
[0294]
通过倒置十次来进混合。
[0295]
稀释液放置在经标记的客户可填充的分配器中,并且标记有通用的复染剂条形码标记。
[0296]
(3)使用合格的symphony mtb(p/n 78t7000),以使用以下测试方案来测试稀释液:
[0297]
选择阴性对照小鼠(ig)p/n 760-2014作为方案中的一抗。选择16分钟的一抗孵育。
[0298]
对于所有苏木精稀释液,选择4分钟的复染剂孵育。
[0299]
选择4分钟的蓝化试剂(p/n 760-2037)孵育。
[0300]
[0301][0302]
苏木精ii稀释液制备和染色
[0303]
1.用如下列出的量的所需材料来制备一系列的稀释液。
[0304]
向一系列适当大小的容器添加适量的水。
[0305]
添加所需量的冰乙酸(p/n 10040)。
[0306]
所需量的聚乙二醇200(p/n 10068)。
[0307]
添加所需量的内部苏木精ii复染剂。
[0308]
通过倒置十次来进混合。
[0309]
以下稀释液放置在经标记的客户可填充的分配器中,并且标记有通用的复染剂条形码标记。
[0310]
2.使用合格的symphony mtb(p/n 78t7000),以使用以下测试方案来测试稀释液:
[0311]
选择阴性对照小鼠(ig)p/n 760-2014作为方案中的一抗。选择16分钟的一抗孵育。
[0312]
对于所有苏木精ii稀释液,选择4分钟的复染剂孵育。
[0313]
选择4分钟的蓝化试剂(p/n 760-2037)孵育。
[0314]
[0315][0316]
运行结束后,按照op2100-028和op2100-030对载玻片进行清洁、脱水并且覆盖盖玻片。
[0317]
用合格的读取器来读取载玻片,选择58%的滴度和4分钟的孵育时间以用于标准制剂。
[0318][0319]
结论
[0320]
总的来说,合成苏木精性能相当于或优于天然制剂。合成性能有问题的唯一情况是在hem i制剂中,其中合成制剂似乎给出了甚至更夸张的细胞质染色,与靶标核染色的强度几乎相同。这似乎是制剂的问题,而不是染料本身的问题。
[0321]
如图10至15所示,使用合成he600制剂的载玻片优于天然制剂。使用合成制剂的所有he600载玻片似乎更清晰,并且提供更多的核染色质细节。在hem ii中使用合成制剂的所有载玻片均非常优异,其中核染色质细节通常优于天然制剂。在图7a和7b(结肠)和图8a和8b(肾脏)中,这更加详细变得更明显。在其中测试了合成制剂的所有特殊染色剂均相当于或优于天然制剂。用合成三色苏木精进行染色(图5a和5b)产生了等同于或略好于天然制剂
的染色。在粘蛋白卡红铁苏木精的情况下(图6a和6b),合成制剂产生了具有高得多的对比度的染色,该染色明显优于由天然制剂产生的染色。应当注意,尽管合成苏木精在弹性载玻片上给出了适当的染色模式,但染色明显比用商业苏木精染色的载玻片要浅。这是预料之中的,因为当按照弹性nf苏木精的sop时,合成苏木精未能完全溶解在乙醇中。
[0322]
本说明书中提到的和/或申请数据表中列出的所有美国专利、美国专利申请公开、美国专利申请、国外专利、国外专利申请以及非专利公开均以引用方式整体并入本文。如有必要,可对实施例的各个方面进行修改,从而采用各类专利、申请和公开的概念来提供其他进一步的实施例。
[0323]
尽管已经参照一些说明性实施例描述了本公开,但应当理解,本领域技术人员可以在本公开原则的精神和范围内设计出许多其他的修改和实施例。更具体地,在不违背本公开的精神的情况下,在上述公开、附图和所附权利要求的范围内,所述主题组合排列的组成部分和/或布置可以进行合理的变化和修改。除了在所述组成部分和/或布置中的变化和修改外,对于本领域技术人员来说,替代用途也将是显而易见的。
[0324]
参考文献:
[0325]
[1]ch.bettinger,h.w.zimmermann,hisotchemistry 1991,96,215
–
228.
[0326]
[2]j.a.kiernan,biotechnic&histochemistry 2018,93(2),133
–
148.
[0327]
[3]o.kel,a.f
ü
rstenberg,n.mehanna,c.niclas,b.laleu,m.hammarson,b.albinsson,j.lacour,e.vauthey,chem.eur.j.2013,19,7173
–
7180.
[0328]
[4]r.corradini,s.sforza,t.tedeschi,r.marchelli,chirality 2007,19,269
–
294.
[0329]
[5]y.xu,y.x.zhang,h.sugiyama,t.umano,h.osuga,k.tanaka,j.am.chem.soc.2004,126,6566
–
6567.
[0330]
[6]h.c.becker,b.norden,j.am.chem.soc.2000,122,8344
–
8349.
[0331]
[7]a)k.okamoto,m.noji,t.tashiro,y.kidani,chem.pharm.bull.1981,29,929
–
939;b)k.vickery,a.m.bonin,r.r.fenton,s.omara,m.j.mckeage,p.j.russell,t.w.hambley,j.med.chem.1993,36,3663
–
3668;c)r.r.fenton,w.j.easdale,h.m.er,s.m.omara,m.j.mckeage,p.j.russell,t.w.hambley,j.med.chem.1997,40,1090
–
1098;d)j.malina,j.kasparkova,g.natile,v.brabec,chem.biol.2002,9,629
–
638.
[0332]
[8]a)b.nord
é
n,f.tjerneld,febslett.1976,67,368
–
370;b)j.k.barton,l.a.basile,a.danishefsky,a.alexandrescu,proc.natl.acad.sci.usa 1984,81,1961
–
1965;c)a.sitlani,e.c.long,a.m.pyle,j.k.barton,j.am.chem.soc.1992,114,2303
–
2312;d)c.l.kielkopf,k.e.erkkila,b.p.hudson,j.k.barton,d.c.rees,nat.struct.biol.2000,7,117
–
121.
[0333]
[9]d.l.boger,d.s.johnson,angew.chem.int.ed.1996,35,1438
–
1474.
[0334]
[10]a.h.j.wang,g.ughetto,g.j.quigley,a.rich,biochemistry 1987,26,1152
–
1163.
[0335]
[11]x.qu,j.o.trent,i.fokt,w.priebe,j.b.chaires jb.,proc natlacad sci usa 2000,97,12032
–
12037.
[0336]
[12]a)m.p.singh,b.plouvier,g.c.hill,j.gueck,r.t.pon,j.w.lown,
j.am.chem.soc.1994,116,7006
–
7020;b)j.w.trauger,e.e.baird,p.b.dervan,nature 1996,382,559
–
561;c)c.l.kielkopf,s.white,j.w.szwewczyk,j.m.turner,e.e.baird,p.b.dervan,d.c.rees,science 1998,282,111
–
115;d)d.m.herman,e.e.baird,p.b.dervan,j.am.chem.soc.1998,120,1382
–
1391;e)p.b.dervan,bioorg.med.chem.2001,9,2215
–
2235;f)p.m.reddy,j.w.toprowski,a.l.kahane,t.c.bruice,bioorg.med.chem.lett.2005,15,5531
–
5536.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1