评价对象的评价方法与流程
本发明涉及评价对象的评价方法。
背景技术:
1、在生物学安全性评价中,已知在试验物中加入测试物并观察其变化(例如,颜色变化)。例如,在ames试验中,作为试验物,使用对氨基酸合成基因实施基因操作、改良为无法合成氨基酸的细胞。然后,在ames试验中,向上述细胞加入测试物后,在一定条件下进行培养。当由于测试物导致细胞的氨基酸合成基因发生突变时,细胞就可以再次合成氨基酸。因此,通过确认有无细胞增殖来评价是否发生突变。此时,例如,如果使用由于细胞增殖而颜色发生变化的指示剂,则可以通过颜色的变化来评价细胞的增殖。
2、近年来,已知ames试验,其为了试验物和测试物的量等的减少等,使用例如如非专利文献1、非专利文献2和非专利文献3中公开的具有多个孔的板。
3、现有技术文献
4、非专利文献
5、非专利文献1:fluckiger-isler s.,kamber m.,“direct comparison of theames microplate format(mpf)test in liquid medium with the stan dard ames pre-incubation assay on agar plates by use of equivocal to weakly positive testcompounds.”,mutation research/genetic toxicology and environmentalmutagenesis 747,p36-45,2012.
6、非专利文献2:sui h.,kawakami k.,sakurai n.,hara t.,nohmi t.,
7、“improvement and evaluation of high throughput fluctuation ames testusing 384-well plate with salmonella typhimurium ta100 and ta98.”,genes andenvironment 31(2),p47-55,2009.
8、非专利文献3:kamber m.,fluckiger-isler s.,engelhardt g.,jaeckh r.,zeiger e.,“comparison of the ames ii and traditional ames test re sponseswith respect to mutagenicity,strain specificities,need for metabo lism andcorrelation with rodent carcinogenicity”,mutagenesis 24(4),p359-366,2009.
技术实现思路
1、发明要解决的课题
2、在使用具有多个孔的板时,例如,如下对评价对象进行评价。将照明光照射到各孔中保持了包含试验物和测试物的评价对象的状态的板,对板进行摄像。根据得到的图像判定各孔的颜色,检测有无菌落,对评价对象进行评价。在该情况中,如果在一个板的摄像中摄像条件发生变化,则评价精度下降,因此无法适当地对评价对象进行评价。
3、因而,本发明的目的在于提供可以适当地对评价对象进行评价的评价对象的评价方法。
4、用于解决课题的手段
5、根据本发明的评价对象的评价方法,其具备:照射步骤,将照明光从光源照射到板所具备的多个孔中保持有评价对象的评价板;摄像步骤,在上述照射步骤中,将上述照明光照射到上述评价板的同时,对上述评价板进行摄像;和评价步骤,根据上述摄像步骤中得到的上述评价板的图像来评价上述评价对象,上述评价对象包含试验物,上述多个孔具有保持了还包含测试物的上述评价对象的测试物用孔,在上述摄像步骤中,在从上述照射步骤中上述照明光向上述评价板开始照射起不足120秒,结束上述评价板整体的摄像,在结束上述摄像步骤中的上述评价板整体的摄像后,结束上述照明光的照射。
6、在上述评价对象的评价方法中,将照明光照射到评价板的同时,对评价板进行摄像。在从照明光开始照射起不足120秒,结束评价板整体的摄像。因此,可以抑制伴随输出照明光的光源的温度变化的照明光的波长移位(各波长成分的亮度变化)。其结果,可以正确地对评价对象进行评价。
7、在上述摄像步骤中,可以在从上述照射步骤中上述照明光向上述评价板开始照射起12秒以上且35秒以下,结束上述评价板整体的摄像。在该情况中,可以进一步降低伴随光源的温度变化的波长移位,因此可以更加正确地对评价对象进行评价。
8、上述照明光可以是波长为520nm以上的光。在该情况中,可以减少伴随光源的温度变化的每个波长成分的亮度方差。
9、在上述摄像步骤中,可以输送上述评价板的同时对上述评价板进行摄像。
10、上述照明光可以是从led输出的光。
11、发明效果
12、根据本发明,可以提供一种能够适当地对评价对象进行评价的评价对象的评价方法。
13、附图简单说明
14、图1为根据一实施方式的评价对象的评价方法中使用的评价板的平面图。
15、图2为孔截面的示意图。
16、图3为根据一实施方式的评价对象的评价方法中使用的评价系统的示意图。
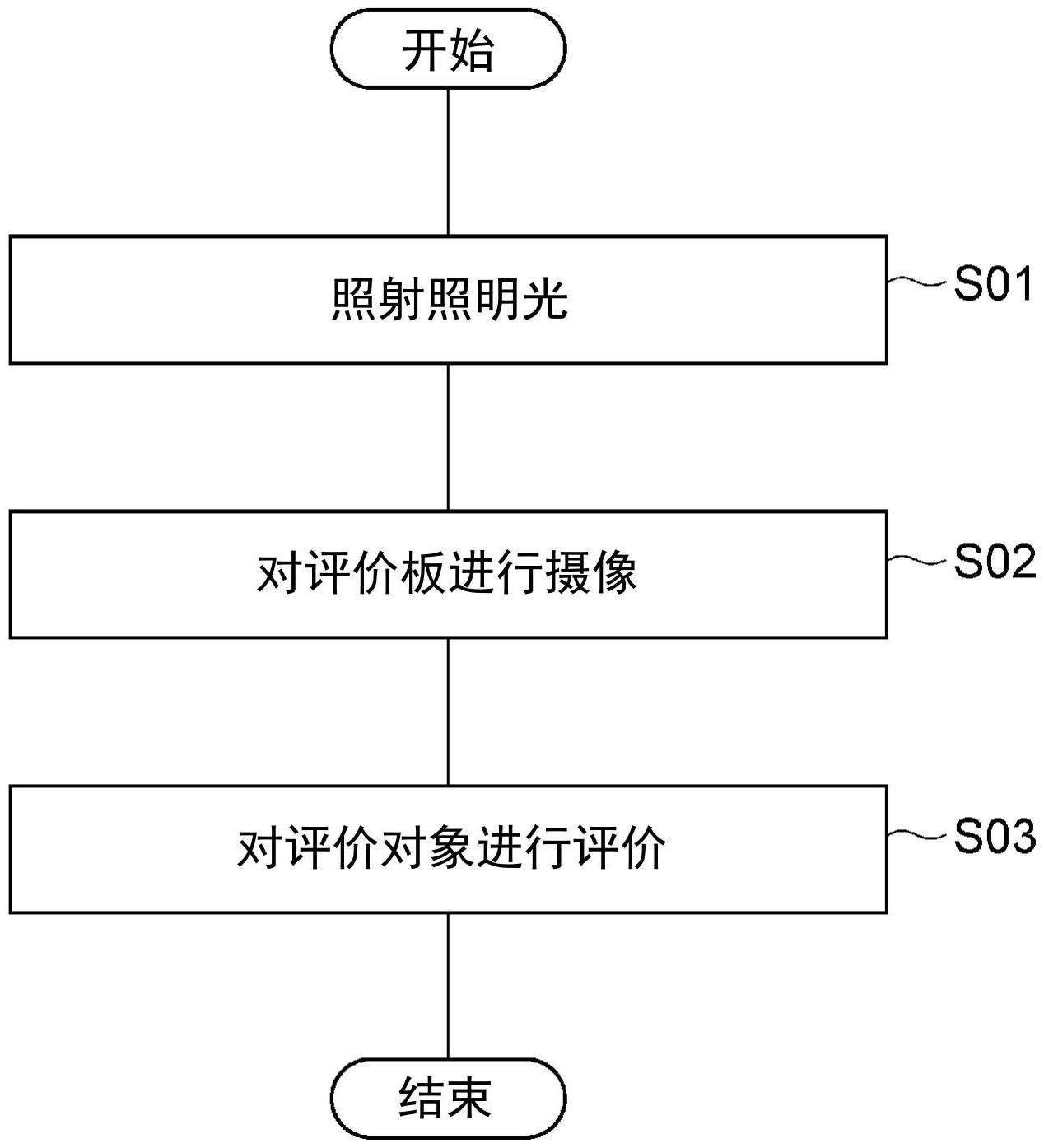
17、图4为根据一实施方式的评价对象的评价方法的流程图。
18、图5为验证实验中使用的装置的说明图。
19、图6为示出验证实验的结果、示出从输出照明光的时间点开始的每个经过时间的波长与亮度的关系的曲线图。
20、图7为示出验证实验的结果、示出从输出照明光的时间点开始的每个经过时间的波长与标准偏差的关系的曲线图。
21、图8为示出验证实验的结果、示出与从输出照明光的时间点开始的经过时间相对的温度和亮度差的曲线图。
22、发明的具体实施方式
23、以下,参考附图说明本发明的实施方式。对相同的要素赋予相同的符号,省略重复的说明。附图的尺寸比例不一定与说明的一致。
24、在本实施方式中,对评价测试物的安全性的实施方式进行说明。具体地,对采用ames试验评价测试物的安全性的情况进行说明。
25、首先,对本实施方式中采用的ames试验的概要进行说明。在ames试验中,将对氨基酸合成基因实施基因操作、改良为无法合成氨基酸的细胞用作试验物。在ames试验中,向上述细胞加入测试物。之后,在一定条件下进行培养。当由于测试物导致细胞的氨基酸合成基因发生突变时,细胞就可以再次合成氨基酸。因此,通过确认有无细胞增殖来评价是否发生突变,由此评价基因毒性。进而,通常在ames试验中进行确认测试物对细胞是否具有毒性的细胞毒性评价。
26、在本实施方式中,对ames试验中可以适用的评价对象的评价方法进行说明。在以下基于ames试验的实施方式的说明中,除非另有说明,否则试验物是细胞。
27、图1是根据一实施方式的评价对象的评价方法中使用的评价板10的平面图。评价板10具有板(plate)11。板11具有多个孔13。在本实施方式中,板11具有二维(16×24)排列的384个孔13。当从板11的厚度方向观察时,板11的形状是长方形。在该情况中,板11的长边长度的示例为127.0mm~130.0mm,板11的短边长度的示例为85.0mm~87.0mm。
28、在板11中,虚拟地设定第1~第n的分区(n为2以上的整数)。在本实施方式中,如图1所示,对n为8时,即虚拟地设定8个分区的情况进行说明。以下将8个分区称为分区se1~se8。分区se1~se8是包含4×12个(48个)孔13的区域。分区se1是溶剂对照分区,分区se8是阳性对照分区。溶剂对照分区作为阴性对照分区发挥功能。
29、孔(well)13是形成在板11上的凹部(凹陷)。孔13保持评价对象14。在对属于每个分区se1~se8的孔13中保持的评价对象14进行区分说明时,将其称为评价对象14a~14h。
30、评价对象14a~14h具有细胞分散的(或悬浮的)培养液。在全部384个孔13中保持相同量的培养液。孔13中保持的培养液内的细胞量在孔13间也相同。细胞的示例是具有氨基酸营养缺陷型突变的微生物、生物来源细胞等。具有氨基酸营养缺陷型突变的微生物是组氨酸营养缺陷型的鼠伤寒沙门氏杆菌(例如,ta1535、ta1537、ta97、ta97a、ta98、ta100、ta92、ta94、ta102、ta104、ta1538、ta7001、ta7002、ta7003、ta 7004、ta7005、ta7006、各种yg株等)、色氨酸营养缺陷型的大肠杆菌(例如,wp2、wp2uvra、wp2/pkm101、wp2uvra/pkm101等)、其他微生物等。生物来源细胞例如是哺乳动物来源培养细胞、其他脊椎动物来源细胞、昆虫来源细胞等。评价对象14a~14h中包含的细胞也可以是混合了多种细胞的细胞。培养液的示例是包含少量氨基酸的磷酸缓冲液。
31、评价对象14a~14h还包含指示剂。指示剂的量在评价对象14a~14h中相同(即在全部孔13中相同)。在本实施方式中,指示剂是ph指示剂。p h指示剂的示例是溴甲酚紫。在本实施方式中,ph指示剂的颜色在阴性结果时(细胞未发生突变时)是紫色,在阳性结果时(细胞发生突变时)是黄色。
32、评价对象14b~14g除了包含上述细胞分散的培养液和指示剂以外,还包含测试物溶解或均匀分散在溶剂中的液体(测试物溶液)。因此,保持评价对象14b~14g的分区se2~se7的孔13是保持测试物的孔(测试物用孔)。测试物是安全性(在本实施方式中为基因毒性)待评价的物质(例如化学物质)。作为溶剂列举水、二甲基亚砜(dmso)等。评价对象14b~14g除了测试物浓度不同以外,其余相同。属于分区se2的全部孔13的评价对象14b内的测试物溶液的量是相同的。在分区se3~分区se7中也是相同的。
33、评价对象14a除了包含含有上述细胞的培养液和指示剂外,还包含溶剂对照液。因此,保持评价对象14a的分区se1的孔13是溶剂对照孔。溶剂对照液是测试物溶液中使用的溶剂。但是,溶剂对照液只要是不影响细胞的液体即可。作为溶剂对照液例如是水、dmso。在属于分区se1的全部孔13中,评价对象14a内的溶剂对照液的量是相同的。
34、评价对象14h除了包含含有上述细胞的培养液和指示剂外,还包含阳性对照液。因此,保持评价对象14h的分区se8的孔13是阳性对照孔。阳性对照液是包含阳性对照化合物和溶剂的溶液。阳性对照化合物是已知对细胞呈阳性的化合物即可。阳性对照化合物的示例包含9aa(9-氨基吖啶,9-aminoacridine)、4-nqo(4-硝基喹啉-n-氧化物,4-nitroquinoline-n-oxide)、2-aa(2-氨基蒽,2-aminoanthracene)及2-nf(2-硝基芴,2-nitroflu orene)。溶剂可以与测试物溶液中使用的溶剂不同。作为溶剂列举水、dm so等。属于阳性分区的分区se8的全部孔13中保持的阳性对照液的量是相同的。
35、在研究测试物代谢活化的有无引起的影响时,评价对象14a~14h还包含s9mix。s9mix是在动物肝脏提取物中添加了辅酶的液体。
36、参考图1和图2,进一步说明孔13的结构。图2是孔截面的示意图。在图2中,示意性地示出了评价对象14。在本实施方式中,孔13的平面视形状(从孔13的深度方向观察的形状)是正方形。孔13的开口部的一边长度示例是3.0mm~4.0mm。孔13的深度示例是9.0mm~15.0mm。具有这种尺寸的孔的板11,作为微板是已知的。在一个实施方式中,如图2所示,孔13朝向底部13a逐渐变细。
37、评价板10是注入与板11的各孔13对应的评价对象14,并实施一定的培养处理后,处于可以进行评价对象14的安全性评价的状态的板。
38、接下来,利用图3对本实施方式的评价对象的评价方法中使用的观察装置30进行说明。
39、观察装置30具有台(板保持部)31、照明装置(光源)32及摄像部33。台31支撑评价板10。评价板10配置在台31上,以使评价板10的底部(孔13的底部13a侧)位于台31侧。台31构成为使从照明装置32输出的照明光l朝向摄像部33通过。例如,台31的材料可以具有透光性,也可以在与评价板10中384个孔13形成的区域对应的区域中,形成开口或透过照明光l的窗部。在本实施方式中,台31构成为可以向图3的箭头的方向输送。
40、照明装置32配置在评价板10上(从评价板10观察与台31相反的一侧)。照明装置32将照明光l照射到评价板10。照明装置32的示例是led照明,照明光l的示例是波长为400nm~780nm的光。在一个实施方式中,照明光l是波长为520nm以上的光。
41、摄像部33接收透过评价板10的照明光l,并对评价板10进行摄像。摄像部33具有摄像器33a和聚光部33b。
42、摄像器33a的示例包含二维传感器(或照相机)和线传感器。二维传感器的示例是ccd照像机和cmos照像机。
43、聚光部33b将照明光l聚光并入射到摄像器33a。聚光部33b包含至少1个透镜。当摄像器33a本身具有聚光光学功能时,摄像部33也可以不具有聚光部33b。
44、接下来,对根据本实施方式的评价对象的评价方法的一个示例进行说明。在此,对输送评价板10的同时获取评价板10的图像的情况进行说明。输送速度可以通过使用以下公式,根据摄像器33a的帧率和分辨率实际可获得的范围等进行确定。
45、输送速度[mm/s]
46、=板11的输送方向的长度[mm]÷撮影时间[s]
47、=摄像器33a的帧率[fps]×摄像器33a的分辨率[mm/pixel]
48、例如在撮影时间不足120秒、摄像器33a的分辨率为60um/frame以上时,如果输送速度为1.17mm/s以上,则在具有19.4fps以上帧率的摄像器33a中,可以以适合评价的方式对评价板10进行摄像。在撮影时间为12秒以上且不足120秒、摄像器33a的分辨率为8um/frame~60um/frame时,如果输送速度为1.17mm/s~11.7mm/s,则在具有19.4fps以上帧率的摄像器33a中,可以以适合评价的方式对评价板10进行撮影。在撮影时间为12秒以上且35秒以下、摄像器33a的分辨率为15um/frame~25um/frame时,如果输送速度为4mm/s~11.7mm/s,则在具有160fps以上帧率的摄像器33a中,可以以适合评价的方式对评价板10进行撮影。在输送评价板10时,也可以设置助跑时段(例如30mm)。
49、图4是根据本实施方式的评价对象的评价方法的流程图。如图4所示,将照明装置32点亮,将照明光l照射到评价板10(照射步骤s01)。
50、用摄像部33对被照明光l照射的评价板10进行摄像(摄像步骤s02)。在摄像步骤s02中,在从照射步骤s01中照明光l开始照射时起不足120秒,结束评价板10整体的摄像。优选地,从照明光l开始照射时起12秒以上且60秒以下,结束评价板10整体的摄像,更优选地,在12秒以上且35秒以下,结束评价板10整体的摄像。结束评价板10整体的摄像后,停止照明光l的照射。下面也将从照明光l开始照射时至评价板10整体的摄像结束的时间称为“摄像时间”。
51、在摄像部33的摄像区域小于评价板10的大小的实施方式中,无法在1次摄像中对评价板10整体进行摄像。在这种实施方式中,对评价板10进行多次摄像,以便合成评价板10的部分图像以形成评价板10的整体图像。在该情况中,上述摄像时间是为了形成评价板10的整体图像,而用于结束评价板10的多个摄像的时间。
52、接下来,根据摄像部33所摄像的图像来对评价对象14进行评价(评价步骤s03)。在评价步骤s03中,评价测试物的基因毒性和测试物的细胞毒性的至少一个。基因毒性和细胞毒性的评价本身按照ames试验中的评价对象的评价方法实施即可。
53、(基因毒性评价)
54、在本实施方式中,当测试物对评价对象14中包含的细胞具有基因毒性时,作为阳性结果,指示剂的颜色从紫色变为黄色。因此,可以通过判定摄像步骤s02中得到的图像中各孔13的颜色(具体地,各孔13中保持的评价对象14的颜色),评价测试物的基因毒性。此时,将分区se1(溶剂对照分区或阴性对照分区)内的孔13和分区se8(阳性对照分区)内的孔13的颜色作为评价基准即可。
55、在本实施方式中,当测试物对评价对象14中包含的细胞具有基因毒性时,有可能产生菌落。即,检测出菌落时相当于阳性结果。因此,可以通过对具有上述菌落的孔13的数量进行计数,评价测试物的基因毒性。此时,将分区se1内的孔13和分区se8内的孔13的状态(有无菌落)作为评价基准即可。
56、各分区se1~se8内的多个孔13中保持的评价对象14的状态(测试物的浓度等)是相同的。因此,对评价对象14进行评价时,综合判定每个分区se1~se8中包含的多个孔13的颜色(或状态)即可。
57、(细胞毒性评价)
58、在本实施方式中,当测试物对评价对象14中包含的细胞具有细胞毒性时,由于细胞死亡等导致孔13的透明度(具体地,评价对象14的透明度)发生变化。因此,可以根据孔的透明度来评价测试物的细胞毒性。此时,将分区se1(溶剂对照分区或阴性对照分区)内的孔13的透明度作为评价基准即可。在培养中析出测试物时,孔13的透明度(具体地,评价对象14的透明度)也发生变化。因此,也可以根据上述透明度来评价有无测试物析出。
59、在本实施方式中,当测试物对评价对象14中包含的细胞具有细胞毒性时,由于细胞死亡而产生异物。因此,可以根据孔内有无异物来评价测试物的细胞毒性。此时,将分区se1内的孔13(有无异物)作为评价基准即可。
60、在细胞毒性评价中,各分区se1~se8内的多个孔13中保持的评价对象14的状态(测试物的浓度等)也是相同的。因此,对评价对象14进行评价时,综合判定每个分区se1~se8中包含的多个孔13的透明度(或状态)即可。
61、上述颜色的判定、菌落的检测、透明度的判定和异物的检测等可以通过评价者目视摄像部33所获取到的评价板10的图像来进行,也可以通过图像解析来进行。
62、在将多个评价板10依次放在输送线上进行摄像时,上述评价对象的评价方法也可以适用于至少1个评价板10(例如,第2个以后的评价板10)。
63、在本实施方式的评价对象的评价方法中,将照明光l照射到评价板10的同时,对评价板10进行摄像。此时,在从照明装置32开始点亮时(即,开始照射照明光l的时间点)起不足120秒,结束评价板10整体的摄像。如果是从照明装置32开始点亮时起不足120秒,则可以抑制伴随照明装置32的温度变化的照明光l的波长移位(各波长成分的亮度变化)。
64、假设,如果伴随照明装置32的温度变化,照明光l中包含的各波长成分的亮度在评价板10的摄像开始阶段和摄像结束阶段之间有很大不同,则在评价板10中摄像开始阶段摄像的区域和摄像结束阶段摄像的区域中,会出现由于摄像条件的变化而导致评价对象14的颜色、状态等发生变化的情况。其结果,无法正确地对评价对象14进行评价。
65、与此相对,如果是从照明装置32开始点亮时(即,开始照射照明光l的时间点)起不足120秒,则可以抑制伴随照明装置32的温度变化的照明光l的波长移位。其结果,可以正确地对评价对象14进行评价。从照明装置32开始点亮时起至结束评价板10整体的摄像的时间(摄像时间),可以是60秒以下,也可以是35秒以下。摄像时间只要超过0秒即可,可以是5秒以上,也可以是12秒以上。如果是12秒以上,则能够相对于摄像器33a的帧率将输送速度设定得足够慢,因此提高摄像分辨率而容易检测出具有一定大小(例如60μm)的菌落和异物。因此,摄像时间可以是12秒以上且不足120秒,也可以是12秒以上且60秒以下,也可以12秒以上且35秒以下。
66、为了适当地检测具有一定大小(例如60μm)的菌落和异物,考虑评价板10的大小和上述摄像时间来确定在摄像步骤s03中使用的摄像器33a的分辨率和输送速度即可。
67、对评价板10的大小为127.7mm×85.6mm、评价板10(板11)内的孔13存在的区域的大小为109.5mm×73.5mm的情况进行说明。在该情况中,根据摄像时间的摄像器33a的分辨率和输送速度的示例如下所述。
68、(1)摄像时间不足120秒的情况
69、分辨率:60um/frame以上
70、输送速度:1.17mm/s以上
71、帧率:19.4fps以上
72、(2)摄像时间在60秒以下的情况
73、分辨率:60um/frame以上
74、输送速度:2.33mm/s以上
75、帧率:38.9fps以上
76、(3)摄像时间在12秒以上且不足120秒的情况
77、分辨率:8um/frame~60um/frame
78、输送速度:1.17mm/s~11.7mm/s
79、帧率:19.4fps以上
80、(4)摄像时间在12秒以上且35秒以下的情况
81、分辨率:15um/frame~25um/frame
82、输送速度:4mm/s~11.7mm/s
83、帧率:160fps以上
84、如果是上述(1)~(4)的各个条件,则在使用127.7mm×85.6mm的评价板10时,可以可靠地检测出上述具有一定大小的菌落或异物等。
85、如果照明光l的波长为520nm以上,则不容易产生亮度方差,因此,当照明光l是波长为520nm以上的光时,可以更正确地对评价对象14进行评价。
86、接下来对验证实验进行说明。在验证实验中,如图5所示,将摄像部42面向照明装置41进行配置。照明装置41是使用了led的面光源装置,是输出波长为400~700nm的照明光l的面光源装置(kos21制造的kdb-100)。在照明装置41中,输出面上安装有温度传感器43。温度传感器43是and制造的ad-5625。摄像部42具有摄像器42a和安装在摄像器42a的聚光部42b。摄像器42a是高光谱相机(resonon制造的pika―l)。摄像器42a的帧率是249.2hz,曝光时间是3.93ms。聚光部42b使用shneider公司制造的xenoplan1.4/23-0902(光圈:f5.6)。
87、在验证实验中,从照明装置41开始点亮(照明光l开始输出)起30分钟,获取到了波长为400nm~700nm的照明光l的亮度光谱和照明装置41的表面温度的数据。
88、具体地,从照明装置41开始点亮起10分钟内每1分钟获取到面照明的384处的毎个波长的亮度的平均值(以下称为“平均亮度”)的同时,获取到了温度数据。从照明装置41开始点亮起10分钟后每5分钟获取到面照明的384处的毎个波长的亮度的平均值(平均亮度)的同时,获取到了温度数据。进而,以照明装置41开始点亮的亮度为基准亮度,对每个波长计算上述基准亮度与平均亮度的亮度差和标准偏差σ。在各亮度数据的获取时间中,上述384处是相同的位置。
89、图6是示出了相对于波长的亮度变化的曲线图,用浓淡线表示从开始点亮起1分钟后、2分钟后、…、30分钟后的数据。图6的横轴表示波长(nm),纵轴表示基准亮度与平均亮度的亮度差。图7是示出了相对于波长的标准偏差的曲线图,用浓淡线表示从开始点亮起1分钟后、2分钟后、…、30分钟后的数据。图7的横轴表示波长(nm),纵轴表示亮度差的标准偏差。
90、图8是示出了与从照明装置开始点亮起的经过时间相对的照明装置的温度和照明光l的亮度变化的曲线图。图8的横轴表示从照明装置开始点亮起的经过时间(分钟)。图8的右侧的纵轴表示温度,左侧的纵轴表示照射开始时(经过时间为0分钟)的亮度与各经过时间的平均亮度的差(亮度差)。图8所示的亮度差是在每个亮度数据的获取时间中,在图7所示的波长400nm~700nm中,与亮度差最大的波长相对应的平均亮度与基准亮度之间的差。图8中的点划线1表示平均亮度差加上3σ(标准偏差)后的结果,点划线2表示平均亮度差减去3σ(标准偏差)后的结果。
91、如图8所示,如果是从照明装置41开始点亮起不足120秒(2分钟),则可以使照明装置41的温度变化不足0.5℃的同时,抑制亮度变化。其结果,如果是不足120秒,则可以正确地对评价对象14进行评价。如果是从照明装置41开始点亮起60秒以下,则可以使照明装置41的温度变化不足0.1℃。从照明装置41开始点亮起,60秒处的亮度变化是0.93±1.10×3σ(σ标准偏差),可以进一步抑制亮度变化。
92、如图7所示,如果波长为520nm以上,则照明光l中每个波长成分的亮度方差小。因此,更不容易受到亮度变化的影响。其结果,可以正确地对评价对象14进行评价。
93、以上与本发明的各种实施方式和变形例一起说明了实验例。然而,本发明并不限于例示的各种实施方式、变形例和实验例,其包括权利要求书所示范围,同时还包括在与权利要求书同等的含义和范围内的所有改变。
94、试验物不限于细胞。测试物不限于化学物质。试验物和测试物可以是任意组合,只要它们的组合可以产生作为安全性评价的判定因素的变化(例如,如示例的颜色变化、透明度变化、菌落的产生、异物的产生等)即可。试验物的其他示例是抗体,测试物的其他示例是抗原。
95、在上述实施方式中,作为评价对象的试验物的形状变化检测出了菌落,但是当评价对象由于试验结果而形状发生变化时,则不限于菌落。异物是与试验物的上述形状变化不同的物质(或结构物),例如最初不包含的物质(或结构物),例如可以是轮廓与内部的边界明确的物质。例如,异物是由与异物周围折射率不同的界面隔开的物质(或结构物)。异物的示例是油块、气泡等。
96、用于获得评价板的图像的观察装置可以采用反射光学系统。即,照明装置和摄像部相对于评价板配置在相同侧,摄像部接收从照明装置输出并由评价板反射的照射光,从而可以获取评价板的图像。
97、照明装置不限于led照明装置,也可以是使用了卤素光源、金属卤化物光源的装置。
98、当获取评价板的图像时,可以在评价板静止的状态下,对评价板进行摄像。
99、在之前的说明中,采用ames试验进行了说明,但是本发明也可以适用于对评价对象进行摄像,根据该图像来评价安全性的其他生物安全性评价。
100、示例的实施方式和变形例等也可以在不脱离本发明宗旨的范围内适当组合。
101、符号说明
102、10:评价板;
103、11:板;
104、13:孔;
105、14、14a~14h:评价对象;
106、32:照明装置(光源)。
- 还没有人留言评论。精彩留言会获得点赞!