CMK-8与GNs联合修饰的电极、电化学传感器及应用
cmk-8与gns联合修饰的电极、电化学传感器及应用
技术领域
1.本发明涉及电化学传感器的修饰技术领域,具体涉及一种cmk-8与gns联合修饰的电极、包含该电极的电化学传感器及其在检测黄芩苷的应用。
背景技术:
2.黄芩是中国、日本、韩国等国药用植物黄芩的干根,是著名的药材。它是天然药物之一,几千年来一直广泛用于中国传统医药中。黄芩苷是黄芩中最重要的生物活性之一。在医学领域,其具有抗过敏、抗焦虑、抗氧化、抗炎和清除自由基的作用,除此之外,黄芩苷也有帮助治疗高血压、宫颈癌、创伤性脑损伤、细胞损伤的能力,同时在动物治疗中可以发挥治疗小鼠禽流感功能、对鞍带石斑鱼成长有所帮助。另外,黄芩苷在化妆品领域有消炎祛痘的作用。在中国,公共卫生部要求黄芩中黄芩苷的含量不得小于8.0%。在《日本药典》规定临床使用的黄芩中黄芩苷的含量应》10%。因此,建立或开发准确、快速、灵敏且经济有效的检测黄芩中黄芩苷含量的方法或仪器显得尤为重要。
3.目前,黄芩苷的检测方法主要有薄层色谱、紫外分光光度法、高效液相色谱-电化学检测法、液相色谱-串联质谱、超高效液相色谱-质谱联用法和毛细管电泳法等。但是,紫外和薄层色谱的灵敏度相对较低。高效液相色谱方法虽然具有较高的灵敏度和稳定性,但它耗时长、仪器昂贵、预处理过程复杂,使用有机溶剂量大。与之相比,电化学方法具有简单、灵敏度高、稳定性好、成本低等优点,已被应用于传统医药检测研究。如使用电化学方法测定中药中槲皮素,原儿茶醛和黄芩苷等中药成分。近些年来,各种功能材料,特别是碳纳米材料,如石墨烯碳纳米片gns和碳纳米管cnts已被用于修饰电极,用以提高电化学传感器的灵敏度和选择性。立方la3d结构介孔碳cmk-8是一种新型的非硅基介孔材料,其因优越的导电性能常用于电池领域。石墨烯是一种新型的二维碳纳米材料gns,它有独特的单层碳原子结构,因此具有优异的光、电、热及机械能。目前这两种碳纳米材料在电化学实验中常被应用于检测各种中药成分,但将gns和cmk-8联合使用于检测药物成分仍未有报道。
技术实现要素:
4.(一)要解决的技术问题
5.鉴于现有技术的上述缺点、不足,本发明提供一种cmk-8(立方la3d结构介孔碳)与gns(石墨烯碳纳米片)联合修饰的电极、包含该电极的电化学传感器及其在检测黄芩苷的应用。本发明的电化学传感器使黄芩苷的检测更加简单快捷、灵敏度更高、检测限极低,重复性和稳定性好,解决了现有黄芩苷检测方法灵敏度低、耗时长或成本高、预处理过程复杂、使用有机溶剂量大等问题。
6.(二)技术方案
7.为了达到上述目的,本发明采用的主要技术方案包括:
8.第一方面,本发明提供一种cmk-8与gns联合修饰的电化学传感器的工作电极,所述工作电极表面采用cmk-8与gns的混合物进行联合修饰;所述工作电极的修饰方法如下:
9.s1、对玻碳电极进行抛光打磨至工作面光滑,纯净水冲洗干净后晾干;
10.s2、配制cmk-8分散液和gns分散液;
11.s3、将gns分散液和cmk-8分散液混合,超声处理,得到混合分散液;
12.s4、取一定量的混合分散液涂覆到打磨后的玻碳电极的工作面上,烘干,得到cmk-8-gns@gce玻碳工作电极。
13.根据本发明的较佳实施例,s1中,使用粒径0.05μm氧化铝抛光粉对玻碳电极进行抛光打磨,8字手法打磨抛光至工作面光滑,纯净水冲洗干净后放置红外线灯晾干;s2中,cmk-8分散液和gns分散液的浓度均为2mg/l;s3中,gns分散液和cmk-8分散液按照体积比1:2-4进行混合。
14.根据本发明的较佳实施例,s3中,gns分散液和cmk-8分散液按照体积比1:3进行混合。
15.根据本发明的较佳实施例,s4中,混合分散液的涂覆量为8-10μl。
16.根据本发明的较佳实施例,s4中,混合分散液的涂覆量为10μl。
17.第二方面,本发明还提供一种检测黄芩中黄芩苷含量的电化学传感器,其包括上述任一实施例的工作电极,还包括对电极和参比电极。优选地,所述参比电极为甘汞电极,所述对电极为钛棒。
18.第三方面,本发明提供上述任一实施例的电化学传感器在检测黄芩苷中的应用。
19.根据本发明交接实施例,在检测黄芩苷含量时,采用差分脉冲伏安法或循环伏安法;在采用差分脉冲伏安法时,以ph=7的pbs缓冲溶液为电解液;富集黄芩苷的电位为0.4v-0.6v,富集时间为860-960s,搅拌速度1500-2000r/min。更优选地,以ph=7的pbs缓冲溶液为电解液;富集黄芩苷的电位为0.4v,富集时间为860s,搅拌速度1500r/min。
20.在检测黄芩苷含量时,电解液在ph4-7范围内,黄芩苷峰电流随ph增加而增加,在ph为7时峰电流达到最大。由于黄芩苷在碱性条件下易水解,故在ph>7时峰电流有所下降。因此,确定缓冲液最佳ph为7。其中,随着富集电位的改变黄芩苷的峰电流也有所变化,在电位为0.4v时出现电流最高峰,大于0.4v和低于0.4v时黄芩苷的峰电流都明显下降。
21.在检测黄芩苷含量时,富集时间低于860s时峰电流随着富集时间的增加而增大,在860s达到最大,860s后开始减小,因此最优富集时间为860s。
22.在检测黄芩苷含量时,随着搅拌速度的增加,峰电流也逐渐变大,在转速为1500r/min时峰电流最大,在1500-2000r/min逐渐减小。据分析,搅拌速度过大,搅拌机震动强度也变大,测试环境不稳定,另一原因是搅拌太快气泡产生过多,占据了一部分富集位点,导致黄芩苷富集减少。因此,最优搅拌速度为1500r/min。
23.根据本发明交接实施例,在采用差分脉冲伏安法时,测定条件为:
24.以0.2mpbs缓冲溶液ph=7为电解液、恒电位富集黄芩苷且富集电位为e=0.4v、富集时间t=860s、搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
25.根据本发明交接实施例,在检测之前先配制黄芩苷的标准溶液并制作待测样品;
26.标准溶液为将黄芩苷粉末用dmf定容并超声分散得到0.002m的黄芩苷的标准溶液;
27.所述待测样品的制备方法为:黄芩饮片研磨成细粉,过50目筛,称取1.0g黄芩粉
末,以60%的乙醇为溶剂提取其中的黄芩苷,料液比为1:16混合,超声30-40min,离心4-6min,取上清液过0.22μm滤膜;滤渣再60%的乙醇按照前述方法重复提取2次,合并三次滤液,用旋转蒸发仪旋蒸至晶体析出,除去全部乙醇;旋干后用10mldmf复溶,制得黄芩苷样液,用dmf稀释100倍,得待测样品。
28.(三)有益效果
29.本发明采用cmk-8和gns联合对玻碳电极的工作面进行包覆修饰,采用差分脉冲伏安法(dpv)对比了黄芩苷在不同碳材料修饰电极上的电化学性能,实验结果显示在相同实验条件下1.0
×
10-6
mol/l的黄芩苷在cmk-8-gns@gce、cmk-8@gce、gns-gce、gce的氧化峰电流分别为81μa、33μa、2μa、0.4μa,该结果说明,黄芩苷在cmk-8-gns@gce表现出响应电流是cmk-8@gce、gns-gce、gce电极是2.5倍、42倍、202.5倍。以gce电极的响应电流为基准,黄芩苷在cmk-8-gns@gce电极上的响应电流的增强倍数是cmk-8@gce、gns-gce二者乘积2倍。因此,采用cmk-8和gns联合修饰玻碳电极后,cmk-8和gns对电极检测灵敏度的增效产生了协同作用,超出了预期。
30.基于cmk-8-gns@gce电极对黄芩苷良好的电化学催化性能,本发明还构建了一种灵敏高的黄芩苷电化学传感器。在最优条件下,黄芩苷在cmk-8-gns@gce电极上的氧化峰电流与黄芩苷浓度在1.0
×
10-9
~3.2
×
10-6
m范围内呈线性关系,i
pa
(μa)=0.4129c(nmol/l)+1.5404(r=0.9989),其检出限为1.0
×
10-9
m(s/n=3)。该电化学传感器成功应用于中药黄芩样品中黄芩苷的检测,加标回收率为113.5~116.9%。检测设备简单、易于操作、检出限低,线性范围宽,对黄芩中黄芩苷的检测方便快捷,且重现性良好,有助于实现实际样品中黄芩苷的自动化检测。
31.本发明进一步优化了cmk-8和gns联合修饰玻碳电极的混合配比、总涂覆量,优化了检测条件,包括电解液ph、富集黄芩苷的富集电位、富集时间和搅拌速度等参数,以便在对黄芩苷的实际检测过程中,提供最优检测条件、获得最大的响应电流,提高电化学传感器对黄芩苷检测的灵敏度、进一步降低检测限,提高检测重复性、稳定性和可靠性,增强抗干扰能力。综上所述,本发明提供了一种准确、快速、灵敏且经济有效的检测黄芩中黄芩苷含量的手段。
附图说明
32.图1为cmk-8-gns@gce、cmk-8@gce、gns@gce、gce电极在含1.0
×
10-6
mol/l黄芩苷pbs溶液中的电化学阻抗谱图。
33.图2为cmk-8-gns@gce在含黄芩苷和不含黄芩苷的电解液中的循环伏安曲线。
34.图3为cmk-8-gns@gce(a)、cmk-8@gce(b)、gns@gce(c)、gce(d)在含1.0
×
10-6
mol/l的黄芩苷电解液中的cv曲线。
35.图4为cmk-8-gns@gce(a)、cmk-8@gce(b)、gns@gce(c)、gce(d)在含1.0
×
10-6
mol/l的黄芩苷电解液dpv曲线。
36.图5为不同比例的gns:cmk-8(1:1、1:2、1:3、1:4)修饰的cmk-8-gns@gce电极在含1.0
×
10-6
mol/l的黄芩苷电解液中测得的dpv电流响应。
37.图6为不同涂覆量的混合分散液(总浓度2mg/ml)修饰的cmk-8-gns@gce电极在含1.0
×
10-6
mol/l的黄芩苷电解液中测得的dpv电流响应。
38.图7为cmk-8-gns@gce电极在不同ph的pbs电解液中测试黄芩苷(1.0
×
10-6
mol/l)时的dpv峰电流响应。
39.图8为1
×
10-6
mol/l黄芩苷在不同富集电位(a),富集时间(b)和搅拌速度(c)下的dpv峰电流响应。
40.图9的(a)为1
×
10-6
mol/l黄芩苷在不同扫速下与氧化还原峰电流与电位的关系图;(b)为不同扫速下与氧化还原峰电流与电位的线性关系图;(c)为cmk-8-gns@gce电极在不同ph值(g
→
l为从4
→
9的ph)的pbs缓冲液下的dpv曲线;(d)为ph与峰电位(e
p
)的关系曲线。
41.图10为黄芩苷在cmk-8-gns@gce上的电极反应机理示意图。
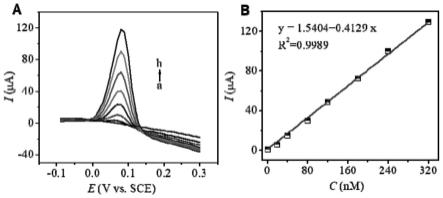
42.图11的(a)为不同浓度的黄芩苷的dpv曲线;(b)为不同浓度的黄芩苷的标准曲线。
43.图12为在1
×
10-6
mol/l黄芩苷溶液中加入1
×
10-4
mol/l的ca
2+
、葡萄糖、黄嘌呤、维生素c、al
3+
时,cmk-8-gns@gce对黄芩苷选择性柱形图。
具体实施方式
44.为了更好的解释本发明,以便于理解,下面结合附图,通过具体实施方式,对本发明作详细描述。在以下的各实施例和对比例中,如无特殊说明(有特殊说明的以该说明为准),dpv测试条件均为:涂覆量10μl、以0.2m pbs缓冲溶液ph=7为电解液、富集电位为e=0.4v、富集时间t=860s、搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
45.实施例1
46.本实施例为cmk-8和gns联合修饰的玻碳电极的制备方法,制备方法为:
47.(1)玻碳电极处理
48.使用0.05μm氧化铝抛光粉对玻碳电极(直径3mm)进行抛光打磨,8字手法打磨抛光至工作面光滑,纯净水冲洗干净后放置红外线灯晾干。用三电极工作体系(工作电极为玻碳电极,参比电极为甘汞电极,对电极为钛棒),在铁氰化钾电解液中,用循环伏安法对抛光好的玻碳电极进行电化学表征,峰电位差小于80mv,证明实验所用的玻碳电极导电性良好。
49.(2)cmk-8和gns联合修饰的玻碳电极
50.称取2mg制备好的cmk-8和2mg石墨烯于10ml容量瓶,加入dmf定容至刻度线,分别制成2mg/ml的cmk-8分散液和2mg/ml的gns分散液。定容后,放入超声仪超声20min,分别获得分散均匀的cmk-8分散液和石墨烯分散液。用移液枪将石墨烯分散液与cmk-8分散液以1:3体积比混合,超声20min,制备cmk-8-gns复合材料。用移液枪移取10μl cmk-8-gns分散液分3次滴涂于已打磨且干燥好的gce电极表面,用红外灯烘干,得到cmk-8-gns@gce修饰电极。
51.对比例1-2
52.对比例1为单独使用10μl的2mg/ml的cmk-8分散液分3次滴涂于已打磨且干燥好的gce电极表面,用红外灯烘干,得到cmk-8@gce修饰电极。对比例2为单独使用10μl的2mg/ml的gns分散液分3次滴涂于已打磨且干燥好的gce电极表面,用红外灯烘干,得到gns@gce修饰电极。
53.测试和比较裸玻碳电极(gce)、石墨烯(gns)、cmk-8、gns-cmk-8修饰的玻碳电极四
种电极的阻抗,并采用差分脉冲伏安法(dpv)、循环伏安法(cv)对比黄芩苷在裸玻碳电极(gce)、石墨烯(gns)、cmk-8、gns-cmk-8修饰的玻碳电极上的电化学行为。
54.测试比对方法和比对结果如下:
55.(1)标准溶液的配制
56.称取0.002g黄芩苷粉末于10ml容量瓶中,用dmf定容至刻度线,超声分散20min,即得0.002m的黄芩苷的标准溶液。
57.(2)电化学阻抗测试
58.在含1.0
×
10-6
mol/l黄芩苷pbs溶液(ph=7)中分别对gce、gns@gce(对比例2)、cmk-8@gce(对比例1)和cmk-8-gns@gce(实施例1)进行电化学阻抗测试。
59.结果如图1所示,cmk-8@gce电极的能奎斯特图由高频区的半圆和低频区的直线组成,半圆越小表明电子传递电阻越小,直线越接近90
°
表明扩散速率越快。在高频区的半圆可知,电子传递速率电阻大小顺序为:cmk-8-gns@gce《cmk-8@gce《gns@gce《gce,说明cmk-8-gns复合有效降低电极增强了电极导电性。与其他电极相比,cmk-8-gns@gce修饰的电极在低频区呈更加接近90
°
的直线,表明修饰后的cmk-8-gns@gce电阻有所减小,更有利于电解液在电极表面扩散,对检测黄芩苷更灵敏更有效。
60.(3)测试cmk-8-gns@gce(实施例1)在含黄芩苷和不含黄芩苷的电解液中的循环伏安曲线。
61.在含1.0
×
10-6
mol/l黄芩苷的pbs溶液(ph=7)和不含黄芩苷的pbs溶液(ph=7)中,测试cmk-8-gns@gce(实施例1)的循环伏安曲线。如图2所示,其中曲线a对应含黄芩苷的电解液,曲线b对应不含黄芩苷的电解液。由图2可知在-0.15v-0.6v的电位范围内,cmk-8-gns@gce对黄芩苷的电流响应非常显著。
62.(4)采用循环伏安法(cv)研究黄芩苷在不同碳材料修饰电极上的电化学行为。
63.在含1.0
×
10-6
mol/l黄芩苷的pbs溶液(ph=7)中,比较cmk-8-gns@gce电极(实施例1)、cmk-8@gce电极(对比例1)、gns@gce电极(对比例2)和gce电极对黄芩苷的电化学传感性能。
64.结果如图3所示,在裸玻碳电极gce上几乎观察不到黄芩苷的氧化还原峰。在gns@gce电极(对比例2)上黄芩苷显示出极弱的氧化还原峰,说明石墨烯对黄芩苷有较弱的电催化作用。同时gns@gce电极(对比例2)的背景电流也是相当弱。这主要是因为:尽管石墨烯有非常大的比表面积,但是在修饰电极过程中,二维的石墨烯可能会在玻碳电极表面重新堆叠,导致电极电化学活性面积剧烈降低,使得该电极的电化学传感性能不佳。而cmk-8@gce电极(对比例1)上黄芩苷的氧化还原峰电流显著增加,说明cmk-8对黄芩苷电化学氧化还原有明显的增强作用。这主要是得益于cmk-8的三维立方介孔结构,使其在修饰电极过程中仍然保持较高的电化学活性面积。
65.实施例1制备的cmk-8-gns@gce上黄芩苷的氧化还原峰进一步增大,表明cmk-8与石墨烯复合材料对黄芩苷电化学氧化还原反应具有协同增强的作用。这是因为随着两者复合,使得石墨烯在介孔碳与介孔碳间建立连接的桥梁,不仅使得cmk-8-gns@gce电化学活性显著增大,附着位点变多,而且有助于提高电子传递速率,减小电阻,促进了黄芩苷电化学反应的电子转移,故使cmk-8-gns@gce表现出增强的电流响应信号。
66.(5)采用差分脉冲伏安法(dpv)对比了黄芩苷在不同碳材料修饰电极上的电化学
性能
67.在含1.0
×
10-6
mol/l黄芩苷的pbs溶液(ph=7)中,比较cmk-8-gns@gce电极(实施例1)、cmk-8@gce电极(对比例1)、gns@gce电极(对比例2)和gce电极对黄芩苷的电化学传感性能。如图4所示,在含1.0
×
10-6
mol/l黄芩苷的pbs溶液中,黄芩苷在cmk-8-gns@gce、cmk-8@gce、gns-gce、gce的氧化峰电流分别为81μa、33μa、2μa、0.4μa。该结果表明:黄芩苷在cmk-8-gns@gce表现出响应电流是cmk-8@gce、gns-gce、gce电极是2.5倍、42倍、202.5倍。
68.通过以上(2)-(5)的比较实验表明,黄芩苷在cmk-8-gns@gce电极上电化催化性能最好。
69.实施例2
70.本实施例是在实施例1中制备cmk-8-gns@gce电极基础上,仅改变gns分散液与cmk-8分散液的混合体积比为1:1、1:2、1:3、1:4,但gns和cmk-8的总浓度依然保持2mg/ml,且混合分散液滴涂量仍为10μl。采用差分脉冲伏安法(dpv)测试不同体积比改性的cmk-8-gns@gce电极的响应电流。实验结果如图5所示,随着混合分散液中,cmk-8的体积比增加黄芩苷的峰电流响应也增大。但是,增大到在gns:cmk-8=1:3时达到最大,gns:cmk-8比例为1:1时最小,1:2和1:4时都低于gns:cmk-8=1:3时的响应电流。由此可见,在对gce电极进行修饰时,gns与cmk的最优复配比例是1:3。
71.实施例3
72.本实施例是在实施例1中制备cmk-8-gns@gce电极基础上,仅改变混合分散液的滴涂量为0μl、2μl、4μl、6μl、8μl、10μl、12μl,平行测定三次取平均值。混合分散液中,gns和cmk-8的总浓度依然保持2mg/ml。采用差分脉冲伏安法(dpv)测试取不同体积量的混合分散液涂覆改性的cmk-8-gns@gce电极的响应电流。
73.测试结果如图6所示,随着涂覆量增加,相应电流逐渐增大,在涂覆量为8-10μl,响应电流达到较大值,其中更优是10μl,此时响应电流达到最大值。当而涂覆量继续增加至12μl,反而会导致电极电阻增加,氧化峰电流发生下降。此外,涂覆量低于8μl时响应电流也较小。
74.实施例4
75.本实施例采用差分脉冲伏安法(dpv)测试不同ph值的pbs电解液对黄芩苷氧化峰电流的影响。测试条件为:配制ph=4、5、6、7、8、9的pbs缓冲溶液,将黄芩苷标准品溶于前述pbs溶液中,得到1.0
×
10-6
mol/l黄芩苷,每个设置3个平行。dpv测试条件均为:涂覆量10μl、以0.2m pbs缓冲溶液为电解液、富集电位为e=0.4v、富集时间t=860s、搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
76.结果如图7所示,在pbs缓冲溶液ph 4-7范围内,黄芩苷峰电流随ph增加而增加,在ph为7时峰电流达到最大。由于黄芩苷在碱性条件下易水解,故在ph>7时峰电流有所下降。因此,缓冲液最佳ph为7。
77.实施例5
78.本实施例采用差分脉冲伏安法(dpv)测试黄芩苷含量时,使用不同的富集电位所得到的峰电流。dpv测试条件均为:ph=7的pbs、1
×
10-6
mol/l黄芩苷、涂覆量10μl、以0.2m pbs缓冲溶液为电解液、富集电位为e=0v、0.2v、0.4v、0.6v、0.8v电位进行平行富集黄芩
苷、富集时间t=860s、搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
79.结果如图8a所示,随着富集电位的改变黄芩苷的峰电流也有所变化,但变化不具有线性关系。其中,在电位为0.4v时出现电流最高峰,大于0.4v和小于0.4v时峰电流都减小。
80.实施例6
81.本实施例采用差分脉冲伏安法(dpv)测试黄芩苷含量时,采用0.4v的恒定电位富集不同时长,再测试dpv曲线。dpv测试条件均为:ph=7的pbs、1
×
10-6
mol/l黄芩苷、涂覆量10μl、以0.2m pbs缓冲溶液为电解液、富集电位为e=0.4v恒电位富集黄芩苷、富集时间t=0s、260s、460s、660s、860s、960s、1060s进行平行实验,搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
82.结果如图8b所示,在富集860s前的峰电流随着富集时间的增加而增大,在860-960s峰电流都处于较大值,且在860s达到最大峰电流,860s后开始减小。因此最优富集时间确定为860s。
83.实施例7
84.本实施例采用差分脉冲伏安法(dpv)测试黄芩苷含量时,采用0.4v的恒定电位富集黄芩苷,在富集过程中采用不同的搅拌速度对黄芩苷电解液进行搅拌,富集时间为860s,再测试dpv曲线。dpv测试条件均为:ph=7的pbs、1
×
10-6
mol/l黄芩苷、涂覆量10μl、以0.2m pbs缓冲溶液为电解液、富集电位为e=0.4v恒电位富集黄芩苷、富集时间t=860s,搅拌速度为0r/min、500r/min、1000r/min、1500r/min、1800r/min、2000r/min进行平行实验,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
85.结果如图8c所示,随着搅拌速度的增加,峰电流也逐渐变大,在转速为1500-2000r/min时峰电流较大,在1500r/min时峰电流达到最大,超过1500-2000r/min后反而逐渐减小。究其原因,主要是搅拌速度过大,搅拌机震动强度也变大,测试环境不稳定,另一原因是搅拌太快气泡产生过多,占据了一部分富集位点,导致黄芩苷富集减少。因此,最优搅拌速度为1500r/min。
86.实施例8
87.本实施例采用cv测试研究不同扫描速率(v)对检测黄芩苷峰电流(i)的影响。测试条件为:黄芩苷浓度为1.0
×
10-6
mol/l,电解液为ph=7的pbs缓冲溶液中,采用0.05v/s、0.1v/s、0.15v/s、0.2v/s、0.25v/s、0.3v/s、0.35v/s、0.45v/s、0.55v/s、0.65v/s、0.75v/s、0.85v/s的扫描速率进行循环伏安测试。
88.实验结果如图9a所示,检测到的氧化还原峰电流随扫描速率增加而增大。由图9b可看出黄芩苷的电流响应与扫描速率呈现出良好的线性关系,氧化峰电流与扫速的线性方程为i
pa
=31.844+264.48υ(r=0.9978);还原峰电流与扫的线性方程为i
pc
=-33.229-202.99υ(r=0.9967)。实验结果显示了电流响应与扫描速率之间良好的线性关系,这表明黄芩苷在cmk-8-gns@gce上的电极反应主要受吸附作用控制过程。
89.实施例9
90.本实施例采用dpv测试研究黄芩苷在不同ph值下的电化学行为,结果如图9c所示。随着ph的增大,黄芩苷的氧化峰峰位置发生了负移,电流逐渐增大后减小,由图9d可知线性方程为ep=-0.043ph+0.4188(r=0.9918),线性的斜率与25℃可逆体系理论值-0.059v/ph相接近。这表明黄芩苷在电极上的反应过程为电子和质子数相等的氧化还原反应过程。推测黄芩苷在cmk-8-gns@gce上的氧化还原反应过程认为是2质子2电子参与的反应,反应机理如图10所示。
91.实施例10
92.本实施例采用dpv法在最优测试条件下测试不同浓度的黄芩苷在cmk-8-gns@gce上的dpv曲线,由图可看出随着黄芩苷浓度的增大,黄芩苷的氧化峰电流响应值也增大。最优测试条件为:ph=7的pbs、1
×
10-6
mol/l黄芩苷、涂覆量10μl、以0.2m pbs缓冲溶液为电解液、富集电位为e=0.4v恒电位富集黄芩苷、富集时间t=860s,搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
93.由图11a可以看出,可看出随着黄芩苷浓度的增大,黄芩苷的氧化峰电流响应值也增大。由图11b可看出黄芩苷的氧化峰电流在1.0
×
10-9
~3.2
×
10-6
mol/l范围内呈现出良好的线性关系,线性回归方程为i
pa
(μa)=0.4129c(nmol/l)+1.5404,r=0.9989,检出限为1.0
×
10-9
mol/l(s/n=3)。进一步说明使用本发明的检测方法检测黄芩苷的灵敏度高,检出限低。
94.实施例11
95.本实施例比较采用不同电化学检测方法对检测黄芩苷的优势。其中,dm-cd-gns@gce电极来自文献1;au-scnt@gce电极来自文献2;ddmimpf6@mwntse电极来自文献3;mos2@gce电极来自文献4。比较结果如下表:
[0096][0097]
注:dm-cd-gns@gce为2,6-二甲基-环糊精功能化修饰石墨烯杂化纳米片修饰的玻碳电极;ddmimpf6@mwntse为1-十二烷基-3-甲基咪唑六氟磷酸盐修饰多壁碳纳米管复合电极;mos2@gce为二硫化钼修饰的玻碳电极;au-scnt@gce为金和切短多壁碳纳米管修饰的玻碳电极。
[0098]
由上述比对可知,本发明的cmk-8-gns@gce电极在检测黄芩苷时,具有明显更低的检测限,线性范围主要集中在低浓度范围内,因此非常适合用于低浓度黄芩苷的定量检测。
[0099]
实施例12
[0100]
本实施例用于测试使用cmk-8-gns@gce电极的电化学传感器在检测黄芩苷时的重复性和稳定性。测试方法为:使用同一根cmk-8-gns@gce电极对浓度为1
×
10-6
mol/l的黄芩苷溶液在最优条件(参见实施例10)下进行dpv测试,平行测定7次。实验结果显示rsd为
2.57%,说明cmk-8-gns@gce电极具有良好的重现。cmk-8-gns@gce置于4℃的冰箱内48小时,再进行测定,发现对黄芩苷的检测几乎不存在影响。由此可见,cmk-8-gns@gce电极具有良好的稳定性。
[0101]
实施例13
[0102]
本实施例用于测试使用cmk-8-gns@gce电极的电化学传感器在检测黄芩苷时的抗干扰性能。测试方法为:选取一些常见的物质(包括cacl2、葡萄糖、黄嘌呤、维生素c和also4)对已知浓度的黄芩苷进行干扰,以测试电化学检测的抗干扰性。测试过程中,在含1
×
10-6
mol/l的黄芩苷工作体系中,分别加入了100倍浓度的cacl2、葡萄糖、黄嘌呤、维生素c和also4进行dpv检测。结果如图12所示,加入干扰物后黄芩苷的电流响应与在最优条件下的差别不大,证明了黄芩苷对这些干扰物有着良好的抗干扰能力。
[0103]
实施例14
[0104]
本实施例为采用cmk-8-gns@gce电极、对电极(钛棒)、参比电极(甘汞电极)组成电化学传感器,在最佳检测条件下对黄芩饮片中黄芩苷的含量进行实际检测。
[0105]
(1)待测样品制备:
[0106]
黄芩饮片研磨成细粉,过50目筛。称取1.0g黄芩粉末,以60%的乙醇为溶剂提取其中的黄芩苷。料液比为1:16混合,超声40min,离心4min,取上清液过0.22μm尼龙滤膜。滤渣再60%的乙醇超声40min,重复提取2次。合并三次滤液,用旋转蒸发仪旋蒸至晶体析出,除去全部乙醇。旋干后用10ml dmf复溶,制得黄芩苷样液。将上述样液稀释100倍后,得到待测样品。待测样品需溶解于电解液中再用传感器进行检测。
[0107]
(2)标准溶液的配制
[0108]
称取0.002g黄芩苷粉末于10ml容量瓶中,用dmf定容至刻度线,超声分散20min,即得0.002m的黄芩苷的标准溶液。
[0109]
(3)确定测试条件:涂覆量10μl(cmk-8:gns=3,总浓度2mg/ml)、以0.2m pbs缓冲溶液ph=7为电解液、富集电位为e=0.4v、富集时间t=860s、搅拌速度为1500r/min,测定参数为:电位区间在-1~0.4v,增幅为10mv,脉冲宽度为0.06s,取样间隔0.02s,脉冲周期0.5s,振幅为50mv,灵敏度100μa。
[0110]
(4)取样品溶液4μl加入20ml pbs缓冲溶液中进行dpv测试,检测出样液中黄芩苷浓度为102nm,计算出黄芩粉中黄芩苷含量的平均值为227.62mg/g。分别向样液中加入3个不同浓度的黄芩苷标准溶液,进行回收率实验,结果下表所示,测得加标回收率为113.5-116.9%,表明该方法对检测黄芩中提取的黄芩苷有效。
[0111][0112]
综上所述,本发明采用cmk-8和石墨烯复合修饰玻碳电极可以显著降低电极的电阻,增强黄芩苷在电极上的电流响应信号强度,提高电极对黄芩苷的响应灵敏度。此外,本发明还对实际检测条件进行了优化,得出了最佳条件为gns和cmk-8比例为1:3,总浓度为2mg/l、涂覆量10μl、缓冲液ph=7、富集电位为e=0.4v、富集时间t=860s、搅拌速度为
1500r/min。本发明的电化学传感器在检测黄芩中的黄芩苷含量适,表现出了很强的检测重复性和稳定性,具有极低的检测限,是一种可靠的具有发展前景的电化学检测方法。
[0113]
cmk-8本身因具有良好的介孔,对于吸附药物成分提供了较多附着位点;石墨烯因具有大比表面积和高导电率及电催化活性。石墨烯是碳纳米片,将其修饰在cmk-8的立体结构中可以让cmk-8的介孔不易因杂质或其他原因减小比表面积,也充当了介孔碳与介孔碳间连接的桥梁,减少电阻。混合后的cmk-8-gns的比表面积增大,从而增加了药物的附着位点,使反应更加灵敏。实验证明,在相同实验条件下,黄芩苷在cmk-8-gns@gce表现出响应电流是cmk-8@gce、gns-gce、gce电极是2.5倍、42倍、202.5倍。以gce电极的响应电流为基准,黄芩苷在cmk-8-gns@gce电极上的响应电流的增强倍数是cmk-8@gce、gns-gce二者乘积2倍。因此,采用cmk-8和gns联合修饰玻碳电极后,cmk-8和gns对电极检测灵敏度的增效产生了协同作用,超出了预期。
[0114]
实施例11中不同电极的记载文献:
[0115]
[1]wang f,lv m x,lu k,et al.electrochemical behaviors of baicalin at an electrochemically activated glassy carbon electrode and its determination in human blood serum[j].journal of the chinese chemical society,2012,59(7):829-835.
[0116]
[2]ji y l,wang g f,fang b.electrocatalysis and determination of baicalin at a nano-au single wall carbonnanotube modified electrode[j].chinese journal of analysis laboratory,2010,29(6):11-14.
[0117]
[3]刘冬菊.黄酮类化合物高灵敏电化学检测方法的研究[d].山东师范大学.2015.
[0118]
[4]chen g,zhang h w,ye j n.determination of baicalein,baicalin and quercetin in scutellariae radix and its preparations by capillary electrophoresis with electrochemical detection[j].talanta,2000,53(2):471-479.
[0119]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1