一种金属有机框架结构介孔碳纳米酶
1.本发明属于金属有机框架材料应用领域,具体涉及一种金属有机框架结构的介孔碳材料其纳米酶效应方面的应用。
背景技术:
2.天然酶是一种活细胞自身合成的,对特定底物起高效催化作用的物质。酶在特殊环境中变性或者解聚均可致其催化活性丧失,因此极大的限制了天然酶的应用范围。
3.mof全称metal organic framework,金属有机框架材料,是由无机金属通过共价键与有机配体键接形成的配合物。mof衍生物不仅能够整合多种催化活性中心,促进多功能催化,而且mof衍生物具有高选择性、高敏感性和使用方便的优点。虽然目前已将金属有机框架结构的介孔碳材料应用于诸多方面,然而在具有纳米酶效应的金属有机框架结构的介孔碳材料研究较少。
技术实现要素:
4.为了解决上述问题,本发明提供了一种金属有机框架结构的介孔碳材料在纳米酶效应方面的应用。研究表明,金属有机框架结构的介孔碳材料不仅在合成方面成品率优良,而且在特殊环境下依然具有活性,因而可以作为具有纳米酶效应的材料使用。本发明制备了掺杂fe的金属有机框架结构介孔碳材料,测试了其作为纳米酶使用时的催化性能的强弱,比如酸碱ph环境或是反应时间等。
5.本发明利用3,3',5,5'-四甲基联苯胺(tmb)作为显色底物,在h2o2共存的情况下,mof衍生物材料催化底物反应,加速tmb的氧化反应生成的蓝色产物氧化tmb(ox-tmb)。
6.具体地,本发明是通过如下所述的技术方案实现的:
7.本发明的第一个方面,提供了一种金属有机框架结构介孔碳纳米酶催化过氧化氢氧化的方法,包括:
8.将缓冲液、tmb、h2o2和fe/zn-n-c材料依次混合均匀,得到混合液;
9.将所述混合液在水浴中进行反应,使过氧化氢分解,即得。
10.本发明的第二个方面,提供了一种金属有机框架结构介孔碳纳米酶检测过氧化氢氧化的方法,包括:
11.将待测溶液、缓冲液、tmb和fe/zn-n-c材料依次混合均匀,得到混合液;
12.将所述混合液在水浴中进行反应,反应完成后,测试溶液的紫外吸收光谱图,根据不同h2o2量与tmb紫外吸收光谱图中峰值的对应关系,确定过氧化氢的浓度,即得。
13.本发明一个或多个技术方案具有以下有益效果:
14.1)本发明提出具有纳米酶效应的金属有机框架结构介孔碳对过氧化物酶底物3,3',5,5'-四甲基联苯胺催化氧化,在h2o2共存的情况下,加速tmb的氧化反应生成的蓝色产物氧化tmb(ox-tmb)。
15.2)本发明发现:以水浴时间作为变量的对照组中,随水浴时间增加峰信号强度逐
渐增加,而在十五分钟后,信号强度达到峰值,反应达到完全。
附图说明
16.构成本发明的一部分的说明书附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。以下,结合附图来详细说明本发明的实施方案,其中:
17.图1为实施例1的fe/zn-n-c制备示意图;
18.图2为实施例1制备完成的fe/zn-n-c的透射电子显微镜图(左),扫描电子显微镜图(右);
19.图3为实施例1制备完成的fe/zn-n-c的c、fe、zn、n元素分布区域图;
20.图4为实施例1制备完成的fe/zn-n-c的红外吸收光谱;
21.图5为实施例1制备完成的fe/zn-n-c的拉曼散射光谱;
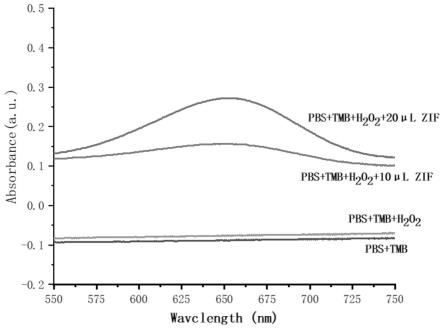
22.图6为实施例2验证制备完成的fe/zn-n-c纳米酶效应的紫外吸收光谱;
23.图7是实施例3中在不同ph值的pbs缓冲液中,fe/zn-n-c纳米酶催化h2o2诱导tmb显色的紫外吸收光谱图;
24.图8是实施例4中在水浴中,反应时间分别为0、5、10、15min值下,fe/zn-n-c纳米酶催化h2o2诱导tmb显色的紫外吸收光谱图;
25.图9是实施例5中fe/zn-n-c纳米酶催化不同含量的h2o2分别为100μl、300μl、500μl、700μl下诱导tmb显色的紫外吸收光谱图。
具体实施方式
26.下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件或按照制造厂商所建议的条件。
27.为了测定现有技术下制备的mof衍生物材料具有的纳米酶效应,多次改变实验条件进行多组对照测试。
28.本发明第一方面,制备fe/zn-n-c为现有技术,只要能制得具有一定框架结构的fe/zn-n-c的保护方法均可。在本发明一个或多个实施方式中,所述fe/zn-n-c的制备方法包括使用六水合硝酸锌、九水合硝酸铁、2-甲基咪唑按照试验方案混合。
29.在一些实施例中,所述金属有机框架材料的制备方法为:将六水合硝酸锌、九水合硝酸铁与2-甲基咪唑制成金属有机框架fe-zif-8。
30.在一些实施例中,对制备的fe-zif-8烧制,在惰性气氛下进行热解制成金属有机框架衍生物材料fe/zn-n-c,即得一种具有纳米酶效应的金属有机框架结构的介孔碳。
31.本发明第二方面,提供fe/zn-n-c催化过氧化氢分解,tmb氧化的验证性实验。对不同参数的体系进行对照,在分光光度计上收集紫外-可见吸收光谱。
32.本发明第三方面,提供三组不同变量的fe/zn-n-c催化tmb氧化的对照实验,包括mof衍生物材料的含量、水浴时间、h2o2含量,在分光光度计上收集紫外-可见吸收光谱。
33.在一些实施例中,缓冲液的ph值范围为5~9。
34.在一些实施例中,水浴中反应条件为30~35℃下反应5~15min。
35.在一些实施例中,所述过氧化氢的加入量为1
×
103~7
×
103mmol。
36.在一些实施例中,所述fe/zn-n-c材料的加入量为0.01~0.02mg。
37.在一些实施例中,所述fe/zn-n-c材料的制备方法为:将fe-zif-8在惰性气体保护下,煅烧,洗涤、冻干,即得。
38.在一些实施例中,所述煅烧的条件为900℃下,煅烧2~3h。
39.在一些实施例中,所述fe-zif-8的制备方法为:以六水合硝酸锌、九水合硝酸铁与2-甲基咪唑为原料,采用溶剂热法制备。
40.本发明第三方面,提供金属有机框架结构介孔碳的纳米模拟酶效应的验证性测试方法。
41.本发明第四方面,提供一种金属有机框架材料在检测过氧化氢领域中的应用,提供一种过氧化氢检测试剂或检测器。
42.在一些实施例中,在分光光度计上收集紫外-可见吸收光谱。
43.下面结合具体的实施例,对本发明做进一步的详细说明,应该指出,所述具体实施例是对本发明的解释而不是限定。
44.实施例1fe/zn-n-c的制备
45.如图1所示,制备方法步骤如下
46.将fe-zif-8的制备:首先用1.34g六水合硝酸锌和80mg硝酸铁溶解到65ml甲醇中形成溶液a。将3.0g的2-甲基咪唑溶解到65ml甲醇中,形成溶液b。将a液加入到b液中,连续均匀搅拌24小时,产物进行离心并用去离子水洗涤,随后进行冷冻干燥至粉末形态,此时得到产物为fe-zif-8。
47.在n2氛围保护下,900℃将fe-zif-8置于马弗炉中加热,煅烧2h,所得煅烧的产物用甲醇洗涤,并进行冷冻干燥至粉末形态,煅烧得到产物即为fe/zn-n-c。
48.图2为实施例1制得的fe/zn-n-c的扫描电子显微镜图,投射电子显微镜图。由图2分析可知,合成的金属有机框架结构的介孔碳有明显的十二面体形态,尺寸均一,有规整的框架结构。框架尺寸主要分布在150nm左右。在其外貌观察下合成的介孔碳材料经过煅烧呈现黑色粉末状态,不会出现聚集联结现象。
49.图3为实施例1制得的fe/zn-n-c中的c、fe、zn、n元素分布图,分析发现碳化后的材料结构分散,且fe、zn元素以均匀的状态复合于c、n元素之间,即分析得金属有机框架结构的介孔碳经过900℃碳化后的材料,fe、zn元素不会发生位点丢失,依然作为原子位点保持其状态。
50.图4为实施例1制得的fe/zn-n-c的红外吸收谱图,其中1585cm-1
和1241cm-1
的吸收峰来自于碳化后的骨架中的n-h弯曲震动以及c-n伸缩振动。与其他本体表征相结合,红外同时也对碳化后的材料进行了佐证。整体特征峰值较少,经过碳化后的材料减少了来自更多的官能团的影响,但依旧保持了主要原子位点的稳定,及其活性点的存在。
51.图5为实施例1制得的fe/zn-n-c的拉曼散射光谱。通过拉曼光谱研究烧制的碳材料的晶体结构及其石墨化的程度,d带(1367cm-1
)与g带(1582cm-1
)的相对强度比(id/ig)对应于数量缺陷,并且反映在sp2石墨碳原子的面内振动中。在较高温度下较高,id/ig比率表明高温下的碳化过程会导致材料的缺陷程度,产生的缺陷可以充当酶促反应的活性中心。石墨碳表面的大量缺陷选择性地促成了电子结构的变形,从而赋予碳化的fe/zn-n-c更优
异的纳米酶活性。
52.实施例2fe/zn-n-c在pbs缓冲液中催化过氧化氢氧化tmb,产生紫外吸收。
53.将实施例1制备的fe/zn-n-c于pbs缓冲液中催化过氧化氢氧化tmb。取四个试管进行材料具有纳米酶效应的测试:
54.取四个试管,第一个加入:2.75ml的ph值为7的缓冲液pbs,50μltmb(30mmol/l)溶液。第二个加入:2.75ml的ph值为7的缓冲液pbs,50μltmb(30mmol/l),100μlh2o2(10mmol/l)。第三个加入:2.75ml的ph值为7的缓冲液pbs,50μltmb(30mmol/l),100μlh2o2(10mmol/l),10μlfe/zn-n-c(1mg/ml)。第四个加入:2.75ml的ph值为7的缓冲液pbs,50μltmb(30mmol/l),100μlh2o2(10mmol/l),20μlfe/zn-n-c(1mg/ml)。
55.配置好的溶液在30℃水浴锅中平稳15min,使其充分反应,随后取出立即进行紫外吸收光谱测试。
56.首先通过图6紫外吸收光谱的对比发现:合成的fe/zn-n-c在催化过氧化氢氧化tmb方面具有明显的效应,其活性位点表现优异,且随着量的增加催化效果越明显。
57.实施例3不同ph值的pbs缓冲液中,tmb紫外吸收光谱图
58.利用ph计,用盐酸调配pbs将其ph值调配至5,用氢氧化钠调配pbs将其ph值调配至9。将实施例1制备的fe/zn-n-c在不同ph值的pbs缓冲液中催化过氧化氢氧化tmb。取六个试管分为两组:
59.a组三个试管,分别加入:1mg/ml的fe/zn-n-c溶液10μl,2.75ml缓冲液pbs(ph值分别为5、7、9),50μltmb(30mmol/l)溶液,100μlh2o2(10mmol/l)。所配置溶液在30℃水浴锅中平稳15min,使其充分反应,随后取出立即进行紫外吸收光谱测试。
60.b组三个试管,分别加入:1mg/ml的fe/zn-n-c溶液20μl,2.75ml缓冲液pbs(ph值分别为5、7、9),50μltmb(30mmol/l)溶液,100μlh2o2(10mmol/l)。配置好的溶液在30℃水浴锅中平稳15min,使其充分反应,随后取出立即进行紫外吸收光谱测试。
61.首先通过图7紫外吸收光谱,对比图7中(a)、(b)两图发现:fe/zn-n-c材料在ph为5偏酸性的环境下对过氧化氢催化氧化tmb的峰值更明显,说明fe/zn-n-c在偏酸性条件下的催化氧化tmb效果更加优异。当缓冲液环境为ph=7时,对比图7中(a)、(b)两张图发现,增大fe/zn-n-c材料用量会增强h2o2催化tmb的能力,并且对比图7中(a)、(b)两图ph为5的谱线也发现增加fe/zn-n-c材料用量的峰信号会更加明显。
62.在ph为9时增加与否fe/zn-n-c材料的含量,谱线并未发生明显变化趋势。这也说明了合成的fe/zn-n-c材料在催化过氧化氢氧化tmb方面偏碱性条件下催化性能受到限制。
63.实施例4不同水浴时间,tmb紫外吸收光谱图
64.取五个不同试管中加入2.75ml,ph为7的pbs缓冲液,50μltmb(30mmol/l),20μlfe/zn-n-c(1mg/ml),100μlh2o2(10mmol/l)。同时放入30℃水浴锅,反应时间分别为0、5、10、15min,随后立即取出测试进行紫外吸收光谱测试。
65.从图8可以得出水浴反应前10分钟,随时间增加峰信号强度逐渐增加。尤其在前五分钟内,吸收信号峰值有较大的跨越,即水浴时间能促进催化氧化的进程。10到15分钟吸收信号峰变化不明显,即反应基本达到完全。通过图8分析得出在10分钟左右达到理论催化效率最优,15分钟反应基本完成,而后催化效率受限于h2o2量,在实际测试中要选取合适的fe/zn-n-c材料以及h2o2用量的配比以达到最优催化效率。
66.实施例5不同h2o2量,tmb紫外吸收光谱图
67.于四个试管中分别加入2.75ml,ph为7的pbs缓冲液,50μltmb(30mmol/l),20μlfe/zn-n-c(1mg/ml),用移液枪分别移取100μl、300μl、500μl、700μlh2o2(10mmol/l)加入四个不同试管中。同时放入30℃水浴锅中稳定水浴15min,使其充分反应,随后取出立即进行测试的紫外吸收光谱图。
68.由图9可以得出随着h2o2量的梯次递增,紫外吸收峰出现明显的升高,但随着过氧化氢量递增,峰值增强范围变小,分析可得在反应平衡中增加了反应物的量,化学反应的动态平衡逆向移动。也体现了fe/zn-n-c在反应平衡中的纳米酶效应,在反应中承担了催化剂的功效而不实际参与化学变化过程。
69.以上所述仅为本技术的优选实施例而已,并不用于限制本技术,对于本领域的技术人员来说,本技术可以有各种更改和变化。凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1