复方氨基酸注射液中半胱氨酸与胱氨酸的检测方法与流程
1.本发明涉及药物领域,具体涉及复方氨基酸注射液中半胱氨酸与胱氨酸的检测方法。
背景技术:
2.氨基酸是构成人体营养所需蛋白质的基本物质,也是机体合成抗体、激素、酶类等其他分子的前体,在体内参与一系列代谢反应,是营养治疗的三大宏量营养素之一。
3.复方氨基酸注射液成分复杂,通常是由多种氨基酸组成,除8种必需氨基酸外,还有多种非必需氨基酸。半胱氨酸虽然是一种非必需氨基酸,但对于早产儿及足月儿、对于肝病患者来说,半胱氨酸是必需氨基酸。同时由于半胱氨酸易被氧化,可在处方中做抗氧剂存在。胱氨酸即半胱氨酸的氧化降解产物。
4.同时,半胱氨酸、乙酰半胱氨酸作为复方氨基酸注射液常用的组分,胱氨酸为其主要降解产物。
5.一方面,同时检测复方氨基酸注射液中胱氨酸与半胱氨酸的含量,可为产品工艺开发及产品存贮,为确保产品质量提供相关依据。另一方面,胱氨酸为复方氨基酸注射液中半胱氨酸等产生的杂质,含量很低,且胱氨酸难溶于水,难以准确测得其含量。再一方面,目前,现有技术(cn 111443151 a)中采用n-(1-芘基)马来酰亚胺乙腈溶液对半胱氨酸进行衍生后,采用荧光检测器进行测定的方法。该方法需要进行衍生化操作,采用荧光检测器检测。故该方法操作繁琐,对设备要求较高,方法可及性较差。
技术实现要素:
6.本发明提供一种可同时测定复方氨基酸注射液中半胱氨酸与胱氨酸的方法,该方法操作简单无需衍生,使用普通c18柱即可实现复方氨基酸注射液中众多组分与半胱氨酸及微量胱氨酸的分离,同时使用普通紫外检测器即可实现分析测定。该方法操作方便,重复性好,更经济。
7.一种复方氨基酸注射液中胱氨酸的检测方法,采用hplc法进行检测;其中,流动相a为硫酸铵缓冲液与甲醇按体积比(85-95):(15-5)的混合液;流动相b为甲醇;所述流动相a的ph值为1.3-3。
8.根据本发明实施例,所述流动相a为硫酸铵缓冲液与甲醇按体积比(88-92):(12-8)的混合液。
9.根据本发明实施例,所述流动相a为硫酸铵缓冲液与甲醇按体积比90:10的混合液。
10.根据本发明实施例,所述硫酸铵缓冲液中硫酸铵的浓度为0.1%-3%(体积分数,g/100ml),或者0.2%-2%,优选为0.5%。
11.根据本发明实施例,所述硫酸铵缓冲液中还含有庚烷磺酸钠;其中庚烷磺酸钠与硫酸铵的重量比为4:(2-8),或者4:(3-6),可选为4:5。
12.根据本发明实施例,可用盐酸、磷酸等调节流动相a的ph值,更优选用盐酸。
13.复方氨基酸注射液中氨基酸种类多,分离困难。本发明人意外的发现,通过控制流动相a的ph值,能够将微量胱氨酸的色谱峰与邻近氨基酸的峰很好的分离,并且胱氨酸的色谱峰的峰形好,可以显著提高微量胱氨酸的测试灵敏度和准确性。
14.进一步地,本发明人还研究发现,通过控制流动相a(即硫酸铵缓冲液)的ph值为1.3-1.7,可以提高半胱氨酸与临近氨基酸峰的分离度,提高半胱氨酸测试的准确度。ph超过该范围不能将半胱氨酸准确分离。在该ph范围内可实现半胱氨酸和胱氨酸的同时检测,且二者的分离度很高。在一些实施例,控制流动相a(即硫酸铵缓冲液)的ph值为1.3、1.4、1.5、1.6或1.7。
15.由于复方氨基酸注射液中半胱氨酸易被氧化成胱氨酸,因此影响半胱氨酸和胱氨酸检测结果的准确性。本发明人意外地发现,通过向复方氨基酸注射液中加入盐酸,可以提高微量半胱氨酸和胱氨酸的测试稳定性,重复测试稳定性高。
16.在一些实施例,向复方氨基酸注射液中加入盐酸;可选地,盐酸的浓度为0.1mol/l-1mol/l。
17.根据本发明实施例,可以使用以十八烷基硅烷键合硅胶为填充剂的色谱柱(phenomenex gemini c18,4.6
×
250mm,5μm)。
18.根据本发明实施例,采用梯度洗脱,梯度洗脱程序为:
19.时间(分钟)流动相a(%)流动相b(%)085-9515-51585-9515-52345-5555-452885-9515-54585-9515-5
20.根据本发明实施例,采用梯度洗脱,梯度洗脱程序为:
21.时间(分钟)流动相a(%)流动相b(%)088-9212-81588-9212-82348-5252-482888-9212-84588-9212-8
22.根据本发明实施例,采用梯度洗脱,梯度洗脱程序为:
23.时间(分钟)流动相a(%)流动相b(%)09010159010235050289010459010
24.研究发现,若改变以上梯度洗脱程序则不能保证半胱氨酸、胱氨酸的分离度。
25.根据本发明实施例,流速为每分钟0.8-1.2ml,例如0.8ml、1.0ml、1.2ml。
26.根据本发明实施例,检测波长为200-210nm,例如200nm、205nm、210nm。
27.根据本发明实施例,柱温为35-45℃,例如35℃、40℃、45℃。
28.在一些实施例,流速为每分钟1.0ml;波长为205nm;柱温为40℃;进样量10μl。
29.在一些实施例,对照品溶液:取盐酸半胱氨酸对照品适量,精密称定,加溶剂(1m盐酸)溶解并定量稀释制成含盐酸半胱氨酸2.0-120.0μg/ml的溶液。
30.在一些实施例,取盐酸胱氨酸对照品适量,精密称定,加溶剂(1m盐酸)溶解并定量稀释制成含盐酸胱氨酸2.0μg/ml的溶液。
31.在一些实施例,将复方氨基酸注射液加盐酸稀释(例如10-20倍)后作为供试品溶液。
32.在一些实施例,按外标法以峰面积进行供试品溶液中的胱氨酸与半胱氨酸的含量。
33.本发明至少具有以下技术效果之一:
34.1)相对于现行技术,本发明中将供试品及对照品溶液的配制方式进行改进,采用1m盐酸溶解各样品,无需衍生,操作简单。
35.2)相对于现行技术,本发明采用紫外检测器进行复方氨基酸注射液中的胱氨酸与半胱氨酸的含量检测,可及性高,操作性更强,经济性好。
36.3)改进后的方法可用于不同组成的复方氨基酸注射液中的胱氨酸与半胱氨酸的含量检测,重现性好,普适性强。
附图说明
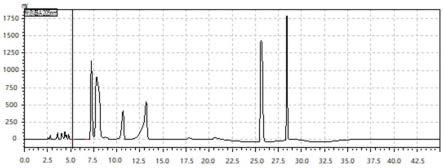
37.图1:实施例1中复方氨基酸注射液样品图(完整图)。
38.图2:实施例1中复方氨基酸注射液样品图(局部图)。
39.图3:实施例2中复方氨基酸注射液样品图(完整图)。
40.图4:实施例2中复方氨基酸注射液样品图(局部图)。
41.图5:实施例3中复方氨基酸注射液样品图(完整图)。
42.图6:实施例3中复方氨基酸注射液样品图(局部图)。
43.图7:实施例4中复方氨基酸注射液样品图(完整图)。
44.图8:实施例4中复方氨基酸注射液样品图(局部图)。
45.图9:实施例5中复方氨基酸注射液样品图(完整图)。
46.图10:实施例5中复方氨基酸注射液样品图(局部图)。
47.图11:实施例6中复方氨基酸注射液样品图(完整图)。
48.图12:实施例6中复方氨基酸注射液样品图(局部图)。
49.图13:实施例7中复方氨基酸注射液样品图(完整图)。
50.图14:实施例7中复方氨基酸注射液样品图(局部图)。
51.图15:实施例8中复方氨基酸注射液样品图(完整图)。
52.图16:实施例8中复方氨基酸注射液样品图(局部图)。
53.图17:实施例9中复方氨基酸注射液样品图(完整图)。
54.图18:实施例9中复方氨基酸注射液样品图(局部图)。
55.图19:实施例10中复方氨基酸注射液样品图(完整图)。
56.图20:实施例10中复方氨基酸注射液样品图(局部图)。
57.图21:对比例1中胱氨酸对照品溶液图谱(完整图)。
58.图22:对比例2中复方氨基酸注射液样品图(完整图)。
59.图23:对比例3中复方氨基酸注射液样品图(完整图)。
具体实施方式
60.以下实施例用于说明本发明,但不用来限制本发明的范围。实施例中未注明具体技术或条件者,按照本领域内的文献所描述的技术或条件,或者按照产品说明书进行。所用试剂或仪器未注明生产厂商者,均为可通过正规渠道商购买得到的常规产品。
61.实施例1
62.对照品溶液:盐酸半胱氨酸对照品:精密称定盐酸半胱氨酸对照品35mg,置100ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。精密量取5ml置50ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。
63.胱氨酸对照品:精密称定胱氨酸对照品10mg,置100ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。精密量取5ml置50ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。
64.供试品溶液:取市售复方氨基酸注射液(18aa
‑ⅶ
)1ml置10ml量瓶中,加1mol/l盐酸溶液稀释至刻度。
65.色谱柱:以十八烷基硅烷键合硅胶为填充剂的色谱柱(phenomenex gemini c18,4.6
×
250mm,5μm)。
66.流动相:以硫酸铵缓冲液与甲醇按体积比90:10的混合液为流动相a;以甲醇为流动相b。
67.硫酸铵缓冲液制备方法:取硫酸铵5.0g和庚烷磺酸钠4.0g,加水1000ml溶解,用盐酸调节ph值至1.5。
68.梯度洗脱程序为:
69.时间(分钟)流动相a(%)流动相b(%)09010159010235050289010459010
70.流速为每分钟1.0min;波长为205nm;柱温为40℃;进样量10μl。对照品溶液与供试品溶液分别进样,按外标法以峰面积进行供试品溶液中的胱氨酸与半胱氨酸的含量。检测结果见图1和图2。
71.供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0072][0073]
1.重复性
[0074]
对照品溶液:盐酸半胱氨酸对照品:精密称定盐酸半胱氨酸对照品35mg,置100ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。精密量取5ml置50ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。
[0075]
供试品溶液:取市售复方氨基酸注射液(18aa
‑ⅶ
)1ml置10ml量瓶中,加1mol/l盐酸溶液稀释至刻度(平行配制六份)。
[0076]
供试品溶液中半胱氨酸检出量的重复性结果见下表:
[0077][0078]
2.准确度
[0079]
盐酸半胱氨酸贮备液:精密称定盐酸半胱氨酸对照品35mg,置100ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。
[0080]
对照品溶液:精密量取盐酸半胱氨酸贮备液5ml,置50ml量瓶中,加1mol/l盐酸溶液稀释至刻度,摇匀。
[0081]
低浓度回收率溶液(50%):精密量取空白辅料1ml,置10ml量瓶中,精密加入盐酸半胱氨酸贮备液0.5ml,加1mol/l盐酸稀释至刻度,摇匀,作为低浓度的供试品溶液。平行配制3份。
[0082]
中浓度回收率溶液(100%):精密量取空白辅料1ml,置10ml量瓶中,精密加入盐酸半胱氨酸贮备液1ml,加1mol/l盐酸稀释至刻度,摇匀,作为低浓度的供试品溶液。平行配制3份。
[0083]
高浓度回收率溶液(150%):精密量取空白辅料1ml,置10ml量瓶中,精密加入盐酸半胱氨酸贮备液1.5ml,加1mol/l盐酸稀释至刻度,摇匀,作为低浓度的供试品溶液。平行配制3份。
[0084]
供试品溶液中半胱氨酸准确度的结果见下表:
[0085][0086]
实施例2
[0087]
本实施例与实施例1的区别仅在于:供试品溶液:取市售小儿复方氨基酸注射液(19aa
‑ⅰ
)5ml置10ml量瓶中,加1mol/l盐酸溶液稀释至刻度。
[0088]
检测结果见图3和图4。
[0089]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0090][0091]
实施例3
[0092]
本实施例与实施例1的区别仅在于:流速为每分钟0.8min;波长为205nm;柱温为40℃;进样量10μl。
[0093]
检测结果见图5和图6。
[0094]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0095][0096]
实施例4
[0097]
本实施例与实施例1的区别仅在于:流速为每分钟1.2min;波长为205nm;柱温为40℃;进样量10μl。
[0098]
检测结果见图7和图8。
[0099]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0100][0101]
实施例5
[0102]
本实施例与实施例1的区别仅在于:流速为每分钟1.0min;波长为205nm;柱温为35℃;进样量10μl。
[0103]
检测结果见图9和图10。
[0104]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0105][0106]
实施例6
[0107]
本实施例与实施例1的区别仅在于:流速为每分钟1.0min;波长为205nm;柱温为45℃;进样量10μl。
[0108]
检测结果见图11和图12。
[0109]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0110][0111]
实施例7
[0112]
本实施例与实施例1的区别仅在于:流速为每分钟1.0min;波长为200nm;柱温为40℃;进样量10μl。
[0113]
检测结果见图12和图14。
[0114]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0115][0116]
实施例8
[0117]
本实施例与实施例1的区别仅在于:流速为每分钟1.0min;波长为210nm;柱温为40℃;进样量10μl。
[0118]
检测结果见图15和图16。
[0119]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0120][0121]
实施例9
[0122]
本实施例与实施例1的区别仅在于:流动相中硫酸铵缓冲液制备方法:取硫酸铵5.0g和庚烷磺酸钠4.0g,加水1000ml溶解,用盐酸调节ph值至1.3。
[0123]
检测结果见图17和图18。
[0124]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0125][0126]
实施例10
[0127]
本实施例与实施例1的区别仅在于:流动相中硫酸铵缓冲液制备方法:取硫酸铵5.0g和庚烷磺酸钠4.0g,加水1000ml溶解,用盐酸调节ph值至1.7。
[0128]
检测结果见图19和图20。
[0129]
供试品溶液中半胱氨酸色谱峰与胱氨酸色谱峰的参数见下表:
[0130][0131]
对比例1
[0132]
与实施例1的区别仅在于:供试品溶液不加入盐酸,仅用纯净水稀释10倍;胱氨酸对照品溶液用水定量稀释制成10μg/ml。
[0133]
结果发现,胱氨酸对照品溶液胱氨酸峰形异常,且放置后析出。检测结果见图21。
[0134]
对比例2
[0135]
与实施例1的区别仅在于:流动相a中不含有庚烷磺酸钠。
[0136]
结果发现,各氨基酸出峰较早,半胱氨酸与其他氨基酸不能完全分离,且胱氨酸与其后氨基酸不能有效分离。检测结果见图22。
[0137]
对比例3
[0138]
与实施例1的区别仅在于:流动相a中不含有甲醇。
[0139]
结果发现,胱氨酸出峰时间延后,且胱氨酸与其后氨基酸不能有效分离。检测结果见图23。
[0140]
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1