一种乙肝抗体阳性B细胞对于乙肝疫苗的抗体分泌作用测试方法与流程
一种乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用测试方法
技术领域
1.本发明涉及乙型肝炎和其他传染病的免疫治疗,包括免疫细胞治疗和免疫因子治疗,疫苗开发研究的应用。具体涉及诱导模板,诱导方法和传染病,肿瘤等多种疾病的细胞治疗,免疫治疗和疫苗开发等技术领域,具体为一种乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用测试方法。
背景技术:
2.随着分子生物学和转基因技术的发展,利用合理的转基因技术,可以定向某些细胞的靶向性,比如,cart治疗肿瘤,只要肿瘤抗原是特异的,理论上就可以获得良好的治疗效果。同样技术也可以用于传染病治疗方法的开发。生物技术的发展为治疗乙肝开辟了广阔的希望。国内外自从90年代,尝试多种生物制剂治疗乙肝,如亚单位治疗性疫苗,基因治疗,细胞免疫治疗等。但是,并未取得突破,直至 2008年,我国经过了三期临床试验的四种治疗性生物制剂,均未达到预期的治疗效果。细胞免疫治疗,大多是以体外经过淋巴因子诱导 dc细胞,尝试打破乙肝患者类似于免疫耐受机制,但是,效果不确切。
3.最近,出自于基因编辑技术,是患者自身杀伤性t细胞具有对乙肝病毒的特异性结合和清除能力;irna技术研制的旨在抑制乙肝病毒转录过程,从而达到彻底杀灭病毒目的,已经进入临床试验阶段;然而,至今为止,上述疗法都与感染乙肝后的自然免疫清除差距甚远。
4.乙肝感染者大多以来自身的免疫系统而自然清除,最关键的标志是能够产生抗乙肝病毒表面抗体,然而,时至今日,并没有在这方面有突破性进展。从过去的细胞免疫治疗实践,以体外激活dc的思路,没有获得理想效果,这与我们对于乙肝发病机制的了解还不透彻,或者没有研究到关节点,至今,没有理想的乙肝动物模型,都有不同的理解。
5.免疫治疗在理论上应该是最有效的,目前主要思路就是激活抗病毒相关的免疫细胞,如tc,nk,lak和b细胞,其中tc,nk和lak的激活治疗方法已经有20年应用历史,效果不确切,而激活b细胞,产生抗乙肝病毒的保护性抗体,仍然是空白。
技术实现要素:
6.(一)解决的技术问题
7.针对现有技术的不足,本发明提供了一种乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用测试方法,具备更有效的激活b细胞和产生抗乙肝病毒的保护性抗体等优点,解决了上述背景技术中所提到的问题。
8.(二)技术方案
9.为实现上述目的,本发明提供如下技术方案:一种乙肝抗体阳性 b细胞对于乙肝疫苗的抗体分泌作用测试方法,包括以下步骤:
10.1)动物分组及剂量:实验动物分组方法:雌、雄动物分别按体重进行分层随机分
组,共分为3组:阳性对照组4只,细胞治疗小剂量组4只,,细胞治疗大剂量组2只,雌雄各半。
11.2)给药相关信息及剂量:给药途径及方法:细胞回输采用静脉注射;给药途径的选择理由:与临床给药途径一致;给药频率及期限:细胞治疗组各只动物均采用单次细胞回输,所有动物乙肝疫苗注射4 次。
12.3)剂量设计:因为此细胞治疗方法没有相关参考文献,所以,根据委托方建议的给药剂量,以60公斤体重人体治疗剂量为单次 1x108细胞,推算本实验食蟹猴给药剂量应该为:1.6x106cells/kg,由于是毒理学研究预实验,采用小剂量组相对等于人类单次治疗剂量,大剂量组为小剂量组5倍。
13.4)基因诱导淋巴细胞体外培养对hbsag的清除方法:
14.试验方法:体外细胞培养法;细胞来源:细胞治疗组动物;细胞处理:非病毒载体基因诱导;阳性对照:来源于阳性对照组pbmc;阴性对照:来源于细胞治疗组pbmc,未经基因诱导。
15.5)自体基因诱导淋巴细胞回输后,血清hbsab产生情况:
16.采血动物:所有动物;采血时间:给药前、首次给药后第2、4 周、8周;采血部位:动物前肢或后肢静脉;采血量及抗凝剂:用惰性分离胶促凝管采集血液约1ml。
17.6)外周血t、b淋巴细胞表型测定:采血动物:所有动物;采血时间:给药前、首次免疫后d15和d24;采血部位:动物前肢或后肢静脉;采血量及抗凝剂:用edta
·
k2真空采血管采集血液约1ml;样品标识:各样品标有专题编号、动物编号、试验天数、样本类型及采集日期;样品的保存与运输:血液样品在采集后室温放置,于2h 内送免疫部检测。
18.优选的,所述在含有乙肝疫苗2ng/ml培养基培养第五天,检测上清中hbsag滴度,1001号动物基因诱导淋巴细胞在1/16稀释后出现阴性结果,非基因诱导自身淋巴细胞在1/64才转阴性,表3。在含有乙肝疫苗4ng/ml培养基培养第10天,检测上清中hbsag滴度, 2003号动物基因诱导淋巴细胞在1/256倍稀释时出现阴性孔,1/1024 时完全转阴,而非基因诱导自身淋巴细胞无转阴孔。
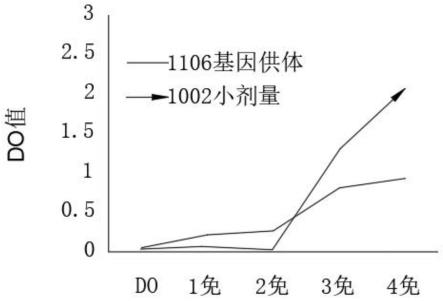
19.优选的,所述体外基因诱导后的淋巴细胞自体回输后,开始为抑制作用,表现为抗体生成时间延迟,1免疫和2免后血清hbsab水平低于阳性基因模板供体动物;到3免,4免,基因诱导的淋巴细胞自体回输动物的hbsab水平呈跳跃式升高,明显高于阳性基因模板供体动物。大剂量组比小剂量组的抑制作用阶段稍强,3免后的hbsab跳跃式抗体分泌增强作用大小剂量组无明显差异。
20.优选的,所述给药前(d0)、及细胞回输后各个时间点比较,t/b 淋巴细胞(cd3/cd4,cd3/cd8和cd20)表型,自身比较和各组比较,除cd3在小剂量组有轻度降低趋势以外,大剂量组无类似变化,总和分析t/b淋巴细胞表型检测结果,各组动物没有明显变化。
21.优选的,所述给药相关信息及剂量恢复期:无;给药时间:09: 03~15:49;给药体积:10ml/只;给药速率:3ml/min。
22.优选的,所述培养基:淋巴细胞专用培养基,含乙肝疫苗2ng/ml 和4ng/ml;培养条件:50000细胞/孔,复孔,接种96孔板,37℃, 5%co2,共培养10天。
23.优选的,所述样本的保存与运输:血液在采集后放入样品运输箱, 2h内送临检部门检测;测定方法:采用成品elisa试剂盒,od值》0.1 为阳性。
24.优选的,所述标本采集:分别于d5和d10离心,收集上清;检测指标:hbsag滴度;检
测方法:采用成品elisa试剂盒。
25.优选的,所述检测指标:外周血t细胞(cd3+)、t细胞亚群 (cd3+cd4+,cd3+cd8+)、b细胞(cd3-cd20+);检测方法:流式细胞仪。
26.(三)有益效果
27.与现有技术相比,本发明提供了一种乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用刺激方法,具备以下有益效果:
28.该乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用刺激方法,通过对食蟹猴静脉注射自体基因诱导淋巴细胞后,初期为轻度抑制作用,表现为抗体产生时间延迟,滴度较阳性对照组少许减弱,可能原因如下:
①
基因诱导淋巴细胞具有清除乙肝疫苗对应抗原的作用,导致有效免疫剂量降低,抗体产生反应减弱。
②
基因诱导与自然对应基因作用相互抑制。随着时间和免疫次数增加,在3免以后(回输后大约1个月以后),淋巴细胞自体回输动物的抗体生成反应呈跳跃式升高,甚至明显高于阳性对照组(数倍以上),本发明没有病毒载体基因转录或其他载体基因编辑方法,却具有激活抗体分泌b细胞的作用。
附图说明
图1为本发明1106与1002对比结构示意图;图2为本发明2018与2004对比结构示意图;图3为本发明1005与9对比结构示意图;图4为本发明2018与10结构示意图。
具体实施方式
29.下面将结合本发明的实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
30.根据图1-4与表2-6,一种乙肝抗体阳性b细胞对于乙肝疫苗的抗体分泌作用测试方法,包括以下步骤:
31.1)动物分组及剂量:实验动物分组方法:雌、雄动物分别按体重进行分层随机分组,共分为3组:阳性对照组4只,细胞治疗小剂量组4只,,细胞治疗大剂量组2只,雌雄各半。
32.2)给药相关信息及剂量:给药途径及方法:细胞回输采用静脉注射;给药途径的选择理由:与临床给药途径一致;给药频率及期限:细胞治疗组各只动物均采用单次细胞回输,所有动物乙肝疫苗注射4 次。
33.3)剂量设计:因为此细胞治疗方法没有相关参考文献,所以,根据公认的人体自体免疫细胞治疗剂量,以60公斤体重人体治疗剂量为单次1x108细胞,推算本实验食蟹猴给药剂量应该为: 1.6x106cells/kg,采用小剂量组相对等于人类单次治疗剂量,大剂量组为小剂量组5倍。
34.4)基因诱导淋巴细胞体外培养对hbsag的清除方法:
35.试验方法:体外细胞培养法;细胞来源:细胞治疗组动物;细胞处理:非病毒载体基因诱导;阳性对照:来源于阳性对照组pbmc;阴性对照:来源于细胞治疗组pbmc,未经基因诱
导。
36.5)自体基因诱导淋巴细胞回输后,血清hbsab产生情况:
37.采血动物:所有动物;采血时间:给药前、首次给药后第2、4 周、8周;采血部位:动物前肢或后肢静脉;采血量及抗凝剂:用惰性分离胶促凝管采集血液约1ml(结合长期毒性试验血液生化指标测定进行,不单独采集)。
38.6)外周血t、b淋巴细胞表型测定:采血动物:所有动物;采血时间:给药前、首次免疫后d15和d24;采血部位:动物前肢或后肢静脉;采血量及抗凝剂:用edta
·
k2真空采血管采集血液约1ml;样品标识:各样品标有专题编号、动物编号、试验天数、样本类型及采集日期;样品的保存与运输:血液样品在采集后室温放置,于2h 内送免疫部检测。
39.在含有乙肝疫苗2ng/ml培养基培养第五天,检测上清中hbsag 滴度,1001号动物基因诱导淋巴细胞在1/16稀释后出现阴性结果,非基因诱导自身淋巴细胞在1/64才转阴性,表3。在含有乙肝疫苗 4ng/ml培养基培养第10天,检测上清中hbsag滴度,2003号动物基因诱导淋巴细胞在1/256倍稀释时出现阴性孔,1/1024时完全转阴,而非基因诱导自身淋巴细胞无转阴孔。
40.体外基因诱导后的淋巴细胞自体回输后,开始为抑制作用,表现为抗体生成时间延迟,1免疫和2免后血清hbsab水平低于阳性基因模板供体动物;到3免,4免,基因诱导的淋巴细胞自体回输动物的 hbsab水平呈跳跃式升高,明显高于阳性基因模板供体动物。大剂量组比小剂量组的抑制作用阶段稍强,3免后的hbsab跳跃式抗体分泌增强作用大小剂量组无明显差异。
41.给药前(d0)、及细胞回输后各个时间点比较,t/b淋巴细胞 (cd3/cd4,cd3/cd8和cd20)表型,自身比较和各组比较,除cd3 在小剂量组有轻度降低趋势以外,大剂量组无类似变化,总和分析 t/b淋巴细胞表型检测结果,各组动物没有明显变化。
42.给药相关信息及剂量恢复期:无;给药时间:09:03~15:49;给药体积:10ml/只;给药速率:3ml/min。
43.培养基:淋巴细胞专用培养基,含乙肝疫苗2ng/ml和4ng/ml;培养条件:50000细胞/孔,复孔,接种96孔板,37℃,5%co2,共培养10天。
44.样本的保存与运输:血液在采集后放入样品运输箱,2h内送临检部门检测;测定方法:采用成品elisa试剂盒,od值》0.1为阳性。
45.标本采集:分别于d5和d10离心,收集上清;检测指标:hbsag 滴度;检测方法:采用成品elisa试剂盒。
46.检测指标:外周血t细胞(cd3+)、t细胞亚群(cd3+cd4+, cd3+cd8+)、b细胞(cd3-cd20+);检测方法:流式细胞仪。
47.自体基因诱导淋巴细胞回输后血清hbsab产生情况:体外基因诱导后的淋巴细胞自体回输后,开始为轻微抑制作用,表现为抗体生成时间延迟,1免疫和2免后血清hbsab水平低于阳性基因模板供体动物;到3免,4免,基因诱导的淋巴细胞自体回输动物的hbsab水平呈跳跃式升高,明显高于阳性基因模板供体动物(数倍以上)。大剂量组比小剂量组的抑制作用阶段稍强,3免后的hbsab跳跃式抗体分泌增强作用大小剂量组无明显差异。(图1-4,看附图)
48.外周血t、b淋巴细胞表型:给药前(d0)、及细胞回输后各个时间点比较,t/b淋巴细
胞(cd3/cd4,cd3/cd8和cd20)表型,自身比较和各组比较,除cd3在小剂量组有轻度降低趋势以外,大剂量组无类似变化,总和分析t/b淋巴细胞表型检测结果,各组动物没有明显变化,详细结果见表5-6。
49.表2.组别和计量
[0050][0051]
表3.含有乙肝疫苗2ng/ml培养第五天上清中hbsag滴度
[0052][0053]
表4.含有乙肝疫苗4ng/ml培养第10天上清中hbsag滴度
[0054][0055]
表5.自体基因诱导淋巴细胞回输后cd3和cd20细胞变化
[0056]
[0057][0058]
表6.自体基因诱导淋巴细胞回输后cd4和cd8细胞变化
[0059][0060]
结论:本实验发现基因诱导淋巴细胞体外培养具有清除乙肝病毒表面抗原的作用,提示临床应用具有特异性清除乙肝病毒的能力。
[0061]
在本试验条件下,食蟹猴静脉注射自体基因诱导淋巴细胞后,对于常规乙肝疫苗的反应减弱,首先是抑制作用,表现为抗体产生时间延迟,滴度较阳性对照组减弱,可能原因如下:
①
基因诱导淋巴细胞具有清除乙肝疫苗对应抗原的作用,导致有效免疫剂量降低,抗体产生反应减弱,
②
基因诱导与自然对应基因作用相互抑制,随着时间和免疫次数增加,在3免以后(回输后大约1个月以后),淋巴细胞自体回输动物的抗体生成反应呈跳跃式升高,甚至明显高于阳性对照组,对于这一现象的解释,目前缺乏文献支持,但是,从现有数据分析,基因诱导的自体淋巴细胞回输,没有造成t/b淋巴细胞亚群的明显变化,只是增强了对于乙肝疫苗免疫后的抗体分泌功能,意味着临床治疗的突破,至今为止,没有类似研究报道。
[0062]
本研究利用抗乙肝抗体阳性健康者作为诱导模板,与其他基因编辑技术不同,本
研究没有病毒载体基因转录或其他载体基因编辑方法,却具有激活抗体分泌b细胞的作用,技术细节属于核心机密,暂时不予公布。
[0063]
尽管已经示出和描述了本发明的实施例,对于本领域的普通技术人员而言,可以理解在不脱离本发明的原理和精神的情况下可以对这些实施例进行多种变化、修改、替换和变型,本发明的范围由所附权利要求及其等同物限定。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1