一种血液总轻链定标品、试剂盒及应用的制作方法
1.本发明涉及检测试剂技术领域,更具体的说是涉及一种血液总轻链定标品、试剂盒及应用。
背景技术:
2.血液中的免疫球蛋白轻链(light chain简写lc),分为依靠二硫键结合于重链上的结合型轻链(binding lc简写blc),以及处于游离状态的游离轻链(free lc简写flc)。血清总轻链total lc,简写tlc=blc+flc
3.血清flc在骨髓瘤以及轻链沉积病等多种疾病中有重要临床意义
4.血液tlc检测,作为多种疾病的辅助诊断+指标,目前在大型三甲医院的检验科广泛开展。但几乎都被德国西门子公司的bnii检测系统及配套试剂,以及美国贝克曼库尔特bc的im800检测系统及配套试剂,以及瑞士罗氏公司的cobas检测系统及配套试剂垄断;其中西门子bnii的lc检测试剂最为主流。国内仅有少量公司有相关检测试剂盒,如宁波普瑞柏公司,重庆博士泰公司等,但是其检测结果和西门子lc差别颇大。
5.例如,如图1“轻链lc lambda临床比对”,相关系数不足0.6。
6.现有的有关lc专利没有提及如何解决临床结果一致性问题,仅仅是解决试剂灵敏度及检测便捷性。
7.此外,目前常见的商用总轻连检测抗体如dako公司(美国安捷伦旗下)的kappa&lambda lc兔多克隆抗体,货号q0498&q0499,以及日本nittobo公司的kappa&lambda lc羊多克隆抗体;商用游离轻链抗体如dako公司(美国安捷伦旗下)的kappa&lambdaflc兔多克隆抗体,货号a0100&a0101。
8.tlc检测,目前所有试剂均采用免疫比浊法或者胶乳免疫比浊法。检测lc的抗体分为:
9.bindingsite antibody,仅识别lc与免疫球蛋白重链结合面表位的抗体,简写bs-ab;
10.outsite antibody,识别lc不与免疫球蛋白重链结合的外表面表位的抗体,简写os-ab;
11.其中bs-ab为flc检测抗体;
12.总轻连的检测抗体实质是bs-ab和os-ab的混合物,bs-ab:os-ab一般的比例在1:1左右,比如q0498&q0499;
13.而a0100&a0101则几乎全为bs-ab。
14.原理上,免疫比浊和胶乳免疫比浊,是通过浊度信号值高低(透射检测为吸光度,散射检测为散射光强度)与已知浓度的被测物(定标品)建立对应关系(标准曲线),再对未知浓度的样品进行检测,通过样品浊度信号值高低由自动化仪器根据标准曲线自动计算被测物浓度。
15.检测准确度:nmpa一般允许的检测偏差为
±
15%
16.但是,tlc检测中,大约的,一个单位的blc只能形成一个单位的浊度;但一个单位的单体flc能形成3个单位的浊度,一个单位的二聚体flc大约能形成3个单位的浊度
……
;可以理解,不同样本中,如果blc,flc单体,二聚体,多聚体含量不一致,将导致浊度与浓度的对应关系乱套,检测偏差远超过nmpa允许的
±
15%;
17.血液中tlc,正常人flc含量很少,约为tlc的1~2%,研究发现,对于flc相关各种疾病不同阶段,这个含量会发生变化,从2%增长到50%;
18.血液tlc检测时,blc和flc形成浊度能力差异的问题,正常人和病患,不同病患间blc和flc含量差异,导致浓度与浊度对应关系混乱问题无法解决。
19.因此,如何提供一种血液总轻链定标品、试剂盒及应用,克服上述技术障碍是本领域技术人员亟需解决的问题。
技术实现要素:
20.有鉴于此,本发明提供了一种血液总轻链定标品、试剂盒及应用。
21.申请人前期研究通过buffer中高nacl以及试剂中高表面活性剂tw-20解决了flc检测的临床结果问题,现在推测可能为通过上述极端条件将被测物中flc二聚体,多聚体解离成单体进行检测,在tlc检测中可以直接借鉴。
22.为了实现上述目的,本发明采用如下技术方案:
23.一种血液总轻链定标品,包括:lambda lc定标品和kappa lc定标品;lambda lc定标品浓度分别为1.5g/l、4g/l、7g/l、11g/l;
24.kappa lc定标品浓度分别为2.00g/l、5.00g/l、9.00g/l、15.00g/l;
25.lambda lc定标品浓度为1.5g/l时,按质量占比包括98%blc和2%flc;
26.lambda lc定标品浓度为4g/l时,按质量占比包括82%blc和18%flc;
27.lambda lc定标品浓度为7g/l时,按质量占比包括66%blc和34%flc;
28.lambda lc定标品浓度为11g/l时,按质量占比包括50%blc和50%flc;
29.kappa lc定标品浓度为2.00g/l时,按质量占比包括98%blc+2%flc;
30.kappa lc定标品浓度为5.00g/l时,按质量占比包括82%blc和18%flc;
31.kappa lc定标品浓度为9.00g/l时,按质量占比包括66%blc和34%flc;
32.kappa lc定标品浓度为15g/l时,按质量占比包括50%blc和50%flc。
33.一种包括上述定标品的检测试剂。
34.一种包括上述定标品的检测试剂盒。
35.经由上述的技术方案可知,与现有技术相比,本发明公开提供了一种血液总轻链定标品、试剂盒及应用,取得的技术效果:本发明研究发现病患不同阶段,虽然血液中tlc和flc都会升高,但flc/tlc占比和疾病严重程度正相关。通过提供不同浓度定标品,改变blc和flc比例,从而获得接近于正常人,病患,不同程度病患的定标品。相关系数均达到0.95以上,样本偏差小于
±
15%。
附图说明
36.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本
发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图。
37.图1附图为本发明提供的现有技术的轻链lc lambda临床比对图。
38.图2附图为本发明提供的检测原理示意图。
39.图3附图为本发明提供的结合型轻链反应原理示意图。
40.图4附图为本发明提供的游离轻链反应原理示意图。
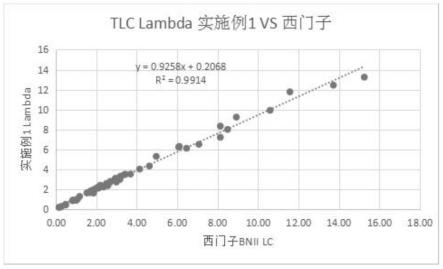
41.图5附图为本发明提供的lambda lc检测对比图。
42.图6附图为本发明提供的kappa lc检测对比图。
具体实施方式
43.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
44.本发明实施例公开了一种血液总轻链定标品、试剂盒及应用。
45.实施例中,未提及的原料、试剂、仪器设备均为市售渠道或现有技术中记载的原料,例如:
46.(试剂)r1:4-羟乙基哌嗪乙磺酸100mmol/l、氯化钠2200mmol/l、吐温-20 1ml/l和防腐剂proclin-3000.3ml/l;
47.(偶联有抗体的胶乳试剂)r2
48.使用商业化tlc抗体,如dako公司(美国安捷伦旗下)的kappa&lambda lc兔多克隆抗体,货号q0498&q0499,或日本nittobo公司的kappa&lambda lc羊多克隆抗体;
49.胶乳微球使用商业化的微球,如成都质捷新公司的胶乳微球ss(货号cm-1-1),活化剂(货号wsc0245),反应终止剂(货号0208e);
50.具体的:1l kappa lc试剂r2制备制备过程为,800ml胶乳微球ss,室温加入20ml活化剂,室温180rpm混匀15min;加入q0498 kappa lc抗体25ml,或3倍质量浓度的羊多抗(羊多抗效价略低,投料量为兔多抗3倍);室温偶联反应3小时,加入20ml终止剂,并加入160ml稀释液(50mm的taps-naoh,ph8.0,含0.5ml每升浓度的pc300防腐剂),加入6ml吐温-20,混匀1小时,制备获得kappa lc试剂r2
51.1l lambda lc试剂r2制备制备过程为,800ml胶乳微球ss,室温加入20ml活化剂,室温180rpm混匀15min;加入q0499 lambda lc抗体18ml,或3倍质量浓度的羊多抗(羊多抗效价略低,mg投料量为兔多抗3倍);室温偶联反应3小时,加入20ml终止剂,并加入160ml稀释液(50mm的taps-naoh,ph8.0,含0.5ml每升浓度的pc300防腐剂),加入6ml吐温-20,混匀1小时,制备获得lambda lc试剂r2。
52.检测原理:如图2~4所示。
53.对于血液tlc检测,tlc检测目前主要采用免疫比浊法进行测定,分为抗体和抗原直接形成浊度的普通免疫比浊法或抗体标记在胶乳微球上,与抗原形成抗体胶乳抗原更大的免疫复合物两种方式。均是在自动化的检测仪器(特定蛋白分析仪,生化分析仪)上,使用已知浓度的定标品定标,由仪器建立浊度信号值(透射为吸光度值,散射为散射光强度值)
与浓度值的关系图(定标曲线),然后检测血液样本浊度信号值,由仪器根据定标曲线自动计算被测物的tlc浓度。
54.实施例1
55.一种血液总轻链定标品:lambda lc(线性范围0.15~11g/l),定标品分布为1.5g/l(质量占比98%blc+2%flc),4g/l(82%blc+18%flc),7g/l(66%blc+34%flc),11g/l(50%blc&flc)。
56.lambda lc在日立3500上参数为,使用波长600nm,样本2μl(仪器自动稀释75倍),r1170μl,r270μl,两点终点法,18~34读点;5点定标(0.00、1.50、4.00、7.00、11.00g/l),样条曲线2拟合定标曲线;使用制备的lambda lc试剂r2搭配通用试剂r1,使用上述配比的定标品定标,在日立3500上测定临床样本,这些样本在西门子bnii上同一天内测定,统计数据,使用excel计算相关性和偏差见表1。
57.表1
58.59.[0060][0061]
实施例2
[0062]
一种血液总轻链定标品:kappa lc(线性范围0.2~15g/l)定标品分布为2g/l(98%blc+2%flc),5g/l(82%blc+18%flc),9g/l(66%blc+34%flc),15g/l(50%blc&flc);
[0063]
kappa lc,在日立3500上参数为,使用波长600nm,样本2μl(仪器自动稀释75倍),r1170μl,r270μl,两点终点法,18~34读点;5点定标(0.00、2.00、5.00、9.00、15.00g/l),样条曲线2拟合定标曲线;使用制备的kappa lc试剂r2搭配通用试剂r1,使用上述配比的定标品定标,在日立3500上测定临床样本,这些样本在西门子bnii上同一天内测定,统计数据,使用excel计算相关性和偏差。
[0064]
表2
[0065]
[0066]
[0067][0068]
技术效果
[0069]
实施例1、2实验结果表明:
[0070]
病患不同阶段,虽然血液中tlc和flc都会升高,但flc/tlc占比和疾病严重程度正相关。不同浓度定标品,改变blc和flc比例,从而获得接近于正常人,病患,不同程度病患的定标品是技术核心。
[0071]
本发明获得与西门子检测结果非常接近的检测结果,如图5、6,相关系数均达到0.95以上,样本偏差小于
±
15%。
[0072]
对比实验
[0073]
对比例1
[0074]
如果采用正常人blc(质量占比98%)和flc(2%)配比配制所有浓度的定标品,中重度病患样本会因为flc占比增加,单位浓度的lc抗原带来的浊度显著增加,导致中高值样本(中重度病患)测定结果大幅度偏高,虽然不影响诊断,但不符合药监局关于准确性的要求。
[0075]
一个kappa lc真实浓度(西门子bnii测定)为14g/l的病人(50%blc,50%flc),使用正常人blc(98%)和flc(2%)配比配制所有浓度的定标品,测定时,50%的blc形成的浊度约7g/l,但是50%的flc每g能形成至少3倍余blc的浊度,从而导致得到至少21g/l的信号值,7+21=28g/l,远远大于样本的真实浓度14g/l,虽然会被诊断为疾病严重,但偏差远远超过了nmpa 15%的要求。
[0076]
对比例2
[0077]
如果采用严重病患,即flc和blc各50%配比的定标品定标,则会导致中低值样本(正常人和中轻度病患)因为blc含量高,单位浓度的lc抗原产生的浊度相对低,从而导致测定结果偏低,病情被低估。
[0078]
一个中值lambdalc病患,真实浓度(西门子bnii测定)3.0g/l(85%blc,15%flc),其中(15%的blc加15%的flc)能在上述定标曲线上测定浊度0.9g/l,但是剩余的70%blc,形成浊度能力只有flc的1/3,估算测定值为0.8g/l,最终测定结果为0.9+0.8=1.7g/l小余参考值2.1g/l,原本是中等阳性3.0g/l病人,被测定为阴性,导致漏诊病情被耽误。
[0079]
上述列举了两种极端情况的对比例,本领域技术人员可以推算,位于本发明研究发现的比例附近的配比配制血液tlc定标品,能使得tlc检测准确性基本符合nmpa要求。
[0080]
实施例3
[0081]
一种血液总轻链定标品的制备方法:
[0082]
flc:商业化纯品,如yashrj的flc抗原纯品(dlckhp 0003/15&dlclhp 0003/15),纯度大于98%;
[0083]
blc纯品(大于99%纯度):可用人免疫球蛋白注射液,使用80~100kd离心超滤管(赛多利斯),去除flc,截留igg(blc),复溶制备。
[0084]
复溶blc可以使用柏荣诊断产品(上海)有限公司在售稀释液,如货号bys92420的稀释液。
[0085]
本说明书中各个实施例采用递进的方式描述,每个实施例重点说明的都是与其他实施例的不同之处,各个实施例之间相同相似部分互相参见即可。
[0086]
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1