一种尿囊素铝中尿素含量的测定方法与流程
本发明属于分析化学方法领域,具体涉及一种利用采用hplc-uv法进行主要有关杂质尿素的含量测定。由于原料药尿囊素铝中尿素含量低于1%,故利用尿素与尿囊素铝溶解性差异,尿囊素铝难溶于有机溶剂,尿素易溶于有机溶剂,通过有机溶剂富集的方式对有关物质尿素进行含量测定。
背景技术:
0、技术背景
1、尿囊素铝(aldioxa),化学名称为二羟基-(5氧-4-脲基-2-咪唑啉基)氧铝,白色结晶性粉末,无臭,无味,在水、乙醇、乙醚中几乎不溶,在稀盐酸或稀硝酸中略溶,常因部分水解而发生浑浊。原料药尿囊素铝为尿囊素与异丙醇铝熔融、缩合、水解后的反应产物,临床主要用于治疗胃及十二指肠溃疡。
2、尿囊素铝原料药的现有药品标准收载滴定法含量测定项,无相关物质检查研究。现有药典标准规定尿囊素铝按干燥品计算,含尿囊素(c4h6n4o3)应为65.3%~74.3%,含铝(al)应为11.1%~13.0%。
3、本实验依照《中国药典》2015年版四部指导原则、《化学药物质量标准建立的规范化过程技术指导原则》、《化学药物杂质研究技术指导原则》等的有关要求,采用hplc-uv法,建立了尿囊素铝原料药含量测定及有关物质检查方法,并进行方法学考察,对药典规定的质量标准进行了完善与提高,为尿囊素铝原料药的质量控制及生产工艺改进提供理论依据。
技术实现思路
1、本发明的目的是,采用hplc-uv法进行主要有关杂质尿素的含量测定。由于原料药尿囊素铝中尿素含量低于1%,故利用尿素与尿囊素铝溶解性差异,尿囊素铝难溶于有机溶剂,尿素易溶于有机溶剂,通过有机溶剂富集的方式对有关物质尿素进行含量测定。
2、为了实现本发明的上述目的,本发明提供了如下技术方案:
3、一种尿囊素铝中尿素含量的测定方法,所述方法,步骤如下:
4、步骤1:取尿囊素铝原料药1000mg,精密称定,置100ml量瓶中,加甲醇适量,超声30min,放至室温,定容至刻度,摇匀;
5、步骤2:取尿囊素对照品10mg,精密称定,置100ml量瓶中,加甲醇适量,超声30min,放至室温,定容至刻度,摇匀,作为尿囊素对照品溶液;
6、步骤3:取尿素对照品10mg,精密称定,置25ml量瓶中,加甲醇超声溶解,放冷定容,作为尿素对照品溶液(0.4mg/ml);
7、步骤4:分别精密吸取对照品溶液与供试品溶液各10μl,注入高效液相色谱仪,记录色谱图;
8、步骤5:根据色谱图计算供试品中尿囊素和尿素的含量;
9、其中的高效液相色谱仪的色谱条件如下:
10、色谱柱:tsk gel amide-80(250×4.6mm,5μm);流动相:乙腈-水(90:10);检测波长:210nm;流速:0.8ml/min;柱温:30℃;进样量:10μl。
11、本发明所述测定方法是经过筛选得到的,筛选过程如下:
12、专属性试验
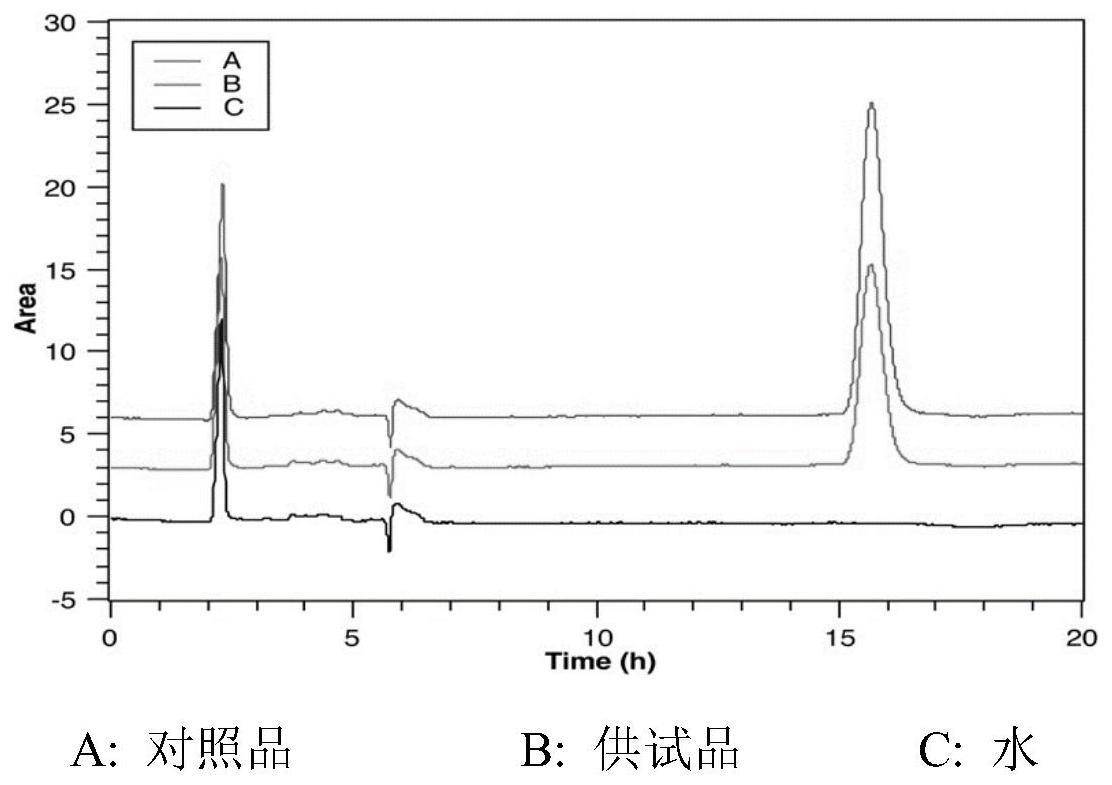
13、精密量取空白溶剂(水)及上述对照品和供试品溶液各10μl,注入液相色谱仪,结果见图1。
14、结果表明,空白溶剂无干扰,供试品溶液主峰的保留时间和对照品溶液一致,本法专属性较强。
15、系统适用性
16、分别精密称取尿囊素对照品和尿素对照品适量,加水溶解稀释制成每1ml中约含尿囊素80μg、尿素50μg的混合溶液作为系统适用性溶液。另精密称取尿囊素对照品和尿素对照品适量,分别加水配制成浓度约为100μg/ml、50μg/ml的溶液,作为定位溶液。分别精密量取水和上述溶液各10μl,注入液相色谱仪,记录色谱图,结果见表1和图2。
17、表1系统适用性试验结果
18、
19、结果表明:出峰顺序依次为尿素和尿囊素,分离度为8.46,主峰理论塔板数为6934,本法系统适用性良好。
20、线性关系及检测限定量限考察
21、精密称取尿囊素对照品10.03mg,置100ml量瓶中,加水溶解并稀释至刻度,摇匀,作为对照品储备液。分别精密吸取储备液0.5ml、1.0ml、2.0ml、4.0ml、6.0ml、8.0ml于10ml量瓶中,加水稀释至刻度,摇匀;精密吸取5μg/ml线性溶液0.5ml、1ml至2ml容量瓶中,加水稀释至刻度,摇匀;分别精密吸取1.25μg/ml、2.5μg/ml线性溶液1ml至2ml容量瓶中,加水稀释至刻度,摇匀;精密吸取1.25μg/ml线性溶液1ml至2ml容量瓶中,加水稀释至刻度,摇匀。
22、分别精密量取上述溶液及储备液各10μl,注入液相色谱仪,记录色谱图,以对照品浓度为横坐标,峰面积为纵坐标,进行线性回归,计算回归方程及相关系数,结果见表2及图3。
23、表2
24、
25、结果表明:尿囊素在0.6269μg/ml~100.3μg/ml范围内,峰面积与浓度成正比,线性回归方程为y=12.36x+1.2869,相关系数r2为1,线性关系良好。
26、尿囊素检测限及定量限数据见表3,图4至5。
27、表3含量测定检测限与定量限
28、
29、结果表明:本法灵敏度较高。
30、进样精密度试验
31、配制对照品溶液,作为进样精密度溶液,精密量取10μl,注入液相色谱仪,重复进样6次,记录色谱图,计算6次进样主峰峰面积与保留时间的rsd,考察进样精密度,结果见表4。
32、表4进样精密度试验结果
33、
34、结果表明:连续6次进样,主峰保留时间rsd为0.20%,峰面积rsd为0.52%,均小于2.0%,仪器进样精密度较好。
35、溶液稳定性
36、(1)供试品溶液稳定性
37、配制供试品溶液,在室温放置0h、2h、4h、6h、8h、12h、24h,分别精密量取10μl,注入液相色谱仪,记录色谱图,结果见表5,考察主峰峰面积变化情况。
38、表5含量测定样品溶液稳定性结果
39、
40、结果表明:供试品溶液在室温下放置24h,样品峰面积无明显变化,rsd为1.21%(小于2.0%),供试品溶液在室温下至少24h内稳定。
41、(2)对照品溶液稳定性
42、对照品溶液在室温放置0h、2h、4h、6h、8h、12h、24h,分别精密量取10μl注入液相色谱仪,记录色谱图,结果见表6,考察主峰峰面积变化情况。
43、表6对照品溶液稳定性结果
44、
45、结果表明:对照品溶液在室温下放置24h,主峰峰面积无明显变化,rsd为1.20%(小于2.0%),对照品溶液在室温下至少24h内稳定。
46、精密度试验
47、(1)重复性试验
48、6份供试品溶液;精密量取10μl注入液相色谱仪,记录色谱图;另取尿囊素对照品适量,精密称定,用水配制成每1ml中约含尿囊素100μg的溶液,作为对照品溶液,同法测定,按外标法以峰面积计算样品中水解产物尿囊素含量,结果见表7。
49、表7含量测定重复性结果
50、
51、结果表明:平均含量为62.66%,rsd为0.35%(n=6),本法重复性较好。
52、(2)中间精密度
53、由另一名分析人员,按照“重复性试验”项下方法,分别于不同时间,不同仪器进行含量测定,结果见表8至表9。
54、表8含量测定中间精密度结果
55、
56、
57、表9精密度试验数据汇总
58、
59、由上表可知,在同一实验室,由不同的实验人员,在不同时间,用不同仪器测定,本品平均含量为63.02%(n=12),rsd为0.76%。本法精密度较好。
60、综上,该含量测定方法系统适用性、线性及进样精密度良好,专属性较强,精密度较好,耐用性较好,适用于尿囊素铝原料药的含量测定。
61、尿囊素铝中尿素的hplc分析
62、取尿囊素铝原料药1000mg,精密称定,置100ml量瓶中,加甲醇适量,超声30min,放至室温,定容至刻度,摇匀。取尿囊素对照品10mg,精密称定,置100ml量瓶中,加甲醇适量,超声30min,放至室温,定容至刻度,摇匀,作为尿囊素对照品溶液。取尿素对照品10mg,精密称定,置25ml量瓶中,加甲醇超声溶解,放冷定容,作为尿素对照品溶液(0.4mg/ml)。分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,记录色谱图,比对尿囊素铝原料药中杂质峰与尿素对照品峰的保留时间与紫外吸收特征,结果见图6至10。
63、结果:hplc检测与尿素对照品保留时间一致,紫外吸收特征一致,故进一步确定该杂质为尿素。
64、色谱条件及系统适用性试验
65、色谱柱:tsk gel amide-80(250×4.6mm,5μm);流动相:乙腈-水(90:10);检测波长:210nm;流速:0.8ml/min;柱温:30℃;进样量:10μl。有关物质含量以尿素含量计,理论塔板数以尿囊素峰计算不低于5000。
66、不同有机溶剂富集有关物质尿素的考察
67、取原料药尿囊素铝(adx)三份,每份约1000mg,精密称定,置100ml量瓶中,分别加乙腈、甲醇和无水乙醇适量,超声30min,放至室温,定容至刻度,摇匀。取尿素对照品10mg,精密称定,置25ml量瓶中,分别加乙腈、甲醇和乙醇超声溶解,放冷定容,作为对照品溶液(0.4mg/ml)。分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定,记录色谱图,计算有关物质尿素含量,结果见表10。
68、表10不同有机溶剂富集有关物质尿素含量测定结果
69、
70、结果表明:分别采用乙腈、甲醇及无水乙醇对adx原料药进行有关物质的富集,测得的尿素含量:甲醇>乙腈>无水乙醇,故采用甲醇溶剂对adx原料药进行有关物质考察。
71、供试品溶液的制备
72、取尿囊素铝约1000mg,精密称定,置100ml量瓶中,加甲醇超声溶解,放至室温,加甲醇稀释定容至刻度,摇匀。
73、对照品溶液的制备
74、取尿素对照品10mg,精密称定,置10ml量瓶中,加甲醇超声溶解,放至室温,加甲醇稀释至刻度,摇匀,作为杂质储备液。精密吸取尿素储备液5ml至100ml容量瓶,加甲醇稀释定容至刻度,摇匀。(0.05mg/ml)
75、测定法
76、分别精密吸取对照品溶液与供试品溶液各10μl,注入液相色谱仪,测定。供试品溶液色谱图中如有尿素峰,按外标法以峰面积计算不得大于2.0%。
77、系统适用性试验
78、分别精密称取尿囊素对照品和尿素对照品适量,加甲醇溶解稀释制成每1ml中约含尿囊素80μg(由于尿囊素难溶于有机溶剂,故本法尿囊素对照品溶液为混悬液稀释)、尿素250μg的混合溶液作为系统适用性溶液。另加甲醇分别配制成浓度约为100μg/ml、250μg/ml的溶液,作为定位溶液。分别精密量取甲醇和上述溶液各10μl,注入液相色谱仪,记录色谱图。结果见表11和图11。
79、表11系统适用性试验结果
80、
81、结果表明:出峰顺序依次为尿素与尿囊素,尿素与主峰的分离度为10.81,主峰理论塔板数为9914,本法系统适用性良好。
82、专属性试验
83、(1)酸破坏试验
84、取本品约10mg,精密称定,置100ml量瓶中,加入1mol/l盐酸5ml,60度加热30min,加等量1mol/l氢氧化钠中和,加水约90ml,超声30min,定容至刻度,摇匀,作为酸破坏溶液。
85、(2)碱破坏试验
86、取本品约10mg,精密称定,置100ml量瓶中,加入0.1mol/l氢氧化钠5ml,加等量0.1mol/l盐酸中和,加水约90ml,超声30min,定容至刻度,摇匀,作为碱破坏溶液。
87、(3)氧化破坏试验
88、取本品约10mg,精密称定,置100ml量瓶中,加入30%双氧水5ml,60度加热30min,加水约90ml,超声30min,定容至刻度,摇匀,作为氧化加热破坏溶液。
89、(4)高温固体破坏试验
90、取本品1g置烧杯中,敞口于105℃烘箱中放置1h,取出,放至室温,取约10mg,精密称定,置100ml量瓶中,加水约90ml,超声30min,定容至刻度,摇匀,作为高温破坏溶液。
91、(5)未破坏溶液
92、取本品约10mg,精密称定,置100ml量瓶中,加水约90ml,超声30min,定容至刻度,摇匀,作为未破坏溶液。
93、分别精密吸取空白溶剂和上述溶液10μl,注入液相色谱仪,记录色谱图。结果见表12和图12。
94、表12专属性试验结果
95、
96、结果表明:空白溶剂不干扰本品有关物质检出,本品在上述条件下的降解产物与主峰完全分离,杂质间分离度较好,各试验条件下主峰峰纯度因子均大于阈值。根据a总/c(其中a总代表供试品溶液总峰面积,c代表供试品溶液的浓度)来计算单位浓度的响应值,以未破坏溶液的响应值为基数(物料回收为100%),计算破坏溶液的物料回收率,结果为酸、碱氧化加热破坏,高温固体破坏条件下基本平衡,本法专属性较强;该原料药在碱性条件下不稳定,易被降解,在工艺生产过程中应严格控制反应体系ph。
97、进样精密度
98、精密称取尿素对照品适量,加甲醇稀释制成约含尿素100μg/ml的溶液。分别精密量取10μl,注入液相色谱仪,连续进样6次,结果见表13。
99、表13尿素进样精密度试验
100、
101、
102、结果表明:有关物质尿素峰面积rsd小于2.0%,仪器进样精密度较好。
103、检测限与定量限
104、称取尿素对照品10mg,精密称定,至25ml容量瓶中,加甲醇超声使溶解,定容,摇匀,作为尿素对照品储备液(400μg/ml);精确吸取储备液5ml至10ml容量瓶中,加甲醇定容,摇匀(200μg/ml);同法稀释得对照品溶液(100μg/ml、50μg/ml);再依次吸取50μg/ml对照品溶液0.5、1、2、5ml至10ml容量瓶中,加甲醇定容至刻度,摇匀,即得(2.5、5、10、25μg/ml)。以信噪比(s/n)为3:1时相应浓度或注入仪器的量确定检测限,表示被测物能被可靠地检测出的最低浓度或量;以s/n为10:1时相应浓度或注入仪器的量确定定量限,表示被测物能被定量测定的最低浓度或量。精密量取10μl,注入液相色谱仪,记录色谱图,结果见表14和图13至14。
105、表14有关物质尿素检测限与定量限
106、
107、结果表明:本法灵敏度较高。
108、线性关系考察
109、称取尿素对照品10mg,精密称定,至25ml容量瓶中,加甲醇超声使溶解,定容,摇匀,作为尿素对照品储备液(400μg/ml);精确吸取储备液5ml至10ml容量瓶中,加甲醇定容,摇匀(200μg/ml);同法稀释得对照品线性溶液(100、50、25μg/ml);精密量取10μl注入液相色谱仪,记录色谱图,以浓度为横坐标,峰面积为纵坐标,进行线性回归。结果见表15和图15。
110、表15尿素线性试验结果
111、
112、
113、结果表明:尿素在25.43~406.80μg/ml范围内,峰面积与浓度成正比,线性回归方程为y=1553.4x-12.408,相关系数r为0.9972,线性关系良好。
114、精密度试验
115、(1)重复性试验
116、对照品溶液1份,供试品溶液6份,分别精密量取对照品溶液和供试品溶液各10μl,注入高效液相色谱仪,记录色谱图,计算尿素杂质含量。结果见表16。
117、表16重复性试验结果(由shenwei操作)
118、
119、结果显示:6份供试品溶液中尿素杂质含量的rsd不大于2.0%(n=6),本法重复性较好。
120、(2)中间精密度
121、由另一名分析人员,按“重复性试验”项下方法,分别于不同时间,不同仪器进行有关物质检测。结果见表17至18。
122、表17中间精密度试验结果(由lisiyuan操作)
123、
124、表18精密度试验结果汇总
125、
126、
127、注:shenwei使用的测试仪器为agilent hplc 1260(dead016640);
128、lisiyuan使用的测试仪器为agilent hplc 1100(de60400285)
129、结果表明:经不同人员于不同时间在不同仪器检测,12份供试品溶液中尿素杂质含量的rsd不大于2.0%(n=12),本法精密度较好。
130、溶液稳定性
131、(1)尿素对照品溶液放置稳定性
132、精密称取尿素对照品20mg至10ml容量瓶,加甲醇超声溶解后稀释定容至刻度,摇匀,作为尿素对照品储备液;精密吸取储备液适量,加甲醇稀释制成每1ml含尿素对照品0.25mg的尿素对照品溶液;精密量取尿素对照品溶液(室温下放置0h、2h、4h、6h、8h、12h)各10μl注入液相色谱仪,记录色谱图。结果见表19。
133、表19尿素对照品溶液放置稳定性试验
134、
135、结果显示:尿素对照瓶溶液主峰峰面积rsd为0.851%,小于2.0%,各时间点杂质对照品峰面积无明显变化,室温12h放置稳定性良好。
136、(2)尿囊素对照品溶液放置稳定性。
137、由于尿囊素难溶于有机溶剂,故本法配制的尿囊素对照品溶液为混悬液,且配制的系统适用性溶液为尿素对照品溶液与尿囊素对照品溶液按比例混合配制。精密称取尿囊素对照品10mg至100ml容量瓶,加甲醇超声,定容至刻度,摇匀,作为尿素对照品溶液;精密量取尿囊素对照品溶液(室温下放置0h、2h、4h、6h、8h、12h)各10μl注入液相色谱仪,记录色谱图。结果见表20。
138、表20尿囊素对照品溶液放置稳定性试验
139、
140、
141、结果显示:尿囊素对照瓶溶液主峰峰面积rsd为0.534%,小于2.0%,室温放置12小时主峰峰面积稳定,且无新杂质产生,稳定性良好。
142、(3)系统适用性溶液放置稳定性
143、分别精密称取尿囊素对照品和尿素对照品适量,加甲醇溶解稀释制成每1ml中约含尿囊素80μg、尿素250μg的混合溶液作为系统适用性溶液。精密量取系统适用性溶液(室温下放置0h、2h、4h、6h、8h、12h)各10μl注入液相色谱仪,记录色谱图。结果见表21。
144、表21系统适用性溶液放置稳定性试验
145、
146、结果表明:系统适用性溶液室温放置24小时内各时间点分离度均符合要求,各组份比例无明显变化。
147、准确度
148、精密称取尿素对照品适量,加甲醇稀释制成每1ml中含尿素约1mg的溶液,作为尿素对照品储备液。精密吸取储备液适量,加甲醇稀释制成每1ml中含尿素0.05mg的溶液,作为杂质对照品溶液。
149、按“3.1.2”项下方法配制供试品溶液9份,分别添加尿素对照品储备液进行加样回收率考察。按加入量80%、100%和120%配制三个浓度的供试品溶液,各三份,依照有关物质检查项下方法进行检测,分别精密量取对照品溶液与各准确度溶液10μl,注入液相色谱仪,记录色谱图,采用外标法以峰面积计算。结果见表22。
150、表22尿素回收率测定结果
151、
152、结果表明:尿素在80%~120%限度浓度范围内的平均回收率为94.72%,rsd为2.90%;回收率在90%~105%之间,rsd小于5.0%,本法准确度较好。
153、结论:综上所述,该法系统适用性良好;专属性较强;灵敏度较高;有关物质尿素在一定浓度范围内峰面积与浓度呈良好的线性关系;精密度较好;杂质加样回收率在90%~105%之间,准确度较高;耐用性较好,可用于尿囊素铝原料药的有关物质检查。
- 还没有人留言评论。精彩留言会获得点赞!