一种氢碘酸混合液中HI含量的测定方法与流程
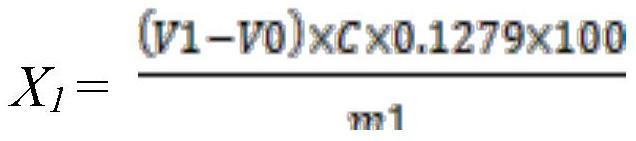
本发明涉及一种氢碘酸中hi含量的测定方法。
背景技术:
1、含碘氢碘酸料液(即碘化氢-碘-水三元混合液,hi-i2-h2o)的成分分析操作,在日常实验室分析、以及氢碘酸生成工艺中都会用到。
2、常规的hi-i2-h2o浓度分析方法是滴定法,使用的标准仍然为中华人民共和国化学工业部部颁暂行标准《化学试剂氢碘酸hgb3181-60》。具体来说是以酸碱滴定法来确定hi的浓度,而以硫代硫酸钠溶液滴定法,即碘量法来确定i2的浓度。当氢碘酸中同时含有游离碘及次磷酸稳定剂时,由于次磷酸的存在,酸碱滴定法就不再适用。因此,需要尝试其它的方法对hi的浓度进行分析。
3、目前还没有合适的方案能够测试含次磷酸这种酸性稳定剂的氢碘酸溶液中hi的含量。
技术实现思路
1、本发明主要是为了克服现有技术中存在的难以准确测量含酸性稳定剂和i2的氢碘酸溶液中hi的客观缺陷,而提供了一种氢碘酸溶液中hi含量的测定方法。采用本发明的测试方法能够准确的测量出含酸性稳定剂和i2的氢碘酸溶液中hi的含量。
2、研发人员在研发过程中,参考现有文献公开的氧化法将碘离子氧化为碘单质的方式借鉴这样的方式实施对氢碘酸溶液中hi的含量测定。该方案具体如下:向含碘单质和碘离子的溶液体系中加入稀硫酸,再加入乙醇和亚硝酸钠,摇匀后加入氨基磺酸铵溶液,之后采用硫代硫酸钠滴定法测试体系中碘单质的含量。其中加入乙醇的目的是考虑到碘单质不溶于体系中的水而易溶于乙醇,加入适量乙醇能够增加碘单质在溶液中的溶解度,同时降低溶液中碘单质的饱和程度,减少碘单质的挥发,降低试验误差。加入氨基磺酸铵溶液和稀硫酸的目的是为了消除亚硝酸盐,其中稀硫酸是为氧化反应和氧化剂消除反应提供酸性环境使得氧化反应和消除反应能够完全。
3、但经过探索实验发现,在氨基磺酸铵与hno2的反应未完全前或是在氨基磺酸铵加入之前的任何时机加入乙醇,均会与溶液体系中的氨基磺酸铵发生反应,这会导致消除亚硝酸的反应程度以及反应是否完全无法预知,而溶液体系中残留亚硝酸,由于其为氧化性,而硫代硫酸钠为还原性,亚硝酸盐的残留将直接导致硫代硫酸钠的消耗量增加,最终将影响碘单质的含量测定。
4、经过多次实验的探索以及构思,研发人员发现,在氨基磺酸铵与亚硝酸的反应完全之后加入乙醇。由于此时消除反应已经完成了,乙醇的加入不影响亚硝酸的消除,溶液中仅剩余过量的氨基磺酸以及生成的固体碘单质,此时加入乙醇不仅可以溶解固体碘单质同时可以消除过量的氨基磺酸铵,如果乙醇省略不加入,那么固体碘单质不能与硫代硫酸钠充分快速反应,滴定分析的结论不正确。
5、本发明主要通过以下技术方案解决上述技术问题。
6、本发明提供了一种氢碘酸混合液中hi含量的测定方法,其包括以下步骤:
7、步骤(1)向待测氢碘酸混合液中添加酸溶液和亚硝酸钠溶液使得所述待测氢碘酸溶液中的hi完全氧化,得溶液体系1;
8、步骤(2)向所述溶液体系1中加入氨基磺酸铵溶液使得所述溶液体系1中生成的hno2完全反应,得溶液体系2;
9、步骤(3)向所述溶液体系2中加入醇类化合物使得所述溶液体系2中的碘单质完全溶解,得溶液体系3;
10、步骤(4)采用硫代硫酸钠标准溶液滴定所述溶液体系3,获得消耗的所述硫代硫酸钠标准溶液的体积,记为v1;
11、步骤(5)通过下述公式计算获得所述待测氢碘酸混合液中hi的质量百分数x1:
12、
13、式中:
14、v0为待测氢碘酸混合液中碘单质消耗所述硫代硫酸钠标准溶液的体积;
15、c为所述硫代硫酸钠标准溶液的浓度;
16、m1为待测氢碘酸混合液的质量;
17、0.1279-----每毫克当量hi的克数。
18、本发明中,所述待测氢碘酸混合液可为本领域常规的含酸稳定剂以及hi的混合液,存在储存条件不当氢碘酸被大量氧化而出现组分大幅变化的情况。实际操作中,所述待测氢碘酸混合液中的hi易被空气中的氧气氧化,因此不在无氧条件下保存的氢碘酸都有可能随着时间的推移出现hi含量大幅较低及碘单质含量增加的问题,事实上,本发明的初衷就是监测市购的氢碘酸混合液实验室分装的过程中,由于没有原厂惰性气体的保护后hi是否会发生大量的氧化现象,如果保存条件不当,hi被完全氧化成碘单质也是有可能的,因此所述待测氢碘酸混合液中hi以及碘单质的含量一般无需作特别限定。
19、在一些具体实施方式中,所述待测氢碘酸混合液中,以质量百分比100%计,hi的含量为55%-58%,百分比为hi的质量占所述待测氢碘酸混合液总质量的百分比。
20、在一些具体实施方式中,所述待测氢碘酸混合液中,以质量百分比100%计,碘单质的含量在1%以下,百分比为碘单质的质量占所述待测氢碘酸混合液总质量的百分比。
21、本发明中,所述酸溶液可为本领域常规的无机酸溶液,本领域技术人员根据所述的测定方法可知,所述酸溶液的加入能够促进所述步骤(1)中氧化反应的进行(反应式为:2hi+2nano2+h2so4=2h2o+na2so4+i2+2no↑)。所述酸溶液较佳地在加入所述亚硝酸钠溶液之前加入。若所述酸溶液在加入亚硝酸钠溶液加入之后加入,则可能会导致氧化反应不能够完全进行,即碘离子不能完全被氧化为碘单质还需要继续加入酸溶液促使氧化反应完成(4hi+2nano2=2h2o+2nai+i2+2no↑)。在一些具体实施方式中,所述酸溶液为稀硫酸溶液。在一些具体实施方式中,所述酸溶液的浓度为1mol/l。
22、本发明中,所述亚硝酸钠溶液的浓度以及添加量按照所需的测定方法添加即可,无需作特别的限定,能够使得步骤(1)中所述待测氢碘酸混合液中的hi反应完全即可,一般以过量的形式添加。在一些具体实施方式中,所述亚硝酸钠溶液的浓度为1mol/l。
23、本发明中,所述待测氢碘酸混合液中通常还含有酸稳定剂,所述酸稳定剂可为本领域常规的能够使得hi稳定的添加剂,在所述氢碘酸混合液中,通常为次磷酸。
24、本发明中,所述步骤(1)中,所述亚硝酸钠溶液的加入还会使得所述待测氢碘酸溶液中的酸稳定剂被完全氧化。在本发明的具体实施方式中,通常酸稳定剂的还原性大于hi,因此所述亚硝酸钠溶液的加入一般会优选氧化所述酸性稳定剂。
25、本发明中,所述溶液体系1中不含醇类化合物,且在制备所述溶液体系1的过程中也不额外添加醇类化合物。即所述溶液体系1中的醇类化合物为0%或仅仅是误差范围内的含量,使得氨基磺酸铵的加入仍然能够完全消除亚硝酸即可。
26、本发明中,所述溶液体系2中不含醇类化合物,且在制备所述溶液体系2的过程中也不额外添加醇类化合物。即所述溶液体系2中的醇类化合物为0%或仅仅是误差范围内的含量,使得氨基磺酸铵的加入仍然能够完全消除亚硝酸即可。
27、在本发明中,所述溶液体系1和在形成所述溶液体系2中的过程中含有醇类化合物,将会无法准确测量hi的含量。这主要是因为所述醇类化合物会与部分氨基磺酸铵反应,导致亚硝酸无法完全消除,进而与硫代硫酸钠反应,最终得到的结果必然受到影响。
28、本发明中,所述醇类化合物可为本领域常规的醇类溶剂一般加入含碘单质的混合液中以使得碘单质溶解,包括但不限于甲醇、乙醇和异丙醇中的一种或多种。但本发明中在形成所述溶液体系2之前不加入所述的醇类化合物是为了防止所述醇类化合物与无机酸发生反应,影响最终测试的准确性,
29、本发明中,所述氨基磺酸铵溶液的浓度可根据实际需要添加,能够使得所述溶液体系1中生成的hno2反应完全即可,一般以过量的形式添加。在一些具体实施方式中,所述氨基磺酸铵溶液的浓度例如为1mol/l。
30、本发明中,步骤(3)中所述的醇类化合物能够使得碘单质完全溶解,如此才能够在采用硫代硫酸钠滴定时得到的结果是准确的,对于种类无特别限定,包括但不限于甲醇、乙醇和异丙醇中的一种或多种。
31、本发明中,为了使得所述步骤(3)中所述溶液体系2中得到的碘单质完全溶解,较佳地对加入所述醇类化合物的溶液体系2的混合物进行超声,以辅助所述碘单质的充分溶解。其中,当所述待测氢碘酸中含有0.04-0.06g的hi时,优选地加入20-30ml的无水醇类化合物。
32、本发明中,在进行所述硫代硫酸钠标准溶液滴定溶液体系中的碘单质之前的溶液体系应当保持在弱酸性,通常ph值在6以下,优选地为3~6。在一些具体实施方式中,所述溶液体系3中的ph值为6以下。
33、本发明中,所述硫代硫酸钠标准溶液的浓度可为本领域常规,优选为0.05~0.1mol/l。
34、本发明中,本领域技术人员知晓,步骤(5)中v0的获得采用的是本领域常规的硫代硫酸钠标准溶液滴定法,可在进行步骤(1)至步骤(4)的过程中同步进行,也可在所述步骤(1)之前进行,v0的获得无特殊的顺序,在本发明中采用同批次的待测氢碘酸混合液取两组同质量的待测氢碘酸混合液分别进行步骤(1)至步骤(4)中v1的测量,以及待测氢碘酸混合液中碘单质消耗硫代硫酸钠标准溶液体积v0的测量。在符合本领域常识的基础上,上述各优选条件,可任意组合,即得本发明各较佳实例。
35、本发明所用试剂和原料均市售可得。
36、本发明的积极进步效果在于:本发明采用亚硝酸钠作为氧化剂将hi氧化成碘单质,这种间接测量碘单质含量的方法,消除了次磷酸对测量的影响,测定结果精密度较高,测定结果平行稳定,且操作简单。
- 还没有人留言评论。精彩留言会获得点赞!