一种用于免疫检测的免疫磁珠、制备及其应用的制作方法
本发明属于免疫检测,具体包含一种用于免疫检测的免疫磁珠、制备及其应用。
背景技术:
1、磁珠是一种直径纳米或微米级别的球形复合材料,其核心是由四氧化三铁或三氧化二铁等超顺磁性材料构成,磁珠的外壳一般包覆有聚苯乙烯、葡聚糖、二氧化硅等材料,这些材料可被修饰产生氨基(nh2)、羧基(cooh)或羟基(oh)等功能基团。通过基团间的偶联反应将抗原、抗体等结合于磁珠表面,使之成为抗原、抗体等物质的载体,我们称之为免疫磁珠(immunomagnetic bead,imb)。免疫磁珠表面的抗原/抗体既可与特异性抗体/抗原结合,形成免疫复合物,又可在外界磁场的作用下发生力学移动,使得磁珠-抗体-抗原复合物与其他物质分离,从而达到目标物分离以及浓缩的目的。
2、目前,常用于免疫检测分析的磁珠载体主要有羧基磁珠、氨基磁珠、链霉亲和素磁珠以及n-羟基琥珀酰亚胺(nhs)修饰的磁珠等。其中,羧基磁珠主要通过对其表面羧基进行活化的方法来实现羧基磁珠与抗原、抗体等物质的偶联。然而,羧基的活化步骤复杂,常用的活化剂乙基(3二甲基氨基丙基)碳酰二亚胺(edc)在水溶液中不稳定,需现用现配,易出现偶联效率低、批间差异大等问题。采用氨基磁珠在制备免疫磁珠时,也需与已经活化好的羧基抗体进行偶联或采用戊二醛作为偶联中间体,偶联步骤复杂且易出现蛋白或磁珠之间自身的偶联反应。nhs修饰的磁珠虽然不需要活化可直接与带有羧基的蛋白发生偶联反应,但是,nhs磁珠表面的nhs官能团仍需要缓冲溶液进行活化且nhs易发生水解反应,从而导致偶联效率不高。此外,还可通过其他方式,如通过巯基和吡啶基二硫基发生共价反应,将引入吡啶二硫基团的抗原共价偶联到巯基磁珠上,得到免疫磁珠。同时也可以通过蛋白g或者蛋白a为基础制备定向免疫磁珠,然而,以上免疫磁珠的制备方法均需通过有机反应来实现,很多时候还需要后续的封闭步骤,大大增加了免疫磁珠制备过程的复杂性,更重要的是,以上方法合成的免疫磁珠表面的免疫配体官能团决定了其表面抗原抗体偶联的最大量,由于免疫磁球表面免疫配体的数量有限,因此通过偶联反应固定到磁珠表面的抗原抗体的量受到限制。
技术实现思路
1、鉴于以上问题,本发明的首要目的是提供一种用于免疫检测的新型免疫磁珠,该免疫磁珠中抗原抗体的量不受磁球表面配体数量的限制,可以通过调节金属有机框架的含量进而调控磁珠表面抗体的浓度。
2、本发明的另一目的是提供一种上述免疫磁珠的制备方法,该方法条件温和,无需任何活化等有机反应步骤,制备方法简单。
3、为达到上述目的,本发明采取以下方案:
4、第一方面,本发明提供一种用于免疫检测的免疫磁珠,包括磁珠载体、金属有机框架和抗体;其中,所述抗体以金属有机框架为连接体包覆于所述磁珠载体的表面。
5、需要说明的是,金属有机框架(mofs)是指由金属离子或金属簇构建单元和有机桥联配体连接形成的具有周期性结构的多孔材料,在本发明中,以金属有机框架为连接体,可以理解为:金属有机框架自组装在磁珠载体表面,而抗体则利用与金属有机框架之间的相互作用包覆在磁珠载体表面;至于抗体是直接包在金属有机框架的表面,从而对磁珠载体形成包覆;还是结合在框架中孔隙结构内表面和/或外表面,进而接触或直接不接触磁珠载体,从而形成包覆;本发明不作特别限定,以上情况均在本发明的保护范围内。
6、本发明的免疫磁珠,首先以磁珠为mofs材料的成核载体,利用mofs材料灵活的自组装性,将mofs材料包覆于磁珠表面,同时利用mofs材料的多孔性以及包裹生物大分子的性能,将大量抗体包覆于磁珠载体表面,以最大限度的提高磁珠表面的抗体的浓度。
7、优选地,所述磁珠载体、抗体和金属有机框架的质量比为2-10:1-5:0.5-3。
8、优选地,所述金属有机框架中,金属中心为锌、钴、铜和铁中的任一种,有机配体为含氮类配体和/或羧酸类配体。
9、优选地,所述磁珠载体为羧基磁珠、氨基磁珠、羟基磁珠、链霉亲和素磁珠、二氧化硅磁珠和n-羟基琥珀酰亚胺(nhs)修饰的磁珠中的任一种。
10、更优选地,所述磁珠载体为纳米磁珠或直径大于1um的磁珠。
11、第二方面,本发明提供一种上述免疫磁珠的制备方法,包括以下步骤:
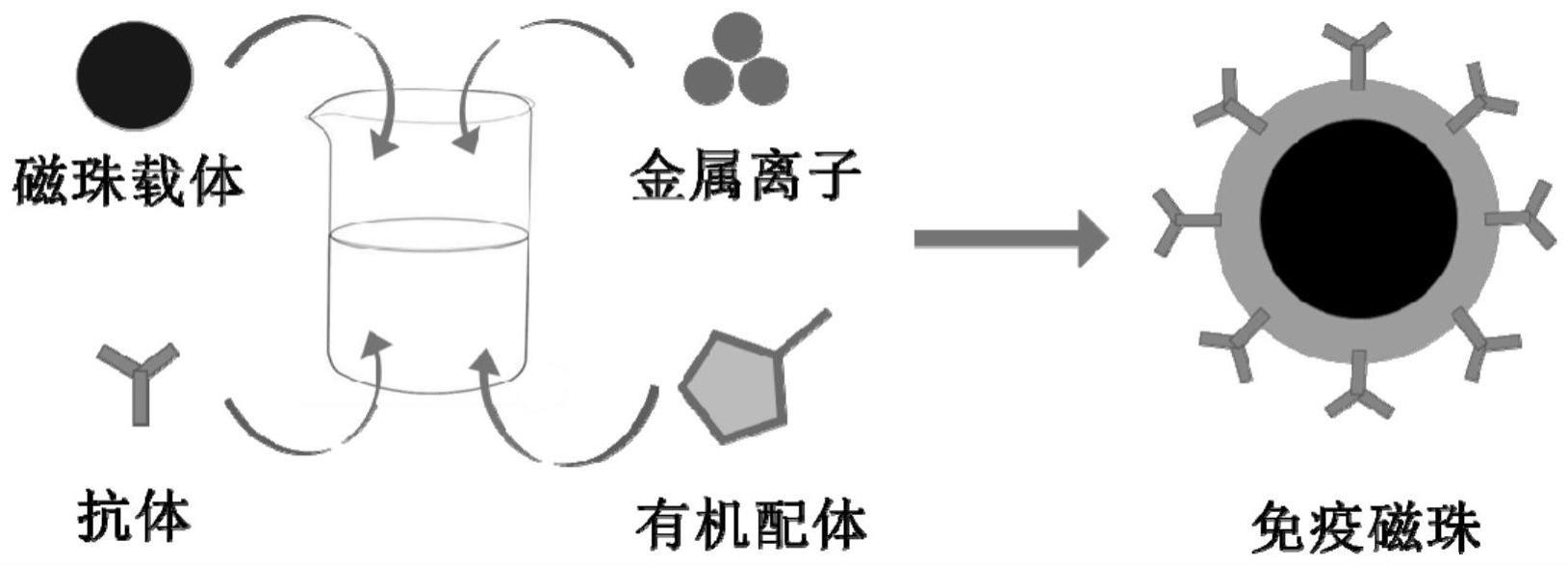
12、将磁珠载体的悬浮液、金属盐溶液、抗体溶液和有机配体溶液混合,在室温下进行反应。
13、其中,上述制备方法中,各原料可以依次加入后直接反应,也可以加入一种后搅拌均匀再加下一种。
14、优选地,所述磁珠载体的悬浮液的浓度为0.2mg/ml-1mg/ml,所述金属盐溶液的浓度为10mg/ml-320mg/ml;所述金属盐溶液与磁珠载体的悬浮液的体积比为2-10:1。
15、优选地,所述抗体溶液的浓度为0.1mg/ml-mg/ml,所述抗体溶液与磁珠载体的悬浮液的体积比为1-10:1。
16、优选地,所述有机配体溶液与金属盐溶液中,有机配体和金属离子的摩尔比为4-10:1。
17、优选地,所述反应的时间为10min-24h。
18、优选地,反应后还包括利用含有一定浓度表面活性剂的缓冲溶液清洗的步骤。
19、示例性地,所述表面活性剂可以为吐温-20、吐温-80、聚乙烯比咯烷酮(pvp)、triton-100、十二烷基硫酸钠(sds)、十二烷基苯磺酸钠中的任一种,优选为吐温-20。
20、示例性地,所述表面活性剂的浓度可以为0.05%-1%(v/v),优选为0.1%。
21、示例性地,所述缓冲溶液可以为3-吗啉丙磺酸(mops)缓冲溶液,吗啉乙磺酸(mes)缓冲溶液,4-羟乙基哌嗪乙磺酸(hepes)缓冲溶液等,优选为mops缓冲溶液。
22、示例性地,所述缓冲溶液的浓度为10mm-100mm,优选为10mm。
23、第三方面,本发明提供一种上述免疫磁珠在真菌毒素、农药残留、过敏原和肿瘤标志物中任一种的富集分离中的应用。
24、可以理解,本发明的免疫磁珠具有广泛的通用性,可根据具体富集分离物质的种类,选择相应的抗体类型。
25、另需注意的是,如果没有特别说明,本发明所记载的任何范围包括端值以及端值之间的任何数值以及以端值或者端值之间的任意数值所构成的任意子范围。本发明中制备方法如无特殊说明则均为常规方法,所用的原料如无特别说明均可从公开的商业途径获得或根据现有技术制得。
26、本发明有益效果:
27、1.本发明提供的免疫磁珠中抗原抗体的量不受磁球表面配体的影响。抗原抗体能够最大限度的被原位合成的mofs材料连接于免疫磁珠表面,而磁球表面生物活性物质浓度的提高有助于后续利用所制备的免疫磁珠进行目标物的高效率捕获、分离、净化和浓缩。
28、2.本发明提供的免疫磁珠能够最大限度的保留或增强抗原抗体的生物活性。具体地:抗原抗体、酶等生物大分子由于其脆弱本质通常在温和条件下才能发挥功能活性作用,由于本发明中提供的免疫磁珠的制备方法条件温和,无需任何活化等有机反应步骤,因此本发明在大大简化制备方法的同时能够最大限度的保留抗原抗体的活性。此外,生物大分子如抗原抗体酶等的蛋白质分子结构在高温、有机溶剂和高强度机械条件下会发生构象变化或解体,从而导致其生物催化和识别性能的显著下降。而mofs材料在维持抗体分子识别及其活性保护方面也具有很好的性能,因此本发明提供的免疫磁珠能够很好的稳定或增强抗原抗体的生物活性。
29、3.本发明提供的免疫磁珠的制备新方法极其简单,耗时短,合成效率高。只需将磁球、金属离子、有机配体、具有生物活性的抗体或抗原在温和条件下孵育即可。与常规的制备方法相比,该方法由于无需借助任何有机反应对磁球或抗原抗体进行活化,无需封闭,无需加热等大大简化了操作步骤。
- 还没有人留言评论。精彩留言会获得点赞!