一种细胞角蛋白18-M30测定试剂盒及其制备方法与流程
本发明属于生化试剂检测,具体涉及一种细胞角蛋白18-m30测定试剂盒及其制备方法。
背景技术:
1、慢性肝病中以chb、nafld常见,干细胞凋亡均是其干细胞损伤的不可忽略的重要机制,多种肝病的发生、发展、肝纤维化、肝硬化均与干细胞凋亡有关。近年来研究发现细胞角蛋白18-m30(cytokeratin 18-m30,ck18-m30)与肝细胞损伤、细胞凋亡等生理病理反应相关,其中ck18的一个凋亡片段m30,作为一个新的抗原在干细胞凋亡早期阶段可以在外周血或者细胞培养上清中检测到,而在细胞坏死时则无法检测。目前广受关注的细胞凋亡检测指标即为ck18-m30。
2、肝活检是诊断nafld的金标准,并且可以准确区分nafl和nasl,但肝活检是有创操作,并且存在采样误差和诊断偏倚等现象,花费相对较高,故临床普及相对困难。ck18-m30作为唯一有病理基础的外显性标志物,因其无创性、可重复、并能准确区分nafl、nash二者,确定疾病分级的特点,已受到临床日益关注。同时血清ck18-m30可作为反映慢性乙型肝炎合并非酒精性脂肪肝患者中肝脏炎症、纤维化的血清学指标之一。目前,临床检测血清中的ck18-m30蛋白的方法有免疫层析法、化学发光法、酶联免疫法等,商品化的产品少,且灵敏度不足。
技术实现思路
1、鉴于此,本发明提供一种细胞角蛋白18-m30测定试剂盒及其制备方法。
2、为达到上述目的,本发明采用以下技术方案:
3、一种细胞角蛋白18-m30测定试剂盒,所述试剂盒包括:试剂m、试剂r1、试剂r2、校准品和质控品;
4、其中,所述试剂m含包被链霉亲和素的磁微粒,且磁微粒与链霉亲和素的质量比为3:(0.1~1.0)磁微粒粒径为0.2~3.0μm;
5、所述试剂r1含生物素化的ck18-m30单克隆抗体,且生物素与ck18-m30单克隆抗体的质量比为(1~5):1;
6、所述试剂r2含标记吖啶酯的ck18-m30单克隆抗体,且ck18-m30单克隆抗体与吖啶酯质量比例为(2~8):1;
7、所述校准品和质控品为含有不同浓度人细胞角蛋白18-m30的抗原稀释液。
8、在一些具体实施例中,优选地,所述试剂m中磁微粒与链霉亲和素的质量比为3:(0.3~1.0),磁微粒粒径为1.0~3.0μm;
9、所述试剂r1中生物素与ck18-m30单克隆抗体的质量比为3:1;
10、所述试剂r2中ck18-m30单克隆抗体与吖啶酯质量比例为(4~8):1。
11、进一步地,所述试剂m、所述试剂r1的组分还包括:ph为5.0~8.0的缓冲液5.0~50.0g/l、无机盐10.0~50.0g/l、表面活性剂1.0~50.0g/l、保护剂100.0~600.0g/l、防腐剂1.0~10.0g/l;
12、所述试剂r2的组分还包括:ph为6.0~9.0的缓冲液5.0~50.0g/l、无机盐1.0~30.0g/l、表面活性剂1.0~10.0g/l、保护剂50.0~200.0g/l、防腐剂1.0~2.0g/l。
13、进一步地,所述缓冲液包括磷酸盐缓冲液、mes缓冲液、gly缓冲液;
14、所述无机盐为nacl、kcl、kh2po4中的至少一种;
15、所述表面活性剂为吐温-20、edta二钠中的至少一种;
16、所述保护剂为蔗糖、bsa、酪蛋白中的至少一种;
17、所述防腐剂为proclin系列防腐剂。
18、进一步地,所述试剂盒还包括预激发液、激发液。
19、一种上述试剂盒的制备方法,包括以下步骤:
20、s1、试剂m的制备:
21、取磁微粒置于包被缓冲液中,加入edc,混匀,外加磁场集磁去除上清液,再加入缓冲液,混匀,得活化磁微粒溶液;
22、取链霉亲和素置于包被缓冲液中,混匀,加入上述活化磁微粒溶液中,混匀,外加磁场集磁去除上清液,加入终止缓冲液ⅰ,混匀,得包被链霉亲和素的磁微粒溶液;
23、将包被链霉亲和素的磁微粒溶液外加磁场集磁去除上清液,加入清洗液,混匀,外加磁场集磁去除上清液,加入保存缓冲液,混匀,即得试剂m;
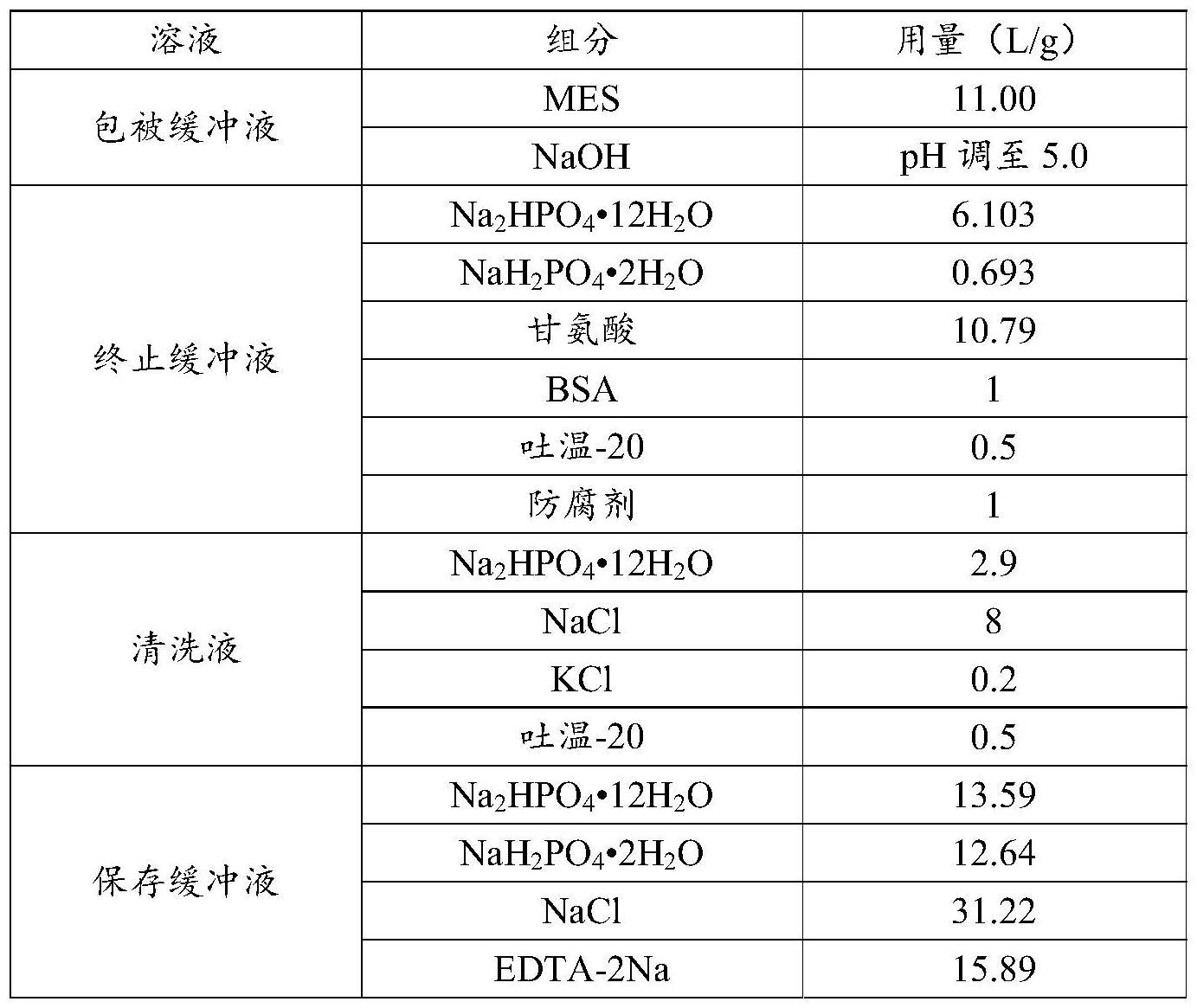
24、其中,包被缓冲液为mes缓冲液;
25、终止缓冲液ⅰ由磷酸盐缓冲液、gly缓冲液、保护剂、表面活性剂、防腐剂混合制备而成;
26、清洗液由磷酸盐缓冲液、无机盐、表面活性剂混合制备而成;
27、保存缓冲液由磷酸盐缓冲液、无机盐、表面活性剂、保护剂、防腐剂混合制备而成;
28、s2、试剂r1的制备:
29、将生物素用置于磷酸盐缓冲液中,加入ck18-m30单克隆抗体,混匀,于18~30℃避光反应30min;反应结束后进行透析,透析完成后加入甘油,过滤,加入r1稀释液,即得试剂r1;
30、其中,r1稀释液由磷酸盐缓冲液、无机盐、表面活性剂、保护剂、防腐剂混合制备而成;
31、s3、试剂r2的制备:
32、取吖啶酯置于标记缓冲液中,加入ck18-m30单克隆抗体,混匀,在18~30℃条件下避光反应30min;反应结束后加入终止缓冲液ⅱ,混匀,在18~30℃条件下避光反应30min;将反应产物进行透析,透析完成后加入甘油,过滤,加入r2稀释液,即得试剂r1;
33、其中,标记缓冲液由磷酸盐缓冲液、无机盐混合制备而成;
34、终止缓冲液ⅱ由磷酸盐缓冲液、gly缓冲液、无机盐混合制备而成;
35、r2稀释液由磷酸盐缓冲液、无机盐、表面活性剂、保护剂、防腐剂混合制备而成。
36、进一步地,步骤s1中所述edc溶液浓度为1mg/ml。
37、进一步地,步骤s2中所述甘油加入量与透析后溶液体积比为0.5:1;
38、步骤s3中所述甘油加入量与透析后溶液体积比为1:1;
39、步骤s2、s3中所述过滤为经过0.22μm滤膜过滤。
40、进一步地,步骤s2中透析条件:10mm磷酸盐缓冲液作为透析液在2~8℃进行透析,每2h更换一次透析液,共透析4次;
41、步骤s3中透析条件:透析液由磷酸盐缓冲液、无机盐混合制备而成,温度2~8℃,每2h更换一次透析液,共透析4次。
42、与现有技术相比,本发明的有益效果为:
43、本发明通过磁微粒上包被链霉亲和素、包被的链霉亲和素再与生物素化的ck18-m30单克隆抗体结合方式,构建了生物素放大系统,很大程度上改善了因空间位阻的影响;进一步摸索出当磁微粒与链霉亲和素的质量比为3:(0.1~1.0)、生物素与ck18-m30单克隆抗体的质量比为(1~5):1、ck18-m30单克隆抗体与吖啶酯质量比例为(2~8):1时,实现了磁微粒粒径的缩小,从而优化试剂盒的最低检测线,避免因磁微粒的粒径增大带来固相载体总表面积下降,进而导致结合在载体上的蛋白量下降等问题;能提高ck18-m30检测的灵敏度同时还扩大了ck18-m30检测的线性范围。
- 还没有人留言评论。精彩留言会获得点赞!