基于4-WJ结构触发的双重RCA扩增的电化学外泌体检测体系及其检测方法
本发明涉及肿瘤检测领域,具体涉及基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,还涉及利用该体系检测外泌体的方法。
背景技术:
1、肿瘤源性的外泌体(约30-150nm),是一种由恶性细胞分泌到细胞外环境,携带亲代癌症细胞的生物学信息的磷脂双分子层囊泡。因此,肿瘤源性外泌体被认为是癌症早期非侵入性液体活检的有应用前景的生物标志物。目前,许多方法,如纳米颗粒跟踪分析(nanoparticle tracking analysis,nta)、流式细胞术、酶联免疫吸附测定(enzyme-linked immunosorbent assay,elisa)、动态光散射(dynamic light scattering,dls)等,已被用于肿瘤源性外泌体测定。然而,这些方法较为昂贵和工艺流程复杂、灵敏度和特异性相对不足以及需要相应的标记的,这些均限制了技术应用。相比之下,电化学生物传感器在精确分析肿瘤源性外泌体方面近年来被逐步研发,因为它具有便携性、样品需求少、高灵敏度、成本低廉、易于信号放大和信号实时监测等优点。这些电化学测定方法利用外泌体表面特异性肿瘤生物标志物和信号探针与肿瘤标志物的高免疫亲和相互作用来鉴定肿瘤相关外泌体。然而,外泌体表面的肿瘤标志物种类繁多,且表达量较低,因此阻碍了对外泌体的高效检测。总之,在癌症早期,迫切需要建立一种具有高灵敏度和高特异性的方法从众多外泌体和非外泌体污染物(如蛋白质聚集物和脂蛋白)中来检测肿瘤来源的外泌体。
技术实现思路
1、有鉴于此,本发明的目的之一在于提供一种基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系;本发明的目的之二在于提供利用所述电化学外泌体检测体系检测外泌体的方法。
2、为达到上述目的,本发明提供如下技术方案:
3、1、基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,电化学外泌体检测体系包括电化学传感器的工作电极,dna四向连接结构,rca扩增体系和亚甲基蓝反应溶液;所述工作电极为功能化aunps修饰的电极;
4、所述功能化aunps修饰的电极为aunps修饰的电极表面连接特异识别外泌体的适配体1;
5、所述dna四向连接结构包括与外泌体识别的适配体2dna链,u链构成的分子信标探针以及由f链和m链构成的二元dna探针;所述适配体2dna链分别与f链和m链互补,所述u链与f链和m互补,杂交能形成dna四向连接结构;
6、所述亚甲基蓝反应溶液包括含1mm亚甲基蓝、ph 8.0、10mm hepes和100mm kcl。
7、本发明优选的,所述适配体1核酸链的序列如seq id no.1所示。
8、本发明优选的,所述适配体2dna链的序列如seq id no.2所示;所述u链的序列如seq id no.3所示;所述f链的序列如seq id no.4所示;所述m链的序列如seq id no.5所示。
9、本发明优选的,所述rca扩增体系包括浓度为10u/μl的phi29 dna聚合酶,10mmdntps,20mg/ml牛血清白蛋白、10×phi29dna聚合酶反应缓冲液,富含c碱基的cdna。
10、2、利用所述电化学外泌体检测体系检测外泌体的方法,包括如下步骤:
11、(1)功能化aunps修饰的电极的制备:将金电极抛光后在haucl4溶液中电沉积得到aunps修饰的电极,然后通过au-s键在电极表面组装硫化的适配体1,再用mch封闭电极,得到功能化aunps修饰的电极;
12、(2)制备待测血清:将待测全血样品以3500rpm离心10分钟,以收集浅黄色上清液作为待测样品;
13、(3)电化学方法检测:将制备的功能化aunps修饰的电极与含外泌体的待测样品孵育以捕获目标外泌体,用pbs漂洗后与含适配体2的结合缓冲液(1mm cacl2·2h2o,6mmmgcl2·6h2o,25mm c6h12o6·h2o)孵育形成apt2-t/exo/mch/apt1/aunps/ge,然后加入含有f链、m链和u链的结合缓冲液滴定到电极上,以形成dna四向连接结构,接着加入rca反应体系,产生大量g重复碱基,再将电极在亚甲基蓝反应溶液中孵育形成mb/g四联体结构,最后用电化学检测在20mm kcl、ph 8.0、20mm hepes中mb/g-四链体结构的电信号;
14、所述结合缓冲液各组分浓度如下:1mm cacl2·2h2o,6mm mgcl2·6h2o,25mmc6h12o6·h2o。
15、本发明优选的,所述rca反应体系中包括浓度为10u/μl的phi29 dna聚合酶,10mmdntps,20mg/ml牛血清白蛋白、10×phi29dna聚合酶反应缓冲液,富含c碱基的cdna。
16、本发明优选的,所述电化学检测参数为电位为-0.1v至-0.6v;脉冲周期:0.1s;振幅:0.01v;脉冲宽度:0.05s。
17、本发明优选的,所述电化学检测使用功能化aunps修饰的电极为工作电极,铂对电极、饱和甘汞参比电极组成的三电极系统。
18、本发明的有益效果在于:本发明公开基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,使用该体系检测具有如下优点:
19、1、恒温检测,避免了高温对肿瘤源性外泌体表面肿瘤标志物的破坏。
20、2、超灵敏检测,基于4-wj结构触发的双重rca扩增技术和亚甲基蓝/g-四联体dna酶技术,实现了低至20个/ml德痕量外泌体的超灵敏检测。
21、3、高特异性检测,双适配体三明治夹心结构和4-wj结构实现了高特异性检测,能够从多种外泌体混合物种准确检测目标外泌体。
22、4、具有普适性,该传感策略结构简单,仅需要根据目标外泌体表面肿瘤标志物更换相应适配体及dna探针,即可完成多种类型肿瘤源性外泌体的高灵敏、高特异性检测,且该传感器价格低廉,检测速度快,具有较高性价比。
技术特征:
1.基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,其特征在于:电化学外泌体检测体系包括电化学传感器的工作电极,dna四向连接结构,rca扩增体系和亚甲基蓝反应溶液;所述工作电极为功能化aunps修饰的电极;
2.根据权利要求1所述基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,其特征在于:所述适配体1核酸链的序列如seq id no.1所示。
3.根据权利要求1所述基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,其特征在于:所述适配体2dna链的序列如seq id no.2所示;所述u链的序列如seq id no.3所示;所述f链的序列如seq id no.4所示;所述m链的序列如seq id no.5所示。
4.根据权利要求1所述基于4-wj结构触发的双重rca扩增的电化学外泌体检测体系,其特征在于:所述rca扩增体系包括浓度为10u/μl的phi29 dna聚合酶,10mm dntps,20mg/ml牛血清白蛋白、10×phi29dna聚合酶反应缓冲液,富含c碱基的cdna。
5.利用权利要求1~4任一项所述电化学外泌体检测体系检测外泌体的方法,其特征在于,包括如下步骤:
6.根据权利要求5所述电化学外泌体检测体系检测外泌体的方法,其特征在于:所述rca反应体系中包括浓度为10u/μl的phi29 dna聚合酶,10mm dntps,20mg/ml牛血清白蛋白、10×phi29dna聚合酶反应缓冲液,富含c碱基的cdna。
7.根据权利要求5所述电化学外泌体检测体系检测外泌体的方法,其特征在于:所述电化学检测参数为电位为-0.1v至-0.6v;脉冲周期:0.1s;振幅:0.01v;脉冲宽度:0.05s。
8.根据权利要求5所述电化学外泌体检测体系检测外泌体的方法,其特征在于:所述电化学检测使用功能化aunps修饰的电极为工作电极,铂对电极、饱和甘汞参比电极组成的三电极系统。
技术总结
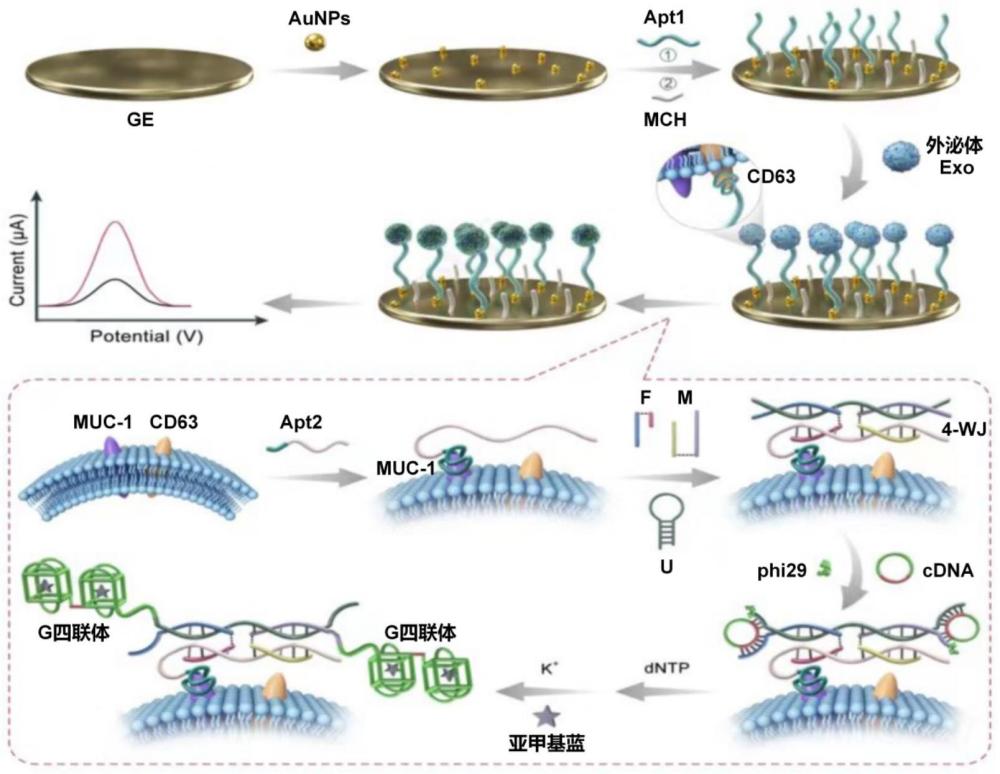
本发明公开了基于4‑WJ结构触发的双重RCA扩增的电化学外泌体检测体系,属于肿瘤检测领域;电化学外泌体检测体系包括电化学传感器的工作电极,通过金电极表面修饰纳米金颗粒以提高金电极表面积并有助于结合适配体1,在适配体1捕获靶外泌体后,外泌体进一步结合适配体2形成“三明治夹心”结构,该结构通过双重适配体可以显著提高检测特异性。随后,通过DNA四向连接结构(DNA four‑way junction,4‑WJ)触发的双重RCA体系实现目标信号的指数扩增;最后,通过亚甲基蓝/G‑四联体DNA酶技术有助于电化学信号的进一步放大,实现高灵敏度检测。
技术研发人员:阳莎,陈鸣,唱凯,赵著洋,冯柳,董振宇,罗兴,陈志国,邓瑞佳,盛静,袁梨嘉,陈卓
受保护的技术使用者:中国人民解放军陆军军医大学第一附属医院
技术研发日:
技术公布日:2024/1/5
- 还没有人留言评论。精彩留言会获得点赞!