T淋巴细胞制剂中的CD3抗体残留物的检测方法和试剂盒与流程
本发明涉及生物,特别涉及t淋巴细胞制剂中的cd3抗体残留物的检测方法和试剂盒。
背景技术:
1、t细胞免疫疗法是目前临床试验上最受关注和发展最快的肿瘤治疗方法之一。其基本操作是将患者自身的或经基因修饰的肿瘤特异性t细胞在体外纯化、激活、扩增培养制备成t淋巴细胞制剂,再回输到患者体内,利用t淋巴细胞的特异性杀伤作用实现靶向清除肿瘤细胞的目的。
2、cd3抗体是t细胞体外活化最常用的抗体。研究表明,tcr/cd3与抗原提呈细胞(apcs)表面特异的mhcⅱ抗原肽复合物结合产生的特异性抗原刺激信号是体内诱导t细胞的活化最重要的信号之一;在体外联合使用cd3抗体刺激t细胞,模拟t细胞活化的信号作用,是进行t细胞激活与扩增应用最广泛的方法。t淋巴细胞制剂中cd3抗体残留物的含量是t细胞制剂质量评价的重要参数之一,对细胞制剂产品的安全性和质量可控性水平都非常重要。目前现有的方法在cd3抗体残留物较少的情况下很难被检测到,特别是在ng/ml级别上的cd3抗体残留物检测准确度较低。因此建立一种高效,操作简便且准确度高的t淋巴细胞制剂中的cd3抗体残留物检测方法非常重要。
技术实现思路
1、有鉴于此,本发明目的在于建立一种高效,操作简便且准确度高的t淋巴细胞制剂中的cd3抗体残留物检测方法。本发明提供了t淋巴细胞制剂中的cd3抗体残留物的检测方法和试剂盒。本发明通过实验发现本发明测出的cd3抗体残留准确度高,能够准确反应测定样品cd3抗体的微量残余。本发明检测范围可达到12.5~800 pg/ml,相对回收率(re%)在80%~120%之间,为客观评价t淋巴细胞制剂的质量提供更准确的数据参考。
2、为了实现上述发明目的,本发明提供以下技术方案:
3、本发明提供了t淋巴细胞制剂中的cd3抗体残留物的检测方法,其包括如下步骤:
4、步骤1、取抗原包被于载体,清洗,封闭;
5、步骤2、清洗;
6、标准品组加入标准品溶液;
7、试验组加入供试品溶液;
8、孵育,清洗;
9、步骤3、空白对照组、所述标准品组和所述试验组分别加入标记抗体,孵育,清洗,显色,终止,于450 nm波长下分别获得所述空白对照组、所述标准品组和所述试验组的吸光度数据;
10、步骤4、以所述标准品组的吸光度数据减去所述空白对照组吸光度数据为纵坐标,以所述标准品溶液的浓度为横坐标,采用logistic曲线拟合获得标准曲线,根据所述试验组的吸光度数据,通过所述标准曲线获得所述cd3抗体残留物的检测结果;
11、所述抗原为cd3e&cd3d异二聚体蛋白;
12、所述标准品为anti-human cd3 mab;
13、所述供试品为含cd3抗体为原料的t淋巴细胞制剂。
14、在本发明的一些具体实施方案中,所述t淋巴细胞制剂包括中央记忆型t淋巴细胞制剂。
15、在本发明的一些具体实施方案中,所述cd3e&cd3d异二聚体蛋白的包被量为0.1 μg/单位载体;
16、所述抗原包被的条件为2~8℃下包被过夜;
17、所述清洗的洗液为磷酸钠盐;
18、所述清洗的次数为3次。
19、在本发明的一些具体实施方案中,所述载体为酶标板;
20、在本发明的一些具体实施方案中,所述cd3e&cd3d异二聚体蛋白的包被量为0.1 μg/孔。
21、在本发明的一些具体实施方案中,所述磷酸钠盐为1×pbst。
22、在本发明的一些具体实施方案中,所述1×pbst的制备方法包括:取pbs粉末1袋,加2 l灭菌注射用水,充分溶解;再加入1 ml tween20,充分混匀,获得所述1×pbst。
23、在本发明的一些具体实施方案中,所述清洗的条件为3次,每次用量为300 μl/单位载体。
24、在本发明的一些具体实施方案中,所述封闭的时间为1小时;
25、所述封闭所采用的封闭液为含质量体积比为2%bsa的pbst溶液或含质量体积比为5%脱脂奶粉的pbst溶液。
26、在本发明的一些具体实施方案中,所述封闭液的用量为300 μl/单位载体。
27、在本发明的一些具体实施方案中,所述封闭所采用的封闭液为含质量体积比为2%bsa的pbst溶液。
28、在本发明的一些具体实施方案中,步骤2所述孵育为25℃±5℃孵育2小时。
29、在本发明的一些具体实施方案中,步骤3所述孵育为25℃±5℃避光孵育1小时。
30、在本发明的一些具体实施方案中,所述标记抗体溶液的浓度为0.05μg/单位载体。
31、在本发明的一些具体实施方案中,所述标记抗体的标记物为辣根过氧化物酶(hrp)、生物素(biotin)、异硫氰酸荧光素(fitc)或碱性磷酸酶(ap)。
32、在本发明的一些具体实施方案中,所述标记抗体的来源为兔抗、鼠抗、羊抗或重组的igg抗体。
33、在本发明的一些具体实施方案中,所述标记抗体为hrp标记的山羊抗小鼠igg2a。
34、在本发明的一些具体实施方案中,所述显色的时间为10~15分钟;
35、所述显色所采用的显色液为显色液tmb。
36、在本发明的一些具体实施方案中,所述封闭液的用量为100μl/单位载体。
37、在本发明的一些具体实施方案中,所述终止所采用的终止液的用量为50μl/单位载体。
38、在本发明的一些具体实施方案中,所述检测方法具体包括如下步骤:
39、步骤1、取cd3e&cd3d异二聚体蛋白蛋白,灭菌注射用水调整其浓度为600 μg/ml,1×包被液进行600倍稀释制成终浓度为1 μg/ml包被蛋白溶液;将1 μg/ml的包被蛋白溶液加入至空酶标板中,每孔100 μl,置于2℃~8℃条件下过夜包被,获得包被酶标板;取出包被酶标板恢复至25℃±5℃,洗液清洗3次,300 μl/孔,最后1次弃液后如果孔内有残留液体,在吸水纸上拍干;每孔加入300 μl封闭液,25℃±5℃封闭1小时;
40、步骤2、洗液清洗3次,300 μl/孔,最后1次弃液后如果孔内有残留液体,在吸水纸上拍干;标准品组加入标准品溶液、试验组加入供试品溶液,100µl/孔,每组设置2个复孔,封板膜封板,25℃±5℃孵育2小时;
41、步骤3、洗液清洗3次,300 μl/孔,最后1次弃液后如果孔内有残留液体,在吸水纸上拍干;空白对照组、所述标准品组和所述试验组每孔分别加入标记抗体溶液,100 µl/孔,封板膜封板,25℃±5℃避光孵育1小时;洗液清洗3次,300 μl/孔,最后1次弃液后如果孔内有残留液体,在吸水纸上拍干;每孔加入显色液tmb,100 µl/孔,封板膜封板,25℃±5℃避光孵育10~15分钟;每孔加入终止液,50 µl/孔,混匀后使用酶标仪测量450 nm波长处的吸光度值;
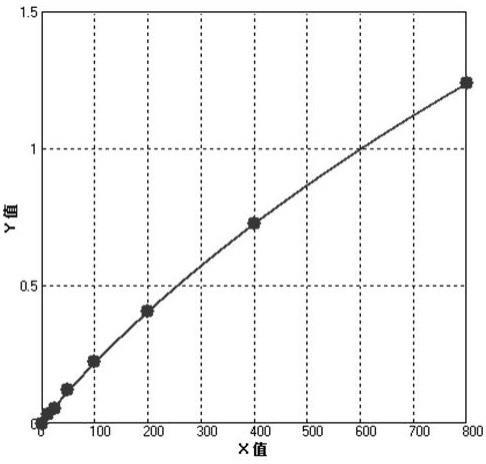
42、步骤4、以标准品组的吸光度值均值减去空白对照组均值为纵坐标y,以标准品理论浓度为横坐标x,采用logistic曲线(四参数)拟合作图,得到标准曲线回归方程及相关系数r2;从标准曲线上由y计算x,得出供试品的实测浓度值;如果供试品经过了预先稀释,根据标准曲线所得出的供试品浓度要再乘以其稀释倍数;
43、所述标准品为anti-human cd3 mab;
44、所述供试品为以cd3为原料的t淋巴细胞制剂。
45、在本发明的一些具体实施方案中,所述检测方法的检测范围为12.5~800 pg/ml。
46、本发明还提供了用于t淋巴细胞制剂中的cd3抗体残留物检测的试剂盒,包括cd3e&cd3d异二聚体蛋白,封闭液和标记抗体;
47、所述cd3e&cd3d异二聚体蛋白和所述标记抗体的质量比为2:1;
48、所述封闭液为含质量体积比为2%bsa的pbst溶液或含质量体积比为5%脱脂奶粉的pbst溶液。
49、在本发明的一些具体实施方案中,还包括显色液tmb。
50、本发明包括但不限于取得了如下有益效果:
51、本发明检测范围可达到12.5~800 pg/ml,相对回收率(re%)在80%~120%之间,为客观评价t淋巴细胞制剂的质量提供更准确的数据参考。
- 还没有人留言评论。精彩留言会获得点赞!