检测肺癌相关自身抗体的试剂盒及其制备方法、检测方法与流程
本发明涉及医学、免疫,体外诊断,具体而言,涉及检测肺癌相关自身抗体的试剂盒及其制备方法、检测方法。
背景技术:
1、癌症是人类第二大死因。其发病率和死亡率双高,且耗费医疗资源巨大,是当今全球公认的一大负担。其中肺癌是癌症最常见的类型,同时也是全球癌症相关死亡的主因之一。发展具有检测最早期肿瘤的敏感性和减少假阳性的特异性的技术是肿瘤早筛领域的一个关键挑战。
2、目前肿瘤检查中使用技术有各类影像学检查,如x光摄影、ct检查、磁共振成像等和超声波检查,以及肿瘤标志物检查。x光摄影受制于影像相互重叠和隐藏。b超检查受气体干扰很大。ct检查费用昂贵,而且辐射通常高于单次x光摄影。磁共振成像检查费用也较贵。组织病理活检往往也因存在机械性损伤和具备感染风险而不被作为肿瘤筛查的首选;由于上述方法灵敏度低,在肿瘤最早期,影像学检查不仅具有滞后性,导致患者无法及时在疾病早期发现肿瘤细胞的存在而错过最佳治疗时期。而在相同时间,肿瘤相关自身抗体已可分泌入血。因此,检测肿瘤标志物是恶性肿瘤早期诊断的最简便、基本无创,有重要价值且不可或缺的方法。
3、肿瘤相关自身抗体作为一种稳定表达的血清学检测指标在肿瘤早期筛查中占据重要地位。不同器官来源的肿瘤细胞,其刺激机体产生的肿瘤相关自身抗体往往也不相同,临床上可通过选择不同类型的自身抗体反映不同器官来源的肿瘤的进展。以肺癌抗原的自身抗体作为肿瘤诊断的标志物,利用肿瘤抗原来检测肿瘤自身抗体,与其他的诊断方法相比具有很高的特异性和敏感性,为真正在临床上对肿瘤进行早期筛查提供可能。
4、目前用于检测肺癌相关自身抗体的免疫分析方法主要有膜条法、间接免疫荧光法、酶联免疫分析法。这些方法都存在着一些不足之处。膜条法和间接免疫荧光法是定性检测,酶联免疫分析法使用专用微孔板,在使用时无法进行独立单人份检测;试剂种类较多,操作繁琐,耗时较长,常需要超过2个小时才能得到测试结果。无法实现全自动化,检测结果的准确度和精密度较差,此外还存在特异性和灵敏度不高,测定范围窄等限制因素。
5、因此,亟需一种高灵敏度的、宽检测范围的、高效率可推广的全自动肺癌相关自身抗体的检测方法。
技术实现思路
1、本发明提供一种检测肺癌相关自身抗体的试剂盒及其制备方法、检测方法,采用管式磁微粒化学发光法用在肺癌相关自身抗体的检测上,可以提高肺癌自身抗体检测的灵敏度,拓宽线性范围的,批次间差异小,高效高通量的全自动检测试剂盒,为肺癌早筛辅助诊断提供支持。
2、为此,本发明的第一目的在于提供一种检测肺癌相关自身抗体的试剂盒;
3、本发明的第二目的在于提供一种检测肺癌相关自身抗体的试剂盒的制备方法;
4、本发明的第三目的在于提供一种检测肺癌相关自身抗体的试剂盒的检测方法;
5、为实现本发明的第一目的,本发明提供一种检测肺癌相关自身抗体的试剂盒,试剂盒包括固相试剂、发光试剂、校准品和质控品,固相试剂为抗原蛋白-磁微粒偶联物,磁微粒的浓度为0.1mg/ml-0.6mg/ml。
6、在本发明的一个技术方案中,抗原蛋白包括lin28b、p53、ny-eso-1、cage、annexin1、sox2、pgp9.5、magea1、gage7、gub4-5、hud、mage a4、top2a、actr3、rps6ka5、psip1、bcl7a、trim33、mterf4、ctag1a、ddx4、magec2、muc17、camsap2、kif13b、smg1、med14、alms1、gcc2、timeless、tns1、atp1a4、hrnr、pgp9.5、gage7、gbu4-5、mage a1、ct47a、page3、vcx、birc5和mageb1中的一种或多种;和/或发光试剂包括吖啶酯标记的抗体液;其中,抗体液包括抗人igg抗体液、抗人igm抗体液、抗人iga抗体液中的一种或多种,抗体液浓度为0.1μg/ml-1.0μg/ml,标记抗体为单克隆抗体或多克隆抗体。
7、在本发明的一个技术方案中,固相试剂、发光试剂、校准品和质控品包括稀释液,稀释液包括缓冲盐、无机盐、表面活性剂、消泡剂、保护剂和防腐剂。
8、优选的,缓冲盐包括tris、hepes、mes、磷酸盐中的一种或多种;和/或缓冲盐的浓度为10mm-100mm;和/或无机盐包括氯化钠、氯化钾、氯化镁中的一种或多种;和/或无机盐的浓度为50mm-500mm;和/或表面活性剂包括吐温20、吐温80、曲拉通-405、聚氧乙烯月桂醚、np-40中的一种或多种;和/或表面活性剂的浓度为0.02%-0.5%;和/或消泡剂包括tsa-530、tsa-830、tsa-850中的一种或多种;和/或消泡剂的浓度为0.01%-0.1%;和/或保护剂包括牛血清白蛋白、牛igg、鱼明胶、蔗糖中的一种或多种;和/或蛋白保护剂的浓度为0.1%-5%;和/或防腐剂包括proclin300、硫柳汞、叠氮钠中的一种或多种;和/或防腐剂的浓度为0.1%-5%。
9、与现有技术相比,采用该技术方案所达到的技术效果:试剂盒包括固相试剂、发光试剂、校准品和质控品,管式化学发光兼具化学发光免疫分析技术的自动化程度高、检测过程高效稳定和灵敏度高等优势,同时又避免了板式化学发光由于底物、方法学、和加样针清洗技术的的限制导致易发生携带污染、重复性差的问题。此外管式化学发光可以做到标本随到随测,无本底与孔间交叉污染,结果可靠,急诊项目可随时优先插入,方便了患者同时也节约了检测科室人力投入,更提高了检测的效率;固相试剂为抗原蛋白-磁微粒偶联物,磁微粒的浓度为0.1mg/ml-0.6mg/ml,将磁微粒作为载体,具有独特的3d表面和较高的比表面积,为捕获目标分子提供了充分的接触面积。与此同时,磁微粒所具有的超顺磁性可以实现短时间内高效多次磁性分离,有利于加快检测速度以及仪器的全自动化。
10、为实现本发明的第二目的,本发明提供一种检测肺癌相关自身抗体的试剂盒的制备方法,制备方法包括:
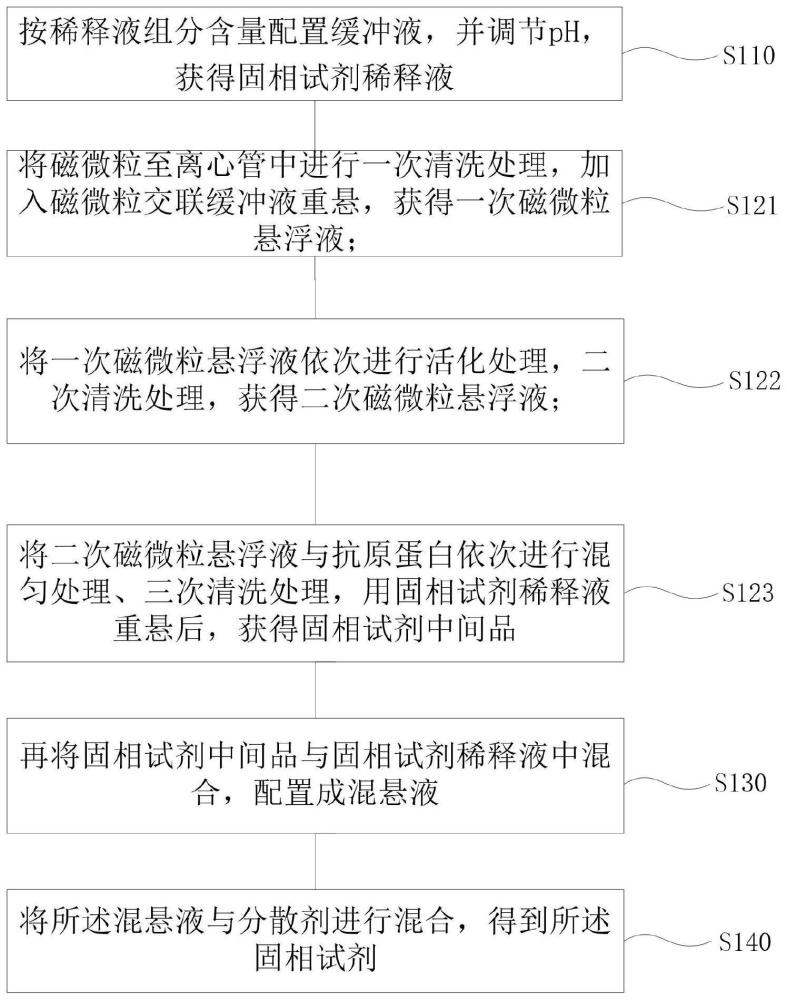
11、s100、制备固相试剂:s110、按稀释液组分含量配置缓冲液,并调节ph,获得固相试剂稀释液;s120、将抗原蛋白与磁微粒混合,制备成固相试剂中间品;s130、再将固相试剂中间品与固相试剂稀释液中混合,配置成混悬液;s140、将混悬液与分散剂进行混合,得到固相试剂;
12、s200、制备发光试剂:s210、按稀释液组分含量配置缓冲液,并调节ph,获得发光试剂稀释液;s220、将吖啶酯标记抗体液上,制备成发光试剂中间品;s230、将发光试剂中间品加入发光试剂稀释液中,配置成发光试剂工作液;
13、s300、制备校准品:s310、按稀释液组分含量配置缓冲液,并调节ph,获得校准质控稀释液;s320、取重组人源化抗体和校准质控稀释液,进行稀释配制,用校准质控稀释液将人源化抗体配置成6点校准品,分别记为s1、s2、s3、s4、s5和s6,按每瓶0.5ml分装,-20℃保存备用;
14、s400、制备质控品:将人源化抗体按照一定的比例添加到校准质控品稀释液中,配置成2点质控品溶液,分别记为qc1、qc2。
15、在本发明的一个技术方案中,在s120中包括:
16、s121、将磁微粒至离心管中进行一次清洗处理,加入磁微粒交联缓冲液重悬,获得一次磁微粒悬浮液;
17、s122、将一次磁微粒悬浮液依次进行活化处理,二次清洗处理,获得二次磁微粒悬浮液;
18、s123、将二次磁微粒悬浮液与抗原蛋白依次进行混匀处理、三次清洗处理,获得固相试剂中间品。
19、优选的,在s121中,一次磁微粒悬浮液的浓度为10mg/ml;和/或在s122中,二次磁微粒悬浮液的浓度为10mg/ml。
20、在本发明的一个技术方案中,在s220中包括:
21、s221、将吖啶酯用有机溶剂溶解后,进行避光干燥处理,得到第一反应物;
22、s222、取抗体液加交联缓冲液进行一次稀释处理,再加入第一反应物充分混匀后,避光反应,制备成第二反应物;
23、s223、将第二反应物经脱盐纯化处理,得到发光试剂中间品。
24、优选的,在s221中,避光干燥处理的温度为-30℃-10℃;和/或在s222中,一次稀释处理后的浓度0.5mg/ml-2mg/ml;和/或在s222中,避光反应的温度为20℃-30℃,时间为0.5h-1.5h。
25、与现有技术相比,采用该技术方案所达到的技术效果:固相试剂制备过程中加入了分散剂的处理步骤,可去除了封闭处理步骤,并且固相发光稀释液中同时引入了消泡剂,可达到拓宽试剂盒线性范围,提高灵敏度、重复性和稳定性,降低批间差的效果,同时降低了客户端使用时由于操作不规范等带来的泡沫增加引起的吸样不一致,蛋白变性等风险。并且校准品及质控品均为液体即用型,稳定性好,避免冻干品复溶、平衡等待等繁杂的操作,提高的操作效率,简化了操作步骤,同时可以减少人为可能引入的误差,结果更准确。
26、为实现本发明的第三目的,本发明提供了一种检测肺癌相关自身抗体的试剂盒的检测方法,测定仪器为ms-i3080全自动化学发光仪,检测肺癌相关自身抗体的试剂盒的检测方法包括以下步骤:将样本和固相试剂,在37℃孵育15min,获得第一反应体系;将发光试剂与第一反应体系混合,在37℃孵育15分钟,获得第二反应体系;将第二反应体系测量相对发光单位rlu,并计算相对应的浓度值;其中以校准品浓度为横坐标,各浓度校准品对应的rlu为纵坐标,作logit-log(4p)函数曲线。
27、与现有技术相比,采用该技术方案所达到的技术效果:本发明试剂盒搭载ms-i3080全自动化学发光仪,实现进样、加试剂、清洗、检测、计算等一系列流程的全自动化,提高检测效率;同时管式化学发光可以做到标本随到随测,无本底与孔间交叉污染,结果可靠,急诊项目可随时优先插入,方便了患者同时也节约了检测科室人力投入,更提高了检测的效率。
28、采用本发明的技术方案后,能够达到如下技术效果:
29、(1)管式化学发光兼具化学发光免疫分析技术的自动化程度高、检测过程高效稳定和灵敏度高等优势,同时又避免了板式化学发光由于底物、方法学、和加样针清洗技术的的限制导致易发生携带污染、重复性差的问题。此外管式化学发光可以做到标本随到随测,无本底与孔间交叉污染,结果可靠,急诊项目可随时优先插入,方便了患者同时也节约了检测科室人力投入,更提高了检测的效率;
30、(2)磁微粒作为载体,具有独特的3d表面和较高的比表面积,为捕获目标分子提供了充分的接触面积。与此同时,磁微粒所具有的超顺磁性可以实现短时间内高效多次磁性分离,有利于加快检测速度以及仪器的全自动化;
31、(3)试剂盒使用的固相试剂中间品制备过程中加入了分散剂的处理步骤可,去除了封闭处理步骤,并且固相发光稀释液中同时引入了消泡剂,可达到拓宽试剂盒线性范围,提高灵敏度、重复性和稳定性,降低批间差的效果,同时降低了客户端使用时由于操作不规范等带来的泡沫增加引起的吸样不一致,蛋白变性等风险;
32、(4)本发明试剂盒搭载ms-i3080全自动化学发光仪,实现进样、加试剂、清洗、检测、计算等一系列流程的全自动化,提高检测效率;
33、(5)校准品及质控品均为液体即用型,稳定性好,避免冻干品复溶、平衡等待等繁杂的操作,提高的操作效率,简化了操作步骤,同时可以减少人为可能引入的误差,结果更准确。
- 还没有人留言评论。精彩留言会获得点赞!