检测人血基质中抗癫痫药物浓度的质控品、试剂盒及方法与流程
本发明属于药物检测,涉及一种检测人血基质中抗癫痫药物浓度的质控品、试剂盒及方法,尤其涉及一种采用液相色谱串联质谱检测人血基质中抗癫痫药物浓度的质控品、试剂盒及方法。
背景技术:
1、癫痫是一种常见的、复杂的慢性神经系统疾病,患病率为0.5-1%,其特征是反复发作。癫痫发作的临床表现是部分或全身性抽搐和意识障碍,癫痫发作的频率和节奏大多无法预测。因此,癫痫发作对患者来说不仅是相当大的心理和生理负担,而且还可能导致严重甚至危及生命的伤害(如摔倒时的颅脑损伤)。临床上癫痫通常采用单一用药或联合用药的方式进行治疗,传统抗癫痫药物如苯妥英钠、卡马西平、丙戊酸钠,治疗范围狭窄,毒性较强,易发生不良反应,需要定期监测血药浓度。随着医药水平的提高,出现了很多新型抗癫痫药物如拉莫三嗪、奥卡西平、托吡酯、左乙拉西坦等,相较于传统抗癫痫药物,它们的治疗效果更好,毒副反应低,但需长期服药。患者服用抗癫痫药物后,在药代动力学上存在较大的个体差异,即便是经同一途径使用相同剂量药物,也会出现各不相同的治疗反应。因此,为了确保患者用药的安全性和有效性,必须确定个别患者的治疗性药物剂量,然后在临床治疗中需要开展及时、准确的治疗药物监测,定期检测患者体内的药物浓度,制定最佳的个体化给药方案。
2、检测人血基质中抗癫痫药物的浓度,对于评估抗癫痫疗效、避免发生不良反应具有重要意义。抗癫痫药物的临床检测方法主要为色谱法,常用的色谱法包括高效液相色谱法(hplc)、液相色谱串联质谱检测法(lc-ms/ms)等。公布号为cn112946101a的中国发明申请,公开了一种同时测定多种抗癫痫药物在血液中含量的方法及其应用,采用蛋白沉淀法结合hplc-ms/ms测定9种抗癫痫药物卡马西平、10, 11-二氢-10-羟基卡马西平、奥卡西平、左乙拉西坦、托吡酯、丙戊酸、苯妥英、苯巴比妥和拉莫三嗪在血浆中的含量。
3、公布号为cn116500158a的中国发明申请,公开了一种血液样本抗癫痫类药物检测方法和试剂盒,该检测方法检测的抗癫痫类药物包括卡马西平、环氧卡马西平、奥卡西平、10,11-二氢-10-羟基卡马西平、苯妥英钠、拉莫三嗪、左乙拉西坦、普瑞巴林、加巴喷丁、托吡酯、丙戊酸、苯巴比妥和拉科酰胺。该检测方法包括将经过前处理的待测样本使用高效液相色谱串联质谱检测,将检测值带入标准曲线中,计算得到血液样本中抗癫痫类药物的含量;前处理包括采用沉淀剂处理待测样本,沉淀剂中含有内标,内标为抗癫痫类药物的同位素。
4、近年来,临床检验行业对检测质量控制重视程度不断提高。而最有效的质量控制手段就是建立完善的“室内质量控制程序”并参与“室间质评活动”。我国自1982年,就开始了全国范围内的临床检验室间质量评价活动,一定程度上提高了检验结果的质量。但室内质控环节却更多地取决于医院应用质控品,建立合理的质控程序对日常检测质量进行监控。同时,合理有效的室内质控也是在室间质评中取得好成绩的必要保证。
5、质控品作为室内质控的载体,对室内质控程序的建立及效果有着至关重要影响。研制与检测系统匹配的质控品,用来监测系统精密度、准确度的抗癫痫药物质控品,成为目前亟待解决的问题。
6、现有的抗癫痫药物浓度检测试剂盒,校准品、质控品的基质一般为人全血、血清或血浆,来源受限,不能商品化买卖,所以需要采用动物全血、血清或血浆作为替代基质。但动物来源的替代基质中可能存在干扰物质,影响试剂盒的稳定性。现有的抗癫痫药物检测方法,不能实现同时检测丙戊酸、卡马西平、卡马西平-10,11-环氧化物、奥卡西平、10, 11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦、氯硝西泮;尤其是奥卡西平与卡马西平-10,11-环氧化物结构类似物、离子对相同,现有检测方法无法实现同时检测。需要开发新的试剂盒和检测方法,解决上述技术问题,更好满足检测人血基质中抗癫痫药物浓度的临床需求。
技术实现思路
1、为了解决现有技术存在的技术问题,本发明的目的是提供一种检测人血基质中抗癫痫药物浓度的试剂盒及方法,通过对动物全血、血清或血浆进行处理,降低基质效应,去除杂质干扰,从而提高试剂盒的稳定性;通过改进测试参数,使得奥卡西平与卡马西平10,11-环氧化物得以分离,10种抗癫痫药物及2种活性代谢物在各自线性范围内线性关系良好,准确度和精密度良好,专属性强,稳定性高,符合生物样品的分析要求,满足常用抗癫痫药物在人血基质中的检测要求,适用于抗癫痫药物监测。本发明的目的通过以下具体技术方案得以实现。
2、本发明的首要方面是提供一种检测人血基质中抗癫痫药物浓度的质控品,所述抗癫痫药物包括丙戊酸、卡马西平、卡马西平-10, 11-环氧化物、奥卡西平、10, 11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦和氯硝西泮;所述质控品为冻干制剂,所述质控品用经过滤和吸附处理除去干扰杂质的动物血液基质配制,动物血液基质中加入所述抗癫痫药物、保护剂、赋形剂、防腐剂和抗氧化剂。
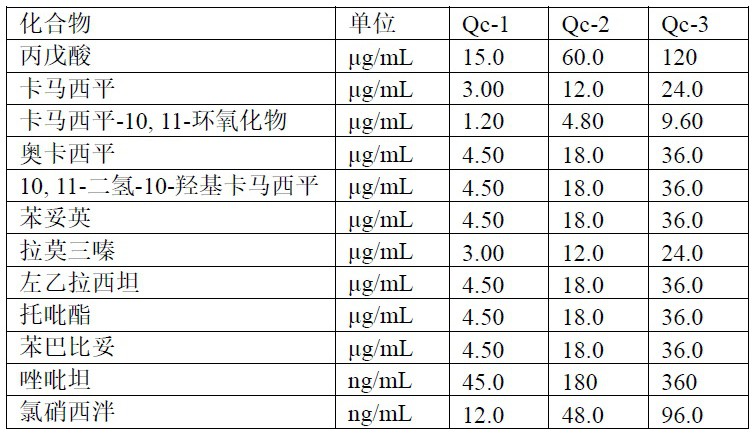
3、进一步的,所述质控品为qc-1、qc-2和qc-3;各质控品中抗癫痫药物的工作浓度如表1所示。
4、表1 各质控品中各物质的工作浓度
5、
6、进一步的,所述动物血液基质为兔血清或血浆。
7、进一步的,所述保护剂为蔗糖和海藻糖中的一种或两种,浓度分别为0.5-1.5wt%、1.0-3.0wt%;赋形剂为甘露醇和甘氨酸中的一种或两种,浓度分别为1.0-3.0wt%、1.0-3.0wt%;防腐剂为proclin300,浓度为0.05-0.3wt%;所述抗氧化剂为抗坏血酸,浓度为0.25-0.75wt%。
8、本发明的再一方面是提供一种检测人血基质中抗癫痫药物浓度的试剂盒,包括校准品、前述质控品、内标、沉淀剂,所述校准品为冻干制剂;所述校准品用经过滤和吸附处理除去干扰杂质的动物血液基质配制,动物血液基质中加入所述抗癫痫药物、保护剂、赋形剂、防腐剂和抗氧化剂。本发明的试剂盒中的校准品、质控品37℃热加速稳定性可稳定存储30天;而使用未去除杂质的基质配制的校准品、质控品,37℃热加速稳定性存储30天后,丙戊酸、奥卡西平、托吡酯、唑吡坦存在趋势性变化。
9、进一步的,所述内标为同位素标记的抗癫痫类药物,分别为卡马西平-d10、卡马西平-10, 11-环氧化物-d10、奥卡西平-d4、10, 11-二氢-10-羟基卡马西平-d4、拉莫三嗪-13c3、左乙拉西坦-d6、唑吡坦-d7、氯硝西泮-d4、丙戊酸-d6、苯妥英-d10、托吡酯-d12、苯巴比妥-d5的混合溶液,卡马西平-d10浓度为1.0μg/ml、卡马西平-10, 11-环氧化物-d10浓度为1.0μg/ml、奥卡西平-d4浓度为1.0μg/ml、10, 11-二氢-10-羟基卡马西平-d4浓度为1.0μg/ml、拉莫三嗪-13c3浓度为1.0μg/ml、左乙拉西坦-d6浓度为1.0μg/ml、唑吡坦-d7浓度为20ng/ml、氯硝西泮-d4浓度为10ng/ml、丙戊酸-d6浓度为1.0μg/ml、苯妥英-d10浓度为1.0μg/ml、托吡酯-d12浓度为1.0μg/ml、苯巴比妥-d5浓度为1.0μg/ml。
10、进一步的,所述沉淀剂为甲醇。
11、进一步的,所述校准品为cal-1、cal-2、cal-3、cal-4、cal-5和cal-6;各校准品中抗癫痫药物的工作浓度如表1所示。
12、表2 各校准品中抗癫痫药物的工作浓度
13、
14、本发明的又一方面是提供上述试剂盒的制备方法,包括以下步骤:
15、s1准备动物血液基质,具体包括:
16、s1-1取动物血液基质原料,用微孔滤膜过滤;
17、s1-2向过滤后的动物血液基质中加入活性炭,活性炭的加入量为血液基质的10-50wt%,吸附、振荡后离心,取上清液;
18、s1-3向活性炭吸附后的上清液中加入吸附树脂,吸附树脂的加入量为活性炭吸附后的上清液的10-50wt%,吸附、振荡后离心,取上清液;吸附树脂可以选自xad-4大孔树脂、交联树脂和110树脂等吸附树脂中的一种;
19、s1-4重复步骤s1-2和s1-3,直至动物血液基质中的杂质含量降到100ppm以下;
20、s1-5加入保护剂、赋形剂、防腐剂和抗氧化剂,得到动物血液基质产品;
21、s2配制校准品和质控品半成品:按照不同水平的校准品和质控品的浓度要求,向步骤s1得到的动物血液基质产品中加入丙戊酸、卡马西平、卡马西平-10, 11-环氧化物、奥卡西平、10, 11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦和氯硝西泮,搅拌均匀,检验丙戊酸、卡马西平、卡马西平-10, 11-环氧化物、奥卡西平、10, 11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦和氯硝西泮的浓度,检验合格后得到校准品和质控品半成品;
22、s3制备校准品和质控品成品:将步骤s2得到的校准品和质控品半成品,按照包装要求分装,然后冻干,得到校准品和质控品成品;
23、s4 制备内标:按照内标浓度要求制备卡马西平-d10、卡马西平-10, 11-环氧化物-d10、奥卡西平-d4、10, 11-二氢-10-羟基卡马西平-d4、拉莫三嗪-13c3、左乙拉西坦-d6、唑吡坦-d7、氯硝西泮-d4、丙戊酸-d6、苯妥英-d10、托吡酯-d12、苯巴比妥-d5的混合溶液;
24、s5组装试剂盒:将步骤s3得到的校准品和质控品成品、s4制备的内标以及沉淀剂组装,得到试剂盒产品。
25、本发明的另一方面是提供采用上述试剂盒检测人血基质中抗癫痫药物浓度的方法,包括以下步骤:
26、s1检测前溶液准备:
27、a)校准品、质控品:在室温下,向盛放校准品和质控品的冻干粉瓶中按要求加入蒸馏水,在室温下孵育20至30分钟;旋转冻干粉瓶,使内容物溶解直至均匀;
28、b)内标:将试剂盒中的内标取出,恢复至室温,使用前涡旋振荡;
29、c)取出样本萃取液,室温放置,充分平衡后使用;
30、s2检测样本制备:
31、a)样本准备:将血清样本取出,恢复至室温备用,使用前涡旋振荡;
32、b)样本制备:使用移液器移取样本至离心管,加入内标及甲醇,涡旋振荡混匀3-5分钟;将离心管置于离心机中,离心后分离上清液;
33、s3 样本检测:
34、转移上清液至u型板中,置于进样器中,使用液相色谱串联质谱仪进行检测,检测参数如下:
35、色谱条件:
36、色谱柱:c18 (100×2 .1mm,3.0μm, 175 å),或其他性能相当者;
37、流动相a1:0.1%甲酸-2mm乙酸铵水溶液,取998 ml纯水+1.0ml甲酸+1.0ml 2m乙酸铵,摇匀,超声5min;
38、流动相b1:0.1%甲酸甲醇溶液,取999 ml甲醇+1.0ml甲酸,摇匀,超声5min;
39、流动相a2:2mm乙酸铵水溶液,取999 ml纯水+1.0ml 2m乙酸铵,摇匀,超声5min;
40、流动相b2:甲醇溶液,取1000 ml甲醇;
41、柱温:30-40℃;
42、流速:0.3-0.4 ml/min;
43、梯度洗脱条件如表3和表4所示:
44、表3 正离子模式洗脱条件
45、
46、表4 负离子模式洗脱条件
47、
48、质谱条件如表5和表6所示:
49、表5 源参数
50、
51、表6 质谱参数
52、
53、通过上述色谱条件梯度洗脱可实现奥卡西平与卡马西平-10,11-环氧化物完全分离,通过上述质谱条件可实现丙戊酸、卡马西平、卡马西平-10,11-环氧化物、奥卡西平、10,11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦、氯硝西泮同时检测,能够满足常用抗癫痫药物在人血基质中的检测要求,适用于抗癫痫药物监测。
54、本发明相对于现有技术具有以下有益技术效果:本发明提供的试剂盒中的校准品、质控品37℃热加速可稳定存储30天,均一性均小于10%,可长期存储使用;本发明所述检测方法可实现奥卡西平与卡马西平-10,11-环氧化物完全分离,可实现同时检测丙戊酸、卡马西平、卡马西平-10,11-环氧化物、奥卡西平、10, 11-二氢-10-羟基卡马西平、苯妥英、拉莫三嗪、左乙拉西坦、托吡酯、苯巴比妥、唑吡坦、氯硝西泮同时检测,能够满足常用抗癫痫药物在人血基质中的检测要求,适用于抗癫痫药物监测;本发明提供的多检测系统赋值的抗癫痫药物浓度质控品可用于监测系统精密度、准确度。
- 还没有人留言评论。精彩留言会获得点赞!