基于布尔网络吸引域模拟干预肿瘤细胞状态的方法与流程
本发明涉及系统生物学研究技术领域,尤其涉及一种基于布尔网络吸引域模拟干预肿瘤细胞状态的方法。
背景技术:
在基因组时代,人们主要探讨的是静态碱基测序的问题,其具体任务是建立可以体现生物全基因组结构的图谱,到了后基因组时代,人们则开始重点探究非静态的功能注释领域的问题,它通过对各种高通量技术所获得的基因表达数据进行具体的分析、处理和建模,来帮助人们理解基因的功能,更好的认清基因与疾病的关系,进而设计适当的干预策略来影响、改变系统的动态行为。因此,人们发现除了直接分析表达数据,还能够更深入地理解基因在影响健康与疾病工程过程中的基本机制。
随着计算机技术的发展,基因调控网络(Genetic regulatory networks,GRN)的研究成为21世纪生物学研究的一个很重要的领域,也成为系统生物学研究的一个热点问题,使得越来越多的科研人员开始关注基因调控网络。基因调控网络是由细胞中参与基因调控作用的DNA,RNA,蛋白质以及代谢中间物所形成的相互作用的网络,其节点会随着时间的变化而变化的,并且基因调控网络中细胞内的蛋白质浓度是基因调控网络动力学机制的最基本的驱动因素,它决定了细胞分化的时间和空间特性,还可以作为细胞的一种“记忆机制”。因此通过构造出的基因调控网络,人们能够更好的认识基因与基因之间的相互作用关系,从而进一步理解特定组织的遗传调控机制,开发合适的疾病(如癌症)治疗方法,这对于揭示生命现象的本质具有重要意义。
因此,亟需一种以基因调控网络为模型来模拟干预肿瘤细胞状态的方法,能够模拟干预肿瘤细胞状态,为肿瘤治疗研究提供一个有力的理论框架。
技术实现要素:
本发明实施例的目的在于提供一种基于布尔网络吸引域模拟干预肿瘤细胞状态的方法,能够模拟干预肿瘤细胞状态,为肿瘤治疗研究提供一个有力的理论框架。
为了解决上述技术问题,本发明实施例提供了一种基于布尔网络模拟干预肿瘤细胞状态的方法,所述方法包括:
a、利用基因芯片采集技术获取生物样本基因的连续表达谱数据,并根据所述获取到的连续表达谱数据,构建布尔网络模型的基因调控网络;
b、确定所述基因调控网络干预前所有状态下的暂态数BOS及其包含的所有期望吸引子和不期望吸引子,并根据所述基因调控网络干预前所有状态下的暂态数BOS及其包含的所有期望吸引子和不期望吸引子,筛选出满足预定条件的干预位,且进一步得到所筛选干预位干预后基因调控网络的暂态数BOS;
c、根据所述得到的所筛选干预位干预后基因调控网络的暂态数BOS,调整所述基因调控网络结构,并根据所述调整后的基因调控网络,模拟肿瘤细胞状态。
其中,所述步骤a具体包括:
确定生物样本,并采用基因芯片采集技术对所述生物样本进行特定时间间隔取样,获取M个基因N个时间的连续表达谱数据;其中,M、N均为自然数;
根据所述获取到的M个基因N个时间的连续表达谱数据,并通过预设的M个基因两两之间的配对关系赋值,得到M个基因两两之间的调控关系距离,且进一步得到M个基因两两之间的调控关系方向及其对应的调控关系相位;
根据所述得到的M个基因两两之间的调控关系距离、调控关系方向和调控关系相位,构建布尔网络模型的基因调控网络。
其中,所述步骤b具体包括:
确定所述基因调控网络在干预前所有状态下的暂态数BOS,并进一步确定所述基因调控网络中所包含的所有吸引子;
将所有吸引子按照期望和不期望分成两大类,并计算期望吸引子的吸引域和不期望吸引子的吸引域;
在所述基因调控网络在干预前所有状态下的暂态数BOS中,查询出对所述期望吸引子的吸引域产生影响的一个或多个干预位;
确定每一个干预位干预后分别对应期望吸引子的吸引域的变化值,并筛选出最大期望吸引子的吸引域的变化值所对应的干预位,且进一步在所述每一个干预位干预后分别对应基因调控网络的暂态数BOS中,得到所筛选干预位干预后基因调控网络的暂态数BOS。
其中,所述确定每一个干预位干预后分别对应期望吸引子的吸引域的变化值的具体步骤包括:
确定每一个干预位干预后分别直接影响的状态,并根据所述确定每一个干预位干预后接影响的状态,计算每一个干预位干预后各状态携带走的净BOS值;
根据布尔函数表,确定所述每一个干预位干预后各状态将会达到的吸引子,寻找满足筛选条件的状态s:干预前状态s所属于的吸引子的类别与干预后状态s所属的吸引子的类别不同;
将每一个干预位干预后满足筛选条件的所有状态s的净BOS值以对期望吸引子的吸引域的变化为参照系统计累加起来分别作为每一个干预位干预后分别对应期望吸引子的吸引域的变化值。
其中,所述方法进一步包括:
若任一满足筛选条件的状态s从期望吸引子中失去,则所述从期望吸引子中失去的状态s的统计量为负值,否则为正值。
实施本发明实施例,具有如下有益效果:
本发明实施例基于布尔网络确定基因调控网络的最佳干预位,使基因调控网络能够通过干预位形成的干预策略逆向回到原来的状态或转移到另外一个期望的状态,最终改善基因调控网络使其往期望的方向发展,从而用于模拟干预肿瘤细胞状态,为肿瘤治疗研究提供一个有力的理论框架。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,根据这些附图获得其他的附图仍属于本发明的范畴。
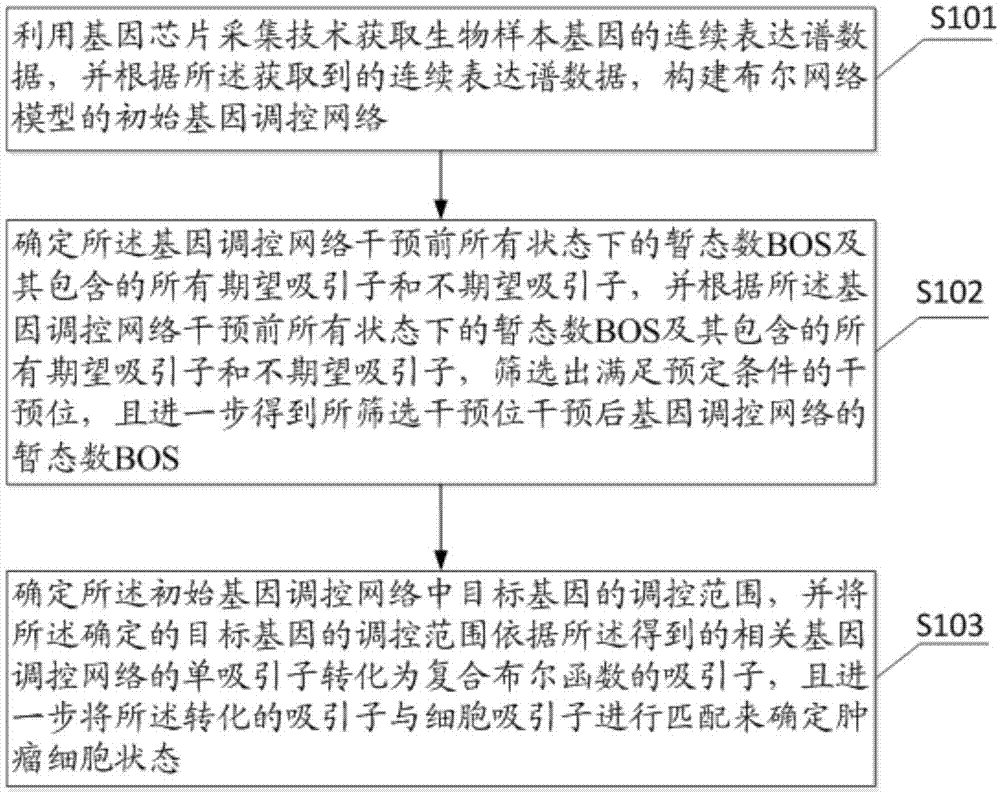
图1为本发明实施例提供的基于布尔网络吸引域模拟干预肿瘤细胞状态的方法的流程图;
图2为本发明实施例提供的基于布尔网络吸引域模拟干预肿瘤细胞状态的方法应用场景中的布尔网络示意图。
具体实施方式
为了使本发明的目的、技术方案及优点更加清楚明白,以下结合附图及实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
如图1所示,为本发明实施例中,提出的一种基于布尔网络吸引域模拟干预肿瘤细胞状态的方法,所述方法包括:
步骤S101、利用基因芯片采集技术获取生物样本基因的连续表达谱数据,并根据所述获取到的连续表达谱数据,构建布尔网络模型的基因调控网络;
具体过程为,步骤S11、确定生物样本,并采用基因芯片采集技术对生物样本进行特定时间间隔取样,获取M个基因N个时间的连续表达谱数据;其中,M、N均为自然数;
步骤S12、根据获取到的M个基因N个时间的连续表达谱数据,并通过预设的M个基因两两之间的配对关系赋值,得到M个基因两两之间的调控关系距离,且进一步得到M个基因两两之间的调控关系方向及其对应的调控关系相位;其中,M个基因两两之间的调控关系方向由其对应的配对关系赋值的正负符号决定;M个基因两两之间的调控关系相位由其对应的调控关系距离与其对应的配对关系赋值的绝对值决定;
步骤S13、根据得到的M个基因两两之间的调控关系距离、调控关系方向和调控关系相位,且按照M个基因两两之间的调控关系距离的绝对值大小顺序进行循环选择,构建布尔网络模型的基因调控网络.
应当说明的是,在步骤S12中,当M个基因两两之间的调控关系距离采用N个时间点对齐计算时,则预设的M个基因两两之间的配对关系赋值为0;当M个基因两两之间的调控关系距离采用小于或等于k个错位计算时,则预设的M个基因两两之间的配对关系赋值可从-k至k,并将计算得到的2k+1个调控关系距离中的最大值作为M个基因两两之间的最终调控关系距离;其中,k为自然数。
应当说明的是,在步骤S13中,当检测到当前循环增加的两个基因与初始基因调控网络中已有的基因具有直接或间接链接关系时,则在后续的选择过程中忽略当前循环增加的两个基因之间的调控关系。
作为一个例子,以M个基因N个时间点的连续表达谱数据为例:
取M个基因中任一个和剩余的M-1个基因两两配对。对于调控关系距离Dp的计算,可以使两个基因的相应的N个时间点对齐,也可以前后进行小于或等于k个错位,得到2k+1个相位调控关系距离:D-k、D-k+1、D-k+2、...、D-1、D0、D1、....、Dk-1、Dk,并通过公式(1)计算出:
式(1)中,N表示总的时间点个数,xi和yi分别表示两基因的表达谱第i个时间点的表达量,和分别表示两个基因的N个时间点表达量的平均值,min和max分别指其中的最大值和最大值。
在2k+1个调控关系距离:D-k、D-k+1、D-k+2、...、D-1、D0、D1、....、Dk-1、Dk中取绝对值|Dp|最大的Dp作为基因x和基因y间可能的调控关系距离,调控关系距离Dp是-1和1之间的一个值,两基因间的通过计算获得的2k+1个候选调控关系距离Dp,选择其中绝对值|Dp|最大的一个作为它们之间的调控关系距离。
此时,调控关系方向由调控关系距离Dp中的p的符号确定:p<0表示基因y调控基因x,p>0表示基因x调控基因y,p=0表示基因x和基因y互相调控(或者是共表达);调控关系相位由调控关系距离Dp和p等于绝对值|p|来决定。
以上计算出M个基因两两之间的调控关系的距离、方向和相位,利用循环选择的方法构建基因调控网络,按照调控关系距离的绝对值大小顺序进行循环选择,每次循环增加两个基因间的一个调控关系进入代构建的基因调控网络。
通过以上步骤,形成了包含M个基因的基因调控关系的网络,即得到布尔网络模型的基因调控网络。
步骤S102、确定所述基因调控网络干预前所有状态下的暂态数BOS及其包含的所有期望吸引子和不期望吸引子,并根据所述基因调控网络干预前所有状态下的暂态数BOS及其包含的所有期望吸引子和不期望吸引子,筛选出满足预定条件的干预位,且进一步得到所筛选干预位干预后基因调控网络的暂态数BOS;
具体过程为,步骤S21、确定基因调控网络在干预前所有状态下的暂态数BOS及各状态与其所属吸引子的距离,并进一步确定所述基因调控网络中所包含的所有吸引子;
步骤S22、将基因调控网络的吸引子,按照期望和不期望分成两大类,并计算期望吸引子的吸引域以及不期望吸引子的吸引域;
步骤S23、在所述基因调控网络在干预前所有状态下的暂态数BOS中,查询出对期望吸引子的吸引域产生影响的一个或多个干预位;
步骤S24、确定每一个干预位干预后分别对应期望吸引子的吸引域的变化值,并筛选出最大期望吸引子的吸引域的变化值所对应的干预位,且进一步在所述每一个干预位干预后分别对应基因调控网络的暂态数BOS中,得到所筛选干预位干预后基因调控网络的暂态数BOS。
在步骤S24中,确定每一个干预位干预后分别对应期望吸引子的吸引域的变化值具体实现过程为:
确定每一个干预位干预后分别直接影响的状态,并根据这些每一个干预位干预后直接影响的状态,计算每一个干预位干预后各状态携带走的净BOS值;
根据布尔函数表,确定所述每一个干预位干预后各状态将会达到的吸引子,寻找满足筛选条件的状态s:干预前状态s所属于的吸引子的类别与干预后状态s所属的吸引子的类别不同;
将每一个干预位干预后满足筛选条件的所有状态s的净BOS值以对期望吸引子的吸引域的变化为参照系统计累加起来分别作为每一个干预位干预后分别对应期望吸引子的吸引域的变化值。
应当说明的是:在任一干预位干预后,若任一满足筛选条件的状态s从期望吸引子中失去,则所述从期望吸引子中失去的状态s的统计量为负值,否则为正值。
作为一个例子,第一步、应用算法1,计算出基因调控网络的所有状态的BOS(干预前),并得到基因调控网络中的所有吸引子;
算法1:
第二步、应用算法2,找出所有可能对原始吸引子造成影响的一位干预位;算法2:
第三步、将布尔网络的吸引子按照期望和不期望分成两大类,并计算期望吸引子的吸引域,以及不期望吸引子的吸引域。
第四步、对可以进行干预的一位干预fi(p),应用算法3计算得到基因调控网络的期望吸引子的吸引域的变化量(干预后);
算法3:
需要说明的是,在算法3中获得某干预位影响的状态集后,确定各个受影响状态的净bos值的方法为:1)将各个状态以属于相同的吸引子为单位进行分组;
2)将每组的状态按照状态与吸引子的距离(算法1中状态的approAttSteps属性)进行降序排序;3)将步骤2排好序的状态队列,从左至右,将属于同一个路径的各状态进行净bos计算(右边状态的bos减去左边相邻状态的bos作为右边状态的净bos值)。
第五步、在得到每一个干预位对应的对期望吸引子的吸引域的变化值中,筛选出最大期望吸引子的吸引域变化值所对应的干预位,得到最优的干预位,进一步得到最优的干预位干预后基因调控网络的暂态数BOS。
步骤S103、根据所述得到的所筛选干预位干预后基因调控网络的暂态数BOS,调整所述基因调控网络结构,并根据所述调整后的基因调控网络,模拟肿瘤细胞状态。
具体过程为,根据所筛选干预位干预后基因调控网络的暂态数BOS,调整所述基因调控网络结构,进一步用于模拟干预肿瘤细胞状态。
实施本发明实施例,具有如下有益效果:
本发明实施例基于布尔网络确定基因调控网络的最佳干预位,使基因调控网络能够通过干预位形成的干预策略逆向回到原来的状态或转移到另外一个期望的状态,最终改善基因调控网络使其往期望的方向发展,从而用于模拟干预肿瘤细胞状态,为肿瘤治疗研究提供一个有力的理论框架。
本领域普通技术人员可以理解实现上述实施例方法中的全部或部分步骤是可以通过程序来指令相关的硬件来完成,所述的程序可以存储于一计算机可读取存储介质中,所述的存储介质,如ROM/RAM、磁盘、光盘等。
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!