一种质谱成像数据的自动配准方法
本发明涉及图像处理技术领域,特别涉及一种质谱成像数据的自动配准方法。
背景技术:
质谱成像(msi)技术是一种能够直接从组织样品中提供多种生物分子的相对含量以及空间分布的方法。而近年来,msi技术逐渐开始用于神经退行性疾病方面的研究(如阿尔茨海默症与帕金森病),证明了msi可用于在疾病模型中发现相关分子生物标志物。但要想进一步拓展msi技术在生物医学方面的应用,需要将所获得的msi数据与组织学信息相结合。由于在组织样品中存在多种细胞类型或不同的组织结构,想要确定生物分子的改变与特定的组织病理学结构之间的关系,需要对组织学样品进行详细的解剖学解释。传统的方法是对染色后的组织学切片进行解剖学划分,但对染色切片进行准确的解剖学注释需要对组织学有深入的了解,且人工手动的对染色脑片进行组织学的划分往往是耗时且容易引入人为偏见的。
为了实现小鼠脑组织学切片的自动解剖学解释,一些计算的方法(如聚类和主成分分析)被用来建立msi数据和组织学图像之间的空间对应关系。虽然这些方法可以对msi数据提供一个近似的组织结构的划分,但其分割结果往往取决于数据处理时所选择的维数。同时,这些计算类的方法有时会丢失一些较为重要的局部解剖结构信息。以大脑为例,虽然目前已经有专门的组织学专家对小鼠的脑组织学结构进行了详细的划分(allenbrainatlas),但是由于个体差异的存在,实验脑片与脑图谱中的参考脑片往往差异较大,无法将二者直接进行对比来划分脑区。为了解决这一问题,m.abdelmoula等人提出了一种配准的方法来实现实验脑片与脑图谱中的脑片的对齐,从而能够进行msi数据的自动解剖学解释。但是目前这项研究多集中在小鼠的冠状面脑片上,而对矢状面的研究仅仅停留在某个特定的脑区,系统的矢状面配准尚未见报道。
但是,自动配准矢状面msi数据与脑图谱中的参考脑片具有重要的研究价值。因为矢状面脑片横跨整个前后大脑,单张的矢状面切片的msi数据与冠状面相比可以提供更多的脑区结构与生物分子之间的关联信息。在配准之后,组织学切片和msi数据可以无需专业的人员进行脑区指认,便可实现自动的解剖学解释。此外,不同小鼠特定大脑区域的msi数据可以在放在同一坐标系下进行比较,消除了个体差异的影响,也使得自动化的数据处理更加容易。但是由于不同小鼠的矢状面脑切片的几何形状差异较大;而且与标准谱图中的参考脑片相比,各个脑区的移位现象比冠状面更为严重。故而直接进行矢状脑片与参考脑片的配准较为困难,局部的解剖结构不能够完全对齐。
同时,除了脑组织学切片之外,其他的一些生物学组织切片(如心脏,肾脏和肝脏等)在进行msi实验后,也需要将成像数据与组织学相结合才能够发挥更大的作用。如确定肿瘤组织边缘,鉴定不同病理组织的类型等。因此,迫切需要一种高效简便的方法来自动配准实验msi数据与参考组织学切片,以充分发挥msi技术在临床应用领域的能力。
技术实现要素:
为了解决上述技术问题,本发明提供一种高效简便的msi数据与参考组织学切片间自动配准的新方法。在配准完成之后能够实现自动的解剖学解释以及特定解剖学结构中msi数据的自动化比较。
本发明的方法利用msi技术同时提供多种生物分子空间分布的特点,筛选出特定的物质来标定特定解剖学结构,然后运用这些能够显示组织学结构信息的msi数据与标准谱图中的参考组织学切片进行自动配准,或者将这些解剖学结构的信息传递给组织学染色脑片进行配准。本发明利用msi数据来标定特定的脑区位置,为msi数据的自动配准提供了一个辅助的地标物,因而能够显著提高配准的准确性。同时,在配准完成之后可以进行自动的解剖学解释,在划分组织学结构时避免了引入人为偏见和繁琐耗时等缺点。最终可将不同组织学切片的msi数据通过配准归一化到同一坐标体系中,便于进行数据的自动化批量处理,实现高效的自动化配准。
本发明的技术方案为,一种质谱成像数据的自动配准方法,包括以下步骤:
步骤(1)、对待测组织学样品进行冷冻切片处理,得到多个组织学切片;
步骤(2)、将步骤(1)中所得的组织学切片进行解吸电喷雾质谱成像(desi-msi)实验,并采集得到多个msi数据;
步骤(3)、将步骤(2)采集的msi数据通过格式的转化和处理,保存预定生物分子的msi数据用于后续的标定预定脑区以及图像配准;
步骤(4)、直接使用msi数据与参考脑片进行配准,或者使用染色切片为桥梁来配准实验msi数据与立体定位图中的参考脑片;
步骤(5)、通过参考组织学切片中的标准谱图对配准后的msi数据进行自动的解剖学解释;
步骤(6)、自动对比预定解剖学区域的msi数据。
进一步的,所述步骤(3)中msi数据的转化和处理包括:首先将原始msi数据从xcalibur格式转换为mzxml格式,然后将每一行采集的msi数据点整合在一起,使用软件工具查看感兴趣的生物分子的空间分布情况;其中,通过脚本来导出预定种类的生物分子,只是针对这些特定的物质进行配准实验,而不是处理所有采集到的成像数据。
进一步的,所述步骤(4)中对于直接使用msi数据与参考脑片进行的配准,具体包括以下步骤:
(a)从多个msi数据中挑选出能够显示特征解剖学结构的物质;
(b)提取出所选物质代表的特征解剖学结构以及其外围轮廓;
(c)将上述特征解剖学结构进行融合,得到特征融合后的msi数据;
(d)从标准谱图中选择待测对象配准时所用的参考组织学切片;
(e)通过仿射配准将特征融合后的msi数据与待测对象的参考脑片进行对齐;
(f)使用自由形变(ffd)模型来设置合适的参数和方法,将步骤(e)中对齐后的msi数据与参考脑片进行配准并输出形变网格;
(g)将形变网格赋值给所有的msi数据使其做相应的变换。
进一步的,所述步骤(4)中使用染色切片为桥梁来配准实验msi数据与标准谱图中的参考脑片,则包括以下步骤:
(a)将与步骤(2)中msi实验所用切片相邻的组织切片进行组织学染色处理;
(b)将所得的组织学染色切片的图像进行预处理;
(c)通过仿射配准将处理后的染色切片与待测对象的参考脑片进行对齐;
(d)将预定类型的msi物质所标定的脑区结构信息传递给组织学染色切片,并在染色切片上以辅助线的形式标定出来,从而为配准过程提供一个辅助的地标物;
(e)从标准谱图中选择待测对象配准时所用的参考组织学切片;
(f)使用自由形变(ffd)模型来设置合适的参数和方法,先将步骤(d)中添加辅助线的染色切片与参考脑片进行配准,然后再将形变网格赋值给msi数据做相应的变换。
进一步的,所述步骤(a)中组织学切片的染色具体操作为:先将组织学切片用4%的甲醛固定1h,然后用pbs洗涤,超纯水灭菌;再在0.25%的甲苯胺蓝溶液中染色15分钟,分别用70%、80%、90%和100%体积比的乙醇有序脱水,然后用中性香脂固定切片;最后使用直立光学显微镜对染色图像进行光学采集,用于后续的配准实验。
进一步的,所述步骤(b)中组织学染色切片的图像进行预处理主要包括:先移除染色切片上的背景干扰;然后再通过脚本自动地框选出移除背景干扰后的切片区域;最终将所有用于配准的图像像素大小归一化。
进一步的,所述步骤(d)中将预定类型的msi物质所标定的脑区结构信息传递给组织学染色切片的具体操作为:选择能够显示出一些对应脑区解剖学结构的物质,然后将msi数据与组织学染色脑片导入到图像处理软件中,通过调节图像的透明度,使下方的msi数据所标定出来的区域的解剖学位置能够清晰的在染色切片上显示出来,然后在对应区域的轮廓上添加线条作为辅助线,再将下方的msi图删除,而上方染色切片的不透明度调节至100%,然后保存图片用于后续配准。
进一步的,所述步骤(e)中选择配准时所用的参考组织学切片的具体操作为:将标准谱图中的脑片数据导入到计算机中,通过编写脚本计算脑切片中centralcanal结构的首尾两端的欧式距离,然后将这些数据制作成一条标准曲线;对于一张实验脑片,通过上述步骤计算其centralcanal结构两端的欧氏距离,然后将其导入到标准曲线数据中,从而自动筛选出最合适的参考脑片用于配准。
进一步的,所述步骤(6)中自动对比特定解剖学区域的msi数据包括:
将步骤(5)中自动解剖学注释的生物学信息导入到计算机中保存,然后读取感兴趣的物质分子,通过编写脚本实现各解剖学结构中的msi数据的自动化比较,最终将所得的数据导入到工具软件中得到一张柱状对比图。
有益效果:
本发明提供的msi数据的自动配准方法,既可以直接配准实验所得的msi数据与参考组织学切片,也可以用组织学染色切片为桥梁,来连接msi数据与脑图谱中的参考脑片间的配准,使整个配准过程在单一的模态下进行。配准后的msi数据在没有组织学专家的帮助下也可以进行自动的解剖学解释;而且将实验组与对照组脑片和同一张参考脑片配准后,使得二者的成像数据可以在同一个坐标体系中进行对比,减小了原本因个体差异所带来的干扰。同时,这样也更易实现特定解剖学结构中msi数据的自动化对比分析。
附图说明
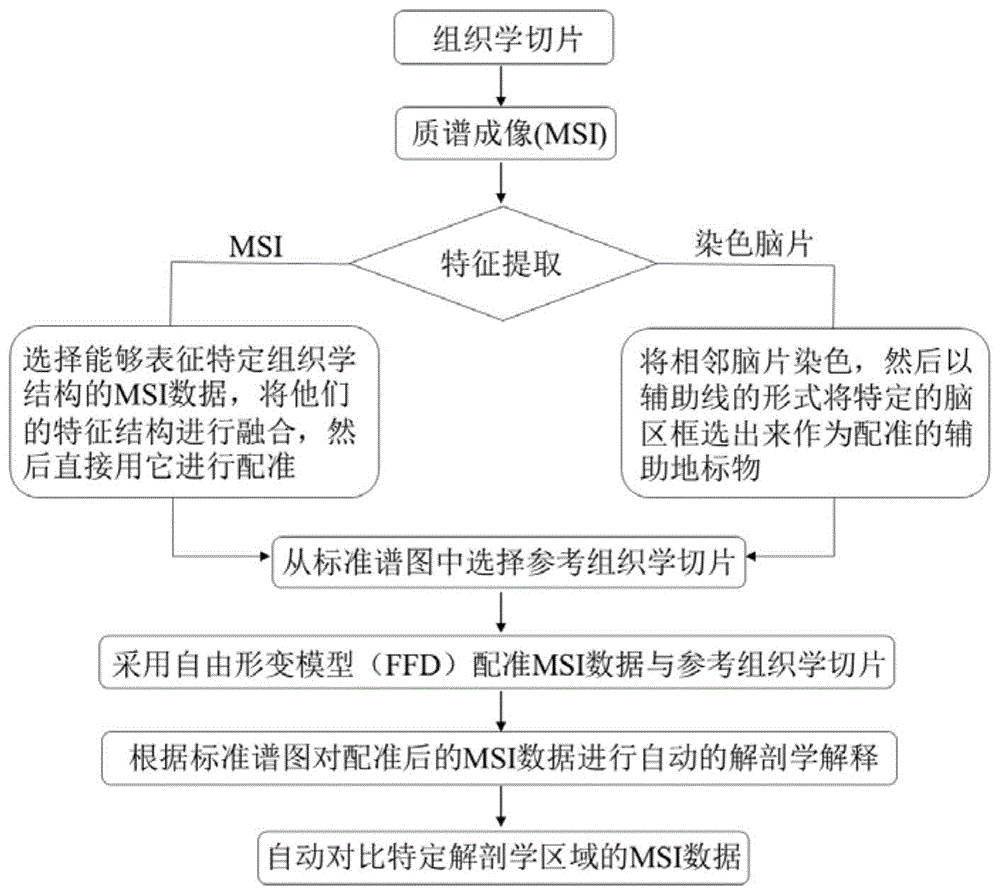
图1为本发明质谱成像数据的自动配准方法的流程图;
图2为自动提取组织学染色切片有效区域的示意图;(a)原始图片;(b)轮廓提取;(c)图片剪裁;
图3为六种能够显示特定解剖学结构的物质的质谱成像图;
图4为自动选择最合适的参考脑片方法的流程图;
图5为利用centralcanal两端的欧式距离自动导出参考脑片的示意图;
图6为小鼠冠状面脑片质谱成像数据与参考组织学切片的配准示意图;
图7为小鼠矢状面脑片质谱成像数据与参考组织学切片的配准示意图;
图8为肾脏组织切片的明场图;
图9为肾脏组织切片的质谱成像数据与参考组织学切片的配准示意图;
图10为将肾脏msi数据配准的形变网格赋值给其他物质进行相应配准变换的示意图;
图11为添加辅助线与未添加辅助线的配准过程示意图;
图12为本发明将辅助线添加在centralcanal和cerebralpeduncle的原因及结果示意图;
图13为添加辅助线与未添加辅助线的胆固醇分子的配准结果对比图;
图14为本发明所选择的18种物质的解吸电喷雾质谱成像示意图;
图15为本发明针对所选择的18种物质在15个脑区中添加辅助线和未添加辅助线时质谱成像数据配准准确性的自动对比图;
图16为选择来自三只不同小鼠(m1,m2,m3)的不同形变程度以及不同染色效果的矢状面脑片配准的示意图;
图17为小鼠(m1)添加辅助线与未添加辅助线时质谱成像数据配准准确性的对比示意图;
图18为小鼠(m2)添加辅助线与未添加辅助线时质谱成像数据配准准确性的对比示意图;
图19为小鼠(m3)添加辅助线与未添加辅助线时质谱成像数据配准准确性的对比示意图;
具体实施方式
为了使本发明的具体流程和优点更加清楚,下面结合附图和具体实施例对本发明作进一步详细的说明。但所述实施例只是为了对本发明作进一步的解释,本发明不限于以下实施例。
根据本发明的一个实施例1,提供一种质谱成像数据的自动配准方法,包括以下步骤:
步骤(1)对待测组织学样品进行冷冻切片处理,得到多个组织学切片;
步骤(2)将步骤(1)中所得的组织学切片进行msi实验,并采集得到多个msi数据;
步骤(3)将步骤(2)采集的msi数据通过格式的转化和处理,保存预定生物分子的msi数据用于后续的标定特定预定脑区以及图像配准所用;
步骤(4)直接使用msi数据与参考脑片进行配准,或者使用染色切片为桥梁来配准实验msi数据与立体定位图中的参考脑片;
步骤(5)通过参考组织学切片中的标准谱图对配准后的msi数据进行自动的解剖学解释;
步骤(6)自动对比预定解剖学区域的msi数据。
所述步骤4中,对于直接使用msi数据与参考脑片进行的配准,具体包括以下步骤:
(a)从多个msi数据中挑选出能够显示特征解剖学结构的物质;
(b)提取出所选物质代表的特征解剖学结构以及其外围轮廓;
(c)将上述特征解剖学结构进行融合,得到特征融合后的msi数据;
(d)从待测对象立体定位图中选择配准时所用的参考组织学切片;
(e)通过仿射配准将特征融合后的msi数据与待测对象的参考脑片进行对齐;
(f)使用自由形变(ffd)模型来设置合适的参数和方法,将步骤(e)中对齐后的msi数据与参考脑片进行配准并输出形变网格;
(g)将形变网格赋值给所有的msi数据使其做相应的变换。
所述步骤(4)中,若使用染色切片为桥梁来配准实验msi数据与立体定位图中的参考脑片,则包括以下步骤:
(a)将与步骤(2)中msi实验所用切片相邻的组织切片进行组织学染色处理;
(b)将所得的组织学染色切片的图像进行预处理;
(c)通过仿射配准将处理后的染色切片与待测对象的参考脑片进行对齐;
(d)将预定类型的msi物质所标定的脑区结构信息传递给组织学染色切片,并在染色切片上以辅助线的形式标定出来,从而为配准过程提供一个辅助的地标物;
(e)从待测对象的立体定位图中选择配准时所用的参考组织学切片;
(f)使用自由形变(ffd)模型来设置合适的参数和方法,先将步骤(d)中添加辅助线的染色切片与参考脑片进行配准,然后再将形变网格赋值给msi数据做相应的变换。
根据本发明的一个实施例,其中,选择将msi数据与参考组织学间的直接配准,具体如下,
该实施例中,msi采用解吸电喷雾质谱成像(desi-msi)实验获取,主要的实验仪器和装置包括:
exactiveplusg高分辨质谱仪(thermoscientific,sanjose,ca,美国);三维移动平台(北京微纳光科有限公司,北京);步径电机控制器(北京长丰电通机电设备有限公司,北京);注射泵(kdscientific,美国);冷冻切片机(vt1200s,徕卡,德国);光学显微镜(axioimagerz2,carlzeiss,德国)。
其中采用的化学试剂包括:
三氟乙酸(tfa,纯度99.5%,购自阿拉丁化学有限公司,中国上海);甲醛、甲苯胺蓝和中性香脂固定培养基(bbi生命科学,中国上海);甲醇(meoh,色谱纯,honeywellburdickandjackson,美国)。该实施例中,所述步骤(1)对待测组织学样品进行冷冻切片处理,得到多个组织学切片;
其中,组织学切片样品的制备具体包括如下过程:
本发明中所使用的小鼠都为c57bl/6j鼠。首先将实验小鼠在异氟醚麻醉下保存30s,然后迅速分离其大脑以及肾脏组织(若组织未及时进行切片,则将其在-80℃冷冻直至使用),然后在冷冻切片机上将组织切成15um厚的切片,并将其固定在洁净的载玻片上待msi实验使用。
进一步的,所述步骤(2)将步骤(1)中所得的组织学切片进行msi实验,并采集得到多个msi数据;
对于组织学切片的msi数据的采集包括如下过程:
将固定有脑(或肾)组织学切片的载玻片置于三维移动平台上,采用绝缘胶带固定载玻片的两端,以防止三维平台移动时待测样品也发生了移动。然后调节载物台位置,使喷雾采样点与所需的样品扫描初始点相重合。然后调节样品载玻片到质谱延长管入口的距离以及喷雾尖端到样品平面的高度,使质谱成像信号稳定且较高。最后在质谱参数设置界面设定所需电压、m/z范围、最大离子注入时间等,并通过步径电机控制器来设定扫面时所需的平台移动速率、行间距、扫描宽度等。主要参数如下:
所用的喷雾溶剂为含0.01m三氟乙酸的甲醇溶液;
实验中所使用的系统参数:
采样模式为正离子模式;
辅气为氮气,气压为0.9mpa;
喷雾电压为3kv;
质量分辨率为70000;
毛细管温度为275℃;
最大离子注入时间为270ms;
微扫描为1;
喷雾溶剂流速为2ul/min;
喷雾毛细管内部毛细管(内径:50um,外径:150um);
喷雾毛细管外部毛细管(内径:250um,外径:365um);
样品移动速率为20mm/min;
扫描的行间距为0.25um;
喷雾毛细管与载玻片表面的距离为1.5mm;
喷雾毛细管与质谱延长管入口的距离为6mm;
喷雾冲击角为55°;
数据采集完毕之后,通过上述的数据处理方式保存特定物质分子的msi数据用于后续的配准实验的探究。
进一步的,所述步骤(3),将步骤(2)采集的msi数据通过格式的转化和处理,保存预定生物分子的msi数据用于后续的标定预定脑区以及图像配准;
为了减少配准时的计算难度,可在配准前先裁剪出每张待配准图像的有效面积。由于人工的裁剪可能会存在误差,而且对于多张图片进行裁剪时是费时费力。故可使用自己编写的matlab脚本,对输入的图片进行自动的边缘提取,裁剪出内部图像。具体的实施思路如下,对于输入的任意一张原始图片a,如图2(a),将其转化为二值图像b=im2bw(a,0.9),然后读取黑色图片边缘与空白交界处的所有数据点,进行轮廓提取,如图2(b),最后寻找这些数据点中最上端、最下端、最左端、最右端处的四个数据点的坐标,将其赋值给原始图片进行裁剪即可,如图2(c)。
进一步的,对desi-msi数据的处理包括:
首先通过msconvert(http://proteowizard.sourceforge.net/)软件将采集到的原始msi实验数据从xcalibur格式转换为mzxml格式。然后将每一行的msi数据点在matlab(r2016b;(mathworks,natick,ma,u.s.a.)中整合在一起。最终,可使用开源成像软件包msireader(免费软件,www.msireader.com)查看各种生物分子的空间分布情况。
在选择配准所用的物质分子前,可使用自己编写的matlab脚本来导出感兴趣的分子,后续只针对这些感兴趣的物质进行配准实验,而不是处理所有采集到的成像数据。由于在msi实验中所设置的离子扫描宽度为60-900(m/z),但是在这个范围内包含了上万张成像图,手动在msireader将每个m/z逐个输入是费时费力的。可通过matlab自己编写脚本,筛选出一些特定离子,这样便可大大减小待分析数据的大小。具体实施思路如下:由于质谱所采集的数据点大多为类似正态分布的峰,在通过xcalibur软件将数据导出时,这个峰上的所有数据点都会被记录。在一定误差范围内的质谱峰所代表的是同一种物质,可将每个峰的数据只保留其最高点的质荷比m/z数据,而其两侧的数据点都去掉,这一步可将数据量缩小十几倍。然后再通过离子强度对数据进行进一步的筛除:通过第一步的筛选,有一些较弱的信号会保留下来,但其质谱成像图的分布是不连续的,对成像实验是没有用处的,可再设置一个最低的信号阈值,将低于这个值的信号的物质全部删去,可使成像图的数量再缩小十倍左右。对于脑片实验而言,最终剩下的质谱成像图大致在一千至三千张之间。再从中挑选出感兴趣的物质进行研究。
根据本发明的实施例,可以自动选择合适的参考脑片,具体操作如下:
配准的一个重要环节是选择最佳的参考脑片,如果选择了与正确切片位置偏离较远的切片作为参考脑切片,会使配准工作变得非常困难且无实际意义。通过仔细观察标准图谱中各组织切片的结构,可以发现centralcanal是图像中最显著的特征之一,它的最大弦长与组织切片的位置密切相关,可用它来确定最匹配的参考脑片。
首先将小鼠立体定位图中与实验脑切片相关范围内的矢状面切片都转化为图片格式保存好,然后在photoshop中采用批量裁剪工具裁剪出每张图片的相同区域,再把这些图片导入到matlab中,通过小鼠立体定位图中所给的比例尺大小来计算每张脑片centralcanal两端的欧氏距离,然后将所得的数据绘制成一条标准曲线保存。而对于一张给定的实验脑片,也通过上述步骤来计算出他centralcanal两端的欧氏距离,然后将此数值输入到标准曲线中即可自动导出最佳的参考脑片。具体的方法和流程如图4,5所示。
根据本发明的实施例,对小鼠脑组织的冠(矢)状面msi数据与参考脑片进行配准
从这些质谱成像图中可以发现,有许多物质在某些特定的脑区中呈现特异性分布。如图3所示,亚精胺在centralcanal和cerebralpeduncle区域信号较高,谷氨酸在皮层区域信号较高。因此可以运用一些计算类的方法,如主成分分析、聚类以及非线性随机嵌入的降维方式,将msi数据所展示出来的解剖学结构的特征整合起来,从而可以对解剖学结构有一个简单的划分。但这样的划分往往只能对一些较大的脑区划分较好,局部精细的脑区无法划分。
本发明利用msi数据展示出的解剖学结构,将其作为辅助配准的地标物,从而提高msi数据与脑图谱中的参考脑片间配准的准确性。当这些选作特征结构的区域配准后,与其相邻位置的解剖学结构也就配准了。首先将采集的msi数据进行预处理,保存能够显示特定解剖学结构的msi数据,对它们进行特征结构的融合;然后将其导入到matlab中计算其centralcanal两端的欧氏距离,再将该数据与小鼠立体定位图中进行匹配从而选择最合适的参考组织学切片;然后将特征结构融合后的msi数据与参考组织学切片在matlab中采用myronenko的医学图像配准工具箱(mirt)中的自由形变(ffd)模型来进行配准,输出配准后的形变网格,将其赋值给需要形变的物质即可做相应的变换。具体流程如图6,7所示,分别对小鼠脑组织学切片的冠状面与矢状面msi数据进行配准实验。从结果上看,该配准方法使得msi数据与参考组织学切片的轮廓趋于一致,而且配准的过程也没有改变成像数据原有的空间分布特点。
根据本发明的实施例,对小鼠肾脏msi数据与参考切片的配准
由于肾脏组织不像脑组织一样具有多个复杂的脑区结构,而且一般情况下是直接对比实验组与对照组的整张肾脏组织的msi数据。所以在选择原始的msi配准物质时,可挑选能够完整展示组织学切片轮廓的物质,以一个二肽分子(glutamylglutamicacid,m/z为277.1035)为例,其质谱成像图的空间分布如图9中“配准前msi”所示。
将肾脏组织的msi数据与参考组织导入到matlab中进行配准,具体的操作流程与上述脑片的一致。配准的结果如图9所示。为了方便对比配准前后msi与参考组织切片的一致性,在肾脏组织切片的轮廓边缘画上一条红色的轮廓线以便于观察。将配准前的msi图与参考组织切片在photoshop中叠加在一起,并调整上方msi图的透明度,可以发现二者在很多地方都没有重叠好(如箭头标出的三处位置存在较大的误差)。但将配准后的msi图与参考组织切片叠加在一起时,msi图的轮廓边缘与明场图的红色轮廓线完美的重叠在一起,说明本配准方法能够使得原本存在较大差异的msi数据与组织学明场图配准的较好。
然后将配准所得到的形变网格赋值给其他的物质进行相应的变换,如图10所示,以四个空间分布各异的物质为代表:胆碱(m/z104.1070)、谷氨酸(m/z148.06)、磷脂酰胆碱(36:4)(m/z820.5201)、磷脂酰胆碱(38:5)(m/z846.5323)。通过配准网格的变换,它们的msi图的形状与参考的明场图变得一致,而且物质的空间分布也没有明显的改变。说明本配准方法能够在不改变物质原有空间分布的情况下使得msi数据与组织学切片变得一致。而且从本例中也可以发现本发明的发明方法对于其他的组织学切片的msi数据的配准具有一定的普适性。
根据本发明的实施例2——通过组织学染色切片的小鼠矢状面msi数据与参考组织学切片间的配准,具体操作如下:
由于使用的参考组织学切片是小鼠立体定位图中进行了组织学染色后的脑切片,为了使整个配准过程在单一的模态(指的是配准时所用的“参考图”与“待配准图”来自于同一种类型的仪器,比如本例中的两张图片都为染色图片)下进行,在进行msi试验后,将其相邻的组织学切片进行染色处理,采用染色切片为桥梁来连接实验msi数据与小鼠立体定位图中的参考脑片。具体的实验步骤如下:
1、组织学切片样品的制备及染色;
将c57bl/6j实验小鼠在异氟醚麻醉下保存30s,然后迅速分离脑(若未及时进行切片实验,则将其在-80℃冷冻直至使用),然后在冷冻切片机上将肾脏切成15um厚的组织学切片,并将其固定在洁净的载玻片上待msi实验使用。
在msi实验完成之后,将与msi实验相邻的脑切片进行组织学染色,具体的操作步骤为:先用4%甲醛固定1h,再进行pbs洗涤,超纯水灭菌。然后在0.25%甲苯胺蓝溶液中染色15分钟后,分别用70%、80%、90%和100%(体积比)乙醇有序脱水。再用中性香脂固定切片。最终配准所用的组织学染色切片的图像是使用直立光学显微镜进行采集的。
2、对步骤1中的脑组织学切片进行desi-msi实验,具体参数如下:
所用的喷雾溶剂为含0.01m三氟乙酸的甲醇溶液;
实验中所使用的系统参数:
采样模式为正离子模式;
辅气为氮气,气压为0.9mpa;
喷雾电压为3kv;
质量分辨率为70000;
毛细管温度为275℃;
最大离子注入时间为270ms;
微扫描为1;
喷雾溶剂流速为2ul/min;
喷雾毛细管内部毛细管(内径:50um,外径:150um);
喷雾毛细管外部毛细管(内径:250um,外径:365um);
样品移动速率为20mm/min;
扫描的行间距为0.25um;
喷雾毛细管与载玻片表面的距离为1.5mm;
喷雾毛细管与质谱延长管入口的距离为6mm;
喷雾冲击角为55°;
3、质谱成像数据与染色脑片的仿射配准
为了拓宽本发明的应用面,本发明采用与msi实验相邻的组织学切片来进行染色。虽然这样会使配准变得稍微复杂一些:因为成像实验与配准时所用的脑片不是同一张,需要在正式配准前添加一步预配准实验使二者对齐。但是由于二者为相邻脑片,差异相对较小,只需要简单的仿射配准即可。虽然desi-msi实验对脑组织学切片的损伤较小(几乎是无损的),组织学切片在成像实验后仍可用于染色配准,但是其它的一些质谱成像的方法(如基质辅助激光解吸电喷雾质谱成像和二次离子质谱成像)对所用的组织学切片的损伤较大,在进行msi试验后脑片一般无法继续用来染色。所以,本发明选择相邻的脑片来染色配准,能够使本发明不仅仅局限于解吸电喷雾质谱成像这一种成像方式,它对于其他的成像方式所采集到的msi数据的配准都同样适用。
首先,对质谱成像数据与染色脑片之间经行一个仿射的配准,主要涉及到质谱成像数据的平移,旋转和缩放变换。本发明首先将msi数据(a)导入到matlab中,查看其成像分布imagesc(a),colormapjet;再将参考的染色图片(b)也导入到matlab中,采用holdon;image(b,’alphadata’,0.7)将其与msi数据叠加在一起;然后通过imrotate以及imresize等函数使二者对齐。当msi数据与染色脑片对齐后便可进行下一步的基于ffd的非刚性配准操作。
4、msi数据的非刚性配准
在将desi-msi所采集到的数据与脑图谱中的参考脑片配准时,以组织学染色切片作为桥梁来连接实验msi数据与小鼠立体定位图中的参考脑片,不仅使配准过程在单一的模态下进行,大大减小了配准的复杂性;同时染色切片的分辨率相对将desi-msi数据更高,配准的精度也会更好。
具体的配准流程如图11所示:
(1)实验所用的组织学染色切片(ca)与参考组织学切片(ra)间的配准;
(2)保存步骤(1)中配准后所产生的形变网格;
(3)将上述形变网格赋值给质谱成像数据(d)作相应的变换。
在整个非刚性配准的过程中,可使用医学图像配准工具箱(mirt)中的自由形变(ffd)模型来实现实验组织学和参考组织学切片之间的配准,选用相关系数(correlationcoefficient)作为相似性测量的方法。
有的时候,本发明对直接配准后的msi数据进行分析时,发现多个脑区的msi数据与配准前相比都存在较大的误差。在此类情况下,可在配准前,以msi所提供的解剖学结构的位置在组织学切片上添加一些辅助线作为地标物辅助整个配准的过程,从而达到提高配准准确性的目的。
所述的添加辅助线的具体操作包括:
通过在多个不同的脑区添加辅助线(如centralcanal,cerebralpeduncle,hippocampus,cerebellum等),然后对质谱成像数据,染色切片以及配准后成像数据进行对比,通过优化后,将辅助线添加在centralcanal和cerebralpeduncle这两个脑区效果最佳。如图12所示,其主要原因为:(1)将矢状面脑片划分为感兴趣的15个脑区后,通过计算每个脑区与之相连的脑区的个数,如图中122,可发现centralcanal和cerebralpeduncle所连接的脑区数量较多(如图中121所示,都为6个)。这主要是由于二者处于矢状面脑片的中心地带,故而关联者较多;(2)胆固醇(m/z369.3503)和亚精胺(m/z146.1652)这两种物质的msi信号在centralcanal和cerebralpeduncle这两个解剖学位置含量较高,故而可用msi数据定位这两个脑区,如图中123;(3)centralcanal和cerebralpeduncle容易和旁边的那些脑区分开,而且调节透明度后这两个脑区更加易于区分,如图中的124;通过msi数据与染色脑片相结合可较容易且准确的找到centralcanal和cerebralpeduncle的位置,如图中的125。具体步骤为:先在matlab中将所有的待配准的组织学染色切片的像素点大小归一化为300*545,然后将图片导入到photoshop中,选中画笔工具并选择4个像素点的宽度在centralcanal和cerebralpeduncle这两个脑区的边界线上描绘出其轮廓作为辅助线,具体结果如图中125所示。
如图13所示,本发明对加/不加辅助线时配准准确性进行了比较。以配准前的胆固醇分子与组织学染色切片为参照,可以发现添加辅助线时配准的准确性大大提高了。首先本发明将配准前的质谱成像图与染色切片重叠起来(centralcanal和cerebralpeduncle脑区结构内被填充了黑色,以便于观察),通过调节上面一张图片的透明度,使二者的轮廓都能够清晰可见。从二者的局部放大图(图中131)可以发现胆固醇分子的高信号区域很好的分布于centralcanal和cerebralpeduncle这两个组织学结构中。然后对加/不加辅助线配准后的msi数据重复上述操作,从图中132可以发现,添加辅助线进行配准后,胆固醇分子的msi数据依旧分布于centralcanal和cerebralpeduncle这两个脑区中。但是未加辅助线进行配准时(图中133),胆固醇分子的高信号区则偏离出了centralcanal和cerebralpeduncle,且较为严重。
除了上述的胆固醇分子外,通过对比其它17种物质(如亚精胺、谷氨酸、谷氨酰胺、磷脂酰胆碱、磷脂酰乙醇胺等),它们的解吸电喷雾质谱成像图如图14所示,充分验证了本配准方法的准确性。同时,还将整张矢状面切片划分为15个精细的脑区,然后对多脑区多物质配准准确性进行了研究。如图15所示,对于整张矢状面切片上15个脑区中的18种物质,在添加辅助线进行配准后,其误差值明显小于未添加辅助线直接进行配准的,这说明添加辅助线的策略并不单单只是提高了centralcanal和cerebralpeduncle这两个脑区的配准准确性,而是对整张矢状面脑片上的各个脑区都有较大改善。
通过三只不同小鼠(m1,m2,m3)的三张不同形变程度和不同染色情况的矢状面脑片的配准,发现本配准方法的准确性很高(如图16所示)。通过对组织学染色切片的配准结果的考察:从图16j,16k,16l中可以发现,虽然这三张矢状面切片的形变程度和染色情况存在较大差异,但在centralcanal和cerebralpeduncle这两个脑区添加上辅助线,配准后的辅助线与参考脑片上的解剖学结构centralcanal、cerebralpeduncle完美的重合了(参考图片上的centralcanal和cerebralpeduncle被填充了黑色,便于对比观察)。这表明在添加辅助线后,不同形变程度和染色情况的矢状面切片都能够配准的较好。此外,对比这三张矢状面切片加/不加辅助线时质谱成像数据配准的结果,如图17,18,19所示。在添加辅助线的情况下,配准后质谱成像数据的分布与形变前几乎完全一致,但是在未添加辅助线直接进行配准时,其msi数据出现了明显的信号偏移。这也充分地证明了本发明具有很好的普适性。
综上,本发明首先通过一些具有特异性分布的msi数据来标定小鼠的脑和肾脏组织的结构,从而直接配准msi与参考组织学切片。通过对比配准前后冠状面脑片(矢状面脑片、肾脏组织切片)的msi数据,可以发现本发明的配准方法使得原本差异较大的msi数据与参考脑片变得一致,同时配准也没有改变msi数据原有的空间分布,充分说明了本发明方法的有效性。然后本发明尝试将这些解剖学信息传递给组织学染色切片,通过染色切片为桥梁来连接msi与参考谱图间的配准,使得配准在单一的模态下进行,具体的实验过程见附图。从结果上看,通过将msi数据所标定的centralcanal和cerebralpeduncle的解剖学结构以辅助线的形式添加在染色脑片上之后,配准准确性有了明显的提高。进而,通过对比18种物质在15个脑区的配准结果,可以发现在添加辅助线的条件下,所选择的15个脑区中的配准误差都有所下降。最后,通过来自三只不同小鼠的三张不同形变程度和染色情况的矢状面脑片的配准结果,进一步证明本发明方法的普适性。
尽管上面对本发明说明性的具体实施方式进行了描述,以便于本技术领域的技术人员理解本发明,且应该清楚,本发明不限于具体实施方式的范围,对本技术领域的普通技术人员来讲,只要各种变化在所附的权利要求限定和确定的本发明的精神和范围内,这些变化是显而易见的,一切利用本发明构思的发明创造均在保护之列。
- 还没有人留言评论。精彩留言会获得点赞!