一种用于识别心肌梗死的相对运动学习方法及装置
1.本发明专利涉及医学图像分析技术领域,具体地说,是一种用于识别心肌梗死的相对运动学习方法及装置。
背景技术:
2.心肌梗死一般指冠状动脉持续性缺血缺氧所引起的心肌坏死。急性期临床上多表现为剧烈而持久的胸骨后疼痛,休息及硝酸酯类药物不能完全缓解,伴有血清心肌酶活性增高及进行性心电图变化,可并发心律失常、休克或心力衰竭,常可危及生命。心脏磁共振可以直观评价心肌收缩功能、心肌形变等特征,对于心肌梗死的预防、诊断具有重要的意义。
3.在临床工作中,钆剂延迟增强(lge)-心脏核磁共振成像(cmr)被认为是目前在体无创性检测梗死区域的金标准。然而,这种方式存在一定的危险,因为钆造影剂是慢性终末期肾病患者的禁忌症。根据美国肾脏数据系统,超过40%的慢性肾脏病患者患有心血管疾病,而大约20%的心肌梗死患者伴有慢性肾病。此外,最近的研究表明,钆剂可能会沉积在肾功能正常患者的皮肤、齿状核和苍白球中。因此,若在没有造影剂的情况下直接识别心肌梗死区域将会是一个巨大的临床进步,不仅可用于识别心肌梗死的存在、位置和透壁范围,还可以预测缺血性心脏病中功能障碍心肌节段的恢复。
4.在深度学习技术出现前,主要有三种方法用于无造影剂的心肌梗死区域分割。其中第一种方法,如noble等人2002年在《医学与生物学中的超声波》提出的统计学图像序列对齐方法,建立了核磁共振图像帧之间的对应关系,并通过计算心肌的位移,从图像序列中快速提取运动特征。第二种方法是shi和liu于2003年在《医学影像分析》杂志上发表的,引入了不同的正则化策略来从医学图像序列中估计心脏运动。第三种方法是hufnagel等人2008 年在《国际计算机辅助放射外科杂志》上提出的统计形状建模方法,其试图通过建模可能的运动和形状的统计表示来引入先验知识来克服数据的内在复杂性。尽管上述方法在一定程度上取得了成功,但在应用于临床环境中仍存在一些问题。
5.由于深度学习技术的蓬勃发展,近几年深度学习在心脏核磁共振成像(cmri)的处理的应用显著增加,尤其是在心脏结构分割方面。也有研究组尝试将深度学习用于无造影剂的心肌梗死分割,通过深度学习来检测心脏的形态学和运动学异常,从而进行心肌梗死的识别和定位。
6.2017年,在第八届心脏统计图谱和计算模型国际研讨会上,khened等人提出了一种全自动的深度学习网络。训练数据经过傅里叶分析处理用于感兴趣区域提取,通过使用双重成本函数(即加权交叉熵和dice系数)进行训练来优化网络的参数,从而实现使用密集卷积神经网络(densenet)从心脏磁共振(mr)图像中分割左心室、右心室和心肌。将提取的11 个心肌特征参数使用随机森林分类器于自动心脏病诊断,可以初步诊断出患者是否患有扩张型心肌病(dcm)、肥厚型心肌病(hcm)、心肌梗塞(mnf)等疾病。
7.2018年,baessler等人在《放射学》杂志和发表文章,基于再现性、机器学习和相关
分析,采用逐步降维和纹理特征选择来选择特征,以延迟增强(de)图片为参考标准,对无造影剂cmri图像进行心肌梗死诊断。该实验表明,对无造影剂cmri图像进行纹理分析,可以区分心肌梗死导致的缺血性瘢痕和正常心肌,从而可以诊断亚急性和慢性心肌梗死,具有较高的准确性。其为之后通过学习梗死区域的像素特征来诊断心肌梗死奠定了基础。
8.2018年,xu等人在《医学影像分析》杂志发表了一种新的联合运动特征学习架构。该架构由三个无缝连接的功能层组成:心脏定位层利用faster r-cnn,可以自动从心脏成像序列中裁剪涉及左心室的感兴趣区域序列;运动特征提取层,使用长短期记忆循环神经网络 (lstm),通过固定大小的像素块序列(从图像序列中裁剪)之间的局部强度变化来构建基于补丁的运动特征,使用光流技术通过相邻图像之间的全局强度变化来构建基于图像的特征来描述每个像素的运动;全连接的鉴别层可以将每个像素中的两种运动特征组合在一起,然后在每个像素中建立运动特征与组织身份(即是否存在梗死)之间的对应关系,由此可以实现像素级别的心肌梗死区域分割。
9.2019年,chen等人在《ieee access》杂志上提出了一个深度学习约束框架,集成光流特征用于医学图像序列的心肌梗死,该框架由两个阶段组成。在第一阶段,首先,通过在左心室心肌区滑动一个固定大小的窗口,获得固定大小的静态像素块,利用光流法提取同一位置的运动信息,通过最小化目标函数和平方误差来训练基本的自动编码器(sdae),利用训练好的堆叠去噪自动编码器提取像素块的强度和运动特征,并加入高斯噪声进行反复训练优化,最后获得包含两个隐藏层的sdae。第二阶段,从第二个sdae隐藏层中提取固定长度特征,通过延迟增强图片生成这个像素块是否为梗死的标签,由支持向量机(svm)对其进行梗死和非梗死的分类。
10.2021年,manchio等人在《欧洲心脏杂志-心血管成像杂志》杂志上发表了关于肥厚型心肌病(hcm)的机器学习研究,因为hcm的瘢痕组织和心肌梗死后修复的组织是一样的,所以其与的研究相通。该研究使用10倍交叉验证的xgboost模型,从全部2613个特征中,提取7个最重要的特征。最后研究发现,因为hcm而存在替代性纤维化可以通过其较高的信号心肌强度、纹理异质性和粗糙性、较低的心肌体积和减少的心肌壁增厚来识别。这为研究心肌梗死(mi)的特征提取部分提供了参考思路。
11.2022年,石润州等人申请了一项专利:用于心肌梗死区域检测的深度学习方法。该方法主要包括两个阶段。在第一阶段,通过u-net模型分割心肌内膜与心肌外膜,以角度为单位对心肌进行运动特征和灰度特征信息的提取;第二阶段,通过以convlstm为核心的神经网络,利用上一阶段提取到的运动特征和灰度信息特征进行训练,最终实现心肌梗死区域分割。
12.现有技术存在如下技术问题:
13.(1)使用钆造影剂的心肌梗死区域分割的缺点:这种方式存在一定的危险,因为钆造影剂对慢性终末期肾病患者是致命的,而大约20%的急性心肌梗死患者伴有慢性肾病。
14.(2)不采用深度学习的无造影剂心肌梗死区域分割方法缺点:首先,分段建立-对应计算应变是一个复杂的过程,这可能是一个限制因素。其次,这些方法既费时又繁琐,需要使用仔细的建模技术。此外,心脏复杂的时空运动可能会导致实施困难。
15.(3)结合光流法和lstm的像素级心肌梗死区域分割方法缺点:整个过程是复杂的,每一步的误差都会导致后续的连续影响。另外,该模型不仅需要大量的标签校准,还包含了
大量的参数,需要超过138m的参数。并且其只能对心肌中间层面有效,会浪费其它层面的影像。
16.(4)利用sdae和svm的心肌梗死区域分割方法缺点:只能对心肌上的10
×
10大小像素块进行梗死和非梗死的分类,最后只能得到30个左右的像素块的分类,所以只能确定梗死的大致范围,而不够精细。并且其也只能对心肌中间层面有效,会浪费其它层面的影像。
17.(5)利用u-net和convlstm的心肌梗死区域分割方法的缺点:以角度为单位进行是否心肌梗死的分类,忽略了在同一角度下不同位置处的心肌梗死情况的差异,因此只能确定梗死的大致位置,不够精确。除此之外,在特征提取过程中需要较为复杂地提取运动特征和灰度信息特征,需要得数据量过多,方法较为繁琐。
技术实现要素:
18.本发明针对现有技术的不足之处做出了改进,提供了一种用于识别心肌梗死的相对运动学习方法及装置。通过u-net模型分割心肌内膜与心肌外膜,对心肌进行运动特征和灰度特征信息的提取,以resmlp网络为核心搭建神经网络,识别基于电影图像的心肌梗死区域,本发明是采用以下技术方案来实现的:
19.本发明工了一种用于识别心肌梗死的相对运动学习方法,包括:
20.获得心脏核磁共振电影序列,通过u-net模型分割心脏核磁共振成像(cmri)电影序列中每一帧的心肌内膜与心肌外膜;
21.将分割好的每一帧的心肌内膜与心肌外膜二值化,得到心肌边界,提取每一帧的像素特征,将其拼接融合,存入36
×
81的二维特征矩阵中;
22.标注二维的特征矩阵中对应序列的有钆造影剂的lge图片的梗死区域,转化成36
×
1的向量作为心肌梗死区域标签;
23.基于获得的二维特征矩阵和对应的心肌梗死区域标签,构建以resmlp为核心的神经网络模型,所述的以resmlp为核心的神经网络模型包括resmlp层、池化层、全连接层;
24.以resmlp为核心的神经网络模型中训练时,将模型输出的36
×
1的向量与真实心肌梗死区域标签进行对比,并使用二元交叉熵“bceloss”作为损失函数;
25.使用“adam”优化器对网络进行迭代训练,优化网络参数,当训练结束时,在测试集上检测精度,保存准确率最高的模型。
26.作为进一步地改进,本发明所述的提取每一帧的像素特征具体为:
27.提取外膜边界的中点为整张图的中心点,以10度的角度间隔从中心点向外做射线,取其与内膜和外膜边界的交点,得到36个方向的内外膜交点坐标,取每一方向上内外膜交点的中点o,将以点o为中心的周围任意大小的像素块的像素矩阵取出,作为该处心肌的形态学特征。
28.作为进一步地改进,本发明所述的拼接融合为将心肌像素特征展开成一维向量,得到1
ꢀ×
81的像素特征向量,对36个角度提取到的特征信息做相同处理,拼接之后归一化,形成特征矩阵,所述的特征矩阵的行数36行(36个角度),列数为81列,所以特征矩阵的大小为36
×
81。
29.作为进一步地改进,本发明所述的标注二维的特征矩阵中对应序列的有钆造影剂的lge 图片的梗死区域,转化成36
×
1的向量作为心肌梗死区域标签具体为:标签是根据延
迟增强 (lge)图片分类的,同样以外膜中心点为中心,在医生的指导下标记对应的36个图像块是否有心肌梗死,无梗死标记为0,有梗死标记为1,大小为36
×
1。
30.作为进一步地改进,本发明所述的以resmlp为核心的神经网络模型的输入是之前提取的特征矩阵,模型的输出为36
×
1的向量。
31.作为进一步地改进,本发明所述的resmlp层对单帧图片的特征矩阵1@36
×
81进行计算,并提取单帧图片中心肌所分成的36个图像块的块内信息和块间关系,得到每一个图像块的像素特征,并存储在输出的矩阵1@36
×
81中,最终得resmlp输出矩阵20@36
×
81。
32.作为进一步地改进,本发明所述的池化层采用平均池化法或空间金字塔池化或中心池化,用于融合一个时间序列的像素特征;所述的全连接层包括任意层数的linear层,最终输出得到36
×
1的特征向量,用于将每一个图像块的特征矩阵映射到样本标记空间。
33.作为进一步地改进,本发明所述的平均池化法为对resmlp输出矩阵20@36
×
81进行平均池化,融合20帧图片的心肌像素特征,得到1@36
×
81的特征矩阵,再通过降维得到的36
ꢀ×
81的二维特征矩阵。
34.作为进一步地改进,本发明所述的全连接层包括两层递减的linear层,第一层linear 将特征矩阵由36
×
81降至36
×
49,第二层linear进一步将特征矩阵化为36
×
1的特征向量。
35.本发明还公开了一种用于识别心肌梗死的相对运动学习方法的装置,包括:
36.分割单元:用于获得心脏核磁共振电影序列,通过u-net模型分割心脏核磁共振成像 (cmri)电影序列中每一帧的心肌内膜与心肌外膜;
37.提取特征单元:将分割好的每一帧的心肌内膜与心肌外膜二值化,得到心肌边界,提取每一帧的像素特征,将其拼接融合,存入36
×
81的二维特征矩阵中;
38.标签单元:标注二维的特征矩阵中对应序列的有钆造影剂的lge图片的梗死区域,转化成36
×
1的向量作为心肌梗死区域标签;
39.构建神经网络模型单元:基于获得的二维特征矩阵和对应的心肌梗死区域标签,构建以 resmlp为核心的神经网络模型,所述的以resmlp为核心的神经网络模型包括resmlp层、池化层、全连接层;
40.训练单元:以resmlp为核心的神经网络模型中训练时,将模型输出的36
×
1的向量与真实心肌梗死区域标签进行对比,并使用二元交叉熵“bceloss”作为损失函数;
41.优化单元:使用“adam”优化器对网络进行迭代训练,优化网络参数,当训练结束时,在测试集上检测精度,保存准确率最高的模型。
42.本发明的有益效果在于:
43.心肌梗死是一种严重的疾病,如何在无造影剂情况下精确、高效、低耗时地分割心肌梗死区域成为了当前重要的研究内容。本发明提供了一种基于深度学习,实现没有造影剂的情况下从心脏磁共振图像序列中直接划定心肌梗死(mi)区域的用于识别心肌梗死的相对运动学习方法及装置。
44.具体地说:
45.(1)使用u-net模型分割心肌内膜和外膜,及训练yolov5得到心脏区域坐标,之后按坐标截取图片,再将图片旋转摆正的预处理方法。
46.(2)以外膜中心为原点,10度的角度间隔做射线,得到其与心肌内膜和外膜交点,
之后进行内外膜中心点周围81个像素的像素特征的提取,以及将像素特征展开成特征矩阵的特征提取方法。
47.(3)一种以resmlp为核心的深度学习模型,输入一个cmri序列的特征矩阵,该模型可以输出梗死区域向量,根据输出的向量可以直观标记出梗死区域。
48.(4)与使用钆造影剂的心肌梗死区域分割方法相比,本方法是一种无造影剂的分割方法,可以避免钆造影剂对人体脏器的伤害,尤其适用于肾病患者。
49.(5)与不使用深度学习的无造影剂心肌梗死区域分割方法相比,本方法是一种结合深度学习的方法,无需复杂的建模和数学计算,节省了时间,且具有更好的普适性和实用性。
50.(6)与结合光流法和lstm的像素级心肌梗死区域分割方法相比,本方法模型结构简单,具有更强的鲁棒性,且需要的标签和存储空间都更小,训练和测试都只需使用家用计算机,计算速度快,能做到实时的要求。并且因为使用了功能强大的u-net网络来分割心肌,可以有效分割更多截面的心肌形状,避免造成数据浪费。
51.(7)与利用sdae和svm的心肌梗死区域分割方法相比,本方法的分割更为细致,将整个心肌分为36个特征向量输出,最后可以达到10度的精准度,有利于获得更细致的心肌梗死特征,且可以有效分割更多的截面的心肌形状,避免造成数据浪费。
52.(8)与利用u-net和convlstm的心肌梗死区域分割方法相比,本方法的分割充分考虑到了心肌不同厚度处梗死情况的差异,使输出结果更具有代表性。另一方面,本方法只需提取灰度信息特征而无需计算较为复杂的距离特征,在数据预处理方面更为简单、迅速。
附图说明
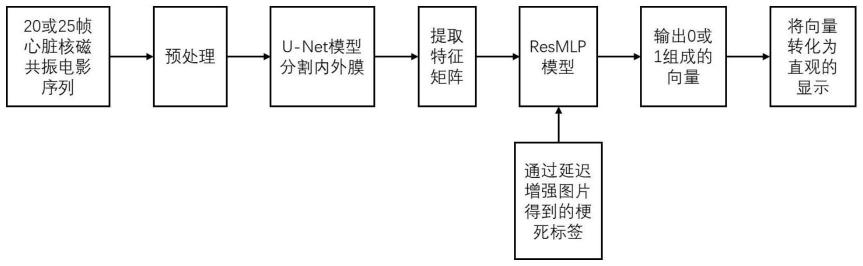
53.图1基于深度学习的无造影剂心肌梗死区域分割模型;
54.图2为心肌分割流程图;
55.图3为预处理与心肌分割结果图;
56.图3(a)心脏核磁共振成像(cmri)电影序列中的一帧,即原始图像;图3(b)为预处理后得到的感兴趣区域;图3(c)为分割得到的心肌外膜;图3(d)为分割得到的心肌内膜。
57.图4为特征矩阵图;
58.图5为卷积神经网络结构图;
59.图6为resmlp层结构及数据流;
60.图7为心肌梗死区域结果图;
61.图7(a)为钆剂延迟增强(lge)心脏核磁共振成像图片;图7(b)的白色区域为在有经验的医生指导下在cmri电影序列第一帧图片上标记的心肌梗死区域;图7(c)中的白色边缘范围为在无造影剂情况下,从对应序列分割出的心肌梗死区域,与有造影剂时的一致。
具体实施方式
62.本发明公开了一种用于识别心肌梗死的相对运动学习方法及装置,通过u-net模型分割心肌内膜与心肌外膜,对心肌进行灰度特征信息的提取,以resmlp为核心的神经网络的搭建,神经网络的训练与心肌梗死区域的呈现技术。图1基于深度学习的无造影剂心肌梗死区域分割模型,包括如下步骤:
63.获得心脏核磁共振电影序列,通过u-net模型分割心脏核磁共振成像(cmri)电影序列中每一帧的心肌内膜与心肌外膜;
64.将分割好的每一帧的心肌内膜与心肌外膜二值化,得到心肌边界,提取每一帧的像素特征,将其拼接融合,存入36
×
81的二维特征矩阵中;
65.标注二维的特征矩阵中对应序列的有钆造影剂的lge图片的梗死区域,转化成36
×
1的向量作为心肌梗死区域标签;
66.基于获得的二维特征矩阵和对应的心肌梗死区域标签,构建以resmlp为核心的神经网络模型,所述的以resmlp为核心的神经网络模型包括resmlp层、池化层、全连接层;模型的输入是之前提取的特征矩阵,模型的输出为36
×
1的向量,利用该向量可以标记出心肌梗死区域。利用心肌梗死区域标签进行训练,使其在测试集的损失最小,得到最高准确率的心肌梗死区域分割模型。
67.以resmlp为核心的神经网络模型中训练时,将模型输出的36
×
1的向量与真实心肌梗死区域标签进行对比,并使用二元交叉熵“bceloss”作为损失函数;
68.使用“adam”优化器对网络进行迭代训练,优化网络参数,当训练结束时,在测试集上检测精度,保存准确率最高的模型。
69.利用得到的心肌梗死区域分割模型,任意给定新病人的cmri电影序列,通过u-net进行分割之后提取像素特征,输入到该心肌梗死区域分割模型中,就可以得到输出的36
×
1的向量,从而标记出心肌梗死区域。
70.分割心肌内膜和心肌外膜
71.图2为心肌分割流程图;
72.预处理:开始后,为了提高心肌分割精度,减小运行时间,故先对cmri电影序列进行预处理。预处理时,先要处理图片的大小,截出感兴趣的区域,记录其四个顶点的坐标值作为训练集,输入yolov5模型中。训练完成后,其可以学习到心脏区域特征,之后对于每一张原始图片,其都能给出感兴趣区域四个顶点坐标。按照这个坐标截取图片,再将图片旋转摆正,使左心室与右心室在图片上处于同一水平线,预处理部分完成。
73.将预先整理好的心肌内膜标签和对应的原始图像放入u-net网络中作为训练集,训练模型 1,其可以从预处理好的图片中提取心肌内膜;将心肌外膜标签和对应的原始图像放入u-net 网络中作为训练集,训练模型2,其可以从预处理好的图片中提取心肌外膜。内膜与外膜边界之间的部分(外膜减去内膜),就是要研究的完整心肌。
74.图3为预处理与心肌分割结果图;图3(a)心脏核磁共振成像(cmri)电影序列中的一帧,即原始图像;图3(b)为预处理后得到的感兴趣区域;图3(c)为分割得到的心肌外膜;图3(d) 为分割得到的心肌内膜。
75.提取心肌特征矩阵
76.心肌的特征为像素特征,提取过程如下。
77.1、对于每一帧图片,对于已经区分好的内外膜进行二值化,提取心肌边界。提取外膜边界的中点为整张图的中心点,以10度的角度间隔从中心点向外做射线,取其与内膜和外膜边界的交点,得到36个方向的内外膜交点坐标。取每一方向上内外膜交点的中点o,将以点o为中心的9
×
9像素矩阵取出,作为该处心肌的形态学特征。对于像素特征的提取的方法采用的是提取内外膜中间点周围的9
×
9大小的像素块,之后将其展开。其替代方法可以
是提取内外膜中间点周围任意大小的像素块,其都可以表征心肌梗死区域的像素特征。
78.2、将心肌像素特征展开成一维向量,得到1
×
81的像素特征向量。对36个角度提取到的特征信息做相同处理,拼接之后归一化,形成特征矩阵。特征矩阵的行数36行(36个角度),列数为81列,所以特征矩阵的大小为36
×
81。图4为特征矩阵图。
79.以resmlp为核心的深度学习模型搭建
80.图5为卷积神经网络结构图;建立的深度学习网络结构如图5所示,其主要由resmlp层, pooling(池化)层,全连接层组成。对于每一个cmri电影序列,输入的特征矩阵大小为20 (或25)
×
36
×
81。20(或25)代表了每个序列都有20(或25)帧图片,36
×
81为对一张图片提取的特征矩阵大小。
81.图6resmlp层结构及数据流,resmlp层由许多结构相同的resmlp子层组成,单一resmlp 子层又可分为交叉图像块线性子层和交叉通道单mlp层。特征矩阵经过resmlp层的数据流以及resmlp内部结构如图所示:resmlp层实际上只对单帧图片的特征矩阵1@36
×
81进行计算,并提取单帧图片中心肌所分成的36个图像块的块内信息和块间关系,得到每一个图像块的像素特征,并存储在输出的矩阵1@36
×
81中。最终20(或25)帧图片组合成resmlp 输出矩阵20@36
×
81。
82.之后对输出的结果进行平均池化,融合20帧图片的心肌像素特征,得到1@26
×
81的特征矩阵,其表示一个cmri电影序列整体的心肌像素特征。再将通过降维得到的36
×
81的二维特征矩阵输入全连接层。池化层选择的是平均池化方法。其替代方法可以是包括空间金字塔池化、中心池化等方法在内的现有池化层方案,其目的均是为了融合一个时间序列的像素特征。
83.全连接层包括两层递减的linear层,第一层linear将特征矩阵由36
×
81降至36
×
49,第二层linear进一步将特征矩阵化为36
×
1的特征向量。通过全连接层,将前面计算得到的特征矩阵映射到样本标记空间,同时两个linear层可以减少过拟合等问题。36维的特征向量与所分割的图像块一一对应,然后用“sigmoid”作为激活函数,将特征向量中每个特征值的大小映射到0-1的范围区间,0表示没有梗死,1表示梗死。全连接层可以替代为任意层数的 linear层,最终输出得到36
×
1的特征向量。其目的均是为了将每一个图像块的特征矩阵映射到样本标记空间。
84.其标签是根据延迟增强(lge)图片分类的,同样以外膜中心点为中心,在医生的指导下标记对应的36个图像块是否有心肌梗死,无梗死标记为0,有梗死标记为1,大小为36
×
1。
85.训练时,使用“adam”优化器,使用二元交叉熵“bceloss”损失函数,因为对于每一个图像块,都是一个单独的二分类问题。对网络输出的特征向量与标签计算损失,对数据进行迭代训练,优化网络参数。当训练结束时,在测试集上检验精度,保存模型。
86.本发明还公开了一种用于识别心肌梗死的相对运动学习方法的装置,包括:
87.分割单元:用于获得心脏核磁共振电影序列,通过u-net模型分割心脏核磁共振成像 (cmri)电影序列中每一帧的心肌内膜与心肌外膜;
88.提取特征单元:将分割好的每一帧的心肌内膜与心肌外膜二值化,得到心肌边界,提取每一帧的像素特征,将其拼接融合,存入36
×
81的二维特征矩阵中;
89.标签单元:标注二维的特征矩阵中对应序列的有钆造影剂的lge图片的梗死区域,
转化成36
×
1的向量作为心肌梗死区域标签;
90.构建神经网络模型单元:基于获得的二维特征矩阵和对应的心肌梗死区域标签,构建以 resmlp为核心的神经网络模型,所述的以resmlp为核心的神经网络模型包括resmlp层、池化层、全连接层;
91.训练单元:以resmlp为核心的神经网络模型中训练时,将模型输出的36
×
1的向量与真实心肌梗死区域标签进行对比,并使用二元交叉熵“bceloss”作为损失函数;
92.优化单元:使用“adam”优化器对网络进行迭代训练,优化网络参数,当训练结束时,在测试集上检测精度,保存准确率最高的模型。
93.对于新病人的梗死区域预测
94.当上述的深度学习网络训练完成以后,即权重值已经确定后,对于新病人的cmri电影序列,进行预处理,之后就可以通过u-net网络分割心肌内外膜,通过提取序列的特征矩阵,将该特征矩阵作为深度学习网络的输入,此时计算出来的特征向量就代表了梗死的区域。将这个区域可视化表达,就是将输出的0和1组成的36
×
1的向量,对应成该部分心肌轮廓的颜色。如果该图像块对应的向量值是1,心肌图像对应的部分就显示为白色,代表该区域有梗死;如果该该图像块对应的向量值是0,心肌图像对应的部分不显示,代表该区域无梗死。医生可以根据显示的图来辅助判断心肌梗死范围。图7为心肌梗死区域结果图,图7(a)为钆剂延迟增强(lge)心脏核磁共振成像图片;图7(b)的白色区域为在有经验的医生指导下在cmri电影序列第一帧图片上标记的心肌梗死区域;图7(c)中的白色边缘范围为在无造影剂情况下,从对应序列分割出的心肌梗死区域,与有造影剂时的一致。
95.本发明经过实验检验;现阶段共有233个确定患有心肌梗死患者的cmri电影序列,经过浙大邵逸夫医院医生指导,对其进行了准确的心肌梗死区域标注。随机取其中50个序列为测试集,20个序列为验证集,100个序列为训练集。使用pytorch架构,在nvidiageforcertx 3070ti 上训练30轮,大约用时130s,其测试集精度可以达到80%左右。使用模型去进行新的序列预测是,一张图片大约用时5ms,其速度非常快,具有良好的实时性。从测试精度可以看出,此方法已经具有一定的实用性,可以作为医生诊断心肌梗死的辅助手段。
96.以上仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1