大分子蛋白和/或核酸用无菌处理剂及其制备方法和应用与流程
[0001]
本发明属于消毒剂技术领域,尤其涉及一种大分子蛋白和/或核酸用无菌处理剂及其制备方法和应用。
背景技术:
[0002]
蛋白和核酸的无菌处理一直以来是难以解决的问题。这类物质对热不耐受,高温高压的灭菌的方法,对物质本身造成不可逆的破坏。巴氏消毒法可以对牛奶进行消毒,这是一个巨大的进步,但是仅用于食品,而且保质期不长,不符合医用的要求。除菌过滤也是常用的方法,但是对于大分子,难以有效通过滤孔,造成巨大的成份损失和堵塞。
[0003]
越来越多的大分子蛋白和核酸被开发出来,如果能够研发出一种能够用于无菌处理的处理剂,必将扩大他们的应用范围,也将具有巨大的经济效益。
技术实现要素:
[0004]
本发明实施例的目的在于提供一种大分子蛋白和/或核酸用无菌处理剂,旨在解决背景技术中提出的问题。
[0005]
本发明实施例是这样实现的,一种大分子蛋白和/或核酸用无菌处理剂,包括以下按照重量份计的组分:5,5-二甲基乙内酰脲0.2~1.5份、吐温-80 0.2~1.5份、人α防御素5 0.5~5份、缓冲溶液3~10份。
[0006]
作为本发明实施例的一个优选方案,所述无菌处理剂包括以下按照重量份计的组分:5,5-二甲基乙内酰脲0.5~1份、吐温-80 0.5~1份、人α防御素5 1~3份、缓冲溶液5~8.5份。
[0007]
作为本发明实施例的另一个优选方案,所述无菌处理剂包括以下按照重量份计的组分:5,5-二甲基乙内酰脲0.7~0.8份、吐温-80 0.7~0.8份、人α防御素5 1.5~2.5份、缓冲溶液6.5~7份。
[0008]
作为本发明实施例的另一个优选方案,所述缓冲溶液为磷酸盐缓冲溶液。
[0009]
本发明实施例的另一目的在于提供一种上述的大分子蛋白和/或核酸用无菌处理剂的制备方法,其包括以下步骤:
[0010]
按照上述各组分的重量份,称取5,5-二甲基乙内酰脲、吐温-80、人α防御素5、缓冲溶液;
[0011]
往缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5进行搅拌混合,得到所述无菌处理剂。
[0012]
作为本发明实施例的另一个优选方案,所述步骤中,搅拌混合的转速为500~1500转/分。
[0013]
本发明实施例的另一目的在于提供一种上述制备方法制得的无菌处理剂。
[0014]
本发明实施例的另一目的在于提供一种上述的无菌处理剂在大分子蛋白和/或核酸的无菌处理中的应用。
[0015]
需要说明的是,该无菌处理剂可用于难以过滤,又不能使用高温高压除菌的一类物质的无菌处理,并不仅限于大分子蛋白和核酸。
[0016]
作为本发明实施例的另一个优选方案,无菌处理时,所述无菌处理剂与大分子蛋白和/或核酸溶液的质量比为1:(100~500)。
[0017]
在本发明中,5,5-二甲基乙内酰脲是一种新型的杀菌剂,其杀菌作用强,已广泛应用于日用化工(如纺织品印染、化妆品)、农业(植物花卉、种子消毒、水果保鲜)、畜牧业、水产业、医药卫生消毒、饮食、饮用水、娱乐场所、游泳池消毒、循环冷却系统(杀灭藻类)等多方面。5,5-二甲基乙内酰脲对细菌繁殖体及芽孢、病毒、真菌和藻类均有杀灭作用,但是细菌在被杀灭的同时,会大量释放出内毒素,内毒素又称为热源,内毒素引发的级联反应造成机体脓毒血症、脓毒性休克和全身炎症反应综合征。在疫苗、抗体药物等蛋白类生物制品的制备过程中,内毒素污染是难以解决的问题。
[0018]
人α防御素5(hd5)是一种阳离子抗菌肽,有广谱抗菌活性,且不易产生耐药性。而且可以中和细菌内毒素,减少了样品中的热源,从而增加了应用中的安全性。hd5可以和5,5-二甲基乙内酰脲协同,在增加对细菌杀灭能力的同时,又不增加热源。但是hd5在溶液中容易水解,杀菌的活性易受到盐离子、阴离子物质的影响。吐温-80为本体系的融合剂,可以使各组分形成均一、稳定的溶液。可以使杀菌效果持久稳定。同时对机体无任何刺激性,使试剂在使用中更安全。
[0019]
本发明实施例提供的一种大分子蛋白和/或核酸用无菌处理剂,可以彻底的杀灭大分子蛋白/核酸溶液中的细菌,对蛋白和核酸没有破坏,而且在杀菌细菌的同时,又不增加溶液中的热源物质,提高了使用的安全性。
具体实施方式
[0020]
为下面将结合本发明实施例中,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0021]
实施例1
[0022]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0023]
s1、准确称取5,5-二甲基乙内酰脲0.2g、吐温-80 0.2g、人α防御素5 0.5g、磷酸盐缓冲溶液10g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0024]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以500转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0025]
实施例2
[0026]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0027]
s1、准确称取5,5-二甲基乙内酰脲1.5g、吐温-80 1.5g、人α防御素5 5g、磷酸盐缓
冲溶液3g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0028]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1500转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0029]
实施例3
[0030]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0031]
s1、准确称取5,5-二甲基乙内酰脲0.3g、吐温-80 0.3g、人α防御素5 4g、磷酸盐缓冲溶液9g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0032]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以800转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0033]
实施例4
[0034]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0035]
s1、准确称取5,5-二甲基乙内酰脲1.4g、吐温-80 1.3g、人α防御素5 0.8g、磷酸盐缓冲溶液4g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0036]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1200转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0037]
实施例5
[0038]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0039]
s1、准确称取5,5-二甲基乙内酰脲0.5g、吐温-80 0.5g、人α防御素5 1g、磷酸盐缓冲溶液8.5g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0040]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0041]
实施例6
[0042]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0043]
s1、准确称取5,5-二甲基乙内酰脲1g、吐温-80 1g、人α防御素5 3g、磷酸盐缓冲溶液5g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0044]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰
脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0045]
实施例7
[0046]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0047]
s1、准确称取5,5-二甲基乙内酰脲0.7g、吐温-80 0.7g、人α防御素5 1.5g、磷酸盐缓冲溶液7g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0048]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0049]
实施例8
[0050]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0051]
s1、准确称取5,5-二甲基乙内酰脲0.8g、吐温-80 0.8g、人α防御素5 2.5g、磷酸盐缓冲溶液6.5g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0052]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0053]
实施例9
[0054]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0055]
s1、准确称取5,5-二甲基乙内酰脲0.5g、吐温-80 0.5g、人α防御素5 1g、磷酸盐缓冲溶液8g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0056]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0057]
实施例10
[0058]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0059]
s1、准确称取5,5-二甲基乙内酰脲1g、吐温-80 1g、人α防御素5 3g、磷酸盐缓冲溶液5g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0060]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0061]
实施例11
[0062]
该实施例提供了一种大分子蛋白和/或核酸用无菌处理剂,其制备方法包括以下步骤:
[0063]
s1、准确称取5,5-二甲基乙内酰脲0.5g、吐温-80 1g、人α防御素5 3g、磷酸盐缓冲溶液5.5g,备用。其中,磷酸盐缓冲液的ph=7.2,其是通过将磷酸氢二钠1.546g、磷酸二氢钠0.262g,氯化钠8.768g,加水溶解并稀释至1000ml得到的。
[0064]
s2、在室温条件下,往上述称取的磷酸盐缓冲溶液中依次加入5,5-二甲基乙内酰脲、吐温-80、人α防御素5,并用磁力搅拌器以1000转/分的速度进行搅拌混合30min,即可得到均一、稳定的无菌处理剂。
[0065]
实施例12
[0066]
该实施例提供了一种利用上述无菌处理剂进行的无菌处理方法,其包括以下步骤:
[0067]
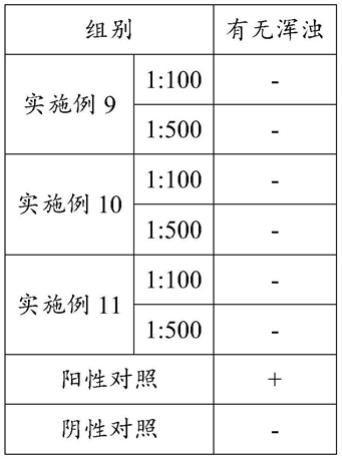
把上述实施例9~11制得的无菌处理剂分别按照1:100和1:500的质量比例加入到含菌的核酸液中,作用1个小时后,分别移种到培养基中,另设一个阳性对照和阴性对照。观察7天后,添加试剂组和阴性对照均无颜色变化(无菌生长),阳性对照出现颜色变化;再把所有接种管再次移种新的培养基中,观察7天后,添加试剂组和阴性对照均无颜色变化(无菌生长),阳性对照出现颜色变化。可见上述实施例9~11制得的无菌处理剂均能彻底杀灭细菌。具体结果见表1和表2。
[0068]
表1各试剂杀菌效果
[0069][0070]
注:表1中,
“-”
代表无浑浊,无菌生长;“+”代表出现浑浊,有菌生长。
[0071]
表2再移植接种后细菌生长情况
[0072][0073]
注:表2中,
“-”
代表无浑浊,无菌生长;“+”代表出现浑浊,有菌生长。
[0074]
实施例13
[0075]
该实施例探索了上述无菌处理剂的对核酸的影响,其包括以下步骤:
[0076]
把上述实施例9~11制得的无菌处理剂分别按照1:100和1:500的比例加入到聚肌胞溶液中,作用48小时后,用紫外分光光度计检测相关参数。结果无菌处理剂组和不添加组没有明显差别。可见上述实施例9~11制得的无菌处理剂对核酸结构没有影响,具体结果见表3。
[0077]
表3各试剂对聚肌胞的影响
[0078][0079]
实施例14
[0080]
该实施例探索了上述无菌处理剂的对大分子蛋白的影响,其包括以下步骤:
[0081]
把上述实施例9~11制得的无菌处理剂分别按照最大浓度1:100的比例加入到表达的大分子蛋白抗原(禽流感)中,作用48小时后,配制成疫苗,免疫sp f(无特定病原)鸡,每组5只,用不处理的蛋白抗原作为对照免疫组。免疫21天后采血检测抗体。结果无菌处理剂组和不添加组没有明显差别。可见上述实施例9~11制得的无菌处理剂对大分子蛋白结构没有影响,具体结果见表4。
[0082]
表4各试剂对大分子蛋白的影响
[0083][0084]
综上所述,本发明实施例提供的无菌处理剂,可以彻底的杀灭大分子蛋白/核酸溶液中的细菌,对蛋白和核酸没有破坏,而且在杀菌细菌的同时,又不增加溶液中的热源物质,提高了使用的安全性。
[0085]
此外,应当理解,虽然本说明书按照实施方式加以描述,但并非每个实施方式仅包含一个独立的技术方案,说明书的这种叙述方式仅仅是为清楚起见,本领域技术人员应当将说明书作为一个整体,各实施例中的技术方案也可以经适当组合,形成本领域技术人员可以理解的其他实施方式。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1