用于膈神经起搏的支撑导管的制作方法
本发明有利地提供了用于例如在标测导管被用于电生理或起搏程序期间为标测导管提供支撑的装置、系统和方法。本发明还有利地提供了用于调整目前可用的标测导管的远侧环形部分的直径的装置、系统和方法。
背景技术:
冷冻消融或利用低温杀死组织常常用来处理诸如心房纤颤的心律失常病症。然而,当通过例如热能交互等处理组织的特定区域时,可能难以导向或控制热传递的深度和强度。对热能或诸如射频或低温施加的其它治疗模式的递送可能并不必然被约束到处理所需的精确区域或深度,因为组织可能具有受周围生理环境影响的不同治疗传导性质。虽然对于诸如射频、微波和/或低温处理程序的某些处理模式来说,热控制或精度可能更重要,但常常希望将热处理或暴露仅限制到所需的组织。做不到这一点可能反而会负面地和不利地影响敏感且易于遭受不期望的损害的周围组织结构或器官。
例如,当尝试处理心脏组织时,有许多附近的敏感组织结构可能会不利地反作用于热施加。特别地,当热处理或消融心脏内部或周围的组织时,重要的是诸如膈神经、窦房结等的重要生理结构不会通过这样的消融治疗而意外受损。膈神经主要由运动神经纤维构成,该神经纤维产生隔膜的收缩并因此影响呼吸模式和状态。此外,膈神经为纵膈和胸膜以及上腹部的许多部分(尤其是肝脏和胆囊)提供感觉神经支配。
膈神经一般被称为两部分:右膈神经和左膈神经。这两个膈神经从C3、C4和C5椎骨沿着前斜角肌向内延伸至颈动脉鞘。右膈神经在头臂动脉上方和锁骨下静脉后方经过,然后从前方横跨右肺根部,接着通过穿过T8水平处的隔膜中的腔静脉裂孔而离开胸部。右膈神经在右心房上方靠近上腔静脉(SVC)处经过。左膈神经在左心室的心包膜上方经过并单独地穿透隔膜。
心脏的右心房和左心房可能是心律失常或其它生理疾病的位置或病源,因此是组织消融的目标,以便消除或者说是纠正异常的电生理现象。在热处理或消融所选的心脏区域过程中,膈神经可能存在被类似地但非故意地消融的风险。这会严重影响患者的正常呼吸功能。此类损伤会表现为瞬时膈功能阻滞、瞬时膈神经麻痹(PNP)或长期膈神经损伤。这些损伤降低呼吸功能,并且可能需要几周或几个月来康复。在最坏的情况下,这种降低的功能需要机械通气辅助来维持呼吸。因此,热能向这一和其它感官结构(cursory structure)的这种非故意和不期望的破坏或施加的风险使得希望在处理期间监测或者说是检测潜在危害性的后果。
这样的监测通常在消融期间利用起搏膈神经和利用连续的荧光镜透视检查以可视化一致的横膈膜响应或腹部触诊,以确认横膈膜运动来进行。两种方法都需要操作者一方的警惕,并且可能分散医师对手头的诊断或处理程序的主要关注。此外,就荧光镜监测而言,患者被暴露于增加的x射线辐射。
膈神经麻痹是心房纤颤的冷冻消融的最常见并发症,它可能引起偏侧膈麻痹。已经开发出用来监测膈神经的各种技术,但所有技术都围绕在靠近诸如左膈神经的膈神经的一部分的方便位置处将起搏能量从SVC内递送至膈神经。通常,病灶导管用来刺激或起搏膈神经,但该导管常常在手术程序期间偏移,导致捕获的损失。对于医师来说,这可能表现为似乎隔膜已停止收缩,并且医师可能决定提前停止消融程序。
诸如标测导管(美敦力公司,明尼苏达州的明尼阿波利斯(Medtronic,Inc.,Minneapolis,Minnesota))的已知标测导管可具有远侧部分,其能够膨胀以使一个或多个电极与诸如肺静脉的内周的靶组织接触。这样的装置可能适合膈神经监测,但膨胀的远侧部分可具有过小的外径,以至于不能使电极接触SVC的内径,SVC的内径可能大于肺静脉的内径。此外,目前已知的标测导管可能缺乏刚度或强度,以便在没有例如低温球囊装置的情况下使用。
因此,希望提供用于从SVC内监测膈神经的装置和系统,该装置和系统比目前已知的标测导管更稳定,并且包括能够调整的可膨胀的远侧部分,以确保在电极和多种脉管尺寸的任一者中的靶组织之间的接触。
技术实现要素:
本发明有利地提供了用于例如在标测导管被用于电生理或起搏程序期间为标测导管提供支撑的装置、系统和方法。本发明还有利地提供了用于调整目前可用的标测导管的远侧环形部分的直径的装置、系统和方法。在一个实施例中,医疗装置支撑装置可包括细长主体,其限定壁且包括至少基本上线性的近侧部分和远侧部分,该远侧部分能够在第一至少基本上线性的构型和第二膨胀构型之间转变,该细长主体限定延伸穿过近侧部分和远侧部分的管腔,该管腔由壁在细长主体的近侧部分中完全包围,并且由壁在细长主体的远侧部分中部分包围。例如,管腔的尺寸可设计成在其中接纳标测导管。当处于第二膨胀构型时,细长主体的远侧部分可以限定弓形构型。细长主体的近侧部分可以限定纵向轴线,并且当远侧部分处于第二膨胀构型时,细长主体的远侧部分可以位于基本上正交于纵向轴线的平面中。细长主体的近侧部分可以由具有第一硬度计硬度的第一材料构成,并且细长主体的远侧部分可以由具有第二硬度计硬度的第二材料构成,第一硬度计硬度大于第二硬度计硬度。此外,处于第二膨胀构型的细长主体的远侧部分可具有可调整的外径。例如,处于第二膨胀构型的细长主体的远侧部分可以是能够在第一最小外径和第二最大外径之间转变的。支撑装置还可以包括一根或多根致动器线,每根致动器线均设置在由细长主体壁限定的封闭通道内。处于第二膨胀构型的细长主体的远侧部分的外径可以通过操纵所述一根或多根致动器线来调整。作为非限制性示例,操纵所述一根或多根致动器线可包括将所述一根或多根致动器线加热至大于预定转变温度的温度和在所述一根或多根致动器线上施加拉力中的至少一种。
在一个实施例中,尺寸被设计成与标测导管一起使用的支撑装置可包括细长主体,该细长主体限定壁且包括限定有纵向轴线的至少基本上线性的近侧部分和能够在第一至少基本上线性的构型和第二膨胀构型之间转变的远侧部分,该细长主体限定延伸穿过近侧部分和远侧部分的管腔,该管腔由壁在细长主体的近侧部分中完全包围并且由壁在细长主体的远侧部分中部分包围,并且处于第二膨胀构型的细长主体的远侧部分具有可调整的直径,该直径能够在第一外径和第二外径之间转变。当细长主体的远侧部分处于第二膨胀构型时,细长主体的远侧部分可以位于基本上正交于细长主体的近侧部分的纵向轴线的平面中。细长主体的近侧部分可以由具有第一硬度计硬度的第一材料构成,并且细长主体的远侧部分可以由具有第二硬度计硬度的第二材料构成,第一硬度计硬度大于第二硬度计硬度。
在一个实施例中,一种用于监测靠近消融部位的神经的系统可包括:支撑装置,其限定壁且包括至少基本上线性的近侧部分和能够在第一至少基本上线性的构型和第二弓形构型之间转变的远侧部分,该支撑装置限定延伸穿过近侧部分和远侧部分的管腔,该管腔由壁在支撑装置的近侧部分中完全包围并且由壁在支撑装置的远侧部分中部分包围,使得壁限定支撑装置的远侧部分中的开口;以及在细长主体的管腔内的标测导管,该标测导管具有至少基本上线性的近侧部分和能够在第一至少基本上线性的构型和第二弓形构型之间转变的远侧部分,该标测导管包括在远侧部分上的一个或多个电极。标测导管的近侧部分可以设置在支撑装置的近侧部分中的管腔内,并且标测导管的远侧部分可以设置在支撑装置的远侧部分中的管腔内。在标测导管的远侧部分上的所述一个或多个电极中的每一个的至少一部分可以通过支撑装置的远侧部分中的壁的开口而暴露。处于第二弓形构型的支撑装置的远侧部分可具有可调整的直径,该直径能够在第一外径和第二外径之间转变。该系统还可包括与标测导管的所述一个或多个电极电连通的能量源和一根或多根致动器线。所述一根或多根致动器线也可以与能量源连通,并且当来自能量源的电流被传输通过所述一根或多根致动器线时,支撑装置的远侧部分可以在第一外径和第二外径之间转变。
附图说明
通过参照结合附图考虑的下面的详细描述,将更容易理解对本发明的更完整的理解和伴随的优点及其特征,在附图中:
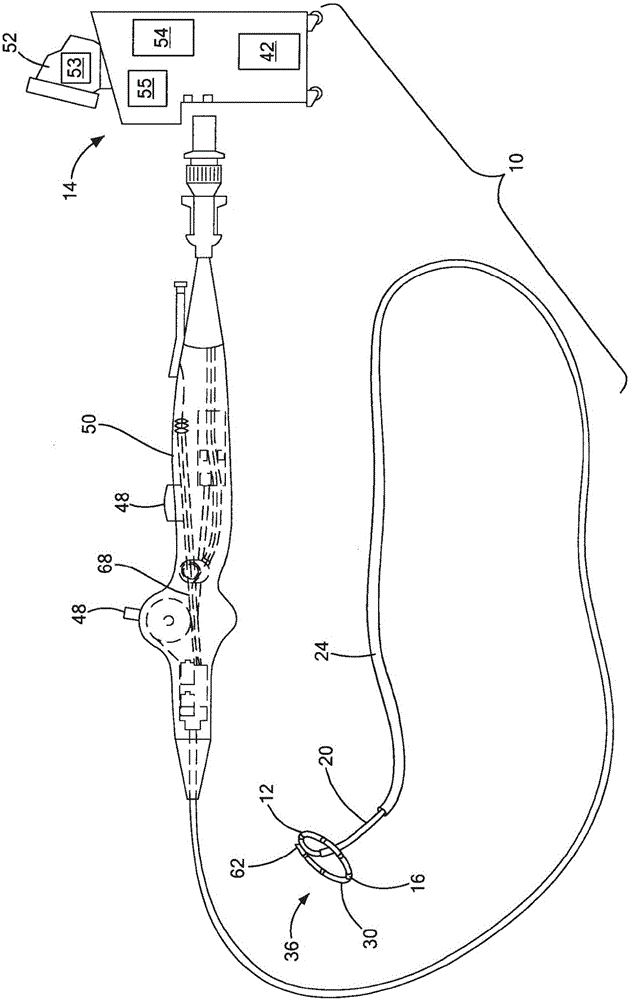
图1示出了包括标测导管和支撑装置的示例性医疗系统;
图2示出了包括标测导管、支撑装置和热处理装置的示例性医疗系统;
图3A示出了支撑装置的近侧部分的第一剖视图;
图3B示出了支撑装置的远侧部分的第一剖视图;
图3C示出了支撑装置的近侧部分的第二剖视图;
图3D示出了支撑装置的远侧部分的第二剖视图;
图4A示出了在护套内的支撑装置的部分剖视图,该支撑装置处于递送构型;
图4B示出了在护套内的支撑装置,该支撑装置处于膨胀构型;
图5示出了处于第二膨胀构型的支撑装置的正视图;
图6示出了可移除地接合在支撑装置内的标测导管的侧视图;
图7A示出了可移除地接合在支撑装置内的标测导管远端的正视图,标测导管远端和支撑装置远端具有为第一直径的弓形形状;
图7B示出了可移除地接合在支撑装置内的标测导管远端的正视图,标测导管远端和支撑装置远端具有为第二直径的弓形形状;
图7C示出了可移除地接合在支撑装置内的标测导管远端的正视图,标测导管远端和支撑装置远端具有为第三直径的弓形形状;
图8示出了位于上腔静脉附近的支撑装置和标测导管,该支撑装置和标测导管处于第一递送构型;
图9示出了位于上腔静脉内的支撑装置和标测导管,该支撑装置和标测导管处于第二膨胀构型,但不与上腔静脉的内径接触;以及
图10示出了位于上腔静脉内的支撑装置和标测导管,该支撑装置和标测导管处于第二膨胀构型。
具体实施方式
本发明有利地提供了用于例如在标测导管被用于电生理或起搏程序期间为标测导管提供支撑的装置、系统和方法。本发明还有利地提供了用于形成和/或调整目前可用的标测导管的远侧环形部分的直径的装置、系统和方法。现在参看附图,其中类似的附图标记是指类似的元件,包括根据本发明的原理的支撑装置的医疗系统的实施例在图1和图2中示出并且大体上标示为“10”。系统10大体上包括医疗装置12,其可以联接到控制单元14或操作控制台。医疗装置12可以被构造成与组织、例如与一个或多个电极16相互作用。例如,医疗装置12可以是标测和/或起搏导管,其被构造成记录来自心脏组织的电信号、在心脏起搏程序期间刺激组织和/或热处理组织。虽然装置12可以用于标测、起搏和/或热处理,但为简单起见,装置12可以在本文中被称为“标测导管”。
系统10也可包括支撑装置20,在支撑装置中具有管腔22。支撑装置20可以是能够可移除地插入到护套24或其它引导元件中的,以用于例如递送通过患者的脉管系统至目标位置。此外,支撑装置20可以可移动地(例如,纵向可滑动地)和/或可旋转地设置在护套24内,使得护套24和支撑装置20可彼此独立地移动。标测导管12可以是能够可移除地插入到支撑装置20的管腔22中的。然而,如在图6-7B中更详细地示出和描述的,标测导管的远侧部分30(包括远侧顶端32)可以是能够与支撑装置23的至少一部分可移除地接合的,使得标测导管12和支撑装置20不能彼此独立地移动,而是作为一个单元一起被操纵、推进通过护套24并且从护套24内的第一递送构型膨胀至护套24外部的第二膨胀构型。该标测导管12/支撑装置20单元可以在本文中被称为“受支撑的标测组件36”。应当理解,除了标测组织之外,受支撑的标测组件36也可以用来起搏和/或热处理组织。
图1的系统10示出为带有标测导管12和支撑装置20。图2的系统10可以附加地包括处理装置,例如处理导管40。作为非限制性示例,处理导管40可包括低温球囊42,其与冷却剂源44流体连通。另外地或备选地,处理导管40可包括球囊42,其具有一个或多个电极并且被构造成递送一种或多种能量形式,例如射频、超声波、微波能量等。另外地或备选地,处理导管40可包括可膨胀的笼子、网片、篮子或除了球囊42之外的其它可膨胀元件。导管40也可包括管腔,支撑装置20可以是能够可移除地插入该管腔内的。导管40又可以是能够可移除地插入护套24内的,以递送至目标处理部位。
标测导管12、支撑装置20和/或护套24可以与一个或多个控制机构48连通,以使装置12、20和护套24转向和膨胀。例如,装置12、20和/或护套24可以与柄部50电气和/或机械连通,如图1和图2所示。备选地,每个装置12、20和护套24可以与其自己的柄部连通。此外,每个装置12、20可以与控制单元14电气连通,控制单元14包括一个或多个计算机52,计算机52具有一个或多个处理器53,处理器53将来自标测导管12的一个或多个信号接收、处理、存储和/或传递给用户(例如,将数据显示在可视显示器上和/或生成可视或可听警报)。根据所使用的能量形式,控制单元14也可包括能量源54(例如,射频能量源)、电流源55和可选地冷却剂源42,它们与标测导管12和/或处理导管40(如使用)连通。
现在参看图3A-7B,更详细地示出了支撑装置20。支撑装置20可包括细长主体,其包括第一或近侧至少基本上线性的部分56。近侧部分56尺寸可设计为并成形为使得它可以穿过护套24或处理导管40的管腔。近侧部分56可以由聚合物构成,例如生物相容性共聚物(例如,)或聚合物/硫酸钡共混物。
支撑装置20的细长主体还可包括第二或远侧部分58,其能够在类似于近侧部分56的第一至少基本上线性的构型(例如,如图4A所示)和第二膨胀构型(例如,如图4B所示)之间转变。例如,支撑装置20可以在近侧到远侧的方向上被推进通过护套24。随着支撑装置20的远侧部分58离开护套24的远侧开口60,远侧部分58可以从第一至少基本上线性的构型转变至第二膨胀构型。如图4B-7B所示,远侧部分58可以呈现弓形形状。作为非限制性示例,远侧部分58可以呈现如下弓形形状,该形状限定大约360°±大约45°的圆周(在图5中示出为角度α2)。即,支撑装置的远侧顶端62可以在从弓形部分的起点64起大约0°±大约45°(在图5中示出为角度α3)内。此外,当处于第二弓形或膨胀构型时,支撑装置20的远侧部分58可以位于基本上正交于第一部分56的纵向轴线66的平面内(如图4B所示)。当支撑装置20的远侧部分58处于第一至少基本上线性的构型时,近侧部分56和远侧部分58可具有相同的纵向轴线66(例如,如图4A所示)。
如图所示,例如,在图3A-3D中,支撑装置20可包括一根或多根致动器线68,每根致动器线均位于支撑装置20的壁72中的封闭通道70内。壁72可以限定或包含一个或多个通道70,而不包括任何厚度增加的区域。另一方面,如图3A和图3B所示,一个或多个通道70可以位于壁72的外部部分72A中(即,靠近壁72的外周边)。壁72可以限定或包含在壁72的外部部分72A上的具有增加的壁厚的区域内的一个或多个通道70(如图3A和图3B所示)。对设置在壁的外部部分72A上的致动器线68的致动(例如,在致动器线68上施加拉力或造成致动器线68收缩)可以允许用户增加支撑装置20的远侧部分58的直径,如在图7A-7C中更详细地示出和描述的。另外地或备选地,一个或多个通道70可以位于壁72的内部部分72B中(即,靠近壁72的内周边)。壁72可以限定有或包含在壁72的内部部分72B上的具有增加的壁厚的区域内的一个或多个通道70(如图3C和图3D所示)。每根致动器线58的远侧部分可以附接到(例如,粘结、粘附、焊接、固定或以其它方式联接到)例如支撑装置远侧顶端62的内表面。每根致动器线58的近侧部分可以与柄部50内的转向机构48机械连通,以用于线68的手动控制。此外,每根致动器线可以与一个或多个处理器53连通,以用于系统10对线68的自动或半自动控制。对设置在壁的内部部分72B上的致动器线68的致动(例如,在致动器线68上施加拉力或造成致动器线68收缩)可以允许用户减小支撑装置的远侧部分58的直径,如在图7A-7C中更详细地示出和描述的。此外,支撑装置20可包括一个或多个通道70,该通道位于壁的内部部分72A和外部部分72B两者中(如图3C和图3D所示)。应当理解,可以使用任意数量的通道70和致动器线68,并且它们可以位于内部部分72A、外部部分72B或两者上。此外,根据支撑装置20的远侧部分58的构型,每根致动器线58的远侧部分可以在除了远侧顶端62的顶端之外的位置附接到支撑装置20。
远侧部分58可以由与近侧部分56相同的材料构成。备选地,远侧部分58可以由具有比近侧部分56材料高的硬度计硬度的诸如聚合物的材料构成。另外地或备选地,远侧部分58可包括金属插件或环73,其增加远侧部分58的刚度。例如,插件或环73可以由镍钛诺构成。备选地,整个远侧部分58可以由诸如合金和聚合物的形状记忆材料构成,该材料响应于温度变化而从第一构型转变至第二构型。例如,远侧部分58可以由这样的材料构成:该材料在室温下具有至少基本上线性的构型,并且在增加的温度下(例如,当在患者体内的医学程序中使用时,在周围的血液和/或组织的温度下)具有弓形的膨胀构型。备选地,当处于膨胀构型时,远侧部分58可具有在第一温度下的第一外径和在第二温度下的第二外径。
备选地,远侧部分58可以由这样的材料构成:当电流穿过远侧部分58时,该材料能够在第一构型和第二构型之间转变。例如,传输至所述一个或多个电极的电能可以造成远侧部分58的温度增加至或超出转变温度。该热量可以造成远侧部分58从至少基本上线性的构型转变至弓形的膨胀构型,和/或当处于膨胀构型时可以造成远侧部分58的外径的变化。另外地或备选地,如下文更详细地讨论的,远侧部分58的构型和/或直径可以使用一根或多根致动器线68来调整。
如上文所讨论的,支撑装置20的近侧部分56限定由装置的壁72完全包围的闭合的管腔22。另一方面,支撑装置20的远侧部分58可包括沿着远侧部分58的至少一部分的“暴露的”管腔74。如本文所用,术语“暴露的管腔”可以指装置管腔的一部分,其中,管腔仅被装置的壁72部分地包围,从而在壁72中留下开口75(例如,如图4A所示)。如下文所讨论的,该暴露的管腔74可以允许标测装置12的一个或多个电极16保持暴露且能够接触组织。相比之下,支撑装置20的远侧顶端62可以限定封闭的管腔72,其完全由装置的壁72包围。作为非限制性示例,封闭的管腔22可以由壁72围绕封闭的管腔22的圆周的约360°而包围,并且暴露的管腔74可以由壁约在大约150°和大约270°之间的角度(在图3B中示出为角度α1)包围。
现在参看图6-7B,示出了可移除地接合在支撑装置内的标测导管。类似于支撑装置20,标测导管12可以限定至少基本上线性的第一部分80和第二部分30,第二部分30能够在当标测导管在支撑装置内时的第一至少基本上线性的构型和当第二部分30从支撑装置20的近侧部分56的封闭的管腔22的远侧开口84穿出时的第二膨胀构型之间转变。第二构型可以是弓形的,类似于支撑装置20的远侧部分58的第二膨胀构型。当支撑装置20在使用时,标测导管12的第一部分80可以设置在支撑装置20的近侧部分56的封闭的管腔22内。支撑装置20的远侧部分58的尺寸可设计成接纳标测导管12的第二部分30。此外,标测导管12的远侧顶端32可以牢固地接纳在支撑装置20的远侧顶端62的封闭的管腔22内。因此,标测导管12的第二部分30和支撑装置20的远侧部分58可以作为一个单元(“受支撑的标测导管36”)一起在所述第一至少基本上线性的构型和所述第二膨胀构型之间转变。
当标测导管12设置在支撑装置20内时,支撑装置20的第二部分30的暴露的管腔74可以允许位于标测导管12的远侧部分58处的所述一个或多个电极16保持暴露(即,不被支撑装置20的壁72的一部分覆盖或遮挡)。这样,电极16可以继续记录标测信号和/或递送起搏能量,而不被支撑装置20阻碍或妨碍。
上腔静脉(SVC)的内径DSVC可以大于例如肺静脉的内径(DPV)。诸如标测导管(美敦力公司,明尼苏达州的明尼阿波利斯(Medtronic,Inc.,Minneapolis,Minnesota))的一些标测导管可具有膨胀成弓形形状的远侧部分,该弓形形状的尺寸设计成与肺静脉的内径基本上接触。然而,这样的导管的远端的尺寸可能不会被设计成足以基本上接触SVC的内径。
如上文所讨论的,支撑装置20的远侧部分58可以是能够从第一至少基本上线性的构型转变至具有弓形形状的第二膨胀构型的。此外,弓形的远侧部分58可具有能够调整的直径,以适应多种标测和/或起搏目标中的任一者。当标测导管12设置在支撑装置20内时,支撑装置20的远侧部分58的膨胀同样可以使标测导管12的第二部分30膨胀。暴露的管腔74中的壁72的一部分和支撑装置远侧顶端62的封闭的管腔中的壁72可以确保当支撑装置20的远侧部分58的直径增加或减小时标测导管12保持牢固地设置在支撑装置20内。例如,远侧部分58可以膨胀,直到标测导管12的第二部分30的所述一个或多个电极16与SVC的内径基本上接触。换句话讲,受支撑的标测组件36(即,作为一个单元一同起作用的支撑装置20和标测导管12)的远侧部分88可具有可调整的直径,以适应一定范围的脉管尺寸。在一个非限制性示例中,远侧部分88的外径可以从第一直径D1(如图7A所示)膨胀至第二直径D2(如图7B所示)或收缩至第三直径D3(如图7C所示)。随着远侧部分88的外径增加,在远侧顶端62和弓形部分的起点64之间的距离和角度α3可以增加。同样,随着远侧部分88的外径减小,在远侧顶端62和弓形部分的起点64之间的距离和角度α3可以减小。事实上,距离和角度α3可以减小到使得远侧顶端62可以与起点64至少部分地重叠(如图7C所示)。
为了调整支撑装置20的膨胀的远侧部分58和由此调整受支撑的标测组件36的远侧部分88的直径,支撑装置20可包括一根或多根致动器线68,每根致动器线设置在支撑装置壁72内的封闭的通道70中(如图3A-3D所示)。如果使用一根或多根致动器线68,支撑装置20的近侧部分56可以由具有足够大的硬度计硬度的材料构成,以抵抗所述一根或多根致动器线68的弯曲、扭结或者说是被施加在其上的拉力的影响。即,牵拉所述一根或多根致动器线68仅可以影响支撑装置20的远侧部分58,而不影响近侧部分56。
所述一根或多根致动器线68可以类似拉线那样被操纵。即,拉力可以施加在线68上,以实现支撑装置20的远侧部分58的构型和/或直径的改变。例如,在位于设置在支撑装置壁72的内部部分72B上的通道70中的致动器线68上施加拉力可以造成支撑装置20的远侧部分58从至少基本上线性的构型转变至膨胀构型,或者可以造成在处于膨胀构型时远侧部分58的外径的减小。类似地,在位于设置在支撑装置壁72的外部部分72A上的通道70中的致动器线68上施加拉力可以造成支撑装置20的远侧部分58从膨胀构型转变为至少基本上线性的构型,或者可以造成在处于膨胀构型时的远侧部分58的外径的增加。
另外地或备选地,远侧部分58的构型和/或直径可以是能够通过使用由诸如金属合金或聚合物的形状记忆材料构成的一根或多根致动器线68调整的,该材料响应于温度变化而从第一构型转变至第二构型。例如,所述一根或多根致动器线68可以由形状记忆材料构成,该材料在室温下具有中性长度,但在增加的温度(即,超过预定转变温度的温度)下,例如当在医疗程序中在患者体内使用时,在周围的血液和/或组织的温度下收缩。
另外地或备选地,远侧部分58的构型和/或直径可以是能够通过将电荷传输通过所述一根或多根致动器线68而调整的。例如,所述一根或多根致动器线68可以由形状记忆合金(Dynalloy公司,加利福尼亚州塔斯廷(Dynalloy,Inc.,Tustin,California))构成,该合金可以随着温度增加超过预定转变温度而收缩。转变温度可以在大约140°F和大约230°F之间(在大约60℃和大约110℃之间),当电荷被传输通过所述一根或多根致动器线68时,可以达到该转变温度。电荷可以由电流源55生成并从近侧部分至远侧部分传输通过每根致动器线68,以便将线68加热至转变温度或超出转变温度。这种加热可以造成线68收缩,由此改变支撑装置20的远侧部分58的构型和/或直径。一旦电流通过线68的传输停止,线68可以冷却至转变温度以下的温度并膨胀至中性长度。作为非限制性示例,致动器线68可以收缩其中性长度的几个百分比。
电流可以独立于传输至标测导管的所述一个或多个电极16的电流而被传输至所述一根或多根致动器线68,其中在整个医疗手术程序期间较低的基线电流被传输至所述一根或多根致动器线68。相比之下,起搏能量可以在每秒几毫秒(ms)的时期内传输至所述一个或多个电极16。系统10可包括第二电流源,其与所述一根或多根致动器线68连通,而第一电流源55可以与标测导管12的所述一个或多个电极16连通。另外地或备选地,可以使用单个电流源55,其与所述一根或多根线68和所述一个或多个电极16连通。在这种情况下,能量传输可以被调制,以使得恒定的低基线电流被传输至所述一根或多根致动器线68,并且起搏信号以所需的间隔和足以激励例如膈神经的水平传输至所述一个或多个电极16。
现在参看图8-10,示出了一种使用受支撑的标测组件36的方法。受支撑的标测组件36可以用来在程序期间记录标测信号和/或递送起搏能量至患者的心血管系统内的区域,例如上腔静脉(SVC),以在用于在治疗心房纤颤的心脏内的冷冻消融期间监测膈神经。作为用途的非限制性示例,护套24可以推进通过患者的脉管系统至心脏的右心房。从右心房起,护套24可以向SVC内推进一段距离至靠近膈神经的目标位置(图8)。
一旦护套24位于目标位置附近,支撑装置20(标测导管12接合在其内,如图1-7B中所示出和描述的)可以被推进通过护套24并离开远侧开口60。当受支撑的标测组件36(即,接合在其中的支撑装置20和标测导管12)的远侧部分88在护套24内时,支撑装置20和标测导管12的远侧部分58、30可以处于第一递送或至少基本上线性的构型。当受支撑的标测组件36的远侧部分88被推进超过并离开护套24的远侧开口60时,支撑装置20和标测导管12的远侧部分58、30可以处于具有弓形形状的第二膨胀构型(图9)。
初始地,标测组件的远侧部分88可具有第一外径D1(例如,如图7A所示)。然而,外径D1可以小于SVC的内径DSVC,并且因此,标测导管12的所述一个或多个电极16可能不与SVC接触。为了解决这个问题,受支撑的标测组件88的远侧部分88可以膨胀至在第一外径D1和最大可能外径之间的任何外径。例如,远侧部分88可以从第一直径D1膨胀至扩大的第二外径D2,第二外径足以使所述一个或多个电极16放置成在靠近膈神经的一部分(例如左膈神经)的位置处与SVC的内周接触(例如,如图7B和图10所示)。此外,远侧部分88可以从第一直径D1或第二直径D2收缩至第三直径D3,以用于在患者的脉管系统的脉管中使用,该脉管具有例如小于典型的肺静脉的内径的内径。可以使用例如一根或多根致动器线68来实现远侧部分88的外径的膨胀,如上文所示出和描述的。相比标测导管12的远侧部分82,支撑装置20的远侧部分58可以更硬或者可具有更高的硬度计硬度。因此,在支撑装置20的远侧部分58的构型和/或直径中的任何调整或变化都可以造成标测导管12的远侧部分82的构型和/或直径中的相同变化。
虽然未示出,但应当理解,在图8-10中示出和描述的相同方法也可以用于包括处理导管40的系统,例如图2中示出和描述的系统10。
本领域的技术人员应理解,本发明不限于上文已特定示出和描述的内容。此外,除非上面提到为相反,应当指出,所有的附图都不是按比例的。在不脱离仅由所附权利要求限制的本发明的范围和精神的情况下,根据上述教导,多种修改和变型是可能的。
- 还没有人留言评论。精彩留言会获得点赞!