一种可核磁共振显像体内植入材料及其制备方法和应用与流程
本发明涉及医疗器械领域,更具体地,涉及一种可核磁共振显像体内植入材料及其制备方法和应用。
背景技术:
核磁共振(Nuclear Magnetic Resonance,NMR)是指原子核在一定条件下与外磁场共振的物理现象,作为一种分析手段广泛应用于物理、化学生物等领域,到1973年才将它用于医学临床检测。为了避免与核医学中放射成像混淆,把它称为核磁共振成像(Magnetic Resonance Imaging,MRI)或磁共振成像或核磁共振显像。核磁共振(NMR)与磁共振成像(MRI)在磁共振基础理论、信号激发、弛豫时间等方面并无差异,通常对核磁共振与磁共振成像两概念不做区分。
核磁共振成像的基本工作原理是将人体置于特殊的磁场中,用无线电射频脉冲激发人体内氢原子核,引起氢原子核共振,并吸收能量。在停止射频脉冲后,氢原子核按特定频率发出射电信号,并将吸收的能量释放出来,被体外的接受器收集,经电子计算机处理获得图像,这一过程称为核磁共振成像。在医学方面,MRI利用人体内物质拥有不同弛豫时间的特点,通过施加射频信号可以得到人体的核磁共振图像,以此来达到区分、判断人体组织状态的目的。MRI提供的信息量不但大于医学影像学中的其他许多成像技术,而且不同于已有的成像技术,因此,它对疾病的诊断具有很大的潜在优势。它可以直接作出横断面、矢状面、冠状面和各种断面的体层图像,无电离辐射,对机体没有不良影响。MRI对检测脑内血肿、脑外血肿、脑肿瘤、颅内动脉瘤、动静脉血管畸形、脑缺血、椎管内肿瘤、脊髓空洞症和脊髓积水等颅脑常见疾病非常有效,同时对腰椎椎间盘后突、原发性肝癌等疾病的诊断也很有效。由于信号强度、采集方式以及原子核丰度的限制,医学核磁共振设备只能探测人体中氢原子的信号,且信号主要来自水质子与脂质子。
人体植入材料作为一种医疗器材已被大量用于医疗领域,高分子材料是现有人体植入材料的重要原料。由于原子核类型、核外电子屏蔽效应等因素的存在,一定频率、一定能量的射频脉冲仅能作用于进动频率匹配的原子核。基于人体的特点,核磁共振的信号主要源自于水分子与脂肪分子中的氢核。高分子材料包含大量非氢原子,且其中氢原子相对水质子与脂质子的外部电子环境差异巨大,不会被射频脉冲激发,或其弛豫时间仅为数十毫秒,小于核磁共振信号采集时间。因而,置入体内的高分子材料,通常在核磁共振下完全无信号,或被组织液浸润进而与周围组织无差别,致使术后很难观察植入的高分子材料在体内的状态,给进一步的治疗和诊断带来不便。
因此,探索一种具有核磁共振特异性响应且外形可控的核磁共振显像高分子基复合材料作为植入材料显得尤为重要。
技术实现要素:
为了克服现有技术中高分子基体内植入材料不能在核磁共振下显像的问题,本发明提供一种在核磁共振下显像的体内植入材料。该材料由高分子材料与具有核磁共振特异性响应材料复合而成,在不同核磁共振扫描序列下具有与人体组织不同的特异性信号,在核磁共振下产生图像,有效解决了现有植入材料在人体内由于与周围环境组织无信号差从而不能获取植入材料信息的缺点。
本发明的另一目的在于提供一种上述核磁共振显像材料的制备方法,采用静电纺丝法将高分子材料与具有核磁共振特异性响应材料制成超细复合纤维。该方法简单可行、重复性好且可纺材料来源广泛,所得纤维材料具有直径超细、比表面积大的特点,且可根据实际需要制备出可控外形。
本发明的再一目的在于提供上述核磁共振显像体内植入材料的应用。
本发明的目的通过下属技术方案实现:
一种可核磁共振显像体内植入材料,所述植入材料由高分子材料与具有核磁共振特异性响应材料复合而成。
优选地,所述高分子材料与具有核磁共振特异性响应材料的质量比为1:(10-5~1.5)。
所述高分子材料为天然高分子材料,合成高分子材料,或天然高分子与合成高分子混合材料;
优选地,所述天然高分子材料聚乳酸、聚己内酯、聚乙交酯、聚丙交酯、聚羟基乙酸、透明质酸、纤维蛋白、丝蛋白、聚乙二醇、壳聚糖、胶原蛋白或明胶中的一种以上;
优选地,所述合成高分子材料为聚乙烯、聚丙烯、聚氯乙烯、聚苯乙烯、聚甲基丙烯酸甲酯、聚酰胺、聚碳酸酯、聚甲醛、聚对苯二甲酸丁二酯、聚对苯二甲酸乙二酯、醋酸纤维素、甲基纤维素、乙基纤维素、羟乙基纤维素、氰乙基纤维素、羟丙基纤维素、羟丙基甲基纤维素、羟乙基淀粉、羧甲基淀粉、聚乙烯吡咯烷酮、聚乙烯醇、聚丙烯腈、聚乙二醇-聚乳酸嵌段共聚物、聚乙二醇-聚己内酯嵌段共聚物、聚乙二醇-聚乙烯吡咯烷酮嵌段共聚物、聚苯乙烯-聚丁二烯嵌段共聚物、苯乙烯-丁二烯-苯乙烯三嵌段共聚物、聚苯乙烯-聚(乙烯-丁烯)-聚苯乙烯嵌段共聚物、苯乙烯-异戊二烯/丁二烯-苯乙烯嵌段共聚物或聚苯乙烯-聚丁二烯-聚苯乙烯嵌段共聚物中的一种以上。
优选地,所述具有核磁共振特异性响应材料为铕化合物、钆化合物、铽化合物、镝化合物、锰化合物、铁磁性材料、多元醇、甘油酯、甾醇化合物或脂肪酸中的一种以上。
更为优选地,所述铕化合物为氧化铕、氯化铕、纳米氧化铕或纳米氯化铕;所述钆化合物为钆二乙基三胺五乙酸螯合物、氧化钆、氯化钆、草酸钆、纳米氧化钆、纳米氯化钆或纳米草酸钆;所述铽化合物为氧化铽、氯化铽、纳米氧化铽或纳米氯化铽;所述镝化合物为氧化镝、氯化镝、纳米氧化镝或纳米氯化镝;所述锰化合物为四氧化三锰、氯化锰、纳米四氧化三锰、纳米氯化锰、柠檬酸螯合锰或乙二胺四乙酸锰;所述铁磁性材料为超顺磁性纳米氧化铁、磁性四氧化三铁、铁酸钠、柠檬酸螯合铁、氨基酸铁、乙二胺二邻苯基乙酸铁;所述多元醇为乙二醇、丙二醇或丙三醇;所述甘油酯为单硬脂酸甘油酯、双硬脂酸甘油酯或三硬脂酸甘油酯;所述甾醇化合物为胆甾醇、谷甾醇、豆甾醇、麦角甾醇或羊毛甾;所述脂肪酸为月桂酸、肉豆蔻酸、软脂酸、硬脂酸、花生酸、木蜡酸、亚油酸、亚麻酸、花生四烯酸、二十碳五烯酸或二十二碳六烯酸。
一种上述可核磁共振显像体内植入材料的制备方法,包括以下具体步骤:
S1.将高分子材料溶于溶剂中,搅拌得到均匀的浓度为1~30wt%的高分子溶液,然后加入具有核磁共振特异性响应材料混合,搅拌均匀得到纺丝混合溶液;
S2.将步骤S1所得纺丝混合溶液装入带有喷射头的储存容器中进行静电纺丝,静电纺丝的条件和参数范围为:高压静电电压范围为9~40kV,环境温度为15~40℃,空气相对湿度为30~95%,喷丝头与收丝装置的距离为5~50cm,用收丝装置进行收集并获得超细纤维;
S3.将步骤S2中收集到的超细纤维,按使用需要造型,室温下空气气氛密封保存,即得到可核磁共振显像体内植入材料。
优选地,步骤S1中所述溶剂为二氯甲烷、三氯甲烷、二氯乙烷、四氯乙烷、丙烯酸甲酯、四氢呋喃、甲基四氢呋喃、N,N-二甲基甲酰胺、N,N-二甲基乙酰胺、二甲基亚砜、乙醚、石油醚、丙酮、甲酸、乙酸、三氟乙酸、四氯化碳、二甲苯、甲苯、苯酚、氯苯、硝基苯、戊烷、正己烷、甲基环己烷、N-甲基吡咯烷酮、苯甲醚、甲醇、乙醇、1-丙醇、2-丙醇、1-丁醇、2-丁醇、戊醇、N-甲基吗啉-N-氧化物、氯化甲基咪唑盐或甲酚中的一种以上;当步骤S1中所述具有核磁共振特异性响应材料为纳米材料时,加入分散剂混合,所述分散剂为脂类分散剂、脂肪烃分散剂、金属皂类分散剂、聚多元醇类分散剂或酸酐分散剂。
更为优选地,所述脂类分散剂为单硬脂酸甘油酯、双硬脂酸甘油酯或三硬脂酸甘油酯;所述脂肪烃分散剂为直链烷烃,其化学通式为CnH2n+2,其中n=3~60;所述金属皂类分散剂为硬脂酸钡或硬脂酸锌;所述聚多元醇类分散剂为聚乙二醇或聚丙三醇;所述酸酐分散剂为水解聚马来酸酐。
优选地,步骤S2中所述收丝装置可为:(1)平板收丝装置,由一块平板构成,接地或与-30~-0.5kV负高压相连;或(2)滚筒收丝装置,由直径为5~30cm的滚筒与驱动电机组成,滚筒转速为50~3000r/min,滚筒接地或与-30~-0.5kV负高压相连。
上述可核磁共振显像体内植入材料在颅神经减压垫片、盆底复合补片、下睑替代材料、疝气修补片、人工胸壁、心脏补片、术后防粘连膜中的应用。
本发明通过选用不同的具有核磁共振特异性响应材料,获得具有不同核磁共振响应信号与强度的核磁共振显像体内植入材料。由于人体组织具有各自的T1、T2弛豫时间,在不同的扫描序列下,具有特定弛豫时间的组织能表现出明显的亮(高信号)或暗(低信号)的图像,如类似脂肪拥有长T2的组织,在T2平扫图像下会表现为较亮(高信号),而肝脏T2较短,则表现为较暗(低信号)。在人体内现有高分子植入材料与周围组织无信号差别,本发明有效解决了这种无信号差别的问题,手术植入后可通过无损伤MRI检测获得植入物位置和形状变化等信息,以实现跟踪和了解病患病情的目的。
与现有技术相比,本发明具有以下有益效果:
1.本发明的可核磁共振显像体内植入材料既保留了高分子材料本身的力学性能和生物学特性,又实现了在核磁共振下的显像效果。可以在核磁共振下获得显著区别于人体周围组织的图像,获得出植入材料的形状与体内位置等信息。
2.本发明采用静电纺丝法制备可核磁共振显像体内植入材料,该方法简单可行、重复性好且可纺材料来源广泛,所得纤维材料具有直径超细、比表面积大的特点,可根据实际需要制备出外形可控,且具有设计信号类型的核磁共振显像材料。
3.本发明通过选用不同的具有核磁共振特异性响应材料,获得具有不同核磁共振响应信号与强度的核磁共振显像材料,使可核磁共振显像体植入材料有效解决了在人体内由于现有高分子植入材料与周围组织无信号差别而不能获取植入材料信息的问题,手术植入后可通过无损伤MRI检测获得植入物位置和形状变化等信息,以实现跟踪和了解病患病情的目的。可在颅神经减压垫片、盆底复合补片、下睑替代材料、疝气修补片、人工胸壁、心脏补片、术后防粘连膜中得到广泛地应用。
附图说明
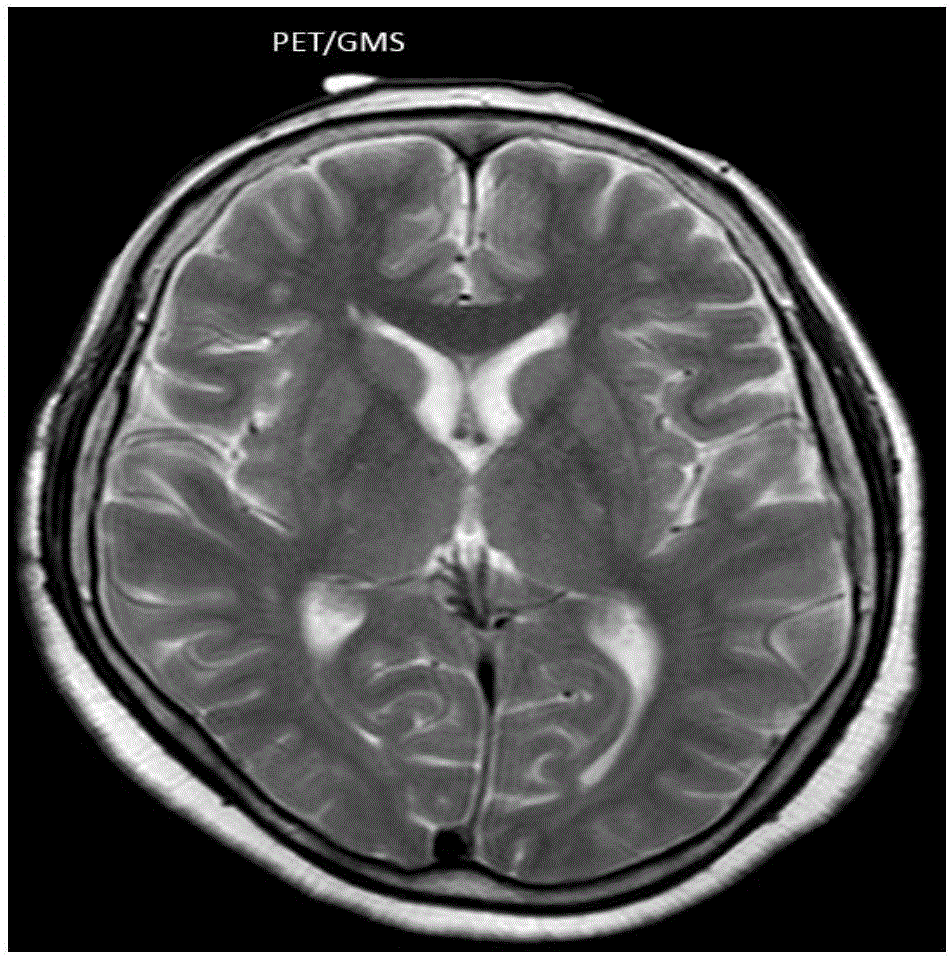
图1为实施例1中聚对苯二甲酸乙二酯(PET)/单硬脂酸甘油酯(GMS)体内植入材料贴附于脑部皮肤的T2平扫MRI图像。
图2为实施例1中聚对苯二甲酸乙二酯(PET)/单硬脂酸甘油酯(GMS)体内植入材料的实物照片。
图3为实施例2中聚对苯二甲酸乙二酯(PET)/丙三醇(GLY)体内植入材料贴附于脑部皮肤的T2平扫MRI图像。
图4为实施例3中聚对苯二甲酸乙二酯(PET)/单硬脂酸甘油酯(GMS)/超顺磁性纳米氧化铁(SPIO)体内植入材料的扫描电子显微镜照片。
具体实施方式
下面结合具体实施例进一步说明本发明的内容,但不应理解为对本发明的限制。
实施例1聚对苯二甲酸乙二酯(PET)/单硬脂酸甘油酯(GMS)体内植入材料的制备
1.将2g PET溶于7g二氯甲烷和7g三氟乙酸的混合溶剂,搅拌得到均匀的高分子溶液,然后将0.5g GMS加入到PET、二氯甲烷和三氟乙酸的高分子溶液中,搅拌至均匀,得到PET/GMS混合溶液;
2.取4ml步骤1所得PET/GMS混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压10kV,采用平板收丝装置收集,平板与-1kV负压相连,喷丝头与收集器间的距离为10cm,控制环境温度为20℃,环境湿度为35%,纺丝得到PET/GMS超细纤维。
3.将步骤2中收集到的PET/GMS超细纤维,造形为0.3cm*5cm*7cm薄片,干燥后室温下,空气气氛密封保存,即得到PET/GMS体内植入材料。图1是PET/GMS体内植入材料贴附于脑部皮肤的T2平扫MRI图像,可以见到眼部上方的高亮区即为PET/GMS可核磁显像材料;PET/GMS体内植入材料的实物如图2所示,可以看到,其为白色片状纤维膜,并可被塑形成其他形状。
实施例2聚对苯二甲酸乙二酯(PET)/丙三醇(GLY)体内植入材料的制备
1.将2g PET溶于7g二氯甲烷和7g三氟乙酸的混合溶剂,搅拌得到均匀的高分子溶液,然后将0.5g GLY加入PET、二氯甲烷和三氟乙酸的高分子溶液中,搅拌至均匀,得到PET/GLY混合溶液;
2.取4ml步骤1所得PET/GLY混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压12kV,采用平板收丝装置收集,平板与-5kV负压相连,喷丝头与收集器间的距离为10cm,控制环境温度为25℃,环境湿度为40%,纺丝得到PET/GLY超细纤维。
3.将步骤2中收集到的PET/GLY超细纤维,造形为10cm*3cm*5cm的长方体,干燥后室温下,空气气氛密封保存,即得到PET/GLY体内植入材料。图3为PET/GLY材料贴附于脑部皮肤的T2平扫MRI图像,可以见到眼部上方的高亮区即为PET/GLY可核磁显像材料。与图1对比可以看出T2平扫下,PET/GMS可核磁显像材料表现为比人体组织亮的高信号,PET/GLY核磁显像材料表现为比人体组织暗的低信号。
实施例3聚对苯二甲酸乙二酯(PET)/单硬脂酸甘油酯(GMS)/超顺磁性纳米氧化铁(SPIO)体内植入材料的制备
1.将2g PET溶于7g二氯甲烷和7g三氟乙酸的混合溶剂,搅拌得到均匀的高分子溶液,然后将0.3g GMS与0.002g SPIO加入到PET、二氯甲烷和三氟乙酸的高分子溶液中,搅拌至均匀,得到PET/GMS/SPIO混合溶液。
2.取4ml步骤1所得PET/GMS/SPIO混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压15kV,采用平板收丝装置收集,平板与大地相连,喷丝头与收集器间的距离为30cm,控制环境温度为30℃,环境湿度为60%,纺丝得到PET/GMS/SPIO超细纤维。
3.将步骤2中收集到的PET/GMS/SPIO超细纤维,造形为单层膜,干燥后室温下,空气气氛密封保存,即得到PET/GMS/SPIO体内植入材料。图4是PET/GMS/SPIO体内植入材料的扫描电镜照片,从图4中可见PET/GMS/SPIO纤维呈圆柱状、平均直径为300纳米左右。
实施例4聚对苯二甲酸乙二酯(PET)/三硬脂酸甘油酯(GTS)/氧化钆(Gd2O3)体内植入材料的制备
1.将20g PET溶于70g二氯甲烷和14g三氟乙酸的混合溶剂,搅拌得到均匀的高分子溶液,然后将2g GTS与0.003g Gd2O3加入PET、二氯甲烷和三氟乙酸的高分子溶液中,搅拌至均匀,得到PET/GTS/Gd2O3的混合溶液。
2.取4ml步骤1所得PET/GTS/Gd2O3混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压18kV,采用滚筒收丝装置收集,滚筒直径30cm,转速60r/min,滚筒与-1kV负压相连,喷丝头与收集器间的距离为25cm,控制环境温度为35℃,环境湿度为80%,纺丝得到PET/TMS/Gd2O3超细纤维。
3.将步骤2中收集到的PET/GTS/Gd2O3超细纤维,造形为单层膜,干燥后室温下,空气气氛密封保存,即得到PET/GTS/Gd2O3体内植入材料。
实施例5聚丙烯(PP)/双硬脂酸甘油酯(GDS)/氧化钆(Gd2O3)体内植入材料的制备
1.将1.5g PP溶于7.0g N,N-二甲基甲酰胺(DMF),搅拌得到均匀的高分子溶液,然后将0.2g GDS与0.001g的Gd2O3加入PP和DMF的高分子溶液中,搅拌至均匀,得到PP/GDS/Gd2O3混合溶液;
2.取4ml步骤1所得PP/GDS/Gd2O3混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压25kV,采用滚筒收丝装置收集,滚筒直径10cm,转速1500r/min,滚筒与-15kV负压相连,喷丝头与收集器间的距离为35cm,控制环境温度为40℃,环境湿度为93%,纺丝得到PP/GDS/Gd2O3超细纤维。
3.将步骤2中收集到的PP/GDS/Gd2O3超细纤维,造形为单层膜,干燥后室温下,空气气氛密封保存,即得到PP/GDS/Gd2O3体内植入材料。
实施例6聚丙烯(PP)/氯化铕(EuCl3)体内植入材料的制备
1.将24g PP溶于56g N,N-二甲基甲酰胺(DMF),搅拌得到均匀的高分子溶液,然后将0.005g EuCl3加入PP和DMF的高分子溶液中,搅拌至均匀,得到PP/EuCl3混合溶液。
2.取4ml步骤1所得PP/EuCl3混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压30kV,采用滚筒收丝装置收集,滚筒直径20cm,转速2000r/min,滚筒与-25kV负压相连,喷丝头与收集器间的距离为50cm,控制环境温度为25℃,环境湿度为70%,纺丝得到PP/EuCl3超细纤维。
3.将步骤2中收集到的PP/EuCl3超细纤维,造形为底面半径2cm,高5cm的圆柱体,干燥后室温下,空气气氛密封保存,即得到PP/EuCl3体内植入材料。
实施例7聚甲基丙烯酸甲酯(PMMA)/四氧化三锰(Mn3O4)体内植入材料的制备
1.将1g PMMA溶于9g N,N-二甲基甲酰胺(DMF),搅拌得到均匀的高分子溶液,然后将0.001g Mn3O4加入PMMA和DMF的高分子溶液中,搅拌至均匀,得到PMMA/Mn3O4混合溶液。
2.取4ml步骤1所得PMMA/Mn3O4混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压9kV,采用滚筒收丝装置收集,滚筒直径5cm,转速3000r/min,滚筒与-15kV负压相连,喷丝头与收集器间的距离为45cm,控制环境温度为25℃,环境湿度为65%,纺丝得到PMMA/Mn3O4超细纤维。
3.将步骤2中收集到的PMMA/Mn3O4超细纤维,造形为底面半径2cm,高5cm的圆柱体,干燥后室温下,空气气氛密封保存,即得到PMMA/Mn3O4体内植入材料。
实施例8聚甲基丙烯酸甲酯(PMMA)/氯化镝(DyCl3)体内植入材料的制备
1.将10g PMMA溶于120g N,N-二甲基甲酰胺(DMF),搅拌得到均匀的高分子溶液,然后将0.001g DyCl3加入到PMMA和DMF的高分子溶液中,搅拌至均匀,得到PMMA/DyCl3混合溶液。
2.取4ml步骤1所得PMMA/DyCl3混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压13kV,采用平板收丝装置收集,平板与-30kV负压相连,喷丝头与收集器间的距离为45cm,控制环境温度为35℃,环境湿度为30%,纺丝得到PMMA/DyCl3超细纤维。
3.将步骤2中收集到的PMMA/DyCl3超细纤维,造形为10cm*3cm*5cm的长方体,干燥后室温下,空气气氛密封保存,即得到PMMA/DyCl3体内植入材料。
实施例9醋酸纤维素(CA)/聚乙二醇(PEG)/超顺磁性纳米氧化铁(SPIO)体内植入材料的制备
1.将12g CA溶于50g N,N-二甲基乙酰胺(DMAc)和100g丙酮的混合溶剂,搅拌得到均匀的高分子溶液,然后将18g PEG与0.001g SPIO加入到CA、DMAc和丙酮的高分子溶液中,搅拌至均匀,得到CA/PEG/SPIO混合溶液;
2.取4ml步骤1所得CA/PEG/SPIO混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压25kV,采用平板收丝装置收集,平板与-7kV负压相连,喷丝头与收集器间的距离为40cm,控制环境温度为25℃,环境湿度为60%,纺丝得到CA//PEG/SPIO超细纤维。
3.将步骤2中收集到的CA/PEG/SPIO超细纤维,造形为单层膜,干燥后常温下,空气气氛密封保存,即得CA/PEG/SPIO体内植入材料。
实施例10聚乙烯吡咯烷酮(PVP)/四氧化三锰(Mn3O4)体内植入材料的制备
1.将20g PVP溶于80g无水乙醇,搅拌得到均匀的高分子溶液,然后将0.005g Mn3O4加入到PVP和无水乙醇的高分子溶液中,搅拌至均匀,得到PVP/Mn3O4混合溶液。
2.取4ml步骤1所得PVP/Mn3O4混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压13kV,采用平板收丝装置收集,平板与-8kV负压相连,喷丝头与收集器间的距离为15cm,控制环境温度为35℃,环境湿度为45%,纺丝得到PVP/Mn3O4超细纤维。
3.将步骤2中收集到的PVP/Mn3O4超细纤维,造形为底面半径2cm,高5cm的圆柱体,干燥后室温下,空气气氛密封保存,即得到PVP/Mn3O4体内植入材料。
实施例11聚乙烯吡咯烷酮(PVP)/钆二乙基三胺五乙酸(Gd-DTPA)体内植入材料的制备
1.将3g PVP溶于10g无水乙醇,搅拌得到均匀的高分子溶液,然后将0.003g Gd-DTPA加入到PVP和无水乙醇的高分子溶液中,搅拌至均匀,得到PVP/Gd-DTPA混合溶液。
2.取4ml步骤1所得PVP/Gd-DTPA混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压15kV,采用平板收丝装置收集,平板与-6kV负压相连,喷丝头与收集器间的距离为15cm,控制环境温度为40℃,环境湿度为45%,纺丝得到PVP/Gd-DTPA超细纤维。
3.将步骤2中收集到的PVP/Gd-DTPA超细纤维,造形为底面半径1cm,高3cm的圆柱体,干燥后室温下,空气气氛密封保存,即得到PVP/Gd-DTPA体内植入材料。
实施例12醋酸纤维素(CA)/氯化钆(GdCl3)体内植入材料的制备
1.将600g CA溶于670g N,N-二甲基乙酰胺(DMAc)和1330g丙酮的混合溶剂,搅拌得到均匀的高分子溶液,然后将0.006g GdCl3加入到CA、DMAc和丙酮的高分子溶液中,搅拌至均匀,得到CA/GdCl3混合溶液;
2.取4ml步骤1所得CA/GdCl3混合溶液,装入带有喷丝头的储存容器内,设置静电纺丝装置,高压静电电压20kV,采用平板收丝装置收集,平板与-6kV负压相连,喷丝头与收集器间的距离为40cm,控制环境温度为25℃,环境湿度为60%,纺丝得到CA/GdCl3超细纤维。
3.将步骤2中收集到的CA/GdCl3超细纤维,造形为单层膜,干燥后室温下,空气气氛密封保存,即得CA/GdCl3体内植入材料。
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合和简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
-
 0访客 来自[中国] 2023年09月29日 16:05该材料是如何植入人体的?
0访客 来自[中国] 2023年09月29日 16:05该材料是如何植入人体的?