用夹竹桃属物种或黄花夹竹桃属物种的提取物治疗神经病症的方法与流程
本申请是申请日为2011年11月3日的第201180065127.6号发明名称为“用夹竹桃属物种或黄花夹竹桃属物种的提取物治疗神经病症的方法”的中国专利申请的分案申请。本发明涉及用夹竹桃属(nerium)物种或黄花夹竹桃属(thevetia)物种的提取物、或含有它们的制剂(组合物、配方)治疗神经病症的方法。本发明特别涉及通过将提取物施用给需要其的对象,用于治疗神经疾病或障碍的方法。本发明还包括含有所述提取物组分或亚组分的药物组合物以及它们的使用和制备方法。
背景技术:
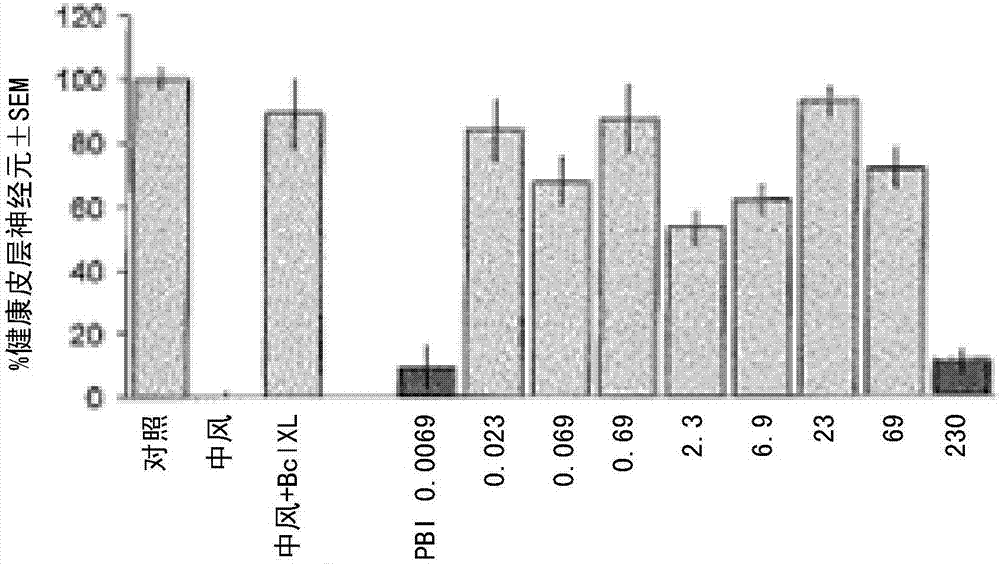
:神经疾病和障碍影响脑部功能。已针对这些疾病和障碍尝试开展了治愈治疗或改善治疗;然而,尽管已证明有许多药物治疗方法对于许多不同疾病和障碍是有效的,还未形成广泛或普遍的治愈治疗。亨廷顿舞蹈症(hd)是一种影响神经系统的脑部遗传疾病。它是由从父母传给孩子的缺陷基因引起的。hd基因干扰称为“亨廷顿(huntington)”的特定蛋白的制造,所述蛋白对于适宜的脑部发育似乎是关键的。hd的典型迹象包括情感、认知和运动障碍。亨廷顿舞蹈症的特征是急速不自主运动(舞蹈症),但有时引起无异常运动下的僵直,在使用四肢方面的改变(失用症),身体机能控制的丧失和痴呆,包括记忆力、思考速度、判断的进行性退化以及问题意识和计划意识的缺乏。不存在亨廷顿舞蹈症的已知治愈。尽管许多药物有助于控制hd有关的症状,例如情感和运动问题,没有治疗来停止或逆转该疾病的进程。亨廷顿舞蹈症已被公认为是具有普遍膜异常的疾病。已观察到,与从亨廷顿舞蹈症患者的皮肤获得的正常(butterfieldda,oesweinjq,pruntyme,hislekc,markesberywr.,increasedsodiumpotassiumadenosinetriphosphataseactivityinerythrocytemembraneinhuntington'sdisease,annneurology,4:60-62,1978)成纤维细胞膜相比,在亨廷顿舞蹈症患者的红细胞和基底神经节的膜中的na,k-atp酶显著升高的水平和活性(10倍的提高)(schroederf,goetzie,robertse,membraneanomaliesinhuntington'sdiseasefibroblasts.j.neurochem.43:526-539,1984)。阿尔茨海默病是一种形式的痴呆—损害脑部智力功能(记忆、方位、计算等)但通常保留其运动功能的一种神经退行性疾病。在阿尔茨海默病中,智力逐渐退化,引起记忆力丧失、混乱、定向障碍、受损的判断和可影响个人行使正常日常活动的其他问题。精神变化的类型、严重程度、顺序和进程有很大不同。没有阿尔兹海默病已知的治愈,也没有已知的方法减缓其进程。对于疾病早期或中期的某些人,例如他克林的药物可缓解某些认知症状。安理申(多奈哌齐)和艾斯能(卡巴拉汀)是指定用于治疗轻微至中度痴呆阿尔兹海默病类型的可逆乙酰胆碱酯酶抑制剂。这些药物(称为胆碱酯酶抑制剂)通过提高神经递质乙酰胆碱的脑部水平起作用,帮助恢复脑细胞之间的联系。某些药物可帮助控制例如失眠、躁动、徘徊、焦虑和抑郁的行为症状。这些治疗的目标在于使患者更加舒适。尽管没有药物已知治愈阿尔兹海默病,胆碱酯酶抑制剂可改善日常活动的表现,或减轻行为问题。目前测试的用于治疗阿尔兹海默病的药物包括雌激素、非类固醇抗炎剂、维生素e、司来吉兰(carbex、咪多吡)和植物药产品银杏。欧洲夹竹桃(neriumoleander)是广泛分布在亚洲亚热带、美国西南部和地中海的观赏性植物。其医药和毒理学性质已得到长久公认。其已用于例如治疗痔疮、溃疡、麻风病、毒蛇咬伤、以及甚至是诱导流产。夹竹桃苷(oleandrin),夹竹桃提取物的一种重要成分但非唯一成分,是一种强心苷。从夹竹桃属植物提取苷类已提供来自欧洲夹竹桃的药理学/治疗学活性成分。其中有夹竹桃苷、黄夹次苷乙(黄花夹竹桃次苷b(nerifolin))和其他强心苷化合物。由欧洲夹竹桃热水提取获得的夹竹桃苷提取物(以商标anvirzeltm出售)含有浓缩形式或粉末形式的欧洲夹竹桃热水提取物。已完成热水夹竹桃提取物(即anvirzeltm)的i期试验(mekhailetal.,am.soc.clin.oncol.,vol.20,p.82b,2001)。推测可提供约57ug夹竹桃苷/天的夹竹桃提取物,可以高达1.2ml/m2/d的剂量安全施用。没有发现剂量相关毒性。技术实现要素:本发明提供一种治疗神经病症的方法,包括向需要其的对象施用有效量的含有夹竹桃属物种或黄花夹竹桃属物种的提取物的组合物,以治疗所述神经病症。本发明提供实施方式,其中使用提取物的组分或提取物组分的亚组分代替未分级提取物,并且其中所述提取物的组分或亚组分不包含夹竹桃苷和黄夹次苷乙。一方面,本发明提供一种用包含夹竹桃属物种或黄花夹竹桃属物种的提取物的组合物在需要其的对象中治疗神经疾病或障碍的方法,所述方法包括:确定对象患有神经疾病和障碍;以及指示向对象施用包含夹竹桃属物种或黄花夹竹桃属物种的提取物的组合物。本发明某些实施方式包括以下那些,其中1)为对象开具并施用治疗相关剂量的组合物;2)使对象按处方给药方案服用组合物;3)提取物包含从夹竹桃属物种或黄花夹竹桃属物种提取的一或多种治疗有效剂;4)组合物进一步包含一或多种其他治疗有效剂;5)通过使用热水、冷水、超临界流体、有机溶剂或其组合提取夹竹桃属物种或黄花夹竹桃属物种获得提取物;6)提取物不包含强心苷;7)提取物不包含治疗有效量的强心苷;8)提取物不包含夹竹桃苷;9)组合物包含夹竹桃属物种或黄花夹竹桃属物种的提取物的组分;10)组合物包含夹竹桃属物种或黄花夹竹桃属物种的提取物的组分,其中所述组分已由提取物的液相色谱分级制备;11)夹竹桃属物种是欧洲夹竹桃,黄花夹竹桃属物种是黄花夹竹桃(thevetianeriifolia);12)提取物不包含黄夹次苷乙;13)组合物包含夹竹桃属物种或黄花夹竹桃属物种的提取物组分的亚组分,其中所述亚组分已由提取物组分的液相色谱分级制备,并且所述亚组分不包含夹竹桃苷和黄夹次苷乙;14)夹竹桃属物种或黄花夹竹桃属物种的提取物,如果其含有强心苷,当以一剂型施用给患有神经疾病或障碍的对象时,与以其他方式类似的剂型以相同剂量的强心苷施用给对象的纯强心苷相比,提供改善的临床反应或临床效果;或15)它们的组合。本发明还提供一种在需要其的对象中治疗神经病症的方法,所述方法包括:确定对象的神经病症是否是阿尔茨海默病、亨廷顿舞蹈症、中风或其他神经病症;指示施用夹竹桃属物种或黄花夹竹桃属物种的提取物;根据处方的初始给药方案向对象施用初始剂量的提取物一段时间;定期测定对象对用提取物治疗的临床反应和/或治疗反应的适当性;以及如果对象的临床反应和/或治疗反应适当,根据需要用提取物继续治疗,直至达到期望的临床终点;或如果对象的临床反应和/或治疗反应在初始剂量和初始给药方案下不适当,那么逐步提高或逐步减少剂量,直至达到对象中期望的临床反应和/或治疗反应。本发明还提供在处于神经病症风险的对象群体中预防或降低神经病症发生率的方法,所述方法包括:在经常性的基础上,以延长时间段向对象群体中的一或多个对象施用有效剂量的夹竹桃属物种或黄花夹竹桃属物种的提取物,所述对象群体处于患神经病症的风险,所述神经病症例如阿尔茨海默病、亨廷顿舞蹈症、中风或其他神经病症,从而预防或降低群体中的神经病症发病率。本发明包括实施方式,其中:a)所述方法进一步包括指示施用提取物至一或多个对象;b)所述方法进一步包括根据处方给药方案向对象施用有效剂量的提取物一段时间;c)所述方法进一步包括定期测定一或多个对象对用提取物治疗的临床反应和/或治疗反应的适当性;d)如果对象的临床反应和/或治疗反应是适当的,那么所述方法进一步包括根据需要用提取物继续治疗,直至达到期望的临床终点;e)如果对象的临床反应和/或治疗反应在初始剂量和初始给药方案下不适当,那么所述方法进一步包括逐步提高或逐步减少剂量,直至达到对象中期望的临床反应和/或治疗反应;f)将提取物施用给群体中的多个对象;g)经常性的基础是每天、每隔一天、每两天、每三天、每四天、每五天、每六天、每周、每隔一周、每两周、每三周、每月、每双月、每半月、每隔一月、每两个月、每季、每隔一季、每三个月、每季节(seasonally)、每半年和/或每年;h)延长时期是一或多个周、一或多个月、一或多个季度和/或一或多年;i)一天内,一或多次施用有效剂量;j)所述方法进一步包括鉴别处于患神经病症风险的对象群体,所述神经病症例如阿尔茨海默病、亨廷顿舞蹈症、中风或其他神经病症;k)处于风险的对象群体的特征是对象增大的年龄、神经病症的家族史、发生神经病症的遗传易感性、对象中apoe4基因的存在和表达、女性(女性患阿尔茨海默病是男性的两倍)、心血管疾病(例如高血压和高胆固醇水平)、糖尿病(尤其是2型或成人发病型糖尿病)、唐氏综合征、头部伤害、低水平的正规教育、吸烟、过量饮酒和/或药物滥用;l)提取物不包含治疗有效量的强心苷;m)提取物不包含强心苷;或n)它们的组合。本发明还提供治疗对象中风的延时(time-delayed)方法,包括:在对象已患中风后的延迟时期,根据初始给药方案施用初始剂量的夹竹桃属物种或黄花夹竹桃属物种的提取物;测定对象对用提取物治疗的临床反应和/或治疗反应的适当性;以及如果对象的临床反应和/或治疗反应是适当的,那么根据需要用提取物继续治疗,直至达到期望的临床终点;或者如果对象的临床反应和/或治疗反应在初始剂量和初始给药方案下不适当,那么逐步提高或逐步减少剂量,直至达到对象中期望的临床反应和/或治疗反应。本发明某些实施方案包括以下那些,其中:1)延迟时期是10小时或更短、8小时或更短、6小时或更短、4小时或更短、3小时或更短、2小时或更短、1小时或更短、45分钟或更短、30分钟或更短、20分钟或更短或10分钟或更短;2)通过评估身体一侧脸部、胳膊和/或腿的任何衰弱、身体一侧脸部、胳膊和/或腿的麻痹、不能理解口头语言、不能说话或清楚说话、不能写、眩晕和/或步态不平衡、复视和异常严重的头痛,已完成测定对象临床和/或治疗反应的适当性;或3)它们的组合。本发明还提供夹竹桃属物种或黄花夹竹桃属物种的提取物在制备用于治疗对象神经病症的药物中的用途。在某些实施方式中,此药物的制备包括:提供夹竹桃属物种或黄花夹竹桃属物种的提取物;将夹竹桃属物种或黄花夹竹桃属物种的提取物或其组分的剂量包括在药物剂型中;以及包装该药物剂型。本发明还提供包含夹竹桃属物种或黄花夹竹桃属物种的提取物用于治疗对象神经病症的药物组合物。在某些实施方式中,可如2006年7月26日提交的pct国际申请pct/us06/29061、2005年7月28日提交的us7,402,325和2008年1月24日提交的美国专利申请12/019,435中所描述的进行所述制备,所述专利或专利申请的全部公开内容通过引用结合至本文。所述制备还可包括一或多个额外步骤例如:将包装的剂型递送给供应商(零售商、批发商和/或经销商);将包装的剂型卖给或以其他方式提供给患有神经病症的对象;在药物内包括标签和包装说明书,其提供关于剂型的使用、给药方案、施用、含量和毒性学性质的说明。在某些实施方案中,神经病症的治疗包括:确定对象患有神经病症或障碍;指示根据给药方案向对象施用提取物或其组分;向对象施用含有提取物的一或多个药物剂型,其中所述一或多个药物剂型是根据给药方案施用的。本发明还提供夹竹桃属物种或黄花夹竹桃属物种的提取物或组合物,即包含夹竹桃属物种或黄花夹竹桃属物种的提取物的药物配方或剂型,用于治疗神经病症。在某些实施方式中,提取物可如在本文或美国专利7,402,325、pct国际专利申请pct/us06/29061、美国专利申请12/019435或newman等(mol.interven.(2008),8,36-49)中所述,获自夹竹桃属物种或黄花夹竹桃属物种,所述专利或专利申请的全部公开内容通过引用结合至本文。本发明提供用于制备夹竹桃属物种或黄花夹竹桃属物种的提取物组分的方法,包括:提取包含夹竹桃属物种或黄花夹竹桃属物种的物质以形成它们的未分级提取物,所述提取物包含用于治疗神经病症的一或多种药理学活性成分;以及将未分级提取物进行分级以形成它们的两种或更多种组分,其中至少一种组分包含一或多种非强心苷的药理学活性成分。在某些实施方案中,a)至少一种组分不包含强心苷;b)至少一种组分至少包含强心苷;c)用超临界液体、水、有机溶剂或它们的组合进行提取;d)用液相色谱或溶剂提取进行分级;e)所述至少一种组分不包含夹竹桃苷和黄夹次苷乙;或f)它们的组合。本发明还提供分级夹竹桃属物种或黄花夹竹桃属物种的提取物,以提供其一或多种治疗有效组分的方法。所述方法包括:a)提供夹竹桃属物种或黄花夹竹桃属物种的提取物;b)分级提取物以提供提取物的两种或更多种组分,包含一或多种药理学活性剂(其不是强心苷)且不包含强心苷(夹竹桃苷和黄夹次苷乙)的第一提取物组分,和包含一或多种强心苷和一或多种药理学活性剂(其不是强心苷)的第二提取物组分。还可如在本文中所述完成分级。在某些实施方案中,对第一提取物组分和第二提取物组分进行进一步分级以提供两种或更多种不同的亚组分,其中第一亚组分包含一或多种类固醇,第二亚组分包含一或多种三萜烯(triterpene)。在某些实施方案中,通过具有固定相和流动相的液相色谱完成分级。本发明还提供包含获自夹竹桃属物种或黄花夹竹桃属物种的提取物组分的组合物,由此所述组分已通过分级获自夹竹桃属物种或黄花夹竹桃属物种的提取物获得。在某些实施方式中,提取物组分包含一或多种类固醇和一或多种三萜烯,并任选地不包含强心苷(夹竹桃苷和黄夹次苷乙)。本发明还提供包含获自夹竹桃属物种或黄花夹竹桃属物种的提取物组分的亚组分的组合物,由此所述亚组分已通过进一步分级获自夹竹桃属物种或黄花夹竹桃属物种的提取物组分获得。在某些实施方式中,提取物组分的亚组分包含一或多种类固醇、强心苷、强心苷的相关苷元,例如夹竹桃苷元、强心甾、或三萜类化合物(triterpenoid)、和一或多种三萜烯。在某些实施方式中,提取物组分的亚组分包含一或多种三萜烯,并不包含类固醇。每个亚组分独立地任选地不包含强心苷(夹竹桃苷和黄夹次苷乙)。在某些实施方式中:a)提取物进一步包含获自(提取自)夹竹桃属物种或黄花夹竹桃属物种的至少两种药理学活性剂;b)当向对象施用提取物时,该至少两种药理学活性剂叠加性地或协同性地促进提取物的治疗功效;c)该至少两种药理学活性剂都不是强心苷;和/或d)至少两种药理学活性剂选自强心苷、强心苷的相关苷元,例如夹竹桃苷元、强心甾、三萜类化合物的组。在某些实施方式中:1)强心苷选自由夹竹桃苷、奥多诺苷(odoroside)、夹竹桃它罗苷、g毒毛旋花苷、蟾毒灵(bufalin)、洋地黄毒苷(digitoxin)、华蟾毒它灵(cinobufatalin)、华蟾酥毒基(cinobufagin)和酯蟾毒配基(resibufogenin)组成的组;2)提取物存在于药物配方或组合物中;3)提取物已从夹竹桃(oleander)植物物质或neriifolia植物物质获得;4)该植物物质包括夹竹桃属物种,例如欧洲夹竹桃;或黄花夹竹桃属物种,例如黄花夹竹桃(thevetianeriifolia)或thevetiaperuviana(另称为黄夹竹桃);5)任选地在修饰剂存在的情况下,由超临界流体(scf)提取制备提取物;6)强心苷是夹竹桃苷;7)提取物是由热水提取、冷水提取、有机溶剂提取或水性有机溶剂提取制备的。在某些实施方案中,提取物(或其组分或亚组分)包含少于1重量%、少于0.5重量%、少于0.1重量%、少于0.05重量%或少于0.01重量%的多糖。在某些实施方式中,提取物(或其组分或亚组分)包含白桦脂醇(乌索-12-烯-3β,28-二醇(urs-12-ene-3β,28-diol));28-去甲乌索-12-烯-3β-醇;乌索-12-烯-3β-醇;3β,3β-羟基-12-齐墩果烯-28-酸;3β,20α-二羟基乌索-21-烯-38-酸(3β,20α-dihydroxyurs-21-en-38-oicacid);3β,27-二羟基-12-乌索烯-38-酸(3β,27-dihydroxy-12-ursen-38-oicacid);3β,13β-二羟基乌索-11-烯-28-酸;3β,12α-二羟基齐墩果烷-28,13β-内酯和3β,27-二羟基-12-齐墩果-28-酸(3β,27-dihydroxy-12-oleanan-28-oicacid)。在某些实施方案中,提取物(或其组分或亚组分)包含选自强心苷的糖基成分的一或多种强心苷前体。在某些实施方案中,糖基选自由葡萄糖苷、果糖苷和葡萄糖苷酸组成的组。在某些实施方案中,提取物(或其组分或亚组分)包含夹竹桃苷元、乌索酸、白桦脂酸、奥多诺苷、夹竹桃它罗苷、齐墩果酸和一或多种三萜烯以及少于0.5%重量的多糖。在某些实施方案中,患有神经病症的对象,即需要其的对象,是这种对象群体的一部分。本发明提供了用于改善患有神经病症的对象群体中统计学显著数目的对象的临床状态,所述方法包括:向对象群体施用夹竹桃属物种或黄花夹竹桃属物种的提取物,或包含夹竹桃属物种或黄花夹竹桃属物种的提取物的组合物;以及确定对象的临床状态。在某些实施方案中,统计学显著数目是群体的至少5%。在某些实施方式中,神经病症是阿尔茨海默病、亨廷顿舞蹈症、中风、滔蛋白病变或其他神经病症,例如本文所描述的。可通过将提取物包含在含有一或多种药学可接受赋形剂的药物剂型中制备药物。根据需要用提取物或含有提取物的组合物的对象继续治疗。可如所需要调整剂量或给药方案,直至患者达到期望的临床终点例如与疾病相关的特定神经学症状的降低或减轻。临床反应和/或治疗反应的适当性的测定可由熟悉被治疗的神经病症的临床医生进行。在某些实施方式中,神经病症选自由神经疾病、神经障碍、滔蛋白病变和中风组成的组。在某些实施方式中,神经疾病是神经退行性疾病。在某些实施方式中,神经退行性疾病选自由亨廷顿舞蹈症、阿尔茨海默病、帕金森氏病、肌萎缩性脊髓侧索硬化症、牛海绵状脑病、多发性硬化、糖尿病神经病变、自闭症和青少年型神经元蜡样脂褐质沉积病组成的组。在某些实施方式中,中风是中风引起的缺血性损伤。在某些实施方式中,神经病症是滔蛋白病变,其是具有与对象中tau3r/tau4r比率失衡有关的病因学的神经退行性疾病。滔蛋白病变是由人脑中滔蛋白(tau)的病理性聚集引起的一类神经退行性疾病。在某些实施方式中,滔蛋白病变是唐氏综合症、皮克氏病、基底节变性、朊病毒病的某些变体、阿尔茨海默病、进行性核上性麻痹或额颞痴呆。本发明方法的单个步骤可以单独的设施或在相同设施内进行。在某些实施方式中,神经元是体外的、离体的或体内的。在某些实施方式中,神经元是ca-1神经元。在某些实施方式中,本发明提供夹竹桃属物种或neriifolia属物种的提取物、或其组分、或其亚组分,它们具有本文所描述的1hnmr谱。在某些实施方式中,本发明提供夹竹桃属物种或neriifolia属物种的提取物、或其组分、或其亚组分,当施用给对象时,显示本文所描述的治疗活性。在某些实施方式中,本发明提供夹竹桃属物种或neriifolia属物种的提取物、或其组分、或其亚组分,它们具有本文所描述的hplc色谱图。在某些实施方式中,本发明方法采用如本文所述的提取物、其组分或其亚组分。在某些实施方式中,本发明组合物包含如本文所述的提取物、其组分或其亚组分。本发明包括本文所述的本发明方面、实施方式和亚实施方式的所有组合。除非本文另外指明,术语“提取物”可指未分级提取物或分级提取物(即提取物的组分)或亚分级提取物(即提取物的组分的亚组分)。附图说明以下附图构成本说明书的一部分,并描述了要求保护的发明的示例性实施方式。本领域技术人员根据本文的这些图和说明书,将能够在不进行过度实验情况下,实施本发明。图1a描绘在神经保护基于脑部切片的“中风”试验中(实施例8),从夹竹桃苷相比于无氧或葡萄糖剥夺(ogd)、对照的比较性评估获得的浓度-响应数据,其中在存在或不存在夹竹桃苷的条件下,在氧气和葡萄糖剥夺(ogd=中风)后5-6分钟测定了健康皮层神经元的数目。图1b描绘在如本文所述的神经保护基于脑部切片的“中风”试验中(实施例8),针对欧洲夹竹桃未分级scf提取物的浓度-响应试验的结果,其中使用无氧或葡萄糖剥夺作为对照。图2a-2c描绘在神经保护基于脑部切片的“阿尔茨海默”试验中(实施例9),夹竹桃苷相比于欧洲夹竹桃未分级scf提取物的比较性评估的结果,其中在不存在或存在不同量的那些制剂的条件下,在app/aβ诱导的退化之后测定了健康皮层神经元的数目。图3a-3d描绘在神经保护基于皮质纹状体共培养神经元的“亨廷顿舞蹈症”试验中(实施例10),来自比较性评估夹竹桃苷(图3a-3b)(图3c-3d)的重复试验的结果,其中在不存在或存在不同量的夹竹桃苷的条件下,测定了相对于对照的,皮层神经元相比于转染了突变形式的亨廷顿(htt)蛋白的纹状体神经元的挽救百分比。图4a-4e描绘如本文所述的神经保护基于脑部切片的“中风”试验的结果,其中含有夹竹桃苷的scf提取物已通过液相色谱分级(实施例13),并且五个不同组分(以下说明)进行了该实验(实施例15):组分o-h(图4a)、组分o-2(图4b)、组分o-3(图4c)、组分o-4(图4d)、组分o-5(图4e)。图5描绘对于欧洲夹竹桃scf提取物的组分o-4相比于总(parent)未分级欧洲夹竹桃scf提取物(pbi或pbi-05204),浓度-响应基于脑部切片的“中风”试验(实施例15)的结果。图6描绘在基于app的“阿尔茨海默”试验中(实施例11),欧洲夹竹桃scf提取物的组分(o-4或o-4a)相比于未处理(细胞未转染app/aβ)的比较性评估的结果,其中在不存在或存在不同量的那些制剂的条件下,在app/aβ诱导的退化之后测定了健康皮层神经元的数目。图7描绘在基于tau4r的“阿尔茨海默”试验中(实施例12),欧洲夹竹桃scf提取物的组分(o-4)相比于未处理(细胞未转染app/aβ)的比较性评估的结果,其中在不存在或存在不同量的那些制剂的条件下,在tau4r之后测定了健康和受损皮层神经元的数目。图8a-8d描绘通过根据实施例13制备的组分的hplc分析获得的色谱图。图9a-9i描绘针对组分o-4欧洲夹竹桃scf提取物中存在的多种成分的hnmr谱。图9a描绘在根据实施例17亚分级之前,o-4组分的hnmr谱。图9b-9i描绘根据实施例17对o-4组分进行硅胶快速色谱获得的多种亚组分的hnmr谱。具体实施方式本发明提供一种通过施用有效剂量的夹竹桃属物种或黄花夹竹桃属物种的提取物给需要其的对象治疗神经病症的方法。根据最适合对象的给药方案施用所述提取物,根据针对需要治疗的神经病症的传统临床实践和临床治疗终点,临床确定剂量和给药方案的适合性。在某些实施方式中,治疗的神经退行性疾病或神经病症具有与对象中tau蛋白过量表达和/或tau3r/tau4r比率失衡相关的病因学。这种病症叫做滔蛋白病变。示例性滔蛋白病变包括唐氏综合症、皮克氏病、朊病毒病的某些变体、阿尔茨海默病、进行性核上性麻痹或额颞痴呆、基底节变性、关岛震颤麻痹痴呆综合症、嗜银颗粒性痴呆、c型尼曼匹克病和运动性痴呆(dementiapugilistic)。在某些实施方式中,治疗的神经退行性疾病或神经病症具有与以下相关的病因学:β-淀粉样前体蛋白的异常或非典型蛋白水解、神经元突触中β-淀粉样蛋白的积累、神经元突触中淀粉样纤维的形成、或神经元突触中淀粉样斑块的形成。这种疾病或病症的实例是阿尔茨海默病。根据本发明治疗的对象会表现出治疗反应。“治疗反应”意思是患有疾病或病症的对象会由于用提取物治疗而享有至少一种下列临床益处:改善疾病或病症、降低与疾病或病症有关的症状的发生、部分缓解疾病或病症、完全缓解疾病或病症、或发展时间延长。换言之,治疗反应可以是完全的或部分的治疗反应。治疗反应还可说明为被神经退行性疾病所累的患者生活治疗改善的治疗反应。生活质量改善可以通过例如与疾病(例如震颤、不自主肌肉运动、丧失或部分丧失神经-肌肉协调、记忆保持等)有关症状的发生、频率或严重性降低发生。“在风险对象群体中防止神经病症的发生”意思是在具有患神经病症风险的人口统计预确定群体中,在预确定时间段内,神经病症不会发生。在预确定时间段内的防止是由于所述群体中的对象已服用根据本发明的提取物。作为实例,当以预确定时间段向具有患中风风险的对象群体中的对象施用提取物或含有提取物的组合物时,在该预确定时间段内在那些对象中不会发生中风。特别是,含有提取物的组合物在一年的时间内长期施用给具有患阿尔茨海默病或任何一种滔蛋白病变(tauopathology)相关疾病的对象群体,且所述群体中的对象在该一年时间内不表现与阿尔茨海默病相关的症状。“在风险对象群体中降低神经病症的发生率”在含义上与“防止发生”相关,除了“降低发生率”允许在人口统计预确定对象群体中神经病症的发生,但是与不服用根据本发明的含有提取物的组合物的、另外的类似人口统计预确定的风险对象群体相比,处于降低的发生率或严重水平。如本文所用,“发展时间”是诊断(或治疗)疾病后,到疾病开始恶化之前的时间段、时间长度或持续时间。这是保持疾病水平,没有疾病进一步发展的时间段,并且当疾病开始再次发展时,该时间段结束。通过在治疗之前或开始之时,将患有神经病症的对象“分期”来确定疾病发展。例如,在治疗之前或开始之时确定对象的神经健康状况。之后用提取物治疗对象,并且定期监测神经健康状况。在某些随后时间点,神经病症的症状可能恶化,由此标志疾病发展以及“发展时间”的结束。期间疾病没有发展或者期间疾病水平或严重程度没有恶化的时间段是“发展时间”。给药方案包括根据给药计划施用的提取物的治疗相关剂量(或有效剂量)。因此治疗相关剂量是观察到针对提取物治疗的疾病或病症的治疗反应的治疗剂量,并且是对象可以在没有过量不期望或有害副作用的情况下服用提取物的治疗剂量。治疗相关剂量对于对象是不致死的,尽管它可能在患者中引起某些副作用。它是对于服用提取物的对象来说,临床益处的水平超过对象由于服用提取物所经历的有害副作用水平的剂量。根据多种已知药理学、药效动力学和药代动力学原理,治疗相关剂量在对象之间不同。然而,治疗相关剂量一般是在0.1至100微克提取物/天的范围内,该提取物是固体、液体或半固体形式。本领域已知在对象中提供目标治疗结果的药理学活性剂的实际量会根据药学基本原理在对象之间不同。根据在神经疾病或失调或神经退行性疾病或失调治疗中通常使用的任何给药方案,可施用治疗相关剂量。可一次、两次、三次或更多次的每日给药安排来施用治疗相关剂量。可每隔一天、每三天、每四天、每五天、每半周、每周、每两周、每三周、每四周、每月、每两个月、每半月、每三个月、每四个月、每半年、每年、或根据任何上述的结合来施用,以实现适合的给药安排。例如,可每日一次施用治疗相关剂量一或多个周。以下实例包括在神经病症例如神经疾病、神经失调或中风中提取物效力的证据。实施例3详述了一种用夹竹桃属物种的提取物、或其组合物、黄花夹竹桃属物种的提取物、或其组合物、或它们的组合连同一或多种其他治疗剂治疗阿尔茨海默病的方法。实施例4详述了一种用提取物或提取物组合连同一或多种其他治疗剂治疗亨廷顿舞蹈症的方法。实施例5详述了一种用提取物或提取物组合连同一或多种其他治疗剂治疗中风引起的缺血性脑损伤或非中风引起的缺血性脑损伤的方法。总体上,以下述治疗患有神经病症的对象。评估表现有神经病症的对象,以确定该神经病症是否是阿尔茨海默病、亨廷顿舞蹈症、中风或其他神经病症。如果对象得到阳性诊断,指示施用提取物或含有提取物的组合物。根据处方给药方案向对象施用起始剂量的提取物或组合物一段时间。定期确定对象的临床反应和治疗反应的水平。如果在一剂量时治疗反应的水平太低,那么根据预确定剂量递增安排将剂量逐步提高,直到对象中达到期望的治疗反应水平。如果对象表现出不期望的副作用或不可接受水平的副作用,那么逐步降低剂量直到对象中达到治疗反应水平相比副作用特征的期望平衡。如所需要,继续用提取物或组合物治疗对象。可如所需要调整剂量或给药方案,直到患者实现期望的临床终点例如疾病本身的中止、疾病有关症状的减少、和/或疾病进程发展的下降。提取物,特别是未分级提取物,包含一或多种药理学活性化合物。某些那些化合物还未被确认,某些可以是夹竹桃苷或其他强心苷、欧夹竹桃苷(oleaside)、夹竹桃苷元、夹竹桃它罗苷、奥多诺苷(wangx,plomleyjb,newmanraandcisnerosa.lc/ms/msanalysesofanoleanderextractforcancertreatment,analyticalchem.72:3547-3552,2000)和其他植物材料。来自超临界流体工艺的未分级scf提取物一般含有重量计0.9%至2.5%理论范围的夹竹桃苷。已经获得含有不同量的夹竹桃苷的scf提取物。在一个实施方式中,scf提取物包含重量计约2%的夹竹桃苷。夹竹桃属物种或黄花夹竹桃属物种的提取物的可提取未确认的成分可包含至少一种(非强心苷)药理学活性成分,其有助于scf提取物或其组分的功效。两种或更多种药理学活性可提取成分可叠加性地或协同性地提供观察到的功效。换言之,本发明夹竹桃属物种或黄花夹竹桃属物种的提取物含有非强心苷的一或多种药理学活性成分,尽管一或多种强心苷可额外包含在提取物中。提取物可分级为多种不同组分,某些组分含有强心苷、一或多种非强心苷的药理学活性成分、或它们的组合。此外,每种提取物组分可进一步分级为两种或更多种不同的亚组分。在scf提取物存在夹竹桃苷之外的一或多种药理活性成分的证据来自将含有纯夹竹桃苷的溶液的浓度-响应曲线与含有scf提取物的相比较。图1a描绘了在如实施例8说明的神经保护基于脑部切片的“中风”试验中,对含有纯夹竹桃苷的溶液的浓度-响应试验结果。溶液中的夹竹桃苷浓度从0.0069至230μg/ml变化。图1b描绘了在如本文(实施例8)中说明的神经保护基于脑部切片的“中风”试验中,对含有夹竹桃苷scf夹竹桃属物种的提取物的浓度-响应试验的结果。数据表明提取物比纯的夹竹桃苷更有效,意味着提取物含有提供神经保护的一或多种药理学活性剂。实施例8详细说明了用来评估提取物、或其组合物用于治疗中风引起的缺血性神经损伤的功效的体外试验。所述试验是针对氧合葡萄糖剥夺(ogd)的基于脑部切片的试验,所述剥夺用来诱导24小时内健康皮层神经元的≥50%的丧失。使用夹竹桃属物种例如欧洲夹竹桃的总未分级scf提取物作为阳性对照。之后根据实施例13分级该总提取物,以提供夹竹桃属物种的提取物的组分。根据实施例6、14和17分析组分。三萜烯的hnmr的特征是高磁场(upfield)的7个甲基信号,约5.3ppm处的烯烃质子和约3.4ppm处的氧化次甲基信号,以及在高磁场(约1.0~2.5ppm)处的许多亚甲基和次甲基质子信号。该hnmr谱(图9b-9i)表明主要成分是类固醇和三萜烯。没有观察到显著量糖苷的信号。没有观察到α,β-不饱和γ-或δ-内酯的信号,它们是强心苷特征性的,表明在fr-o-4组分中不存在强心苷或它的苷元。图9c中的hnmr谱对应于含有至少一种类固醇和至少一种或至少两种不同三萜烯的亚组分。图9b中的hnmr谱对应于含有至少两种不同三萜烯例如两种乌索烷的混合物并不包含类固醇的亚组分。相应地,组分o-4含有至少一种三萜烯和至少一种类固醇。在某些实施方式中,组分o-4含有至少两种不同的三萜烯和至少两种不同的类固醇,或者该组分含有多种不同的三萜烯和多种不同的类固醇。在该实施例中评估的o-4组分不包含治疗有效量的强心苷。在某些实施方式中,组分o-4不包含强心苷。在某些实施方式中,组分o-4的第一亚组分含有至少一种类固醇和至少一种三萜烯或至少两种不同的三萜烯,第二亚组分含有至少两种不同的三萜烯,不包含类固醇。在某些实施方式中,第一和第二亚组分的每一个不包含强心苷。在ogd处理的脑切片(中风模型)和非ogd处理(即对照)的脑切片(非中风模型)中测试了组分o-4。数据表明当使用100ng/ml至1μg/ml浓度范围的提取物o-4组分的溶液时,提取物o-4组分提供了实质的神经保护,并且当使用1μg/ml至1mg/ml浓度范围的提取物o-4组分溶液时,提供了甚至更高的神经保护。因此,含有每ml液体剂型100ng/ml至1mg/ml提取物组分的液体剂型将在施用其的对象中提供神经保护。尽管在提取物的全身剂量之后,没有在人脑中进行直接测定,推测当施用给对象时,提取物组分中的一或多种生理活性成分会穿越血脑屏障。夹竹桃苷,作为纯化合物或者包含在称之为pbi-05204的scf提取物中,已被表明在啮齿动物(小鼠)模型中有效穿越血脑屏障并进入脑。有理由预期夹竹桃苷对于人的血脑屏障亦会如此。相应地,本发明提供一种保护神经元避免由氧剥夺或氧-葡萄糖剥夺引起的活性丧失的方法,其通过将氧剥夺和/或葡萄糖剥夺的神经元暴露给有效量的夹竹桃属物种或黄花夹竹桃属物种的提取物,以最小化活性丧失、降低活性丧失率、停止活性丧失、减缓活性丧失发生、和/或保护由暴露氧剥夺和/或葡萄糖剥夺的条件引起的神经元的功能。在某些实施方式中,该方法采用有效量的夹竹桃属物种提取物或黄花夹竹桃属物种提取物的组分或亚组分。在某些实施方式中,组分或亚组分已由提取物的液相色谱分级制备。在某些实施方式中,组分不包含强心苷,且在其他实施方式中,组分或亚组分包括一或多种强心苷,特别是本文描述的那些。实施例9详细说明了用于评估提取物治疗阿尔茨海默病的功效的体外试验。该试验是针对app/aβ引起的(app:β-淀粉样前体蛋白)皮层锥体神经元退化的基于脑切片的试验。被分泌酶分裂后,app被分解为aβ肽,其据信是形成β-淀粉样斑块的致病因素。aβ蛋白与形成β-淀粉样斑块有关,并且据信是阿尔茨海默病的标志(如果不是病因)。生物射弹转染用于将必要标记例如yfp(标记黄色荧光蛋白)和疾病基因构建体导入到脑切片的相同神经元群体中。yfp与app同种型共转染,导致在脑切片制备和转染后的三至四天的时期内,皮层锥体神经元的进行性退化。数据(图2a-2c)表明夹竹桃属物种scf提取物对app-转染的脑切片提供浓度依赖的神经保护,从而挽救水平几乎至由bace抑制剂药物,即β-分泌酶抑制剂药物,所提供的相同水平。β-分泌酶将app前体蛋白分裂为毒性aβ蛋白。含有夹竹桃苷的scf提取物显示提供比单独的夹竹桃苷更高的神经保护。图2a-2c中的数据的重要性在于,文献中几乎没有化合物或治疗策略在代表阿尔茨海默病的本体外试验中表现出任何显著的神经元保护。使用欧洲夹竹桃scf提取物的组分重复app-wt基于脑切片的阿尔茨海默病试验(实施例11)。在app/aβ引起的退化之后,在不同量的scf提取物o-4a组分(0.01至100μg/ml)的存在条件下,确定健康皮层神经元的数目。暴露于氧和葡萄糖剥夺用作内部阳性对照,产生类似中风的引起的神经元损伤。阴性对照仅仅是相对健康的脑切片神经元,无ogd处理或暴露于处理。数据描绘于图6,其中较浅颜色的柱指示相对于app-wt条件的显著差异,依据anova及随后的0.05置信水平的杜纳法事后比较试验(dunnett’sposthoccomparisontest)。数据表明o-4a组分在该试验中提供神经保护,即使它不包含强心苷。利用tau4r基于脑切片的阿尔茨海默病试验评估黄花夹竹桃scf提取物的组分o-4(o-4a)(实施例12)。测定健康皮层神经元的数目。本试验中的功效定义为以下或基于以下定义:在不同量的scf提取物o-4a组分存在的条件下(0.3-100μg/ml,浓度已根据提取物的重量得以确定),健康的相比于不健康数目的相对总数目以及降解神经元的百分比。这些实验中的阴性对照由没有暴露于ogd的脑切片组成,然而暴露于ogd但没有被来源于未分级欧洲夹竹桃提取物的组分处理的脑切片用作内部阳性对照。数据描绘于图7,其中较浅颜色的柱指示相对于损害神经元的显著差异,依据anova及随后的0.05置信水平的杜纳法事后比较试验。数据表明o-4a组分在该试验中提供神经保护,即使它不包含强心苷。相应地,本发明提供一种保护神经元避免阿尔茨海默病引起的活性丧失的方法,该方法包括:将表现出阿尔茨海默病特征的神经元暴露于有效量的夹竹桃属物种或黄花夹竹桃属物种的提取物,以最小化活性丧失、降低活性丧失率、停止活性丧失、减缓活性丧失发生、和/或由阿尔茨海默病引起的神经元的关键功能。在某些实施方式中,该方法采用有效量的夹竹桃属物种提取物或黄花夹竹桃属物种提取物的组分。在某些实施方式中,组分已通过提取物的液相色谱分级制备。在某些实施方式中,组分不包含强心苷,并且在其他实施方式中,组分包含一或多种强心苷,特别是本文中说明的那些。实施例10详细说明了用于评估提取物治疗亨廷顿舞蹈症的功效的试验。通过电穿孔将突变htt蛋白导入皮层神经元、纹状体神经元和神经胶质的高密度的、混合的共培养物。纹状体神经元和皮层神经元由不同颜色荧光蛋白转染,从而有利于单独确认共培养物中不同类型的神经元。颜色荧光蛋白是荧光的,并且在用合适波长的光源激发后“发射”颜色。数据(图3a-3d)表明夹竹桃苷和欧洲夹竹桃的scf提取物在提供更多数目的存活神经元方面,比kw6002(腺苷2a受体拮抗剂)更加有效。数据还表明scf提取物比单独的夹竹桃苷更有效,提示提取物进一步包含除夹竹桃苷以外的一或多种治疗有效剂,其能用于治疗亨廷顿舞蹈症。这样其他的剂可随同夹竹桃苷或其他强心苷一起使用,或在无夹竹桃苷或其他强心苷的条件下使用。相应地,本发明提供一种保护神经元避免亨廷顿舞蹈症引起的活性丧失的方法,该方法包括:将表现出亨廷顿舞蹈症特征的神经元暴露于有效量的夹竹桃苷或含有夹竹桃苷的提取物,以最小化活性丧失、降低活性丧失率、停止活性丧失、减缓活性丧失发生、和/或由亨廷顿舞蹈症引起的神经元的正常功能。实施例16详述了能用于评估提取物中风后的延迟时期后,在对象中治疗中风的功效的示例性脑切片试验。如本文说明进行利用氧葡萄糖剥夺的脑切片试验;然而,不是用提取物预防性地处理脑切片,在0、1、2、4和6小时的延时时期后用提取物处理它们。数据将证明包含提取物针对中风后长达1小时、长达2小时、长达3小时、长达4小时、长达5小时、长达约6小时的延迟时期,有效提供显著的神经保护。相应地,本发明提供了一种在对象中治疗中风的延时方法,其通过在对象患中风之后,向对象施用夹竹桃属物种或黄花夹竹桃属物种的提取物剂量。在对象患中风后的可接受延迟时期内,根据初始给药方案施用初始剂量的提取物。之后,确定对象对提取物治疗的临床反应和/或治疗反应的适当性。如果对象的临床反应和/或治疗反应是适当的,那么如所需要继续用提取物治疗,直到达到期望的临床终点。或者,如果对象的临床反应和/或治疗反应在初始剂量和初始给药方案下不适当,逐步提高或逐步降低剂量直到达到对象中期望的临床反应和/或治疗反应。可连同给药方案的改变,完成剂量逐步提高或逐步降低,给药方案的改变例如给药频率或剂量施用总周期的改变。本文的某些脑切片试验在以下条件下进行:其中ogd之前,脑组织由提取物处理。在那些条件下,数据证实了提取物在预防性地提供神经保护避免中风引起的损害的实用性。如果临床医生试图用提取物的组合或它的组合物以及一或多种其他治疗剂治疗具有神经病症的对象,并且已知对象具有的该特定神经病症至少部分地治疗响应于用所述一或多种其他治疗剂的治疗,那么本方法发明包括:向需要其的对象施用治疗相关剂量的提取物(或它的组分或亚组分)以及治疗相关剂量的所述一或多种其他治疗剂,其中根据第一给药方案施用提取物(或它的组分或亚组分),且根据第二给药方案施用所述一或多种其他治疗剂。在某些实施方案中,第一和第二给药方案相同。在某些实施方式中,第一和第二给药方案不同。如果处于治疗的神经症状是阿尔茨海默病,一或多种其他治疗剂可选自由bace抑制剂或乙酰胆碱酯酶抑制剂组成的组。在某些实施方案中,一或多种其他治疗剂可选自由盐酸美金刚tm(namendatm,memantinehcl)、安理申tm(多奈哌齐)、加兰他敏tm(razadynetm,galantamine)、艾斯能tm(卡巴拉汀)和康耐视tm(他克林)组成的组。如果治疗的神经病症是亨廷顿舞蹈症,一或多种其他治疗剂可选择由天然产物、抗痉挛药、nmda(n-甲基d-天冬氨酸)受体拮抗剂和钠离子通道阻断剂组成的组。示例性治疗剂包括维生素e、巴氯芬(coq10衍生物)、拉莫三嗪(抗痉挛药)、瑞马酰胺(作为低亲和性nmda拮抗剂的麻醉剂)和利鲁唑(na离子通道拮抗剂)。认为这些剂中的每一个的功效就其本身是低的(mestret.etal,chochranedatabasesystematicreviewsjuly8,2009;8(3):cd006455);然而,预期将含有提取物的剂型施用给接受一或多种这些其他试剂的对象,将为患有神经疾病的对象提供与施用这些试剂而不施用所述提取物相比,改善的临床影响。如果治疗的神经病症是中风引起的缺血性脑损伤(缺血性中风),那么除了提取物,可以采用文献(gutierrezm.etal.“cerebralprotection,brainrepair,plasticityandcelltherapyinischemicstroke”cerebrovasc.dis.2009;27suppl1:177-186)中公开的治疗处理,例如静脉溶栓。在某些实施方式中,一或多种治疗剂可选自由药物例如阿替普酶(溶栓剂)组成的组。可以剂量且根据临床医生认可为治疗有效的给药方案,或者以临床医生认可为亚治疗有效的剂量施用一或多种其他治疗剂。通过施用提取物和一或多种其他治疗剂的组合提供的临床益处和/或治疗效果可以是叠加性的或协同性的,此益处或效果的水平通过将组合的施用与单独的提取物和一或多种其他治疗剂的施用比较确定。可以剂量并根据如美国食品药品监督管理局(u.s.f.d.a.)、世界卫生组织(w.h.o)、欧洲药品管理局(e.m.e.a.)、药物管理局(tga,澳大利亚)、泛美卫生组织(paho)、药物和医疗器械安全局(medsafe,新西兰)或全世界多个卫生部建议或说明的给药方案施用一或多种其他治疗剂。如果根据本发明使用强心苷,其可以是已知具有na,k-atp酶结合活性的任何强心苷。强心苷应能够穿越血脑屏障,并在施用后以延长的时期保留在脑组织中。就此而言,强心苷应在施用强心苷后在脑中保留至少8小时,归因于组织结合和随之发生的低清除率。如果存在,强心苷可以纯的形式或以与一或多种其他化合物的混合物存在。强心苷可以提取物存在。提取物可由临界流体(scf)二氧化碳(co2)提取或如此提取物的化学改性形式(例如包括乙醇或使用scfco2和乙醇制备的提取物;实施例1)制备。提取物可通过用有机溶剂提取植物材料获得,所述有机溶剂例如乙醇、甲醇、丙醇或其他这样的溶剂。提取物可从植物材料获得。植物材料可以是例如获自夹竹桃属物种例如欧洲夹竹桃植物物质,或黄花夹竹桃属物种例如黄花夹竹桃(另称为黄夹竹桃)的植物物质。提取过程可在欧洲夹竹桃叶的干粉上进行,所述干粉是根据在以下文献中说明的过程制备的:以阿丁顿(addington)名义在2005年2月15日提交的当前审理的美国临时申请60/653,210、以阿丁顿名义在2006年1月26日提交的美国专利申请11/340,016、以阿丁顿名义在2006年7月28日提交的美国专利申请11/191,650(现在是2008年7月22日授权的美国专利7,402,325)、或2006年7月26日提交的pct国际专利申请pct/us06/29061、或newman等(mol.interven.(2008),8,36-49),这些的全部公开通过引用结合至此,或是根据本文说明的过程制备的。这些方法还可用于制备夹竹桃属物种或黄花夹竹桃属物种的未分级提取物。除非另外指明,本文所用术语“提取物”可意指“未分级提取物”或提取物的组分或提取物组分的亚组分。术语“未分级提取物”通常意指通过提取植物材料获得的提取物,其中提取物还未经过分级,例如在提取物初始制备之后,通过色谱法或溶剂萃取分级或分离为单个成分或成分的组。如本文中使用,术语“夹竹桃苷”意指夹竹桃苷的所有已知形式,除非另外指明。夹竹桃苷可以外消旋形式、光学纯形式或光学富集形式存在。欧洲夹竹桃植物材料可以例如从商业植物供应商aldridgenursery(得克萨斯州,亚他斯科)获得。未分级提取物可通过含强心苷植物物质的改性(例如乙醇)或未改性超临界流体提取获得,所述植物物质例如含有夹竹桃属物种或黄花夹竹桃属物种的植物物质。超临界流体提取物可包含从植物物质提取的一或多种药理活性剂,其当施用给对象时,有助于提取物的治疗功效。当存在两种或更多种此活性剂时,它们叠加性地或协同性地有助于提取物的治疗功效。可通过多种不同过程制备未分级提取物。可如上或根据由huseyinziyaozel博士(美国专利5,135,745)开发的过程制备提取物,说明了用于在水中制备植物提取物的热水提取程序。水性提取物据报道含有分子量从2kd至30kd变化的数种多糖、夹竹桃苷、夹竹桃苷元、奥多诺苷和夹竹桃它罗苷。多糖据报道包括酸性高多聚半乳糖醛酸聚糖(homopolygalacturonans)或阿拉伯半乳糖醛酸聚糖(arabinogalaturonans)。授权给selvaraj等的美国专利5,869,060公开了夹竹桃属物种的热水提取物及其生产方法,例如实施例2。所得提取物可之后被冻干以产生粉。美国专利6,565,897(selvaraj的美国预授权公开20020114852和pct国际公开wo2000/016793)公开了用于制备实质上无菌提取物的热水提取过程。erdemoglu等(j.ethnopharmacol.(2003)nov.89(1),123-129)公开了比较植物(包括欧洲夹竹桃)的水性提取物和乙醇提取物的结果,基于它们的抗伤害性活性和抗炎活性。adome等(afr.healthsci.(2003)aug.3(2),77-86;乙醇提取物)、el-shazly等(j.egyptsoc.parasitol.(1996),aug.26(2),461-473;乙醇提取物)、begum等(phytochemistry(1999)feb.50(3),435-438;甲醇提取物)、zia等(j.ethnolpharmacol.(1995)nov.49(1),33-39;甲醇提取物)和vlasenko等(farmatsiia.(1972)sept.-oct.21(5),46-47;醇提取物)公开了欧洲夹竹桃的有机溶剂提取物。singh等的美国预授权专利申请公开20040247660公开了制备用于治疗癌症的夹竹桃苷的蛋白稳定化脂质体配方。singh等的美国预授权专利申请公开20050026849公开了含有环糊精的夹竹桃苷的水溶性配方。singh等的美国预授权专利申请公开20040082521公开了制备来自热水提取物的夹竹桃苷的蛋白稳定化纳米颗粒配方。scf提取可在超临界流体中改性剂的存在下进行,例如醇诸如甲醇,以增强期望化合物从植物物质的提取(2005年7月26日提交的pct/us06/29061;us7,402,325和2008年1月4日提交的ussn12/019435、或newman等(mol.interven.(2008),8,36-49),其全部公开通过引用结合至此)。改性剂通常具有超临界流体与被提取化合物之间的挥发性,并且它们必须与超临界流体混溶。在某些实施方式中,改性剂是环境条件下的液体。通过实例并非限制,改性剂可选择由乙醇、甲醇、丙醇、丙酮、乙酸乙酯、二氯甲烷等组成的组。可能的是,如在本文所包括的试验中通过功效所确定,提取物还在它们的相对性能方面不同。即使如此,如果一或多种药理学活性剂以足够高的量或浓度存在于提取物中,以能够制备治疗相关剂量,那么认为该提取物是本发明的一部分。实施例13说明了用于分级scf提取物为五种不同组分的色谱方法:o-h、o-2、o-3、o-4和o-5。组分通过以下制备:将未分级提取物负载至用水平衡的ods-硅胶柱上,接下来通过使甲醇含量不同(30%、55%、80%和100%)的多部分水性流动相顺序流过柱以洗脱提取物的不同组分,收集各自的流出物(组分),和通过减压溶剂蒸发以移除溶剂来浓缩流出物,从而提供组分o-1(或o-h)、o-2、o-3、o-4和o-5。根据实施例14分析组分,通过薄层层析使用附着至(因此可用于检测)强心苷的灵敏染料指示剂测定它们在强心苷和其他成分方面的组成。此外,使用液相色谱/串联质谱或dad-uv检测分析这些组分中强心苷的存在或不存在。通过液相色谱采用不同于ods-硅胶的固定相和/或通过采用不同于水的流动相,可分析提取物的组分或亚组分。本文进一步描述了示例性合适的固定相。图8a-8d描绘了hplc分析实施例13的组分fr-o-1、fr-o-2、fr-o3和fr-o-4之后获得的色谱图。基于比较使用相应外部参照样品获得的保留时间,确定了(fr-o-2和fr-o-3)组分含有夹竹桃苷衍生物(强心苷)、夹竹桃苷(rt=8.3min)和其他未确认的成分。在原始未分级scf提取物中发现的大部分夹竹桃苷主要在fr-o-3组分中。fr-o-4不含有可计量的量的任何强心苷。相应地,组分的组成根据夹竹桃苷含量、强心苷和其他未确认的成分而不同。组分夹竹桃苷(y/n)其他强心苷(y/n)神经保护(y/n)o-hnnyo-2nyno-3yyyo-4(o-4a)nnyo-5nnn之后对这些组分进行在实施例15中详述的神经保护基于脑部切片的实验,以测定每种所提供的神经保护的水平。在图4a-4e中描绘了数据,其中将含有scf提取物(23μg/ml)的水溶液的神经保护活性与含有0.03、0.3或3μg/ml其他成分的其他溶液的进行比较。称出所有组分,并在同等的质量重量基础上比较。确定了含有夹竹桃苷或强心苷的组分(本文所描述的)以及不含有夹竹桃苷或强心苷的某些组分可提供神经保护。将scf提取物的o-4组分在基于脑切片的中风试验中的表现与未分级scf提取物(pbi-05204)的表现比较。将不用量(0.03至300μg/ml)的o-4组分的表现与固定量(23μg夹竹桃苷ml)的提取物的表现相比较。数据(图5)清楚地表明欧洲夹竹桃scf提取物的o-4组分保留了其功效,尽管它并不含有夹竹桃苷或可检测量的任何其他强心苷。图5中的浅色柱表示相对于中风病症(设为0)的显著差异,依据anova及随后的0.05置信水平的杜纳法事后比较试验。相应地,本发明提供夹竹桃属物种或黄花夹竹桃属物种的提取物的多个治疗组分,所述组分选自由以下组成的组:a)包含一或多种药理学活性剂但不包含夹竹桃苷和其他强心苷的组分,其中组分提供神经保护;b)包含一或多种药理学活性剂、夹竹桃苷和一或多种其他强心苷的组分,其中组分提供神经保护;以及c)包含一或多种药理学活性剂(不同于以上a)中的那些)但不包含夹竹桃苷和其他强心苷的不同组分,其中组分提供神经保护。本发明还提供一种分级夹竹桃属物种或黄花夹竹桃属物种的提取物以提供它的一或多种治疗有效组分的方法。该方法包括:a)提供夹竹桃属物种或黄花夹竹桃属物种的提取物;b)分级提取物以提供提取物的两种或更多种组分,包含一或多种药理学活性剂(其不是强心苷)并不包含强心苷的第一提取物,和包含一或多种药理学活性剂(其不是强心苷)和一或多种强心苷的第二提取物。在某些实施方案中,通过具有固定相和流动相的液相色谱完成分级。在某些实施方式中,固定相包含介质,所述介质选自由以下组成的组:“反相”树脂,一种用于色谱法的实现充分填装的惰性非极性物质,例如由结合至硅胶的短碳链(c8至c18)、氰基结合硅胶或苯基结合硅胶组成、离子交换树脂(基于阳离子或阴离子)、“正相(normal)”树脂,例如具有氰基和氨基官能团的硅胶或有机部分。在某些实施方式中,流动相包含溶剂,所述溶剂选自由水、甲醇、乙醇、乙腈、四氢呋喃、基于水的缓冲溶液或它们的混合物组成的组。在某些实施方式中,流动相包含水甲醇,其中甲醇含量从约30%至100%顺序升高,并且固定相是ods-硅胶。可使用梯度洗脱流动相、分阶洗脱流动相或固定组合物流动相进行色谱法。提取物组分可以被亚分级以提供提取物组分的两种或更多种不同的亚组分。可通过组分的液相色谱完成亚分级。用于液相色谱的合适的固定相可包含硅胶或其他树脂例如离子交换介质、氧化铝或非结合c18材料,用于液相色谱的合适的流动相可包含极性不同的两种或更多种有机溶剂的组合:较小极性的有机溶剂和较大极性的有机溶剂。适合的极性有机溶剂可以是四氢呋喃、二氯甲烷、乙酸乙酯、丙酮、二甲基甲酰胺、乙腈、正丁醇、异丙醇、正丙醇、乙醇、甲醇、乙酸和水。适合的非极性有机溶剂可以是乙酸乙酯戊烷、环戊烷、己烷、环己烷、苯、甲苯、1,4-二噁烷、氯仿或乙醚。用于缓冲溶液的缓冲剂包括在液相色谱领域中任何已知的那些。示例性缓冲剂包括含有磷酸盐、醋酸盐、柠檬酸盐、甲酸盐、磷酸盐、三氟乙酸、氯醋酸盐、磺酸盐、烷基氨、tae、tbe、氨、buffar、碳酸盐、hepes、mes、硫氰酸盐、caps、ches、胍、mops、pipes、tris、硫酸盐、氢氧化物、碱金属卤化物、三甲基甘氨酸或氨基酸离子、或它们的组合的那些。一或多种离子配对剂和/或一或多种有机改性剂也可包含在流动相中。可用于分级提取物的其他类型的色谱法包括体积排阻色谱、正相色谱、离子交换色谱、疏水作用色谱、或它们的组合。也可能使用不同类型色谱的组合形式。固定相可以包含为两种或更多种不同介质的组合的介质,所述两种或更多种不同介质用于反相色谱、体积排阻色谱、离子交换色谱或疏水作用色谱,例如反相固定相和体积排阻固定相的组合、反相固定相和离子交换固定相的组合、或其他此类组合或两种、三种或四种不同固定相介质。固定相介质可以是多孔的、非多孔的、表面多孔的、散布性多孔的或完全多孔的。本发明提供了一种分级提取物的方法,包括:a)提供获自夹竹桃属物种或黄花夹竹桃属物种的提取物;b)通过利用ods-硅胶作为固定相和含水甲醇作为流动相的柱色谱法分级提取物,以提供至少两种不同的组分:包含至少一种强心苷和至少一种非强心苷的药理活性剂的第一组分,和不包含强心苷和包含至少一种非强心苷的药理活性剂的另一组份;c1)通过利用硅胶作为固定相和极性不同的至少两种有机溶剂的混合物作为流动相的柱色谱法亚分级b)的另一组份,以提供至少两种不同的亚组分:包含一或多种类固醇和一或多种三萜烯的亚组分,和包含两种或更多种不同三萜烯、不包含类固醇的另一亚组分,其中所述亚组分不包含强心苷。在某些实施方式中,所述方法进一步包括:c2)通过利用硅胶作为固定相和极性不同的至少两种有机溶剂的混合物作为流动相的柱色谱法亚分级b)的第一组份,以提供至少两种不同的亚组分:包含一或多种类固醇和一或多种三萜烯的第一亚组分,和包含两种或更多种不同三萜烯、不包含类固醇的另一亚组分,其中所述亚组分的任一种或两种进一步包含强心苷。提取物或其组分或亚组分可以配制为任何合适的药学可接受的剂型。肠胃外剂型、耳部剂型、眼部剂型、鼻部剂型、可吸入剂型、口腔剂型、舌下剂型、肠部剂型、外用剂型、口服剂型、经口剂型和注射剂型特别有用。特定剂型包括固定或液体剂型。示例性的合适剂型包括片剂、胶囊、丸剂、囊片(caplet)、锭剂、囊剂(sache)、溶液、悬浮液、分散液、小瓶(vial)、袋、瓶、注射液体、i.v.(静脉内)、i.m.(肌内)或i.p.(腹膜内)可施用的液体以及药学领域的技术人员已知的其他此类剂型。本发明药剂中含有的提取物或其组分或亚组分的量会是至少一或多种剂型,并根据已知的药学原则选择。特别预期有效量或治疗相关量的治疗化合物。通过术语“有效量”,理解为相对于于例如药物,预期了药学有效量。药学有效量是对于要求的或期望的治疗反应来说,足够的活性成分的量或质量,换言之,当施用给患者时,足以引起可感知生物反应的量。该可感知生物反应可以是因为施用单剂或多剂的活性物质发生的。所述剂量(dose)可包含一或多种剂型。将理解,对于任何患者来说,特定的剂量水平将依赖于多种因素,包括正在治疗的适应症、适应症的严重程度、患者健康状况、年龄、性别、体重、饮食、药理反应、施用的特定剂型和其他此类因素。对于口服,期望的剂量是多达5种剂型,尽管少至一种剂型和多至十种剂型可作为单剂服用。示例性剂型含有每剂型0.1至5mg的scf提取物,适用于每剂量总共0.1至500mg(1至10的剂量水平)。将根据预先确定的和/或经调整以在对象中达到特定治疗反应或临床益处的给药方案来施用剂量。对于治疗哺乳动物的应用,提取物或其组分或亚组分可以包含在剂型中。剂型的某些实施方式不是肠溶的,且在0.5至1小时或更短时间内释放它们的提取物负载。剂型的某些实施方式是肠溶的,且在胃的下游例如从空肠、回肠、小肠和/或大肠(结肠)释放它们的强心剂负载。肠溶剂型将在口服后1-10小时内将提取物释放入体循环。应注意到本文化合物在本发明配方中可具有一或多种功能。例如,化合物可作为表面活性剂和水混溶性溶剂两者,或作为表面活性剂和水不溶性溶剂两者。液体组合物可包含一或多种药学可接受液体载体。液体载体可以是含水、不含水、极性、非极性和/或有机的载体。通过实例而非限制,液体载体包括水混溶性溶剂、水不混溶性溶剂、水、缓冲剂和它们的组合。如本文所使用,可交换使用的术语“水溶性溶剂”或“水混溶性溶剂”指不与水形成双相混合物的有机液体,或充分水溶以提供含有至少百分之五溶剂而无液相分离的含水溶剂混合物的有机液体。该溶剂适合施用给人或动物。通过实例而非限制,示例性水溶性溶剂包括peg(聚乙二醇)、peg400(具有约400大概分子量的聚乙二醇)、乙醇、丙酮、烷酮、醇、醚、丙二醇、甘油、三乙酸甘油酯、聚丙二醇、pvp(聚乙烯吡咯烷酮)、二甲亚砜、n,n-二甲基甲酰胺、甲酰胺、n,n-二甲基乙酰胺、吡啶、丙醇、n-甲基乙酰胺、丁醇、soluphor(2-吡咯烷酮)、pharmasolve(n-甲基-2-吡咯烷酮)。如本文所用,可交换使用的术语“水不溶性溶剂”或“水不混溶性溶剂”指与水形成双相混合物或当溶剂在水中的浓度超过百分之五时出现相分离的有机液体。该溶剂适合施用给人或动物。通过实例而非限制,示例性水不溶性溶剂包括中/长链甘油三酯、油、蓖麻油、玉米油、维生素e、维生素e衍生物、油酸、脂肪酸、橄榄油、softisan645(双二甘油(辛酸/癸酸/硬脂酸/羟基硬脂酸己二酸)酯)、米格列醇(miglyol)、captex(captex350:辛酸/癸酸/月桂酸甘油三酯(tricaprylate/caprate/lauratetriglyceride)、captex355:辛酸/癸酸甘油三酯(glyceryltricaprylate/capratetriglyceride)、captex355ep/nf:辛酸/癸酸中链甘油三酯(glyceryltricaprylate/capratemediumchaintriglyceride))。合适的溶剂列于“人用药物注册技术要求国际协调会(ich)工业指南q3c杂质:残余溶剂”(1997)”,其推荐了关于什么量的残余溶剂在药物中被认为是安全的。示例性溶剂被列为第2类或第3类溶剂。第3类溶剂包括例如乙酸、丙酮、苯甲醚、1-丁醇、2-丁醇、乙酸丁酯、甲基叔丁基醚、异丙基苯、乙醇、乙醚、乙酸乙酯、甲酸乙酯、甲酸、庚烷、乙酸异丁酯、乙酸异丙酯、乙酸甲酯、甲基-1-丁醇、甲基乙基酮、甲基异丁基酮、2-甲基-1-丙醇、戊烷、1-戊醇、1-丙醇、2-丙醇或乙酸丙酯。本发明中可用作水不混溶性溶剂的其他材料包括:captex100:丙二醇二癸酸酯;captex200:丙二醇二辛酸酯/二癸酸酯;captex200p:丙二醇二辛酸酯/二癸酸酯;丙二醇辛癸酸酯(propyleneglycoldicaprylocaprate);captex300:辛酸/癸酸三甘油酯(glyceryltricaprylate/caprate);captex300ep/nf:辛酸/癸酸中链甘油三酯;captex350:辛酸/癸酸/月桂酸三甘油酯;captex355:辛酸/癸酸三甘油酯;captex355ep/nf:辛酸/癸酸中链甘油三酯;captex500:三乙酸甘油酯;captex500p:三乙酸甘油酯(医药级);captex800:丙二醇双(2-乙酸己酯);captex810d:辛酸/癸酸/亚油酸甘油三酯;captex1000:三癸酸甘油酯;captexca:中链甘油三酯;captexmct-170:中链甘油三酯;capmulgmo:单油酸甘油酯;capmulgmo-50ep/nf:单油酸甘油酯;capmulmcm:中链单甘油酯&双甘油酯;capmulmcmc8:单辛酸甘油酯;capmulmcmc10:单癸酸甘油酯;capmulpg-8:丙二醇单辛酸酯;capmulpg-12:丙二醇单月桂酸酯;caprol10g10o:十油酸十甘油酯;caprol3go:三聚甘油单油酸酯;caprolet:混合脂肪酸的聚甘油酯;caprolmpgo:六聚甘油二油酸酯;caprolpge860:十聚甘油单油酸酯,十聚甘油二油酸酯。如本文所用,“表面活性剂”指包含极性或带电荷亲水部分以及非极性疏水(亲脂)部分的化合物;即表面活性剂是两亲性的。术语表面活性剂可指一种化合物或化合物的混合物。表面活性剂可以是增溶剂、乳化剂或分散剂。表面活性剂可以是亲水的或疏水的。亲水的表面活性剂可以是适合用于药物组合物的任何亲水表面活性剂。此类表面活性剂可以是阴离子、阳离子、两性离子或非离子的,尽管非离子亲水表面活性剂是目前优选的。如上所述,这些非离子亲水表面活性剂通常会具有大于约10的hlb值。亲水表面活性剂的混合物也在本发明范围之内。类似地,疏水表面活性剂可以是适合用于药学组合物的任何疏水表面活性剂。通常,合适的疏水表面活性剂具有小于约10的hlb值。疏水表面活性剂的混合物也在本发明范围之内。其他合适的增溶剂的实例包括:醇和多元醇,例如乙醇、异丙醇、丁醇、苯甲醇、乙二醇、丙二醇、丁二醇及其同分异构体、甘油、季戊四醇、山梨醇、甘露醇、还原二元醇、二甲基异山梨醇、聚乙二醇、聚丙二醇、聚乙烯醇、羟丙基甲基纤维素和其他纤维素衍生物、环糊精和环糊精衍生物;具有平均分子量约200至约6000的聚乙二醇的醚,例如四氢糠醇peg醚(四氢呋喃聚乙二醇醚,可从basf以商品名tetraglycol商业获得)或甲氧基peg(美国联合碳化物公司(unioncarbide));酰胺,例如2-吡咯烷酮、2-哌啶酮、己内酰胺、n-烷基吡咯烷酮、n-羟基烷基吡咯烷酮、n-烷基哌啶酮、n-烷基己内酰胺、二甲基乙酰胺和聚乙烯吡咯烷酮;酯,例如丙酸乙酯、柠檬酸三丁酯、乙酰柠檬酸三乙酯、乙酰柠檬酸三丁酯、柠檬酸三乙酯、油酸乙酯、辛酸乙酯、丁酸乙酯、三乙酸甘油酯、丙二醇单乙酸酯、丙二醇二乙酸酯、己内酯及其同分异构体、戊内酯及其同分异构体、丁内酯及其同分异构体;以及本领域已知的其他增溶剂,例如二甲基乙酰胺、异山梨醇二甲基醚(arlasolvedmi(ici))、n-甲基吡咯烷酮(pharmasolve(isp))、单辛精、二乙二醇单乙基醚(可从嘉法狮公司(gattefosse)以商品名transcutol获得)和水。增溶剂的混合物也在本发明范围之内。除非如指明,本文涉及的化合物可从标准商业来源容易获得。透明液体组合物对于肉眼是视觉上清澈的,因为它将含有基于组合物的总重量少于5%、少于3%或少于1%以重量计的悬浮固体。尽管不必要,本发明组合物或试剂盒可含有螯合剂、防腐剂、抗氧化剂、吸附剂、酸化剂、碱化剂、消泡剂、缓冲剂、着色剂、电解液、盐、稳定剂、渗透修饰剂、稀释剂、其他药用赋形剂、或它们的组合。如本文所用,术语“抗氧化剂”意指抑制氧化且因此用于防止制品被氧化过程劣化的试剂。通过实例而非限制,此类化合物包括抗坏血酸、抗坏血酸棕榈酸酯、维生素e、维生素e衍生物、丁基羟基苯甲醚、丁基羟基甲苯、次磷酸、单硫代甘油、没食子酸丙酯、抗坏血酸钠、亚硫酸氢钠、甲醛次硫酸氢钠、焦亚硫酸钠(sodiummetalbisulfite)和本领域技术人员已知的其他此类材料。如本文所用,术语螯合剂意指螯合溶液中金属离子的化合物。示例性螯合剂包括edta(乙二胺四乙酸四钠)、dtpa(二乙烯三胺五乙酸五钠)、hedta(n-(羟乙基)-乙烯基-二胺三乙酸的三钠盐)、nta(次氮基三乙酸三钠)、乙醇二甘氨酸二钠(na2edg)、二乙醇甘氨酸钠(degna)、柠檬酸和本领域技术人员已知的其他化合物。如本文所用,术语“吸附剂”意指能够通过物理或化学(化学吸附)方式将其他分子保持在其表面的试剂。通过实例而非限制,此类化合物包括粉状活性碳和本领域技术人员已知的其他材料。如本文所用,术语“碱化剂”意指用于提供碱性介质的化合物。通过实例而非限制,此类化合物包括氨水、碳酸铵、二乙醇胺、单乙醇胺、氢氧化钾、硼酸钠、碳酸钠、碳酸氢钠、氢氧化钠、三乙醇胺和本领域技术人员已知的其他化合物。如本文所用,术语“酸化剂”意指用于提供酸性介质的化合物。通过实例而非限制,此类化合物包括乙酸、氨基酸、柠檬酸、延胡索酸和其他α-羟基酸、盐酸、抗坏血酸和本领域技术人员已知的其他化合物。如本文所用,术语“消泡剂”意指防止或降低形成在填充组合物表面的发泡量的化合物。通过实例而非限制,合适的消泡剂包括二甲聚硅氧烷(dimethicone)、二甲基硅油(simethicone)、辛基酚聚醚和本领域技术人员已知的其他消泡剂。如本文所用,术语“缓冲剂”意指用于在稀释或加入酸或碱时,对抗ph改变的化合物。通过实例而非限制,此类化合物包括偏磷酸钾、磷酸钾、单碱式乙酸钠和无水和脱水柠檬酸钠和本领域技术人员已知的其他此类材料。如本文所用,术语“稀释剂”或“填充剂”意指作为填充剂以在片剂和胶囊的制备中生成期望体积、流动性和压缩特征的惰性物质。通过实例而非限制,此类化合物包括二碱式磷酸钙、高岭土、乳糖、蔗糖、甘露醇、微晶纤维素、粉状纤维素、沉淀碳酸钙、山梨醇和淀粉和本领域技术人员已知的其他材料。如本文所用,术语“防腐剂”意指用于防止微生物生长的化合物。通过实例而非限制,此类化合物包括氯化苯甲烃胺、苄索氯铵、苯甲酸、苯甲醇、氯化十六烷基吡啶、氯丁醇、苯酚、苯乙醇、硝酸苯汞、醋酸苯汞、硫柳汞、间甲酚、米吡氯铵、苯甲酸钾、山梨酸钾、苯甲酸钠、丙酸钠、山梨酸、百里酚和甲基、乙基、丙基或丁基苯甲酸酯和本领域技术人员已知的其他化合物。如本文所用,术语“着色剂”意指用于赋予药物制品颜色的化合物。通过实例而非限制,此类化合物包括fd&c红色3号、fd&c红色20号、fd&c黄色6号、fd&c蓝色2号、fd&c绿色5号、fd&c橙色5号、fd&c红色8号、焦糖、和氧化铁(黑色、红色和黄色)、其他fd&c染料和自然着色剂例如葡萄皮提取物、甜菜红粉、β-胡萝卜素、酪黄、胭脂红、姜黄、红椒、它们的组合和本领域技术人员已知的其他此类材料。如本文所用,术语“稳定剂”意指用于稳定活性剂,对抗否则会降低活性剂治疗活性的物理、化学或生化过程的化合物。通过实例而非限制,合适的稳定剂包括白蛋白、唾液酸、肌酸酐、甘氨酸和其他氨基酸、烟酰胺、乙酰色氨酸钠(sodiumacetyltryptophonate)、氧化锌、蔗糖、葡萄糖、乳糖、山梨醇、甘露醇、甘油、聚乙二醇、辛酸钠和糖精钠和本领域技术人员已知的其他稳定剂。如本文所用,术语“渗透修饰剂“意指用于调整液体配方的渗透压的化合物。合适的渗透修饰剂包括甘油、乳糖、甘露醇、右旋糖、氯化钠、硫酸钠、山梨醇、海藻糖和本领域技术人员已知的其他渗透修饰剂。本发明组合物还可包含油例如固定油、花生油、芝麻油、棉籽油、玉米油和橄榄油;脂肪酸例如油酸、硬脂酸和异硬脂酸;和脂肪酸酯例如油酸乙酯、豆蔻酸异丙酯、脂肪酸甘油酯和乙酰化脂肪酸甘油酯。组合物还可包含醇例如乙醇、异丙醇、十六烷基醇、甘油和丙二醇;甘油缩酮例如2,2-二甲基-1,3-二氧戊环-4-甲醇;醚例如聚乙二醇450;石油烃例如矿物油和矿脂;水;药学合适的表面活性剂、悬浮剂或乳化剂;或它们的混合物。应理解在制药配方领域使用的化合物通常提供多种功能或目的。因此,如果本文指定的化合物仅被提及一次或用于定义本文一种以上的术语,它的目的或功能不应解释为仅限制为被指定的目的或功能。配方中的一或多种成分可以其自由基或药学或分析上可接受的盐形式存在。如本文所用,“药学或分析上可接受的盐”指通过使化合物与所需要的酸反应形成离子结合对而已被修饰的化合物。可接受的盐的实例包括形成的常规非毒性盐,例如从非毒性无机酸或有机酸形成的。合适的非毒性盐包括从无机酸衍生的那些,所述无机酸例如盐酸、氢溴酸、硫酸、磺酸、氨基磺酸、磷酸、硝酸和本领域技术人员已知的其他无机酸。从有机酸制备的盐,所述有机酸例如氨基酸、乙酸、丙酸、琥珀酸、乙醇酸、硬脂酸、乳酸、苹果酸、酒石酸、柠檬酸、抗坏血酸、扑酸、顺丁烯二酸、羟基马来酸、苯乙酸、谷氨酸、苯甲酸、水杨酸、磺胺酸、2-乙酰基苯甲酸、反丁烯二酸、对甲苯磺酸、甲磺酸、乙烷二磺酸、草酸、羟乙磺酸和本领域技术人员已知的其他有机酸。其他合适的盐的列表见于remington′spharmaceuticalsciences,17th.ed.,mackpublishingcompany,easton,pa,1985,p.1418,其相关公开通过引用结合于本文。本文使用术语“药学可接受的”来指在足够医学决定范围内,适合用于与人类和动物的组织接触,且没有过度毒性、刺激、过敏反应或任何其他问题或并发症,与合理益处/风险率相当的那些化合物、材料、组合物和/或剂型。可以制药工业已知的任何传统方法制备剂型。液体剂型可通过提供至容器中的至少一种液体载体和夹竹桃苷或含夹竹桃苷的提取物来制备。在液体剂型中可包含一或多种其他赋形剂。固体剂型可通过提供至少一种固体载体和夹竹桃苷或含夹竹桃苷的提取物来制备。一或多种其他赋形剂可包含在固体剂型中。可使用常规包装设备和材料包装剂型。它可被包容在包、瓶、小瓶、袋、注射器、包膜、小包、罩板、盒、安瓿或其他此类容器中。本发明包括一种用于改善具有神经病症的群体中,统计学显著数目的对象的临床状态的方法,该方法包括:向对象群体施用夹竹桃属物种或黄花夹竹桃属物种的提取物,或它们的组合物;并确定对象的临床状态以建立改善的临床状态。在某些实施方式中,统计学显著的数目是群体的至少5%、至少10%、至少20%、至少30%、至少40%、至少50%、至少60%、至少70%、至少80%或至少9%。在某些实施方式中,提取物包含一或多种其他药理活性化合物。在其他实施方式中,提取物包含一或多种其他药理活性化合物,包含与夹竹桃苷或其他强心苷协作以改善对象的临床状态的那些。根据以上说明和以下实施例,本领域技术人员将能够在无需过度试验的情况下实施本发明。参照详述用于准备/制备本发明实施方式的特定工艺的以下实施例,将更好地理解前述内容。对这些实施例的所有参考都用于解释目的。以下实施例不应认为是穷尽的,而只是解释本发明所预期的许多实施方式的仅少数实施方式。可从西格玛化工公司(sigmachemical)(圣路易斯,密苏里洲)购买夹竹桃苷。实施例1:粉状夹竹桃叶的超临界流体提取方法a用二氧化碳通过收获、洗涤和干燥夹竹桃叶材料,之后使夹竹桃叶材料通过粉碎和脱水设备例如美国专利5,236,132、5,598,979、6,517,015和6,715,705中所描述的那些来制备粉状夹竹桃叶。所使用的起始材料的重量是3.94kg。在提取器设备中,在压力300巴(30mpa,4351psi)和温度50℃(122°f)下将起始材料与纯co2结合。总共使用197kgco2,以使得溶剂比原材料的比率为50:1。之后使co2与原材料的混合物通过分离器装置,所述装置改变混合物的压力和温度,并从二氧化碳分离提取物。获得作为褐色、粘稠材料的提取物(65g),其具有宜人的芳香。颜色有可能是由叶绿素引起的。为了确定精确的产量,用丙酮冲洗试管和分离器,挥发丙酮,得到添加的9g提取物。提取物总量为74g。基于起始材料的重量,提取物的产量为1.88%。提取物中夹竹桃苷的含量经高压液相色谱和质谱计算为560.1mg,或0.76%的产量。方法b用二氧化碳和乙醇的混合物通过收获、洗涤和干燥夹竹桃叶材料,之后使夹竹桃叶材料通过粉碎和脱水设备例如美国专利5,236,132、5,598,979、6,517,015和6,715,705中所描述的那些来制备粉状夹竹桃叶。所使用的起始材料的重量是3.85kg。在提取器设备中,在压力280巴(28mpa,4061psi)和温度50℃(122°f)下将起始材料与纯co2和5%乙醇结合。总共使用160kgco2和8kg乙醇,以使得溶剂比原材料的比率为43.6比1。之后使co2、乙醇与原材料的混合物通过分离器装置,所述装置改变混合物的压力和温度,并从二氧化碳分离提取物。在移除乙醇之后,获得作为深绿色、粘性物质的提取物(207g),其明显含有一些叶绿素。基于起始材料的重量,提取物的产量为5.38%。提取物中夹竹桃苷的含量经高压液相色谱和质谱计算为1.89g,或2.1%的产量。实施例2:粉状夹竹桃叶的热水提取热水提取典型地用于从夹竹桃叶中提取夹竹桃苷和其他活性成分。热水提取方法的实例见于美国专利5,135,745和5,869,060。使用5g粉状夹竹桃叶实施热水提取。将十体积的沸水(以夹竹桃起始材料的重量计)加入至粉状夹竹桃叶,持续搅拌混合物6小时。之后过滤混合物,收集并在相同条件下再次提取叶残渣。将滤液合并且冻干。提取物呈褐色。干燥的提取物重约1.44g。将34.21mg提取物材料溶解在水中,并使用高压液相色谱和质谱进行夹竹桃苷含量分析。测定夹竹桃苷的量为3.68mg。基于提取物的量,夹竹桃苷产量计算为0.26%。下表表明了针对实施例1两种超临界二氧化碳提取和热水提取的夹竹桃苷产量之间的对比。产率对比提取介质基于提取物总重量的夹竹桃苷产率超临界二氧化碳:实施例1,方法a0.76%超临界二氧化碳:实施例1,方法b2.1%热水提取:实施例20.26%实施例3:包括但不限于阿尔茨海默病的神经病症的治疗方法a提取物疗法为表现阿尔茨海默病的对象开具强心苷的药方,并且根据处方的给药方案向对象施用治疗相关剂量一段时间。定期测定对象的治疗反应的水平。如果治疗反应水平在一剂量时太低,那么根据预先确定的剂量递增安排逐步提高剂量,直到在对象中实现期望水平的治疗反应。如所需要继续用提取物、或其组分或亚组分治疗对象,并且可如所需要调整剂量或给药方案直到患者达到期望的临床终点。方法b组合疗法:提取物和另一治疗剂遵循以上方法a,除了向对象开具和施用一或多种其他治疗剂用于治疗阿尔茨海默病或其症状。那么可在提取物之前、之后或同时施用一或多种其他治疗剂。还可逐步升高(或逐步降低)一或多种其他治疗剂的剂量。合适的一或多种其他治疗剂包括盐酸美金刚tm(memantinehcl)、安理申tm(多奈哌齐)、加兰他敏tm(galantamine)、艾斯能tm(卡巴拉汀)、康耐视tm(他克林)和金刚烷胺。实施例4:包括但不限于亨廷顿舞蹈症的神经病症的治疗方法a提取物疗法为表现亨廷顿舞蹈症的对象开具提取物的药方,并且根据处方的给药方案向对象施用治疗相关剂量一段时间。定期测定对象的治疗反应的水平。如果治疗反应水平在一剂量时太低,那么根据预先确定的剂量递增安排逐步提高剂量,直到在对象中实现期望水平的治疗反应。如所需要继续用提取物治疗对象,并且可如所需要调整剂量或给药方案直到患者达到期望的临床终点。施用的剂量可以类似于实施例3的那些,或者如本文另外说明。方法b组合疗法:提取物和另一治疗剂遵循以上方法a,除了向对象开具和施用一或多种其他治疗剂用于治疗亨廷顿舞蹈症或其症状。可在强心苷之前、之后或同时施用一或多种其他治疗剂。还可逐步升高(或逐步降低)一或多种其他治疗剂的剂量。合适的一或多种其他治疗剂包括维生素e、巴氯芬(coq10的衍生物)、拉莫三嗪(抗痉挛药)、瑞马酰胺(作为低亲和性nmda拮抗剂的麻醉剂)和利鲁唑(na离子通道拮抗剂)。实施例5:包括但不限于缺血性中风的神经病症的治疗方法a提取物疗法为表现缺血性中风的对象开具提取物的药方,并且根据处方的给药方案向对象施用治疗相关剂量一段时间。定期测定对象的治疗反应的水平。如果治疗反应水平在一剂量时太低,那么根据预先确定的剂量递增安排逐步提高剂量,直到在对象中实现期望水平的治疗反应。如所需要继续用提取物治疗对象,并且可如所需要调整剂量或给药方案直到患者达到期望的临床终点。施用的剂量可以类似于实施例3的那些,或者如本文另外说明。方法b组合疗法:提取物和另一治疗剂遵循以上方法a,除了向对象开具和施用一或多种其他治疗剂用于治疗缺血性中风或其症状。可在提取物之前、之后或同时施用一或多种其他治疗剂。还可逐步升高(或逐步降低)一或多种其他治疗剂的剂量。实施例6:含有夹竹桃苷的溶液的hplc分析使用以下条件在hplc(waters)上分析样品(夹竹桃苷标准品、scf提取物和热水提取物):symmetryc18柱(5.0μm,150×4.6mmi.d.;waters);流动相为甲醇:水=54:46(v/v)以及流速1.0ml/min。检测波长设为217nm。通过将化合物或提取物溶解在固定量的hplc溶剂中制备样品,以达到夹竹桃苷的近似目标浓度。实施例7:测定正常神经组织中的α3和α1表达可遵循在2008年11月6日以phoenixbiotechnology,inc.(菲尼克斯生物技术公司)名义提交的pct国际申请pct/us08/82641中陈述的程序,其全部公开通过引用结合于本文。实施例8:在针对中风和非中风的体外试验中,对强心苷和本发明提取物的评估方法a中风:制备皮层脑切片和ogd从pnd7sprague-dawley新生大鼠制备新皮层脑切片。解剖大脑皮层,切成400μ厚的切片,并转移至容器,所述容器含有冷的人工脑脊液,其在贴片之前含有1μmmk-801;在任何随后程序中都不包含mk-801。为了使用瞬时氧-葡萄糖剥夺(ogd)来模拟缺血性损伤,将来自每个大脑一半球的切片在低o2(0.5%)环境中暴露于无葡萄糖、n2-鼓泡的人工脑脊液中7.5min。之后将ogd切片与来自对侧半球的对照切片并排铺片在硝化纤维或millicell(millipore)可透过膜上,其除了无ogd以外是同样制备的。铺片后三十分钟,将成对脑切片转染,转移至24孔板,并在37℃、5%co2的湿室中孵育。在每个试验中,使用5-6分钟的氧-葡萄糖剥夺(ogd),以引起24小时内健康皮层细胞的>50%的丧失。使用设定浓度(3μm)的黄夹次苷乙(强心苷)作为内部阳性对照。对于夹竹桃苷(强心苷),从0.3到3μm的所有三个浓度在头两轮试验中显示提供神经保护,因此在第三轮中降低所测试的夹竹桃苷浓度,提示神经保护的阈浓度在0.1和0.3μm之间。还可如针对夹竹桃苷所说明的那样,使用未分级提取物,例如夹竹桃属物种的未分级提取物,或其组分方法b非中风:脑切片试验在“非中风”脑切片上测试夹竹桃苷和pbi-05204(欧洲夹竹桃的未分级scf提取物);所述切片即切片的和转染yfp的,但没有进行经由ogd的额外创伤的切片。参见以上概述的试验程序。我们已观察到许多神经保护化合物,包括黄夹次苷乙,能对此脑切片提供适度水平的神经保护,推测是通过保护避免由切片过程和培养本身引起的创伤。数据证明夹竹桃苷和提取物显示能够对这样的“非ogd”脑切片提供与黄夹次苷乙类似水平的神经保护,预示强心苷甚至在氧和葡萄糖剥夺不存在的情况下介导神经保护。实施例9:在针对阿尔茨海默病的体外试验中评估强心苷和提取物在针对app/aβ引起的皮层锥体神经元退化的大鼠脑切片模型中,使用生物射弹转染必要标记例如yfp以及疾病基因构建体导入脑切片的相同神经元群体中。因此,app/aβ脑切片模型共转染yfp与app同种型,导致在脑切片制备和转染后的三至四天的时期内,皮层锥体神经元的进行性退化。数据证明夹竹桃苷和pbi-05204两者、欧洲夹竹桃的未分级scf提取物显示能够为app转染的脑切片提供浓度依赖的神经保护,从而挽救水平几乎至由bace抑制剂药物所能提供的水平。实施例10:在针对亨廷顿舞蹈症的体外皮质纹状体共培养试验中评估强心苷和提取物在该试验中,不使用完整的脑切片,通过电穿孔将突变htt蛋白导入96孔板中排列的皮层神经元、纹状体神经元和神经胶质的高密度的、混合的共培养物。该试验平台的目标是将复杂的原代培养系统的生物/临床相关性与进行大规模完全自动化筛选的能力相结合,所述原代培养系统概括了体内疾病相关神经元群体的相互关联性的关键方面。在该试验中,在体外1-2周的时期内,转染的突变htt构建体引起纹状体神经元和锥体神经元两者的进行性退化,之后使用自动图像采集和对象检测算法在cellomicsarrayscanvti平台上对所述神经元进行量化。每个数据点获自6个孔,每孔具有在cellomicsarrayscan上使用在与curehuntington'sdiseaseinitiative联合进行大规模筛选期间开发的程序捕获、处理和分析的16个图像。在完整的一轮中,每周期收集并分析约25,000图像,每周4个周期。皮层-纹状体共培养试验平台在神经元平板接种之前制备纯的神经胶质培养物,以建立具有融合神经胶质床的96孔板。之后单独分离皮层和纹状体组织,并用恰当的dna构建体进行“核转染”,随后通过不同荧光蛋白例如yfp、cfp和mcherry的表达可区分皮层和纹状体组织。之后将这些单独转染的皮层和纹状体神经元充分混合,并平板接种至含有之前接种的神经胶质单层的96孔板中。在该皮层-纹状体共培养平台中测试了夹竹桃苷和pbi-05204(欧洲夹竹桃的超临界co2提取物)两者,初步地,这些化合物显示在该试验系统中已评估的>400个晚期药物分子中,是我们迄今为止观察到的最强目标。用于对比,包括了kw6002(腺苷2a受体拮抗剂)的剂量-反应图表,且包含了我们常规地包含作为该共培养试验的阳性对照的化合物。夹竹桃苷的功效与kw6002具有同等水平,然而其效能显示高约100倍(图3a-3d)。实施例11:在针对阿尔茨海默病的体外app试验中评估欧洲夹竹桃的scf提取物的组分根据实施例13制备组分。类似于实施例9进行该试验。图6中的数据证明在防止与app构建体导入相关的神经退化中,存在组分o-4a的浓度依赖效应。特别是,数据证明3至30μg/ml浓度范围之间的神经保护。实施例12:在针对阿尔茨海默病的体外tau4r试验中评估欧洲夹竹桃的scf提取物的组分根据实施例13制备组分。图7中的数据证明在防止与tau构建体导入相关的神经退化中,存在组分o-4a的浓度依赖效应。特别是,数据证明3至30μg/ml浓度范围之间的神经保护。在tau构建体处理的细胞和暴露于组分o-4a溶液的细胞之间存在显著差异。实施例13:scf提取物的色谱分级将夹竹桃叶的超临界提取物(5g)(如本文所述,通过用超临界co2和作为助溶剂/修饰剂加入的乙醇的混合物提取植物物质获得)悬浮在水(150ml)中,并用己烷分配三次(每次150ml)。通过将水层直接负载到水平衡的ods树脂床上,对水层进行odsc-18(十八烷基功能化的硅胶,标记20-22%,200-400目)开柱(400mm(l)x38mm(id))分级。用水与甲醇混合物(水中30%甲醇1000ml,水中55%甲醇1000ml,水中80%甲醇1000ml,100%甲醇1000ml)以及丙酮:甲醇混合物(2体积:1体积;1000ml)依次处理柱。收集来自每个混合物的流出物(1000ml)。通过蒸发从每个组分去除溶剂,产生五个组分,即fr-o-1、fr-o-2、fr-o-3、fr-o-4和fr-o-5。之后如实施例14通过hplc色谱法分析组分。实施例14:scf提取物组分的hplc分析本试验的目的是确定含有强心苷的(来自上述的)提取物组分。如下分析根据实施例13获得的每个组分的样品。将组分1-3mg)溶解在1-5ml含水甲醇中(水中80%甲醇)中。利用agilentzorbaxsb-c18柱,使用水中的80%甲醇作为流动相,流速0.7ml/min,和以下述波长的dad-uv流出物监测,分析稀释的样品(10-25μl):203、210、217、230、254、280、310和300nm。实施例15:用于测定由提取物组分提供的神经保护的脑切片试验根据实施例8进行该试验。数据证明相比于未处理的中风(ogd)引起的脑切片神经元损伤,pbi-05204提供显著水平的保护。类似水平的保护由组分o-4a(图4a和5)以及组分o-3(图4c)和组分o-1(图4d)提供。相反,组分o-2(图4b)和o-5(图4e)证明在中风引起的缺血性脑损伤的该ogd模型中无神经保护效应。实施例16:用于测定神经保护的延时脑切片试验根据实施例8进行该试验,除了以下改变。在ogd和导入建议的神经保护剂之间允许特定的持续时间。测定了如果相对于ogd处理时间而延迟了治疗,pbi-05201为脑切片提供神经保护的能力。数据表明欧洲夹竹桃提取物的2小时延时得到良好耐受,显示与在紧接着ogd处理之后施用pbi-05204获得的类似的神经保护水平。神经保护益处在4至6小时延时施用pbi-05204时下降,但处于仍然显著和生理相关的神经保护水平。实施例17:确定根据实施例13获得的欧洲夹竹桃scf提取物组分中的化合物在减压下蒸发去除fr-o-4组分中的水和甲醇。对来自实施例13fr-o-4组分的残余进行硅胶色谱(以下)以提供亚组分,所述亚组分之后由薄层色谱(tlc)分析。将具有类似tlc特征的组分组合,且通过减压蒸发去除其溶剂。通过hnmr分析剩下的残余。薄层色谱在常规分析级tlc板上,使用己烷:乙酸乙酯(7:3v:v)的混合物完成tlc。用h2so4显示化合物,由此类固醇呈现蓝色,三萜烯呈现紫色。通过快速色谱进一步分级之前,fr-o-4组分的tlc分析表明一个主要点和超过五个小点的存在。显色反应表明该主要点含有类固醇和三萜烯的混合物,多数小点含有类固醇。硅胶快速色谱将硅胶(biotage;10-15g))装柱,用乙酸乙酯(3%)和己烷(97%)的混合物平衡。将来自fr-o-4组分的残余放入乙酸乙酯(3%)和己烷(97%)的混合物(0.2-0.5ml),并负载到柱上。使用乙酸乙酯(3%-30%)在己烷(分别97%-70%)中的溶剂梯度和随后的100%甲醇进行快速色谱。通过tlc(以上)分析从柱收集的亚组分,将具有类似tlc显色特征的那些组分组合并浓缩以去除溶剂。hnmr色谱法通过hnrm,使用常规方法分析来自快速色谱的每个浓缩亚组分的样品,以确定主要成分的结构类型。实施例18:确定未分级形式的根据实施例1(方法b)获得的欧洲夹竹桃scf提取物中的化合物通过ms-darttof分析如下分析scf提取物。使用jeolaccutof-dart质谱仪(jeol美国,peobody,马萨诸塞州,美国)。使用jeolaccutof-dart质谱仪(jeol美国,peabody,马萨诸塞州,美国)。在正离子模式(dart+)下进行分析,产生对应于由dart-ms产生的m+h+离子的质量。使用仪器的一系列设置来确定对于欧洲夹竹桃分析的最佳条件。dart+的一般设置包括:针电压3500v;孔(orifice)1-2–20v;环透镜2–5v;孔2-2–5v;和峰电压1000v。以每个样品使用peg600的10%溶液内部完成校准,所述溶液在整个要求的质量范围100–1000质量单位内提供质量标志物。其他分析在datr模式下进行,这些由以下构成:针电压3500v;加热元件250℃;电极1-150v;电极2-250v;he气体流速3.79lpm。质谱仪设置:mcp2600v;孔1-15v;环透镜-5v,孔2-5v;和峰电压1000v。以每个样品使用全氟化的羧酸溶液内部完成校准,所述溶液在整个要求的质量范围100–1000质量单位内提供标志物。使用硼硅酸盐玻璃熔点管的封闭端将欧洲夹竹桃样品导入dart氦等离子体。每次分析将毛细管保持在he等离子体中约3-5s。通过jeolaccutofdart-ms仪器提供的元素组成和同位素匹配程序确定分子式。使用herbalscience(naples,佛罗里达州,美国)开发的欧洲夹竹桃成分的可搜索数据库。发现scf提取物含有以所标明的相对丰度(%)存在的至少下列成分。成分相对丰度(%)夹竹桃苷2.99夹竹桃苷元3.31乌索酸/白桦脂酸15.29奥多诺苷0.80齐墩果酸0.60乌索-12-烯-3β,28-二醇/白桦脂醇5.443β,3β-羟基-12-齐墩果烯-28-酸14.2628-去甲乌索-12-烯-3β-醇4.94乌索-12-烯-3β-醇4.76如本文所用,除非另外指明,术语“约”或“近似”的含义是特定数值的±10%、±5%、±2.5%或±1%。如本文所用,除非另外指明,术语“实质”含义是“在很大程度上”、“至少大部分”、高于70%、高于85%、高于90%、高于95%、高于98%或高于99%。以上是本发明特定实施方式的详细说明。将理解,尽管本文出于解释目的已说明了本发明特定实施方式,但是可在不脱离本发明精神和范围的条件下进行各种更改。相应地,本发明不受除所附权利要求以外的限制。根据本公开,在不进行过度试验的情况下,可做出和实施本文所公开和要求保护的所有实施方式。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1