利用黑色素校正确定组织氧饱和度的制作方法
本申请要求2016年4月21日递交的62/325,919、2016年4月22日递交的62/326,630、62/326,644和62/326,673以及2016年7月18日递交的62/363,562的美国专利申请的权益。这些申请以及这些申请中引用的所有其他参考文献通过引用并入本申请。
背景技术:
本发明总体涉及监测组织中氧含量的光学系统。更具体地,本发明涉及光学探头(例如,血氧计),其包括光学探头的传感器头上的源和检测器,并且使用局部存储的模拟反射曲线来确定组织的氧饱和度。
血氧计是出于各种目的用于测量人类和生物中组织的氧饱和度的医疗装置。例如,血氧计在医院和其他医疗设施中用于医疗和诊断目的(例如,手术、患者监测、或救护车或用于诸如缺氧等的其他移动监测);运动场上的运动和竞技目的(例如,专业运动员监控);对个体进行个人或家庭监控(例如,一般健康监测、或马拉松人员训练);和兽医目的(例如,动物监测)。
脉搏血氧计和组织血氧计是以不同的原理操作的两种类型的血氧计。脉冲血氧计需要脉冲以起作用。脉搏血氧计通常测量由脉动的动脉血引起的光吸收。相反,组织血氧计不需要脉冲以起作用,并且可以用于对已经与血液供应断开的组织瓣进行氧饱和度测量。
例如,人体组织包括各种光吸收分子。这种发色团包括氧合血红蛋白、脱氧血红蛋白、黑色素、水、脂质和细胞色素。在大部分可见光和近红外光谱范围内,氧合血红蛋白、脱氧血红蛋白和黑色素是组织中最主要的发色团。在某些波长的光下,氧合血红蛋白和脱氧血红蛋白的光吸收显著地不同。组织血氧计可以通过利用这些光吸收差异来测量人体组织中的氧含量。
尽管现有的血氧计成功,但是,仍然希望通过例如提高测量精度;减少测量时间;降低成本;减小尺寸、重量或形状因数;降低功耗;以及其他原因以及这些测量的任何组合来改进血氧计。
具体地,在区域和局部层评估患者的氧合状态非常重要,这是因为它是患者局部组织健康状况的指标。因此,血氧计通常用于怀疑患者的组织氧合状态可能是不稳定的临床环境中(例如,在手术和恢复期间)。例如,在手术期间,血氧计应能够在各种非理想条件下快速地传送准确的氧饱和度测量。虽然现有的血氧计已经足以用于绝对准确性并不重要且仅趋势数据就足够了的术后组织监测,但是在手术期间需要准确性,在手术中,可以使用点检查来确定组织是否仍然存活或需要被移除。
因此,需要改进的组织血氧计探头和使用这些探头进行测量的方法。
技术实现要素:
一种血氧计探头,其在确定组织的氧饱和度时考虑组织颜色(例如,肤色或黑色素含量)以提高准确度。光从光源传输到具有黑色素(例如,真黑素或黑色素)的组织中。由检测器接收从组织反射的光。确定补偿因子以考虑由于黑色素引起的吸收。血氧计使用该补偿因子并确定黑色素校正的氧饱和度值。
在实施方式中,为了计算氧饱和度,血氧计探头利用相对大量的模拟反射曲线来快速确定所研究组织的光学性质。组织的光学性质允许进一步确定组织的氧合血红蛋白浓度和脱氧血红蛋白浓度以及组织的氧饱和度。
在一个实施方式中,血氧计探头可以在不需要脉搏或心跳的情况下测量氧饱和度。本发明的血氧计探头适用于许多医学和手术领域(包括整形手术)。血氧计探头可以在没有脉搏的情况下对组织进行氧饱和度测量。这种组织可能已经与身体(例如组织瓣)分离,并将被移植到身体的其他位置。本发明的各方面也可适用于脉搏血氧计。与血氧计探头相比,脉搏血氧计需要脉搏才能起作用。脉搏血氧计通常测量由脉动的动脉血引起的光吸收。
组织血氧计可以对具有不同黑色素含量的组织产生偏斜的血氧测量。在实施方式中,血氧计探头可以对组织进行血氧测量,其中黑色素的浓度倾向于影响计算的相对氧饱和度测量值。血氧计探头利用黑色素的吸收系数的相对恒定的斜率,其中无论组织的黑色素含量是相对高还是相对低,该斜率都倾向于不改变。血氧计探头使用数学确定性方法,使得黑色素浓度对确定的相对氧饱和度的贡献变为零。因此,不需要确定实际的黑色素浓度以进一步确定目标组织的相对氧饱和度。
在实施方式中,方法包括,将来自血氧计探头的光源的光在待测量的第一位置处传输到第一组织,其中,第一组织包含第一黑色素组分,并且,第一黑色素组分包含真黑素和褐黑素中的至少一种;响应于传输光在血氧计探头的检测器处接收被第一组织反射的光,其中,所接收的光包括由第一黑色素组分引起的第一黑色素吸收分量;确定由组织的黑色素组分引起的黑色素吸收分量的黑色素补偿分量,其中,黑色素吸收分量包含第一黑色素分量并且黑色素组分包括第一黑色素组分;和,使用黑色素补偿分量获得第一组织的黑色素校正的氧饱和度值,其中,黑色素校正的氧饱和度值考虑黑色素吸收分量。
在实施方式中,方法包括:提供包括探头前端的血氧计装置,探头前端包括源结构和检测器结构,其中,血氧计装置将测量包含真黑素和褐黑素的组织的氧饱和度;向血氧计装置提供待测组织的肤色指示;使用肤色指示来计算包含真黑素和褐黑素的组织的氧饱和度,以获得黑色素校正的氧饱和度值;和,在显示器上显示黑色素校正的氧饱和度值。
在实施方式中,系统包括:包括探头前端的血氧计装置,探头前端包括在装置的远端上的源结构和检测器结构以及靠近探头前端的显示器。血氧计装置计算黑色素校正的氧饱和度值并且在显示器上显示黑色素校正的氧饱和度的值。血氧计装置具体地配置为:使用探头前端进行第一测量和第二测量,以确定黑色素校正的氧饱和度值,以及,接收基于第一位置处的第一组织的第一测量的第一信息。在进行第一测量之后和进行第二测量之前,黑色素校正的氧饱和度值不可用于显示。血氧计装置具体地配置为接收基于第二位置处的第二组织的第二测量值的第二信息,其中,第二位置与第一位置不同;使用第一信息和第二信息来确定黑色素校正的氧饱和度值。黑色素校正的氧饱和度值考虑第一组织和第二组织的黑色素组分,并且黑色素组分包括真黑素和褐黑素。以及,血氧计装置配置成在显示器上显示黑色素校正的氧饱和度。
考虑到以下详细描述和附图,本发明的其他目的、特征和优点将变得显而易见,其中在所有附图中相同的附图标记表示相同的特征。
附图说明
图1示出了实施方式中的血氧计探头。
图2示出了实施方式中的探头前端的端视图。
图3示出了实施方式中的血氧计探头的框图。
图4示出了实施方式中的用于通过血氧计探头确定组织(例如,真实组织)的光学性质的方法的流程图。
图5示出了实施方式中的用于通过血氧计探头确定组织的光学性质的方法的流程图。
图6示出了实施方式中的用于通过血氧计探头确定组织的光学性质的方法的流程图。
图7示出了反射曲线的示例图,其可以用于源结构和检测器结构的特定配置,例如,探头前端的源结构和检测器结构配置。
图8示出对于组织中的氧合血红蛋白、脱氧血红蛋白、黑色素和水、任意单位的吸收系数μa与光的波长的曲线图。
图9示出了实施方式中的存储在血氧计探头的存储器中的、针对组织的均匀模型的、模拟反射曲线的数据库的表格。
图10示出了实施方式中的存储在血氧计探头的存储器中的、针对组织的分层模型的、模拟反射曲线的数据库的表格。
图11a-11b示出了用于组织的分层模型的数据库的表格,其中数据库中的各行是从模拟源结构发射并且由模拟检测器结构检测的四个波长的光的四个模拟反射曲线。
图12a-12b示出了用于通过血氧计探头确定组织(例如,真实组织)的光学性质的方法的流程图,其中,血氧计探头使用反射数据和模拟反射曲线来确定光学性质。
图13示出了用于通过血氧计探头确定组织的光学性质的其他方法的流程图。
图14示出了用于加权由选择检测器结构生成的反射数据的方法的流程图。
图15示出了用于确定由血氧计探头测量的组织的相对组织参数的方法的流程图,其中,从相对组织参数中移除组织中黑色素的贡献。
图16a和图16b示出了由多个光波长(例如,760纳米、810纳米、845纳米和895纳米)照射的第一目标组织和第二目标组织的吸收系数的示例图。血氧计探头可以使用其他波长,包括更多或更少的光波长。
图17a示出了第二目标组织(例如,正在重建的乳房)的吸收系数的示例曲线。示例曲线沿曲线的整个长度具有负斜率。
图17b示出了第一目标部位的相对于波长的吸收系数的一阶导数的示例曲线。
图17c示出了第一目标部位的相对于波长的吸收系数的二阶导数的示例曲线。
图17d示出了第一目标组织(例如,健康乳房组织)的吸收系数的示例性第一曲线(例如,第一光谱)和第二目标组织(例如,重建乳房组织)的吸收系数的示例性第二曲线(例如,第二光谱)。
图17e示出了第一目标组织的相对于波长的吸收系数的一阶导数的第一示例图(例如,三个高点),并且示出了第二目标组织的相对于波长的吸收系数的一阶导数的第二示例图(例如,三个低点)。
图17f示出了第一目标位置的相对于波长的吸收系数的二阶导数的第一示例图(例如,两个低点),并且示出了第二目标位置的相对于波长的吸收系数的二阶导数的第二示例图(例如,两个高点)。
图18示出了彼此相对绘制的二阶导数的值在“角度”空间中的矢量。
图19示出了“角度”空间中的第一矢量(θ1,φ1)和第二矢量1903(θ2,φ2)。
图20示出了向量空间中的增量角δθ和δφ中的一者。
图21a示出了完全氧合测量的吸收系数(例如,光谱)的曲线图和完全脱氧测量的吸收系数的曲线图。
图21b示出了完全氧合光谱的相对于波长的一阶导数的曲线图和完全脱氧光谱相对于波长的一阶导数的曲线图。
图21c示出了完全氧合光谱相对于波长的二阶导数的曲线图和完全脱氧光谱相对于波长的二阶导数的曲线图。
图22示出了角度空间中的矢量(δθ,δφ),其中δθ和δφ彼此相对绘制。
图23示出了用于模体的基线校正矢量和校正的计算矢量,其通过比例因子校正了模体和患者组织的血液体积之间的血液体积差异。
图24示出了投射到模体矢量上的患者组织的矢量。
具体实施方式
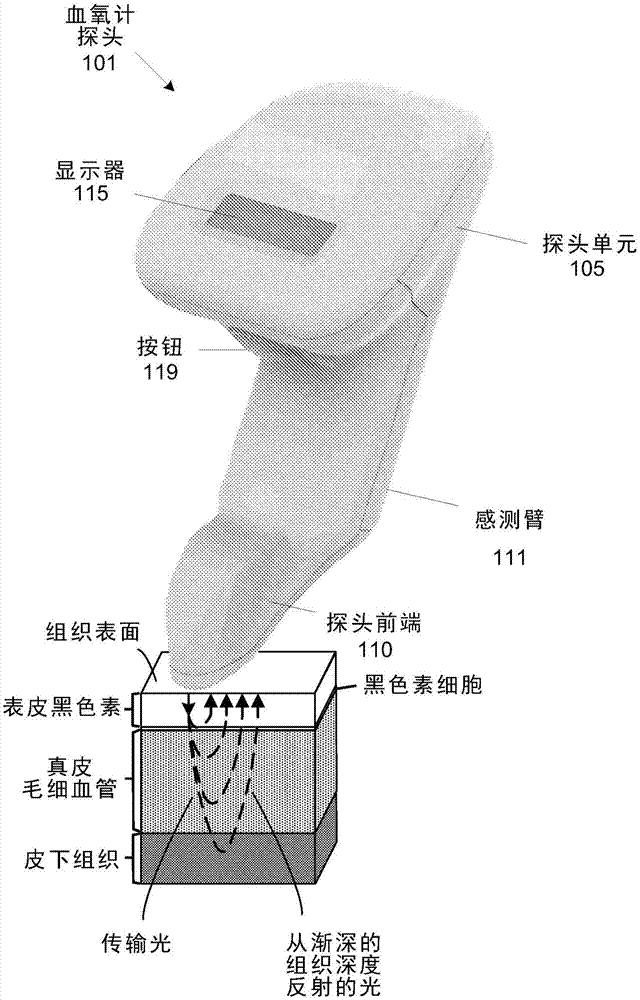
图1示出了实施方式中的血氧计探头101的图像。血氧计探头101被配置为(例如,在术中和术后)进行组织血氧测量。血氧计探头101可以是手持装置,该手持装置包括探头单元105、可以位于感测臂111的一端处的探头前端110(也称为传感器头)。血氧计探头101被配置为通过从探头前端110向组织发射光(例如,近红外光)并且在探头前端处收集从组织反射的光来测量组织的氧饱和度。
血氧计探头101包括向用户通知由血氧计探头进行的氧饱和度测量的显示器115或其他通知装置。虽然探头前端110被描述为被配置为与作为手持装置的血氧计探头101一起使用,但是,探头前端110可以与其他血氧计探头一起使用,例如,模块化血氧计探头,其中,探头前端位于耦合到基本单元的线缆装置的一端处。线缆装置可以是配置为与一个患者一起使用的一次性设备,并且,基本单元可以是配置为重复使用的装置。这种模块化血氧计探头对于本领域技术人员是很好理解的,并且不再进一步描述。
图2示出了实施方式中的探头前端110的端视图。探头前端110被配置成接触将要进行组织血氧测量的组织(例如,患者的皮肤)。探头前端110包括第一源结构120a和第二源结构120b(统称为源结构120)并且包括第一检测器结构、第二检测器结构、第三检测器结构、第四检测器结构、第五检测器结构、第六检测器结构、第七检测器结构和第八检测器结构125a-125h(统称为检测器结构125)。在替代实施方式中,血氧计探头包括更多或更少的源结构,包括更多或更少的检测器结构,或以上两者。
每个源结构120适于发射光(例如,红外光)并且包括一个或多个光源,例如,产生发射光的四个光源。每个光源可以发射一个或多个波长的光。每个光源可包括发光二极管(led)、激光二极管、有机发光二极管(oled)、量子点led(qmled)或其他类型的光源。
每个源结构可包括一个或多个光纤,该光纤将光源光学地链接到探头前端的面127。在实施方式中,每个源结构包括四个led并且包括将四个led光学耦合到探头前端的面的单个光纤。在替代实施方式中,每个源结构包括多于一个的光纤(例如,四个光纤),其将led光学耦合到探头前端的面。
每个检测器结构包括一个或多个检测器。在实施方式中,每个检测器结构包括适于检测从源结构发射并从组织反射的光的单个检测器。检测器可以是光电探测器、光敏电阻器或其他类型的检测器。检测器结构相对于源结构定位,使得产生两个或更多(例如,八个)唯一源-检测器距离。
在实施方式中,最短源-检测器距离近似相等。例如,在源结构120a和检测器结构125d之间(s1-d4)以及源结构120b和检测器结构125a之间(s2-d8)的最短源-检测器距离近似相等。源结构120a和检测器结构125e(s1-d5)之间以及源结构120b和检测器结构125a之间(s2-d1)的下一个较长源-检测器距离(例如,比s1-d4和s2-d8中的每一个长)大致相等。源结构120a和检测器结构125c之间(s1-d3)以及源结构120b和检测器结构125g之间(s2-d7)的下一个较长源-检测器距离(例如,比s1-d5和s2-d1中的每一个长)大致相等。源结构120a和检测器结构125f之间(s1-d6)以及源结构120b和检测器结构125b之间(s2-d2)的下一个较长源-检测器距离(例如,比s1-d3和s2-d7中的每一个长)大致相等。源结构120a和检测器结构125c之间(s1-d2)以及源结构120b和检测器结构125f之间(s2-d6)的下一个较长源-检测器距离(例如,比s1-d6和s2-d2中的每一个长)大致相等。源结构120a和检测器结构125g之间(s1-d7)以及源结构120b和检测器结构125c之间(s2-d3)的下一个较长的源-检测器距离(例如,比s1-d2和s2-d6中的每一个长)大致相等。源结构120a和检测器结构125a(s1-d1)之间以及源结构120b和检测器结构125e之间(s2-d5)的下一个较长源-检测器距离(例如,比s1-d7和s2-d3中的每一个长)大致相等。在源结构120a和检测器结构125h之间(s1-d8)以及源结构120b和检测器结构125d之间(s2-d4)的下一个较长源-检测器距离(例如,最长源-检测器距离,比s1-d1和s2-d5中的每一个长)近似相等。在其他实施方式中,所有源-检测器距离可以都是唯一的,或者具有少于八个的大约相等的距离。
以下表1示出了根据实施方式的八个唯一的源-检测器距离。最接近的源-探测器距离之间的增加约为0.4毫米。
表1
在实施方式中,检测器结构125a和125e关于在连接源120a和120b的直线上的点对称地定位。检测器结构125b和125f关于该点对称地定位。检测器结构125c和125g关于该点对称地定位。检测器结构125d和125h关于该点对称地定位。该点可以在连接线上相对于源结构120a和120b居中。
源-检测器距离与由检测器结构125检测的反射的关系图可以提供反射曲线,其中数据点沿x轴良好地间隔开。源结构120a和120b与检测器结构125之间的距离的这些间距减小了数据冗余并且可以导致产生相对精确的反射曲线。
在实施方式中,源结构和检测器结构可以布置在探头表面上的各个位置处以给出期望的距离(例如上面指出的)。例如,两个源形成一条线,并且在该线的上方和下方将有相同数量的检测器。以及,(在该线的上方的)探测器的位置与(在该线的下方的)其他探测器关于两个源的线上的选择点点对称。作为示例,选择点可以是两个源之间的中间点,但这不是必需的。在其他实施方式中,可以基于形状(例如,圆形、椭圆形、卵形、随机地、三角形、矩形、正方形或其他形状)来布置定位。
以下专利申请描述了各种血氧计装置和血氧测定操作,并且以下申请中的讨论可以以任何组合与本申请中描述的本发明的方面组合。以下专利申请通过引用与这些申请中引用的所有参考文献一起并入本申请,2015年11月17日递交的14/944,139、2013年5月3日递交的13/887,130、2016年5月24日递交的15/163,565、2013年5月3日递交的13/887,220、2016年7月19日递交的15/214,355、2013年5月3日递交的13/887,213、2015年12月21日递交的14/977,578、2013年6月7日递交的13/887,178、2016年7月26日递交的15/220,354、2013年8月12日递交的13/965,156、2016年11月22日递交的15/359,570、2013年5月3日递交的13/887,152、2016年4月16日递交的29/561,749、2012年5月3日递交的61/642,389、61/642,393、61/642,395、61/642,399和2012年8月10日递交的61/682,146。
图3示出了实施方式中的血氧计探头101的框图。血氧计探头101包括显示器115、处理器116、存储器117、扬声器118、一个或多个用户选择装置119(例如,与显示器115相关联的一个或多个按钮、开关、触摸输入装置)、源结构组120、检测器结构组125和电源(例如,电池)127。前面列出的部件可以通过总线128链接在一起,总线128可以是血氧计探头101的系统总线架构。尽管这个图示出了连接到每个部件的一个总线,但是,该总线用于说明用于链接这些部件或包括在血氧计探头101中的其他部件的任何互连方案。例如,扬声器118可以通过端口连接到子系统或具有到处理器116的内部直接连接。此外,在实施方式中,所描述的部件容纳在的血氧计探头101的移动壳体(参见图1)中。
处理器116可以包括微处理器、微控制器、多核处理器或其他处理器类型。存储器117可以包括各种存储器,例如,易失性存储器117a(例如,ram)、非易失性存储器117b(例如,硬盘或flash)。血氧计探头101的不同实施方式可以包括任何组合或配置的任何数量的列出的部件,并且还可以包括未示出的其他部件。
电源127可以是电池,例如,一次性电池。一次性电池在储存的电荷消耗后被丢弃。一些一次性电池化学技术包括碱性、锌碳或氧化银。电池具有足够的存储电量,以允许手持装置使用数小时。在实施方式中,血氧计探头是一次性的。
在其他实施方式中,电池是可充电的,其中,电池可以在存储的电荷消耗之后多次充电。一些可充电电池化学技术包括镍镉(nicd)、镍金属氢化物(nimh)、锂离子(li离子)和锌空气。例如,可以通过带有连接到手持单元的电源线的ac适配器对电池进行充电。手持单元中的电路可以包括充电器电路(未示出)。具有可充电电池化学的电池有时可用作一次性电池,其中,电池不充电但在使用后丢弃。
组织分析。图4示出了在实施方式中用于通过血氧计探头101确定组织(例如,真实组织)的光学性质的方法的流程图。血氧计用于测量具有黑色素的组织,例如皮肤。黑色素影响氧饱和度测量,因为黑色素吸收光。肤色因人而异,从非常黑的皮肤到非常浅的皮肤。取决于存在的黑色素的量(其将根据例如肤色而变化),吸收量可对测量产生实质性影响,使得测量值不准确。
因此,需要一种考虑被测组织的黑色素成分的血氧计,使得无论肤色如何,所测量的氧饱和度值都是准确的。计算并补偿组织的黑色素成分的测量的氧饱和度值可以称为黑色素校正的氧饱和度值。
皮肤中的黑色素是真黑素(eumelanin)和褐黑素(pheomelanin)(例如,两种黑色素组分),其是各种相对百分比的天然存在的黑色素。相反,人体内的大多数内部器官和组织都没有黑色素。因此,当使用血氧计对这种内部组织进行氧饱和度测量时,不需要考虑黑色素。然而,人脑具有神经黑色素,其在身体的其他部位、尤其是皮肤中不存在。
在实施方式中,血氧计确定并校正具有真黑素和褐黑素色素的皮肤组织(和任何其他组织)中的黑色素吸收。这种血氧计不考虑和校正神经黑色素或合成黑色素,这是因为在皮肤中没有发现它们。在其他实施方式中,血氧计确定并校正由于多种黑色素(包括真黑素、褐黑素、神经黑色素或合成黑色素、或其任何组合)引起的黑色素吸收。
血氧计探头使用确定的黑色素含量(例如,真黑素含量、褐黑素含量、或者真黑素和褐黑素两者的含量)用于组织,以校正由血氧计探头测量的各种组织参数。流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在400处,黑色素读取器光学地耦合到(例如,接触)组织。黑色素读取器是光电装置,其适于将光发射到组织中(步骤405),并且在光已经透过组织或从组织反射之后检测光(步骤410)。由黑色素读取器检测到的光被转换成电信号(步骤415),该电信号由装置用于确定组织的黑色素含量(步骤420)。黑色素读取器可以在读取器的显示器上或通过有线或无线输出来输出黑色素含量的值(步骤425)。黑色素含量的值表示真黑素含量、褐黑素含量或真黑素和褐黑素两者含量的值。
在实施方式中,在430处,将关于黑色素含量的信息(例如,数值)输入血氧计探头101。可以经由用户(例如,人类用户)或通过黑色素读数器和血氧计探头之间的有线或无线通信将该信息输入血氧计探头。
在第一实施方式中,在435处,血氧计探头使用黑色素含量的信息来调节由探头产生的一个或多个测量值。在实施方式中,血氧计探头确定组织的氧饱和度的值。之后,血氧计探头使用黑色素含量的信息(例如,真黑素含量、褐黑素含量或真黑素和褐黑素两者含量的信息)调节氧饱和度的值。血氧计探头可以通过一个或多个算术运算、数学函数或两者来调节氧饱和度的值。例如,黑色素含量的信息可以用作偏移(例如,加法偏移)、比例因子或两者以用于调节氧饱和度的值。
在替代实施方式中,在435处,血氧计探头针对由血氧计探头发射和检测的多个波长的光(例如,四个波长的光),确定组织的吸收系数μa(mua)、约化散射系数μs’(musprime)或两者。此后,血氧计探头使用关于黑色素含量(例如,真黑素含量、褐黑素含量或者黑色素和褐黑素素两者的含量)的信息针对每个波长的光,调节确定的吸收系数(μa)值。血氧计探头可以通过一个或多个算术运算、数学函数或两者来调节吸收系数(μa)值。例如,黑色素含量的信息可以用作偏移(例如,加法偏移)、比例因子或两者以用于调节吸收系数(μa)值。此后,血氧计探头使用吸收系数(μa)值来确定组织的氧饱和度值。下面描述吸收系数(μa)和约化散射系数(μs)的确定。
在其他实施方式中,在435处,血氧计探头将一个或多个黑色素校正函数应用于由检测器结构产生的反射数据。黑色素校正函数基于黑色素含量(例如,真黑素含量、褐黑素含量、或真黑素和褐黑素两者的含量)的信息。反射数据可以是在由血氧计探头的一个或多个电子部件数字化之前由检测器结构产生的模拟反射数据,或者反射数据可以是数字化的反射数据。黑色素校正函数可以应用于模拟反射数据或数字化反射数据。黑色素校正函数包括应用于反射数据的一个或多个数学运算。比例因子由血氧计探头基于输入血氧计探头的黑色素含量的信息确定。对于由血氧计探头发射的每个波长的光,可以针对黑色素含量调节反射数据。
在实施方式中,黑色素校正函数可以是与一个或多个校准函数(例如,具有比例因子)组合的组合函数(例如,具有比例因子)。校准函数可以包括用于基于各种因素(例如,由于制造而产生的差异、由于检测器结构的温度漂移而产生的差异、或者其他考虑因素而产生的差异)校正检测器响应的比例因子。在通过血氧计探头调节反射数据之后,探头可以确定待测组织中血液的氧饱和度。
图5示出了实施方式中的用于通过血氧计探头101确定组织的光学性质的方法的流程图。血氧计探头使用关于组织的黑色素含量的信息(例如,真黑素含量、褐黑素含量、或者真黑素和褐黑素含量两者的信息)来校正由血氧计探头测量的各种组织参数。流程图表示一个示例实施方式。在不偏离实现范围的情况下,可以在流程图中添加、移除或组合步骤。
在500处,将组织的颜色与多个颜色样本(有时称为颜色样品)的两个或更多个颜色样本进行比较,以确定颜色样本的一个颜色是否与组织的颜色大致匹配。用于颜色比较的每种颜色样本与黑色素含量的值相关联。标识颜色样本的黑色素含量的信息(例如,数值)可以位于颜色样本上。在实施方式中,颜色是新泽西州卡尔士达特市的彩通公司(pantonellc)的
组织的颜色和颜色样本的颜色之间的比较可以通过颜色比较工具(例如,密歇根州的大急流城成立的x-rite的一个或多个颜色比较工具)来执行。在实施方式中,比较可以由人(例如患者或医疗提供者)在视觉上执行。在实施方式中,血氧计探头适于确定组织的黑色素含量的值,该值可以显示在探头的显示器上。
在505处,在比较之后,基于比较确定组织的黑色素含量的值。
在替代实施方式中,黑色素含量的值是基于有限范围的黑色素含量值由含量的估计值确定的。黑色素含量范围内的值的数量可包括两个或更多个值。
例如,黑色素含量范围内的值的数量可以是2(例如,二元水平),例如,对于浅色组织为1(例如,第一水平黑色素含量的第一皮肤水平)以及对于黑色组织为2(例如,第二水平黑色素含量的第二皮肤水平),该数量可以是3(例如,对于浅色组织颜色为1,对于比1深的中等颜色组织为2,对于比1和2深的深色组织为3),或该数量对于不同肤色为4、5、6、7、8、9、10或更多。可以由患者或医疗提供者提供对黑色素含量的值的估计。
在510处,可以将关于黑色素含量的信息输入血氧计探头。可以在其中血氧计探头确定黑色素含量的值的方法中跳过步骤510。可以将按钮119激活预定次数以将血氧计探头置于数据输入模式,其中,可以在数据输入模式中输入黑色素含量的信息。此后,可以经由与探头的有线通信、经由与探头的无线通信、经由显示器(如果显示器是触摸界面显示器)、经由可听接口(例如,探头中的麦克风和语音识别软件)、或经由其他输入技术,通过进一步激活按钮将黑色素含量的信息输入到探头中。或者,按钮接口可以在屏幕上提供(例如,通过与处理器的交互)用于黑色素含量(例如,针对浅色和深色皮肤为1和2,针对浅色、中等和深色皮肤为1、2和3,或更多用户可选择水平)的可选择的选项(或以其他方式提供的选项,例如点亮的led)。在显示器是触摸界面显示器的情况下,用于黑色素水平的用户可选择的选项可以显示在显示器上,其中用户可以触摸那些选择。在血氧计装置的实施方式中,可以使用其他输入装置(例如,鼠标、外部键盘或其他装置)操作,用户可以使用这些装置中的一个或多个来选择用户可选择的黑色素选项。
在515处,血氧计探头适于使用关于黑色素含量的信息来调节由血氧计探头执行的一个或多个测量或计算。例如,血氧计探头可以使用该信息来调节组织的氧饱和度值、调节吸收系数(μa)、约化散射系数(μs’)、调节由一个或多个探测器产生的值,或者这些调节的一个或多个的组合。以上关于步骤435进一步描述了这些调节中的每一个。
图6示出了实施方式中的用于通过血氧计探头101确定组织的光学性质的方法的流程图。血氧计探头使用组织的确定的黑色素含量来校正由探头测量的各种组织参数。流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在600处,用血氧计探头进行组织的一次或多次对侧测量。在使用血氧计探头对待测量的目标组织(例如,要确定组织健康的乳房组织,例如右乳房、第一目标组织是乳房左侧的所在乳房的右侧)进行测量之前,使用血氧计探头在组织的一部分上(例如,健康的乳房组织、左乳房、乳房的左侧)进行对侧测量。可以针对由血氧计探头发射的每个波长的光进行组织的对侧测量。
在605处,由检测器结构产生的反射数据由血氧计探头的电子元件数字化并存储在存储器中。反射数据为随后的组织测量提供了比较的基础。例如,对侧测量提供对侧组织的黑色素含量的基线测量,其中处理器可以使用该基线测量来校正由血氧计探头进行的各种测量。
在610处,通过血氧计探头进行待测量的目标组织的血氧测量。
在615处,在实施方式中,处理器使用血氧测量来生成目标组织的氧饱和度值。此后,处理器检索在605处存储的对侧组织的存储反射数据,并使用检索的值来调节氧饱和度值。也就是说,处理器使用健康对侧组织的黑色素含量的基线测量来调节目标组织的氧饱和度值。
在615处,在替代实施方式中,处理器由目标组织的血氧测量来确定吸收系数μa、约化散射系数μs’或两者。此后,处理器检索在605处存储的对侧组织的反射数据,并使用检索的值来调节μa、μs或两者。然后,处理器使用调节后的μa值来计算目标组织的氧合血红蛋白、脱氧血红蛋白的值或其他值。也就是说,处理器使用健康对侧组织的黑色素含量的基线测量来调节目标组织的μa。
在615处,在另一替代实施方式中,处理器检索在605处存储的对侧组织的存储反射数据,并使用所检索的值来调节由检测器结构针对目标组织生成的反射数据。由处理器施加到反射数据的调节可以是简单的偏移(例如,加法偏移)、比例因子(例如,乘法偏移)、功能校正、其他校正、或任何一个或这些调节的任何组合。也就是说,处理器使用针对健康组织的黑色素含量的基线测量来调节由检测器结构产生的值,以调节目标组织的反射数据。
存储的模拟反射曲线。根据实施方式,存储器117存储多个蒙特卡罗模拟的反射曲线315(“模拟反射曲线”),其可以由计算机生成以随后存储在存储器中。每个模拟反射曲线315表示从一个或多个模拟源结构发射到模拟组织中并从模拟组织反射到一个或多个模拟检测器结构中的光(例如,近红外光)的模拟。模拟反射曲线315用于模拟源结构和模拟检测器结构的特定配置,例如,具有以上关于图2描述的源-探测器间距的探头前端110的源结构120a-120b和探测器结构125a-125h的配置。
因此,模拟反射曲线315模拟从源结构发射并由血氧计探头101的检测器结构收集的光。此外,每个模拟反射曲线315表示独特的真实组织状况,例如,与特定浓度的组织发色团和特定浓度的组织散射体有关的特定组织吸收值和组织散射值。例如,可以针对具有各种黑色素含量、各种氧合血红蛋白浓度、各种脱氧血红蛋白浓度、各种水浓度、水浓度静态值、各种脂肪浓度、脂肪浓度的静态值、或各种吸收(μa)值和约化散射(μs’)值的模拟组织生成模拟反射曲线。
存储在存储器117中的模拟反射曲线的数量可以相对较大并且可以代表可以存在于通过血氧计探头101分析其存活力的真实组织中的光学性质和组织性质的几乎全部(如果不是全部)实际组合。虽然存储器117被描述为存储蒙特卡罗模拟的反射曲线,但是,存储器117可以存储通过除蒙特卡罗方法之外的方法(例如,使用扩散近似)产生的模拟反射曲线。
图7示出了反射曲线的示例图,其可以用于源结构120和检测器结构125的特定配置,例如,探头前端110的配置源结构和检测器结构。图的横轴表示源结构120和检测器结构125之间的距离(即,源-检测器距离)。如果适当地选择源结构120和检测器结构125之间的距离,并且模拟反射曲线是针对源结构120和检测器结构125的模拟,则模拟反射曲线中的数据点之间的横向间距将是相对均匀的。在图7中的模拟反射曲线中可以看到这种均匀间距。图的纵轴表示从组织反射并由检测器结构125检测的光的模拟反射。如模拟反射曲线所示,到达探测器的结构125的反射光随着源结构和探测器结构之间的距离而变化,并且在较小的源-探测器距离处检测到的反射光多于在较大的源-探测器距离处检测到的反射光。
图8示出了对于一些重要组织发色团的吸收系数μa与光的波长的关系图,上述组织发色团包括:含有氧合血红蛋白的血液、含有脱氧血红蛋白的血液、黑色素和水。在实施方式中,用于产生模拟反射曲线的蒙特卡罗模拟是可能存在于组织中的一种或多种选择发色团的函数。发色团可以包括黑色素、氧合血红蛋白、脱氧血红蛋白、水、脂质、细胞色素或其他发色团的任何组合。在大部分可见光和近红外光谱范围内,氧合血红蛋白、脱氧血红蛋白和黑色素是组织中最主要的发色团。
在实施方式中,存储器117存储每个模拟反射曲线315的选择数量的数据点,并且可以不存储整个模拟反射曲线。针对每个模拟反射曲线315存储的数据点的数量可以与源-检测器对的数量匹配。例如,如果探头前端110包括两个源结构120a-120b并且包括八个检测器结构125a-125h,则血氧计探头101包括十六个源-检测器对,并且存储器117因此可以针对由源结构120a或源结构120b发射的每个波长的光,为每个模拟反射曲线存储十六个选择数据点。在实施方式中,所存储的数据点用于探头前端110的特定源-测器距离,例如,表1中所示的那些距离。
因此,存储在存储器117中的模拟反射曲线数据库的大小可以是16×5850,其中,对于可以由每个源结构120生成和发射并由每个检测器结构125测量的每条曲线存储16个点,其中,存在跨越光学性质范围的总共5850条曲线。或者,存储在存储器117中的模拟反射曲线数据库的大小可以是16×4×5850,其中,对于可以由每个源结构生成和发射的四个不同波长每条曲线存储16个点,并且存在跨越光学性质范围的总共5850条曲线。例如,5850曲线来自39个散射系数μs’值和150个吸收系数μa值的矩阵。在其他实施方式中,更多或更少的模拟反射曲线存储在存储器中。例如,存储在存储器中的模拟反射曲线的数量可以从大约5000条曲线、到大约250,000条曲线、到大约400,000条曲线或更多。
约化散射系数μs’值可以在5:5:24/厘米的范围内。μa值可以在0.01:0.01:1.5/厘米的范围内。应当理解,前面描述的范围是示例范围,并且源-检测器对的数量、每个源结构产生和发射的波长数和模拟反射曲线的数量可以更小或更大。
图9示出了实施方式中的存储在血氧计探头的存储器中的模拟反射曲线315的数据库900。该数据库用于均匀的组织模型。数据库中的每一行表示从蒙特卡罗模拟生成的一个模拟反射曲线,该蒙特卡罗模拟针对从两个模拟源结构(例如,源结构120a-120b)发射到模拟组织中并且在从模拟组织反射之后由八个模拟检测器结构(例如,检测器结构125a-125h)检测到的模拟光。用于生成数据库的模拟反射曲线的蒙特卡罗模拟用于均匀组织模型。均匀组织模型的模拟组织具有从组织表面到表皮、真皮和皮下组织的均匀光学性质。也就是说,对于蒙特卡罗模拟,表皮、真皮和皮下的光学性质是相同的。在数据库中,每个模拟的反射曲线与吸收(μa)值和约化散射(μs’)值相关联。数据库中的每个模拟反射曲线可以与其他发色团的值相关联。
模拟反射曲线的数据库可以包括模拟反射的实际值(例如,浮点值),或者可以包括模拟反射的实际值的索引值(例如,二进制值)。如
图9所示,数据库包括模拟反射的实际值的索引值(例如,二进制值)。数据库可以包括例如根据输入的准确性的各种长度的二进制字。二进制字可以是2位长度、4位长度、8位长度、16位长度、32位长度或其他长度。
在实施方式中,在将用于曲线的值输入数据库之前,将一个或多个数学变换应用于模拟的反射曲线。数学变换可以改善由检测器结构产生的反射数据到模拟反射曲线的拟合。例如,可以将对数函数应用于模拟反射曲线,以改善由检测器结构生成的测量数据到模拟反射曲线的拟合。
当进行血氧测量时,每个波长的发射光的反射数据由检测器结构检测并分别拟合到数据库900的模拟反射曲线。对于拟合为模拟反射曲线的每个波长的发射光的反射数据,血氧计探测器确定吸收μa值、约化散射μs’值或这两者的数值。例如,针对第一波长的光的第一组反射数据被拟合为模拟反射曲线,以确定吸收μa和约化散射μs’中的一个或多个(例如,第一组组织参数)。以下进一步描述将反射数据拟合为模拟反射曲线。
此后,将针对第二波长的光的第二组反射数据拟合为数据库900中的模拟反射曲线,以确定针对第二波长的吸收μa和约化散射μs’中的一个或多个(例如,第二组组织参数)。此后,将针对第三波长的光的第三组反射数据拟合为数据库900中的模拟反射曲线,以确定吸收μa和约化散射μs’中的一个或多个(例如,第三组组织参数)。此后,将针对第四波长的光的第四组反射数据拟合为数据库900中的模拟反射曲线,以确定针对第四波长的吸收μa和约化散射μs’中的一个或多个(例如,第四组组织参数)。
然后,血氧计探头可以利用全部四组组织参数来确定组织的各种值,例如,氧合血红蛋白浓度、脱氧血红蛋白浓度、黑色素含量或其他参数。
图10示出了实施方式中的存储在血氧计探头的存储器中的模拟反射曲线的数据库1000。该数据库用于组织的分层模型(例如,分层皮肤)。生成模拟反射曲线的蒙特卡罗模拟使用分层组织模型进行模拟。分层组织可包括两层或更多层。在实施方式中,分层组织包括两层组织。两层组织具有不同的光学性质,例如不同的吸收μa、约化散射μs’、或这两种性质都不同。
在一个实施方式中,第一模拟组织层用于表皮,第二模拟组织层用于真皮。蒙特卡罗模拟中使用的表皮的厚度可以为约40微米至约140微米。例如,表皮的厚度可以是40微米、50微米、60微米、70微米、80微米、90微米、100微米、110微米、120微米、130微米、140微米或其他厚度。蒙特卡罗模拟中使用的真皮的厚度可以从小于1毫米到有效无限厚度,例如12毫米或更大。
当针对真皮产生模拟反射曲线时,可以改变表皮的一种或多种光学性质。例如,当针对真皮产生模拟反射曲线时,可以改变表皮的黑色素含量。或者,当针对真皮产生模拟反射曲线时,可以改变表皮的μa。
在实施方式中,数据库1000包括针对由表皮和真皮的组合反射的光的模拟反射曲线。
用于由血氧计探头测量的真实组织的、针对由源结构发射并由检测器结构检测的每个波长的光的反射数据由处理器一次一个地拟合为模拟反射曲线。基于对数据库中的一个或多个模拟反射曲线的拟合,血氧计探头针对一层或两层的真实组织确定吸收μa和约化散射μs’中的一个或两个。由针对一层确定的吸收(μa)值,血氧计探头确定组织的氧合血红蛋白浓度和脱氧血红蛋白浓度。
图11a-11b示出了在实施方式中存储在血氧计探头的存储器中的模拟反射曲线的数据库1110。该数据库用于分层组织模型。数据库中的每行包括针对从模拟源结构发射并由模拟探测器结构检测的四个波长的光中的每一个的模拟反射曲线。四个模拟反射曲线的每行包括针对每个模拟反射曲线的16个值。更具体地,每行包括针对源结构120a-120b和检测器结构125a-125h的16个源-检测器距离的16个值。总的来说,每行包括针对从两个模拟源结构发射并由八个模拟探测器结构检测的四个波长的光的四个模拟反射曲线的64个值。
如果从源结构发射更多或更少的波长,则数据库1110的分层组织模型可以每行包括更多或更少的模拟反射曲线。如果例如在探头前端中包括一个或多于两个源结构、在探头前端中包括更多或更少的检测器结构或者两者,则数据库1110可以针对每个模拟反射曲线包括多于或少于16个值。
数据库1110的每行的四个模拟反射曲线中的每一个与四个组织参数(包括黑色素含量、血液体积、散射和氧饱和度(氧合血红蛋白相对于组织的总血红蛋白的分数))相关联。数据库1110中可以包括更多或更少的组织参数。
当用于由血氧计探头测量的组织的、由检测器结构125a-125h生成的一组检测器值被处理器拟合为一个或多个行时,血氧计探头由此以任何组合确定一种或多种组织参数,例如黑色素含量、血液体积、散射和氧饱和度。在实施方式中,血氧计探头适于确定组织的氧饱和度并在显示器上显示氧饱和度的值。
如上面简要描述的,数据库1110包括用于分层组织模型的模拟反射曲线315。模拟组织的层可包括表皮、真皮、皮下组织或这些层中的一个或多个的任何组合。这些层可以包括更高分辨率的皮肤形态,例如网状真皮和浅表丛。产生模拟反射曲线的蒙特卡罗模拟可以针对包括在组织层中的各种发色团模拟组织。例如,蒙特卡罗模拟可以使用针对具有各种黑色素含量的表皮的组织模型,但是可以不使用针对包括血液的表皮的组织模型。蒙特卡罗模拟可以使用针对具有各种血液体积和各种氧饱和度的真皮层的组织模型。在实施方式中,蒙特卡罗模拟不使用针对包括黑色素的真皮的组织模型。类似地,蒙特卡罗模拟可以使用具有各种血液体积和各种氧饱和度的脂肪组织的组织模型。在实施方式中,蒙特卡洛模拟不使用针对具有黑色素的脂肪组织的组织模型。针对组织层的组织模型可以包括其他组织发色团的浓度,例如水和脂肪,其中这些发色团的浓度是相对典型的生理值。
在实施方式中,蒙特卡罗模拟生成模拟反射曲线所使用的各种发色团浓度跨越存在于真实组织中的相对大且相对准确的实际生理值范围。可以改变包括在实际生理值范围内的值的数量,以平衡组织血氧计测量的各种参数。例如,用于模拟组织中发色团浓度范围的值的数量可以相对较高或较低,并且影响由血氧计探头进行的测量的准确度。在实施方式中,对于模拟表皮组织中的光吸收,在蒙特卡洛模拟中使用黑色素含量范围的355个值。在实施方式中,对于模拟真皮组织中的光吸收,在蒙特卡洛模拟中使用黑色素含量范围的86个值。对于模拟表皮组织和模拟真皮组织中的散射,在蒙特卡罗模拟中使用65个值。在其他实施方式中,这些值的数量是不同的。
组织分析。图12a-12b示出了用于通过血氧计探头101确定组织(例如,皮肤)的光学性质的方法的流程图,其中,血氧计探头使用反射数据和模拟反射曲线315来确定光学性质。光学性质可以包括组织的吸收系数μa和约化散射系数μs’。以下进一步详细描述组织的吸收系数μa转换为组织的氧饱和度值的另一种方法。流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在1200处,血氧计探头101将光(例如,近红外光)从源结构120之一(例如源结构120a)发射到组织中。当光从源结构发射时,血氧计探头通常与组织接触。在发射的光从组织反射之后,检测器结构125检测该光的一部分(步骤1205),并且产生组织的反射数据点(步骤1210)。可以针对多个波长的光(例如,红色、近红外光或两者)和一个或多个其他源结构(例如,源结构120b)重复步骤1200、1205和1210。如果例如组织血氧计探头115具有十六个源-检测器距离,则单个波长的反射数据点可以包括十六个反射数据点。反射数据点有时被称为反射数据点的n向量。
在1215处,针对源-检测器对的增益校正反射数据点(例如,原始反射数据点)。在校准源-检测器对期间,针对源-检测器对产生增益校正并将其存储在存储器117中。以下进一步详细描述增益校正的产生。
在1220处,处理器116将(例如,通过误差平方和计算)反射数据拟合为模拟反射曲线315,以确定对反射数据点拟合最佳(即,具有最低拟合误差)的特定反射数据曲线。存储在存储器中并且拟合为反射数据的数据库可以是数据库900、数据库1000或数据库1100。在特定实施方式中,作为模拟反射曲线的数据库的“粗”网格的、相对较小的模拟反射曲线组被选择并且并用于拟合步骤1220。例如,对于给定39个散射系数μs’和150个吸收系数μa值的数据库900,模拟反射曲线的粗网格可以由处理器116通过采用针对粗网格中的总共40个模拟反射曲线的每第5个散射确定系数μs’值和每第8个吸收系数μa来确定。可以理解,前述特定值是用于示例实施方式的,并且处理器116可以利用其他尺寸的粗网格。将反射数据点拟合为粗网格的结果是最佳拟合模拟反射曲线的粗网格中的坐标(μa,μs’)粗。对于数据库1000,粗网格将覆盖每层中的吸收和约化散射。用于数据库1000的方法的以下每个步骤将针对每层的μa和μs’进行调节。对于数据库1100,粗网格将覆盖黑色素含量、氧饱和度、血液体积和散射。用于数据库1100的方法的以下每个步骤将针对黑色素含量、氧饱和度、血液体积和散射而非μa和μs’进行调节。
在1225处,处理器116利用来自具有最低拟合误差的粗网格的特定模拟反射曲线来定义模拟反射曲线的“细”网格,其中,细网格中的模拟反射曲线在来自具有最低拟合误差的粗网格的模拟反射曲线周围。
也就是说,细网格是定义的尺寸,其以来自粗网格的最低误差模拟反射曲线定义精细网格的中心。细网格可以具有与粗网格相同数量的模拟反射曲线,或者它可以具有更多或更少的模拟反射曲线。细网格具有细度,以便在细网格中提供足够数量的点来确定附近吸收系数μa值和散射系数μs’值的峰面阵列(步骤1230)。具体地,处理器116可以利用来自粗网格的最低误差值加上指定的偏移来设置阈值。可以全部标记具有低于阈值的误差的散射系数μs’和吸收系数μa在细网格上的位置,以用于确定峰面阵列从而进一步确定反射数据的散射系数μs’和吸收系数μa。具体地,对峰值进行误差拟合以确定峰值处的吸收系数μa值和散射系数μs’值。血氧计探头可以利用峰值处的吸收系数μa值和散射系数μs’值的加权平均值(例如,质心计算)来确定组织的反射数据点的吸收系数μa值和散射系数μs’值(步骤1240)。
用于加权平均的吸收系数μa值和散射系数μs’值的权重可以由处理器116确定为阈值减去细网格误差。因为细网格上的点选择为具有低于阈值的误差,所以这会给出正权重。加权平均的加权计算(例如,质心计算)为组织的反射数据点提供预测的散射系数μs’和吸收系数μa(即,(μa,μs’)细)。血氧计探头可以使用其他方法(例如用各种非线性最小二乘法中的一个或多个拟合)以确定吸收系数μa的真实最小误差峰值。
在实施方式中,处理器116计算反射数据点和模拟反射曲线的对数,并将每个对数除以源-检测器距离(例如,以厘米为单位)的平方根。除以源-检测器距离的平方根的这些对数值可由处理器116用于前述步骤中的反射数据点和模拟反射曲线(例如,步骤1215、1220、1225和1230)以改善反射数据点到模拟反射曲线的拟合。
根据另一实施方式,偏移基本上设置为零,这有效地给出粗网格最小值和细网格最小值之间的差的偏移。以上关于图12a-12b描述的方法依赖于来自粗网格的最小拟合误差,因此细网格上的最小误差通常较低。理想地,阈值是由细网格上的最低误差确定的,这通常需要处理器的额外计算。
以下是实施方式中的用于寻找最佳拟合细网格中的反射数据点的特定模拟反射曲线的进一步详细描述。图12b示出了实施方式中的用于寻找最佳拟合细网格中的反射数据点的特定模拟反射曲线的方法的流程图。流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在确定了最佳拟合反射数据点的来自粗网格的特定模拟反射曲线(μa,μs’)粗(步骤1225)之后,处理器116计算在模拟反射数据的完全模拟反射曲线数据库(即,16×5850(μa,μs’)数据库)中关于(μa,μs’)粗的区域中的误差表面(步骤1250)。误差表面表示为:err(μa,μs’)。此后,处理器116定位在err((μa,μs’)中的最小误差值(也称为errmin)(步骤1255)。然后,处理器116由err(μa,μs’)生成峰面阵列,其中,如果锋面大于零则表示为pksurf(μa,μs’)=k+errmin-err(μa,μs’),如果峰面小于或等于零则表示为pksurf(μa,μs’)=k+errmin-err(μa,μs’)=0(步骤1260)。在表达式中,k选自err(μa,μs’)的最小点处的峰值,并且具有大约为10个元素的零以上的宽度。该pksurf(μa,μs’)中峰值的质心(即,质心计算)使用点的高度作为权重(步骤1265)。质心的位置是针对组织的反射数据点的吸收系数μa和散射系数μs’的插值结果。
可以针对由每个源结构120生成的每个波长(例如,3或4个波长)重复用于确定组织的反射数据点的吸收系数μa和散射系数μs’的上面参照图12a和12b所描述的方法。
氧饱和度确定。根据第一实施方式,处理器116通过利用针对由每个源结构120产生的3或4个波长的光确定(如上所述)的吸收系数μa(例如,3或4个吸收系数μa)来确定由血氧计探头101探测的组织的氧饱和度。根据第一实施方式,生成氧饱和度值的查找表以求出吸收系数μa与氧饱和度的最佳拟合。可以通过假设可能的总血红蛋白、黑色素和氧饱和度值的范围并且针对这些情景中的每一个计算μa来生成查询表。然后,吸收系数μa点通过除以单位矢量的范数转换为单位矢量以减小系统误差,并且仅取决于曲线的相对形状。然后将单位矢量与查找表进行比较以找到最佳拟合,这给出氧饱和度。
根据第二实施方式,处理器116通过计算脱氧血红蛋白和氧合血红蛋白的净分析物信号(nas)来确定组织的氧饱和度。nas被定义为与系统中的其他光谱分量正交的光谱部分。例如,在含有氧合血红蛋白和脱氧血红蛋白的系统中的脱氧血红蛋白的nas是与氧合血红蛋白光谱和黑色素光谱正交的光谱部分。脱氧血红蛋白和氧合血红蛋白的浓度可以通过相应的nas与先前确定的每个波长的吸收系数的矢量乘法来计算。然后,氧饱和度容易计算为氧合血红蛋白的浓度除以氧合血红蛋白和脱氧血红蛋白的总和。lorber的anal.chem.58:1167-1172(1986)通过引用结合于此,并提供了用于进一步详细理解用于确定组织的氧饱和度的第二实施方式的框架。
在血氧计探头101的实施方式中,反射数据由检测器结构125以30赫兹产生,并且氧饱和度值以大约3赫兹计算。可以在显示器115上显示确定的氧饱和度值的连续观测平均值(例如,至少三个氧饱和度值),其可以具有1赫兹的更新速率。
光学性质。如上面简要描述的,存储在存储器117中的每个模拟反射曲线315表示组织的独特的光学性质。更具体地,对于给定波长,模拟反射曲线的独特形状表示组织的光学性质的独特值,即,可以确定组织性质的散射系数(μs)、吸收系数(μa)、组织的各向异性(g)和组织的折射率。
检测器结构125针对相对小的源-检测器距离检测的反射主要取决于约化散射系数,μs’。约化散射系数是包含散射系数μs和组织的各向异性的“集中”性质,其中,μs’=μs(1-g),并且用于描述在大小为1/μs’的许多步骤的随机游走中光子的扩散,其中每个步骤涉及各向同性散射。这样的描述相当于使用许多小步骤1/μs的光子移动的描述,其中,如果在吸收事件之前存在许多散射事件(即,μa<<μs’),则每个小步骤仅包括部分偏转角。
相反,检测器结构125针对相对大的源-检测器距离检测的反射主要取决于有效吸收系数μeff,有效吸收系数μeff定义为
因此,通过测量相对小的源-探测器距离(例如,图2的s1-d4和s2-d8)处的和相对大的源-探测器距离(例如,如图2所示的s1-d8和s2-d4)处的反射,可以彼此独立地确定μa和μs’两者。组织的光学性质转而可以为计算组织的氧合血红蛋白浓度和脱氧血红蛋白浓度以及因此计算氧饱和度提供足够的信息。
用于数据收集优化的迭代拟合。图13示出了用于通过血氧计探头101确定组织的光学性质的其他方法的流程图。该流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在1300处,血氧计探头101将光(例如,近红外光)从源结构之一(例如源结构120a)发射到组织中。步骤1305,在发射的光从组织反射之后,检测器结构125检测光,以及步骤1310,产生组织的反射数据。步骤1300、1305和1310可以针对多个波长的光以及针对一个或多个其他源结构(例如源结构120b)重复。在1315处,血氧计探头101将反射数据拟合为模拟反射曲线315并确定反射数据具有最佳拟合的模拟反射曲线。存储在存储器中并且适合反射数据的数据库可以是数据库900、数据库1000或数据库1100。此后,步骤1320,血氧计探头101基于最佳拟合反射数据的模拟反射曲线的光学性质,确定组织的光学性质(例如,针对数据库900或数据库1000的μa和μs’、或针对数据库1100的黑色素含量、氧饱和度、血液体积和散射)。
在1325处,血氧计探头101根据在步骤1320处确定的光学性质确定组织中光的平均自由程(例如,mfp=1/(μa+μs’))。具体地,可以由包括针对所有源-检测器对(例如,对1:源结构120a和检测器结构125a;对2:源结构120a和检测器结构125b;对3:源结构120a和检测器结构125c;对4:源结构120a和检测器结构125d;对5:源结构120a和检测器结构125e;对6:源结构120a和检测器结构125f;对7:源结构120a和检测器结构125g;对8:源结构120a和检测器结构125h;对9:源结构120b和检测器结构125a;对10:源结构120b和检测器结构125b......等等)的反射数据的累积反射曲线获得的光学性质确定平均自由程。
在1330处,血氧计探头101确定针对组织的给定区域计算的平均自由程是否长于最短源-检测器距离的两倍(例如,图2的s1-d4和s2-d8)。如果平均自由程长于最短源-探测器距离的两倍,则将收集的反射数据重新拟合到模拟反射曲线(即,重新分析),而不利用针对具有最短源-检测器距离的源-检测器对从检测器结构收集的反射数据。例如,重复步骤1315-1330而不使用以源结构120a用作检测器结构125d的源的来自检测器结构125e的反射数据,并且不使用以源结构120b用作检测器结构125h的源的来自检测器结构125h的反射数据。可以重复计算平均自由程并舍弃一个或多个源-探测器对的反射数据的过程,直到没有对拟合贡献反射数据的源-探测器对具有短于计算出的平均自由程的一半的源-探测器距离。此后,步骤1335,由血氧计探头101从最佳拟合模拟反射曲线确定氧饱和度并且例如,在显示器115上报告该氧饱和度。
从一个源结构120发射到组织中并且行进小于平均自由路径的一半的光被非漫反射。该光的再发射距离有力地取决于组织相功能和局部组织成分。因此,与经历多次散射事件的光的反射数据相比,使用该光的反射数据易于导致光学性质和组织性质的不太准确的确定。
数据加权检测器结构。随着距离源结构120的距离增加探测器结构125从组织接收到的反射量减少。因此,与具有相对长源-检测器距离(例如,图2的s1-d8和s2-d4)的检测器结构产生的反射数据相比,具有相对短源-检测器距离(例如,图2的s1-d4和s2-d8)的检测器结构125产生的反射数据易于表现出本质上更高的信号。因此,与由具有相对长源-检测器距离(例如,源-检测器距离大于源结构和检测器结构之间的平均距离)的检测器结构产生的反射数据相比,拟合算法可以优选地将模拟反射曲线更紧密地拟合到由具有相对短源-检测器距离(例如,源-检测器距离小于或等于源结构和检测器结构之间的平均距离)的检测器结构125生成的反射数据。为了由反射数据相对精确地确定光学性质,与距离成比例的偏离可能是不希望的,并且可以通过如下所述的加权反射数据来校正。
图14示出了用于加权由选择检测器结构125生成的反射数据的方法的流程图。该流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
在1400处,血氧计探头101将光从源结构中的一个(例如源结构120a)发射到组织中。步骤1405,在发射的光从组织反射之后,检测器结构125检测光,以及步骤1410,产生组织的反射数据。步骤1400、1405和1410可以针对多个波长的光以及针对一个或多个其他源结构(例如,源结构120b)重复。在1415处,血氧计探头101将反射数据的第一部分拟合到模拟反射曲线315。存储在存储器中并且拟合反射数据的数据库可以是数据库900、数据库1000或数据库1100。反射数据的第一部分由探测器结构的到源结构小于阈值距离的第一部分产生。阈值距离可以是源结构和检测器结构之间的平均距离(例如,近似中间距离)。在1420处,将反射数据的第二部分拟合到模拟反射曲线。反射数据的第二部分由探测器结构的第一部分和其他探测器结构产生,其中,该其他探测器结构与阈值距离相比处于距离源的下一个最大源-探测器距离。例如,如果检测器结构的第一部分包括检测器结构125c、125d、125e和125f,则处于下一个最大源-检测器距离的检测器结构是检测器结构125g(参见表1)。
在1425处,将在步骤1415产生的拟合与在步骤1420产生的拟合进行比较,以确定在步骤1420产生的拟合是否优于在步骤1415产生的拟合。如本领域技术人员将理解的,基于各种参数可以量化数据到曲线的拟合的“接近度”,并且拟合的接近度可直接比较以确定具有与曲线更接近拟合(更接近拟合)的数据。如将进一步理解的,更接近拟合有时也被称为更好拟合或更紧密拟合。如果在步骤1420生成的拟合优于在步骤1415生成的拟合,则重复步骤1420和1425,其中,反射数据由包括位于距离源的下一个增加的源-探测器距离处的附加检测器结构(根据所考虑的示例,检测器结构125c)的检测器结构生成。或者,如果在步骤1420产生的拟合不优于在步骤1415产生的拟合,则位于大于阈值距离的源-检测器距离处的探测器结构125的反射数据不用于拟合。此后,步骤1430,血氧计探头101使用在1415处产生的拟合或步骤1420产生的拟合(如果优于在步骤1415确定的拟合)以确定组织的光学性质和氧饱和度。此后,步骤1435,通过血氧计探头101报告(例如,在显示器115上)氧饱和度。
根据替代实施方式,如果在步骤1420生成的拟合不优于在步骤1415生成的拟合,则针对具有大于阈值距离的源-检测器距离的检测器结构,反射数据通过加权因子加权,使得该加权反射数据对拟合的影响减小。未在拟合中使用的反射数据可以被认为具有零加权并且可以与来自感兴趣的组织层下方的组织的反射相关联。据说来自感兴趣的组织层下面的组织的反射在反射曲线中表现出特征性的扭结,其表明该特定的反射。
应注意,将反射数据拟合到模拟反射曲线的曲线拟合算法可以考虑反射数据的不确定性量以及反射数据的绝对位置。反射数据的不确定性对应于来自由检测器结构中的一者产生反射数据时的噪声量,并且该噪声量可以随着反射数据的量值的平方根来缩放。
根据其他实施方式,血氧计探头101基于与反射数据的测量相关联的噪声量对反射数据进行迭代加权。具体地,与具有相对短的源-检测器距离的检测器结构产生的反射数据相比,由具有相对大的源-检测器距离的检测器结构产生的反射数据通常具有较低的信噪比。对由具有相对大的源-检测器距离的检测器结构产生的反射数据进行加权允许该数据与其他反射数据同等或近似相等地贡献于拟合。
描述为用于将反射数据拟合到多个蒙特卡罗的模拟反射曲线的方法提供了由血氧计探头探测的真实组织的光学性质的相对快速和准确的确定。与术后探头相比,确定组织的光学性质的速度是术中探头设计中的重要考虑因素。此外,所描述的蒙特卡罗方法允许稳健的校准方法,在与相对光学性质相比时,该方法转而允许产生绝对光学性质。与术后血氧计探头相比,报告绝对光学性质而非相对光学性质对于术中血氧计探头而言相对重要。
图15示出了用于确定由血氧计探头测量的组织的相对组织参数的方法的流程图,其中,从相对组织参数中移除组织中黑色素的贡献。流程图表示一个示例实施方式。可以在不偏离实施方式的范围的情况下,在流程图中添加、移除或组合步骤。
该方法包括在患者身体的不同组织位置(例如,第一目标组织和第二目标组织)上进行血氧计测量,并使用血氧计测量来确定一个目标组织(例如,第二目标)的相对组织参数。不同的目标位置可以是具有相同或相似黑色素浓度的组织,例如对侧组织。例如,在乳房重建手术期间(例如,在重建中使用组织瓣),第一目标组织可以是健康的乳房组织,第二目标组织可以是需要血氧计读数的组织(例如,正在重建的乳房)。第一乳房组织可以来自相同的乳房或不同的乳房或其他组织(例如,其他胸部组织)。两个组织应当具有相同或相似的黑色素含量。然后,使用第一目标组织和第二目标组织的血氧计测量来产生相对组织参数(例如,相对氧饱和度值),该相对组织参数是第一目标组织(例如,健康乳房组织)的第一组织参数(例如,第一氧饱和度)和第二目标组织(例如,用于重建的组织瓣或正在重建的乳房组织)的第二组织参数(例如,第二氧饱和度)之间的差值,其中从测量移除黑色素的光吸收对相对氧饱和度的贡献。
如以下进一步描述的,该方法利用波长为约700纳米至约900纳米(例如,红外波长)的光的组织中黑色素吸收系数的曲线的近似恒定的斜率。该方法使用吸收系数的导数方法以从血氧测量测量和确定(例如,最终结果、中间结果或两者)中移除黑色素的贡献(例如,来自黑色素的光吸收)。参见图8中黑色素吸收系数的斜率。该方法还利用了黑色素的和含氧血红蛋白的吸收系数的曲线的斜率差值以及黑色素的和脱氧血红蛋白的吸收系数的曲线的斜率差值。参见图8中氧合血红蛋白和脱氧血红蛋白的吸收系数的曲线。另外,如以下进一步解释的,该方法利用针对第一目标组织和第二目标组织的吸收系数的曲线斜率的变化,其中这些组织可能具有不同浓度的含氧血红蛋白和脱氧血红蛋白。
在该方法的实施方式中,在准备使用探头进行血氧计测量时,用户在第一位置(例如,与第二目标组织不同的位置)将血氧计探头的探头前端接触第一目标组织。参见图15中的1500。此后,血氧计探头从探头面上的源结构(例如,两个源结构)中的一个或多个发射光(例如,2、3、4或更多个波长的红外光(ir))到第一个目标组织。在光从第一目标组织反射或透射通过第一目标组织之后,探测面上的检测器结构检测光,并基于检测到的光产生第一反射数据。第一反射数据包括针对第一目标组织的黑色素含量(例如,第一目标组织的第一黑色素含量)的反射数据的第一黑色素吸收分量。见图15中的1505。
然后,血氧计探头针对从源结构传输到组织中的每个波长的光使用第一反射数据来确定第一目标组织的多个第一血氧计参数。参见图15中的1510。如上所述血氧计探头可以通过将反射数据拟合为模拟反射曲线确定第一血氧计参数。血氧计探头将这些第一血氧计参数存储在探头的存储器中。第一血氧计参数可以是第一目标组织的针对每个传输波长的光的吸收系数的值。第一目标组织(例如,健康组织)的第一血氧计参数是基线参数。在进行第一测量之后和进行第二测量之前,第一血氧计参数(例如,中间值,例如角度测量、吸收系数、氧饱和度值、其他值)可能不可用于显示(例如,以下在图15的1515、1520和1525处描述的)。
图16a和16b示出了由多个光波长(例如,760纳米、810纳米、845纳米和895纳米)照射的第一目标组织和第二目标组织的吸收系数的示图。血氧计探头可以使用其他波长,包括更多或更少光波长。
在1515处,用户将血氧计探头的探头面移动到第二目标组织(例如,经历重建手术的乳房组织)。此后,血氧计探头从探头面上的一个或多个源结构发射光(例如,2、3、4或更多个ir波长)到第二目标组织中。在光从第二目标组织反射或透射通过第二目标组织之后,探头面上的检测器结构检测光,并基于检测到的光产生第二反射数据。第二反射数据包括针对第二目标组织的黑色素含量(例如,第一目标组织的第二黑色素含量)的反射数据的第二黑色素吸收分量。见图15中的1520。
然后,血氧计探头针对从源结构传输到组织中的每个波长的光,使用第二反射数据确定第二目标组织的多个第二血氧计参数。参见图15中的1525。第二血氧计参数可以由血氧计探头通过将第二反射数据拟合到如上所述的模拟反射曲线确定。血氧计探头可以将这些第二血氧计参数存储在探头的存储器中。第二血氧计参数可以是第二目标组织的针对传输的波长的光的吸收系数的值。
在1530处,血氧计探测器确定针对760纳米和810纳米之间的线1605(例如,在图16a中显示为虚线的线1605的投影1605a)以及在810纳米和845纳米之间的线1610的、第一吸收系数的第一曲线(例如,形成曲线的线)的第一角度偏差θ1(参见图16a)。
血氧计探测器确定针对在810纳米和845纳米之间的线1610(例如,在图16a中显示为虚线的线1610的投影1610a)以及在845纳米和890纳米之间的线1615的、第一吸收系数的第一曲线(例如,形成曲线的线)的第二角度偏差φ1。
血氧计探测器确定针对在760纳米和810纳米之间的线1620(例如,在图16b中显示为虚线的线1620的投影1620a)以及在810纳米和845纳米之间的线1625的、第二吸收系数的第二曲线(例如,形成曲线的线)的第三角度偏差θ2(参见图16b)。
血氧计探测器确定针对在810纳米和845纳米之间的线1625(例如,在图16b中显示为虚线的线1625的投影1625a)以及在845纳米和890纳米之间的线1630的、第二吸收系数的第二曲线(例如,形成曲线的线)的第四角度偏差φ2。
由血氧计探头通过对用于第一目标组织(例如,健康乳房组织)的相对于波长的吸收系数第一曲线取二阶导数,计算图16a中示出的第一角度偏差θ1和第二角度偏差φ1。图16b中所示的第三角度偏差θ2和第四角度偏差φ2由血氧计探头通过对用于第二目标组织(例如,重建的乳房组织)的相对于波长的吸收系数的第二曲线取二阶导数来计算。
图17a示出了第一目标组织(例如,健康乳房组织)的吸收系数的示例曲线(例如,第一光谱)。示例曲线沿曲线的整个长度具有负斜率。图17b示出了第一目标组织的相对于波长的吸收系数的一阶导数的示例曲线。图17b中的曲线图是针对750nm和850nm之间的波长。图17b的示例曲线的负值与图17a中所示的负斜率匹配,并且示例曲线沿曲线的整个长度具有正斜率。图17c示出了第一目标位置的相对于波长的吸收系数的二阶导数的示例曲线。图17c中的曲线图是针对800和850纳米之间的波长(例如,具体地针对810纳米和845纳米之间的波长)。图17c中所示的示例曲线的正值与图17b中的曲线的正斜率匹配。
图17d示出了第一目标组织(例如,健康乳房组织)的吸收系数的示例第一曲线(例如,第一光谱)1701和第二目标组织(例如,重建的乳房组织)的吸收系数的示例第二曲线(例如,第二光谱)1703。曲线之间的相对小的位移表明第一目标组织和第二目标组织之间的吸收系数的相对小的变化。每个示例曲线沿曲线的整个长度具有负斜率。
图17e示出了第一目标组织的相对于波长的吸收系数的一阶导数的第一示例曲线1711(例如,三个高点),并且示出了第二目标组织的相对于波长的吸收系数的一阶导数的第二曲线1713(例如,三个低点)。图17e中的曲线用于750nm和850nm之间的波长。图17e的示例曲线的负值与图17d中所示的负斜率匹配,并且示例曲线沿曲线的整个长度具有正斜率。
图17f示出了第一目标位置的相对于波长的吸收系数的二阶导数的第一示例曲线1721(例如,到低点),并且示出了第二目标位置的相对于波长的吸收系数的二阶导数的第二示例曲线1723(例如,到高点)。图17d中的曲线针对800至850纳米之间(例如,特别针对810纳米和845纳米之间)的波长。图17f中所示的示例图的正值与图17e中的曲线的正斜率匹配。
图18示出了彼此相对绘制的二阶导数值θ1和φ1在“角度”空间中的矢量(θ1,φ1)。在角度空间中,纵轴和横轴分别是两个波长的光的二阶导数的值θ1和φ1。在特定的示例中,纵轴和横轴是针对810纳米和845纳米的二阶导数的值。如果其他波长的光照射组织,也可以从二阶导数选择其他波长值。即,角度空间中的矢量1801的终点1801a表示彼此相对绘制的针对第一组织(例如,健康乳房组织)的二阶导数的两个值。
图19示出了“角度”空间中的第一矢量1901(θ1,φ1)和第二矢量1903(θ2,φ2)。即,θ1和φ1彼此相对绘制,并且θ2和φ2彼此相对绘制。两个矢量之间的差值是增量角δθ=θ1-θ2和δφ=φ1-φ2,并且表示对于810nm和845nm波长第一目标组织和第二目标组织的吸收系数的曲线(有时也称光谱)之间的曲率变化。可以由处理器通过将矢量1903投影到矢量1901上来确定增量角δθ和δφ。参见图15的1535和1540。
图20示出了向量空间中的增量角δθ和δφ之一。吸收系数的曲率变化可归因于第一目标组织部位和第二目标组织部位之间的氧饱和度的相对变化。因为黑色素的吸收系数的曲率对于第一目标组织和第二目标组织是固定的或近似固定的(例如,对于对侧测量的单个患者,第一目标组织和第二目标组织的黑色素浓度相同或相似),所以吸收系数的曲率的变化δθ和δφ不归因于组织部位中的黑色素。也就是说,黑色素对二阶导数的任何贡献都归零。
由增量角δθ和δφ计算第一目标组织和第二目标组织之间的氧饱和度的相对变化,并且在血氧计探头的显示器上显示氧饱和度的相对变化的值(例如,百分比差值)。参见图15的1545和1550。血氧计探头的处理器执行该计算。具体地,角度变化δθ和δφ具有任意尺度,该尺度可被校正以使其是针对血液的。校正可以基于比例因子、校正矢量或两者。比例因子、校正矢量或两者可以存储在非易失性存储器中,并且当血氧计探头与电源分离时(例如,从探头移除电池)保持存在于存储器中。当血氧计被首次制造并测试使用时,可以生成这些值。从存储器中检索这些值并将其加载到处理器中以供使用。校正矢量可以是处理器用来校正角度空间中的矢量或校正角度空间中的角度变化δθ和δφ的角度空间中的矢量。
使用组织模体确定校正矢量。组织模体可以是液体组织模体、一个或多个刚性组织模体、或液体和刚性组织模体的组合。在组织模体具有100%的初始血氧饱和度(例如,完全氧合)并且降低至0%(例如,完全脱氧)的一段时间内,血氧计探头对组织模体进行氧饱和度测量。
由血氧计探头针对组织模体生成的反射数据(例如,对于2、3、4或更多波长的光,例如ir)被拟合到模拟反射曲线以确定最佳地拟合反射数据的一个或多个模拟反射曲线。确定与一个或多个模拟反射曲线相关联的吸收系数。确定吸收系数的曲线(例如,光谱)的一阶导数和二阶导数。
图21a示出了完全氧合测量的吸收系数(例如,光谱)的曲线图2100和完全脱氧测量的吸收系数的曲线图2105。图2ib示出了曲线图上相对于波长的完全氧合光谱的一阶导数的第一曲线2110和曲线图上相对于波长的完全脱氧光谱的一阶导数的第二曲线2115。图21c示出了曲线图上相对于波长的完全氧合光谱的二阶导数的第一曲线2120和曲线图上相对于波长的完全脱氧光谱的二阶导数的第二曲线2125。
此后,针对与上述第一目标组织和第二目标组织测量相同的波长,确定完全氧合测量的曲线的角度偏差(例如,θ1到φ1)(例如,从760纳米到810纳米的线和从810纳米到845纳米的线之间的角度偏差θ1,以及从810纳米到845纳米的线和从845纳米到890纳米的线之间的角度偏差φ1)。
针对与上述第一目标组织和第二目标组织测量相同的波长确定完全脱氧测量的曲线的角度偏差(例如,θ2到φ2)(例如,从760纳米到810纳米的线和从810纳米到845纳米的线之间的角度偏差θ2,以及从810纳米到845纳米的线和从845纳米到890纳米的线之间的角度偏差φ2)。
图22示出了彼此相对绘制的δθ和δφ在角度空间中的矢量(δθ,δφ)。增量角可用于比例缩放(或校准)第一目标组织和第二目标组织的组织测量(例如,对侧乳房组织测量)。
这些角度变化δθ=θ1-θ2和δφ=φ1-φ2由处理器确定。增量角表示完全氧合测量和完全脱氧测量之间的吸收光谱的曲率的变化。增量角δθ和δφ表示组织中的氧合作用100%的变化预期是什么样的,并且提供了校正增量角δθ和δφ的其他较小变化(例如,针对对侧乳房组织)的参考从而按比例缩放任意尺度的δθ和δφ(例如,针对对侧乳房组织)。
将计算出的组织模体的矢量(δθ,δφ)乘以校正因子,以校正模体中的血液体积和患者组织中的血液体积的差异。校正因子可以是10或其他因子,以考虑使用的特定模体中的10%的血液体积与患者组织的1%的血液体积(或其他百分比的血液体积,1.25%、1.2%、1.15%、1.1%、1.05%、0.95%、0.9%、0.85%、0.8%或其他值)之间的差值。或者,与模体的测量相比,校正因子可以应用于患者组织的测量。
图23示出了针对模体的基线校正矢量2401和计算的校正矢量2403,其通过比例因子校正了模体和患者组织的血液体积之间的血液体积差值。针对血液体积差值校正的增量角δθ和δφ指示组织的氧合作用的100%变化预期是什么样的,并且提供了校正患者组织(例如,对侧乳房组织)的增量角δθ和δφ的其他较小变化的参考,从而为患者组织按比例缩放任意尺度的δθ和δφ。
在实施方式中,通过将用于患者组织的矢量投射到用于模体矢量的矢量上,以通过模体的矢量按比例缩放患者组织的矢量。图24示出了投射到模体的矢量2503上的患者组织的矢量2501。投射的结果用附图标记2505标记。
在实施方式中,患者组织的矢量通过模体的矢量按比例缩放(图15的1550),即,将归一化的患者组织矢量除以归一化的模体矢量(例如,确定百分比差值)并且乘以100%和-1。
δso2=(-1)*(归一化被投射矢量/归一化模体矢量)*100%
因子-1表示由血氧计探头测量的患者组织的氧饱和度降低的测量。在图24的示例中,患者的对侧目标组织之间的脱氧的相对增加(例如,氧合作用的减少)约为18%。
在实施方式中,血氧计探头使用非线性变换以通过模体的矢量(δθ,δφ)按比例缩放患者组织的矢量(δθ,δφ)。
在实施方式中,血氧计探头将来自血氧计探头的至少一个光源(例如,源结构)中的光在待测量的第一位置处传输到第一组织(第一乳房组织)中。
第一组织包含第一黑色素组分,例如,第一黑色素含量。第一黑色素组分包括真黑素、褐黑素或真黑素和褐黑素两者。若干检测器结构在光透过第一组织或从第一组织反射之后接收光。
由于第一黑色素组分而导致所接收的光包含第一黑色素吸收组分。即,所接收的光包括第一组织中黑色素的信息,这是因为黑色素吸收传输到第一组织中的一部分光。
之后,血氧计探头确定由于组织的黑色素组分引起的黑色素吸收组分的黑色素补偿分量(例如,角度校正(例如θ1,θ2,φ1,φ2,δθ,δφ或其任何组合),由反射数据拟合到模拟反射曲线确定的吸收系数,任何初步的、任何中间的、任何最终的计算结果,或这些的任何组合)。
黑色素吸收组分包括第一黑色素组分。黑色素组分包括第一黑色素组分。血氧计探头使用黑色素补偿分量来获得第一组织的黑色素校正的氧饱和度值。黑色素校正的氧饱和度值考虑黑色素吸收组分。
在实施方式中,一种方法包括使血氧计探头的探头前端接触患者的第一目标组织,其中,第一目标组织是健康组织;使用血氧计探头,对第一个目标组织进行第一次血氧测量;通过血氧计探头的处理器确定第一多个吸收系数,所述第一多个吸收系数取决于当在第一目标组织上执行测量时从血氧计探头发射到第一目标组织中的多个波长的光;使探头前端接触患者的第二目标组织,其中,第二目标组织是要测定血氧饱和度值的组织;使用血氧计探头,在第二目标组织上进行第二次血氧测量;通过血氧计探头的处理器确定第二多个吸收系数,所述第二多个吸收系数取决于当在第二目标组织上执行测量时从血氧计探头发射到第二目标组织中的第一多个波长的光;处理器计算第一目标组织的第一多个吸收系数的曲线的第一角度偏差和第二角度偏差;处理器计算第二目标组织的第二多个吸收系数的曲线的第三角度偏差和第四角度偏差;处理器计算第一角度偏差和第二角度偏差之间的第一角度差以及第三角度偏差和第四角度偏差之间的第二角度差;由处理器基于第一角度差和第二角度差计算第一目标组织和第二目标组织之间的氧饱和度的相对变化;以及,通过血氧计探头的显示器显示相对氧饱和度的值。
该方法可以包括将来自血氧计探头的源结构的第一光传输到第一目标组织中;由血氧计探头的多个检测器结构检测从第一目标组织反射的第一反射光;由检测器产生针对检测器结构检测到的第一反射光的第一反射数据;将反射数据拟合到多个模拟反射曲线;从第一反射数据到多个模拟反射曲线的拟合中确定模拟反射曲线中的一个或多个最佳拟合曲线,其中,每个模拟反射曲线与吸收系数的值相关联;以及,确定针对第一反射数据的模拟反射曲线的一个或多个最佳拟合曲线的第一多个吸收系数。
该方法可以包括将来自血氧计探头的源结构的第二光传输到第二目标组织中;由血氧计探头的多个检测器结构检测从第二目标组织反射的第二反射光;由检测器产生针对检测器结构检测到的第二反射光的第二反射数据;将第二反射数据拟合到多个模拟反射曲线;从第二反射数据到多个模拟反射曲线的拟合中确定模拟反射曲线中的一个或多个最佳拟合曲线;以及,确定针对第二反射数据的模拟反射曲线的一个或多个最佳拟合曲线的第二多个吸收系数。
该方法可以包括由处理器利用缩放矢量按比例缩放第一角度差和第二角度差,其中,缩放矢量表示组织模体的氧合作用的100%差异。按比例缩放包括将包括角度空间中的第一角度差和第二角度差的数据点的第一矢量投射到角度空间中的缩放矢量上。按比例缩放或者包括将包括角度空间中的第一角度差和第二角度差的数据点的归一化第一矢量除以归一化缩放矢量。
该方法可以包括由处理器计算归一化第一矢量除以归一化缩放矢量的的商的百分比差;并且商的负数包括第一目标组织和第二目标组织之间的氧合作用的减少。显示器上显示的值是商乘以负一的乘积。
在实施方式中,系统实施该方法,其中,该系统包括血氧计探头,血氧计探头包括手持式壳体;容纳在手持式壳体中的处理器;存储器,其容纳在手持式壳体中并且电子耦合到处理器以及存储用于控制处理器的第一代码;显示器,其能够被从手持式壳体的外部访问并且电子耦合到处理器;电池,其容纳在手持式壳体中并且耦合到处理器、存储器和显示器以及向其供电,其中,代码包括可由处理器执行的指令以执行以下方法的步骤:在患者的第一目标组织上进行第一血氧测量;确定第一多个吸收系数,所述第一多个吸收系数取决于在对第一目标组织进行测量时从血氧计探头发射到第一目标组织中的多个波长的光;在患者的第二目标组织上进行第二血氧测量;确定第二多个吸收系数,所述第二多个吸收系数取决于在对第二目标组织进行测量时从血氧计探头发射到第二目标组织中的第一多个波长的光;计算第一目标组织的第一多个吸收系数的曲线的第一角度偏差和第二角度偏差;计算第二目标组织的第二多个吸收系数的曲线的第三角度偏差和第四角度偏差;计算第一角度偏差和第二角度偏差之间的第一角度差以及第三角度偏差和第四角度偏差之间的第二角度差;基于第一角度差和第二角度差计算第一目标组织和第二目标组织之间的氧饱和度的相对变化;以及,显示相对氧饱和度的值。
在实施方式中,一种方法包括使探头前端接触患者的第一目标组织,其中,第一目标组织是健康组织;使用血氧计探头对第一个目标组织进行第一血氧测量;由血氧计探头的处理器基于第一目标组织的第一血氧测量测量确定第一吸收系数;使探头前端接触患者的第二目标组织,其中,第二目标组织是要测定血氧饱和度值的组织;使用血氧计探头在第二目标组织上进行第二血氧测量;由血氧计探头的处理器确定基于第二目标组织的第二血氧测量测量的第二吸收系数;由处理器通过使用第一吸收系数调节第二吸收系数产生第三吸收系数;由第三吸收系数确定第二目标组织的氧饱和度值;以及,显示第二目标组织的氧饱和度值。该方法可以包括将第一血氧测量的第一反射数据拟合到多个模拟反射曲线,以由处理器确定基于第一目标组织的第一血氧测量的第一吸收系数,其中,模拟反射曲线包括黑色素在模拟组织中的建模;以及,由处理器从模拟反射曲线中的一个或多个最佳拟合曲线确定第一吸收系数。
已经出于说明和描述的目的呈现了对本发明的描述。其并非旨在穷举或将本发明限制于所描述的精确形式,并且鉴于上述教导,可以作出许多修改和变化。选择和描述实施方式是为了最好地解释本发明的原理及其实际应用。该描述将使得本领域的其他技术人员能够在各种实施方式中以及使用适合于特定用途的各种修改来最好地利用和实践本发明。本发明的范围由以下权利要求限定。
- 还没有人留言评论。精彩留言会获得点赞!