一种用于治疗血管性痴呆的中药组合物及其制备方法和应用与流程
本发明涉及一种中药组合物及其制备方法和应用,特别涉及一种用于治疗血管性痴呆的中药组合物及其制备方法和应用。本发明属于医药技术领域。
背景技术:
目前,血管性痴呆(vasculardementia)是一种老年人常见疾病之一,其主要发病机制为血管阻塞伴有血栓形成,脑血流量灌注降低,伴有炎症反应(guoll,wangds,xuyy,etal.effectsofil-1βonhippocampuscellapoptosisandlearningabilityofvasculardementiarats[j].eurrevmedpharmacolsci,2018,22(18):6042-6048.),出现脑内β-淀粉样蛋白(amyloidbeda,aβ)沉积(boespflugel,simonmj,leonarde,etal.targetedassessmentofenlargementoftheperivascularspaceinalzheimer'sdiseaseandvasculardementiasubtypesimplicatesastroglialinvolvementspecifictoalzheimer'sdisease[j].jalzheimersdis,2018,66(4):1587-1597.),血脑屏障(blood-brainbarrier,bbb)血管内皮细胞结构异常,最终引起脑内神经元和神经胶质细胞的结构和功能发生改变。
血管性痴呆会危及老年人的健康和生命,其发病机制还不清楚,其主要学说和假说包括很多,例如aβ蛋白学说、炎症介质学说、胆碱能学说、自由基学说、免疫学说、病毒学说、铝中毒假说、钙超载学说、tau蛋白学说、性激素学说等,说明血管性痴呆与aβ蛋白、炎症介质、胆碱、自由基、免疫球蛋白、铝金属、tau蛋白、雌激素(lij,hangl,lijj,etal.effectsofestrogenonlearning-memoryandexpressionofcalbindin-d28kinhippocampusinvasculardementiarats[j].pakjpharmsci,2017,30(4):1403-1406.)等均有关,提示血管性痴呆发病机制比较复杂。
通常而言,血管阻塞伴有血栓形成后,脑部血液供应减少,脑血流量灌注降低,引起脑部缺血缺氧,会加速脑内aβ蛋白的产生。资料显示,机体脑内aβ蛋白是由β-淀粉样蛋白前体蛋白(amyloid-βprecursorprotein,app)通过β、γ-分泌酶水解产生,aβ蛋白主要包括aβ1-40蛋白、aβ1-42蛋白,aβ1-40蛋白含量与aβ1-42蛋白含量比值约为9:1,aβ1-42蛋白在脑内神经元外侧可以形成老年斑(senileplaques,sp),sp会对神经元造成损伤,引起脑内神经元数量减少及其神经元功能降低,尤其是脑内海马区域神经元损伤较为严重。研究表明,机体脑内海马与学习记忆密切相关,血管性痴呆会出现脑微血管内皮功能障碍(demontgolfier,pincona,pouliotp,etal.highsystolicbloodpressureinducescerebralmicrovascularendothelialdysfunction,neurovascularunitdamage,andcognitivedeclineinmice[j].hypertension,2019,73(1):217-228.),多表现为学习记忆能力下降,使用多奈哌齐或者牛磺酸锌可以改善学习记忆能力和脑内海马结构(tiwarin,bhatiap,kumara,etal.potentialofcarnosine,ahistamineprecursorinratmodelofbilateralcommoncarotidarteryocclusion-inducedvasculardementia[j].fundamclinpharmacol,2018,32(5):516-531.;齐汝霞,张鹏,孙涛,等.牛磺酸锌对血管性痴呆小鼠学习和记忆能力的影响[j].中国病理生理杂志,2018,34(7):1297-1300.)。
资料显示,机体脑血流量灌注减少,引起脑部缺血缺氧,脑内aβ蛋白异常积累后,会引起小胶质细胞体积变大、突起变短、获得吞噬功能,最终活化脑内小胶质细胞,同时aβ蛋白还可以活化星形胶质细胞,促使小胶质细胞及星形胶质细胞产生大量炎症介质,例如白介素-1β(interleukin-1β,il-1β)、白介素-6(interleukin-6,il-6)(nga,tamww,zhangmw,etal.il-1β,il-6,tnf-αandcrpinelderlypatientswithdepressionoralzheimer'sdisease:systematicreviewandmeta-analysis[j].scirep,2018,8(1):12050.)、肿瘤坏死因子-α(tumornecrosisfactor-α,tnf-α)等,使用二氢杨梅素可以抑制小鼠脑内小胶质细胞活化(fengj,wangjx,duyh,etal.dihydromyricetininhibitsmicroglialactivationandneuroinflammationbysuppressingnlrp3inflammasomeactivationinapp/ps1transgenicmice[j].cnsneuroscither,2018,24(12):1207-1218.),进而改善神经性炎症反应。
一般而言,aβ蛋白异常积累会引起脑内毛细血管内皮细胞、毛细血管内皮细胞间紧密连接(tightjunction,tj)、星形胶质细胞和基膜等结构异常,导致血脑屏障通透性增加,进而加速aβ蛋白沉积于机体脑组织,这与机体脑内晚期糖基化终产物受体(receptorforadvancedglycationendproducts,rage)(chany,chenw,wanw,etal.aβ1-42oligomerinducesalterationoftightjunctionscaffoldproteinsviarage-mediatedautophagyinbend.3cells[j].expcellres,2018,369(2):266-274.)、低密度脂蛋白相关蛋白1(lipoproteinreceptor-relatedprotein1,lrp1)、载脂蛋白j(apolipoproteinj,apoj)、核转录因子-κbp65(nucleartranscriptionfactor-κbp65,nf-κbp65)(gengl,zhangt,liuw,etal.inhibitionofmir-128abatesaβ-mediatedcytotoxicitybytargetingppar-γvianf-κbinactivationinprimarymousecorticalneuronsandneuro2acells[j].yonseimedj,2018,59(9):1096-1106.)、闭锁小带蛋白-1(zonulaoccluden-1,zo-1)(leejm,parkjm,songmk,etal.theameliorativeeffectsofexerciseoncognitiveimpairmentandwhitematterinjuryfromblood-brainbarrierdisruptioninducedbychroniccerebralhypoperfusioninadolescentrats[j].neuroscilett,2017,18(638):83-89.)等表达异常有关。
研究表明,机体脑血流量灌注减少,伴有脑内aβ蛋白异常积累,还会引起抗氧化功能降低,将会干扰机体对自由基的清除,脑内总抗氧化能力(totalantioxidantcapacity,t-aoc)、超氧化物歧化酶(superoxidedismutase,sod)、谷胱甘肽过氧化物酶(glutathioneperoxidase,gsh-px)降低及其氧化产物丙二醛(malondialdehyde,mda)增加,使用苯乙醇苷可以使脑内gsh-px、sod含量增加,mda含量降低(jiajx,yanxs,songw,etal.theprotectivemechanismunderlyingphenylethanoidglycosides(phg)actionsonsynapticplasticityinratalzheimer'sdiseasemodelinducedbybetaamyloid1-42[j].jtoxicolenvironhealtha,2018,81(21):1098-1107.),可见,gsh-px、sod、mda等可以初步评价机体脑内的抗氧化功能。
已知,现代医学许多药物对血管性痴呆具有治疗作用,例如抗aβ药物、维生素b6(lip,zhuml,pangp,etal.vitaminb6preventsisocarbophos-inducedvasculardementiainratsthroughn-methyl-d-aspartatereceptorsignaling.clinexphypertens,2018,40(2):192-201.)、雌激素、抗神经元细胞凋亡药物、抗氧化剂、新型纳米硒、美金刚等,但是这些药物均有明显副作用。而依据中医学理论可以选择具有副作用小、较多靶点、彼此协同、整体调节的中药来治疗血管性痴呆,因此,探寻副作用小且具有整体调节的中药组合物非常重要。
中医理论认为,血管性痴呆又称络病、痴呆症、老年呆病等。王清任在《医林改错》中提出年高无记性者,脑髓渐空也,提示血管性痴呆多与脑有关。在《千金翼方》中指出人五十以上阳气始衰,损与日至,心力渐退,提示血管性痴呆会出现学习记忆能力减退。王肯堂在《证治准绳》中指出有病癫人,善痰为癫,络脉瘀滞,气结痰故也,提示血管性痴呆多因络脉瘀滞、气结痰故致病,络脉瘀滞会引起营卫失和、气血渗灌失常、郁而化热、卫气壅滞、肝肾亏虚、痰邪瘀滞、湿邪凝聚,同时老年人出现老年而健忘、魂魄离散、记忆力衰退、言语混乱等,将会促进血管性痴呆的发生发展。综合分析,血管性痴呆病位在脑,络脉瘀滞、气结痰故所致经络不通、血流不畅、痰风湿毒瘀滞、痰浊阻络等,同时老年人多伴有肝肾亏虚、气血不畅、神明失养、脑髓损伤等。国外资料显示,线粒体因子和细胞因子在血管性痴呆的发病中起重要作用,尤其是肾精亏虚、痰浊阻窍等症候均与sod、il-6异常有关(sunl.mitochondrialfactorandcellcytokinesassociatewithtcmsyndromescaleinvasculardementiapatients[j].expthermed,2018,15(1):131-138.)。因此,最终我们确定治疗血管性痴呆的基本治疗原则为通络活血、化痰祛风、除湿止痛、补肝补肾、温中理气。根据血管性痴呆的基本治疗原则,经过科学组方,本发明提供了包括12味中药材组成的中药组合物,该12味中药材包括丝瓜络、马钱子、茺蔚子、骨碎补、三叶香茶菜、地肤子、紫花地丁、青木香、青羊参、沙苑子、阴香皮以及紫苏梗。实验证明,本发明的中药组合物通过作用于多个靶点来治疗血管性痴呆,治疗效果好,且无副作用。
技术实现要素:
本发明的目的在于提供一种用于治疗血管性痴呆的中药组合物及其制备方法和应用。
为了达到上述目的,本发明采用了以下技术手段:
本发明提供了包括12味中药材组成的中药组合物,该12味中药材包括丝瓜络、马钱子、茺蔚子、骨碎补、三叶香茶菜、地肤子、紫花地丁、青木香、青羊参、沙苑子、阴香皮以及紫苏梗。其中,丝瓜络,又名天罗线,味甘,性平、寒,归胃经、肺经、肝经,具有通络祛风、下乳活血的功效;马钱子,又名番木鳖,味苦,性温,归肝经、脾经,具有通络消肿、散结止痛的功效;茺蔚子,又名益母草子,味甘、辛,性微寒,归心包经、肝经,具有活血清肝、明目调经的功效;骨碎补,又名飞蛾草,味苦,性温,归肝经、肾经,具有活血止血、补肾杀虫的功效;三叶香茶菜,又名细叶香茶菜,味微苦,性温,归肺经、肝经,具有化痰祛风、散寒除湿的功效;地肤子,味甘、苦,性寒,归肾经、膀胱经,具有祛风清热、除湿止痛、和血止痒的功效;紫花地丁,又名光瓣堇菜,味苦、辛,性寒,归心经、肝经,具有除湿清热、凉血消肿的功效;青木香,味辛、苦,性寒,归肝经、胃经,具有止痛消肿、平肝解毒的功效;青羊参,味甘、微苦,性温,归肝经、肾经,具有补肝强筋、补肾壮骨的功效;沙苑子,味甘,性温,归肾经、肝经,具有补肾明目、固精清肝的功效;阴香皮,味辛,性温,归脾经,具有温中祛风、除湿消肿、散寒解毒的功效;紫苏梗,又名紫苏杆,味辛,性温,归肺经、脾经,具有理气止痛、安胎宽中的功效。综合分析,在本发明治疗血管性痴呆的中药组合物中,君药丝瓜络、马钱子、茺蔚子、骨碎补主要具有通络活血的功效;臣药三叶香茶菜、地肤子主要具有化痰祛风的功效,紫花地丁、青木香主要具有除湿止痛的功效,即臣药可以发挥化痰祛风、除湿止痛的功效;佐药青羊参、沙苑子主要具有补肝补肾的功效;使药阴香皮、紫苏梗主要具有温中理气的功效。
为了明确该中药组合物的功效,本发明开展了大量实验研究,主要探讨中药组合物高剂量、中药组合物中剂量、中药组合物低剂量对血管性痴呆小鼠学习记忆能力、血脑屏障通透性、海马app相关蛋白、海马炎症介质、海马抗氧化能力、脏器指数的影响,还测定了各组小鼠海马lrp1、apoj、rage、zo-1蛋白和基因表达。
一般认为,血管性痴呆可以表现为学习记忆能力减退(jiangx,niux,guoq,etal.foxo1-mediatedautophagyplaysanimportantroleintheneuroprotectiveeffectsofhydrogeninaratmodelofvasculardementia[j].behavbrainres,2019,356:98-106.),本实验使用bw-mwm101型morris水迷宫(安徽淮北正华生物仪器有限公司)测定小鼠学习记忆能力,结果表明,对照组与假手术组学习记忆能力相似,排除手术对模型建立的相关干扰;与对照组比较,模型组小鼠尚不能将可移动平台的位置记忆到自己的脑内,寻找可移动平台较为困难,提示模型组小鼠的学习记忆能力下降,模型建立的实际效果很好,利于后续开展实验研究。经过中药组合物治疗后,与模型组比较,中药组合物高、中剂量可以促使小鼠记住可移动平台位置,提示中药组合物高、中药组合物中剂量可以改善血管性痴呆小鼠模型的学习记忆能力,这对后续开展相关实验研究奠定了基础。
血管性痴呆主要特征在于脑血流不足,促进aβ积累,加重神经性炎症反应,一旦bbb通透性增加,会引起神经元损伤和认知缺陷(maema,lit,bertuzzig,etal.prolongedsystemichyperglycemiadoesnotcausepericytelossandpermeabilityatthemouseblood-brainbarrier[j].scirep,2018,8(1):17462.;naessensdmp,devosj,vanbavele,etal.blood-brainandblood-cerebrospinalfluidbarrierpermeabilityinspontaneouslyhypertensiverats[j].fluidsbarrierscns,2018,15(1):26.)。本实验使用酶标仪测定脑eb浓度和eb含量。结果表明,对照组小鼠脑eb浓度和eb含量较低,说明对照组小鼠脑bbb通透性正常,而模型组小鼠脑eb浓度和eb含量升高,说明模型组小鼠脑eb的渗出量增加,bbb通透性增加,结合模型组小鼠的学习记忆能力下降,提示模型组小鼠出现神经元损伤和认知缺陷。经过中药组合物的治疗后,中药组合物高中剂量组eb浓度和eb含量降低,结合中药组合物高、中药组合物中剂量可以改善血管性痴呆小鼠模型的学习记忆能力,提示中药组合物高剂量、中药组合物中剂量可以改善脑bbb的通透性,降低异常物质进入脑,中药组合物高剂量、中药组合物中剂量对于改善血管性痴呆小鼠模型的学习记忆能力有一定的积极作用。
研究指出,血管性痴呆出现脑血流量灌注不足,app相关蛋白表达增加,将会促进aβ的生成(hilals,ikramma,verbeekmm,etal.c-reactiveprotein,plasmaamyloid-βlevels,andtheirinteractionwithmagneticresonanceimagingmarkers[j].stroke,2018,49(11):2692-2698.)。本实验通过酶联免疫吸附实验方法测定海马app相关蛋白,实验结果表明,对照组小鼠海马app相关蛋白较低,而模型组小鼠海马app相关蛋白含量增加,结合模型组小鼠的学习记忆能力下降,说明血管性痴呆小鼠海马区域淀粉样物质增加同时伴有血管性痴呆小鼠学习记忆能力下降。经过中药组合物治疗后,中药组合物高剂量、中药组合物中剂量可以有效地降低海马app相关蛋白含量,说明中药组合物高剂量、中剂量可以通过下调海马app相关蛋白来治疗血管性痴呆,且下调海马app相关蛋白利于小鼠学习记忆能力不断改善。
血管性痴呆会出现脑血液供应不足,会激活小胶质细胞和星形胶质细胞,出现炎症介质含量等异常(dusq,wangxr,zhuw,etal.acupunctureinhibitstxnip-associatedoxidativestressandinflammationtoattenuatecognitiveimpairmentinvasculardementiarats[j].cnsneuroscither,2018,24(1):39-46.)。本实验通过酶联免疫吸附实验方法测定海马炎症介质il-1β、tnf-α和il-6含量,结果表明,对照组炎症介质il-1β、tnf-α和il-6含量较低,说明对照组小胶质细胞和星形胶质细胞并未活化,脑炎症反应不明显。模型组海马炎症介质il-1β、tnf-α和il-6含量增加,说明模型组小鼠脑内部小胶质细胞和星形胶质细胞异常活跃,结合模型组海马app相关蛋白含量增加,模型组小鼠的学习记忆能力下降,提示模型组脑内海马炎症介质变化与app相关蛋白变化趋势正向同步,而与小鼠的学习记忆能力负向同步,这与海马app和海马aβ1-42含量增加促使脑炎症介质il-1β、tnf-α和il-6释放有关。经过中药组合物的治疗后,中药组合物高剂量、中药组合物中剂量可以降低海马炎症介质il-1β、tnf-α和il-6含量,减弱小胶质细胞和星形胶质细胞活跃程度,这与海马app和海马aβ1-42含量降低有关,进一步说明了aβ蛋白学说与炎症介质学说彼此相互关联。
文献报道,血管性痴呆会出现脑血液供应不足,能量供应不足,自由基的清除效率下降,这与机体抗氧化能力降低有关,一旦机体抗氧化能力降低,常伴有氧化产物堆积,增强机体抗氧化能力有利于血管性痴呆的积极治疗(yadava,sunkariaa,singhaln,etal.resveratrolloadedsolidlipidnanoparticlesattenuatemitochondrialoxidativestressinvasculardementiabyactivatingnrf2/ho-1pathway[j].neurochemint,2018,112:239-254.)。本实验使用试剂盒测定小鼠海马sod、gsh-px、t-aoc、mda含量。结果表明,对照组小鼠海马sod、gsh-px、t-aoc含量较高,伴有mda降低,说明对照组小鼠抗氧化酶减较多,自由基大部分被清除;模型组小鼠海马sod、gsh-px、t-aoc含量较低,伴有mda增加,说明模型组小鼠海马的抗氧化能力减弱,自由基的清除效率下降,这与机体抗氧化能力降低有关。而经过中药组合物的治疗后,中药组合物高剂量、中药组合物中剂量可以增加海马sod、gsh-px、t-aoc含量,减少mda含量,以此来改善血管性痴呆小鼠海马的抗氧化能力。
实验使用免疫组织化学方法、real-time-pcr方法测定了与血管性痴呆密切相关的lrp1、apoj、rage、zo-1蛋白和基因表达。结果表明,对照组小鼠海马lrp1和apoj蛋白和基因表达上调,rage、zo-1蛋白和基因表达下调,说明血管性痴呆aβ并没有大量沉积于脑,而是aβ主要通过rage/lrp1系统进行转运出脑,脑内aβ含量较低,结合对照组学习记忆能力正常、炎症介质含量较低,提示对照组小鼠通常不会引发机体学习记忆能力下降、炎症反应。模型组海马lrp1和apoj蛋白和基因表达下调,rage、zo-1蛋白和基因表达上调,说明aβ并没有通过rage/lrp1系统进行转运出脑,aβ在脑内堆积,形成sp,结合模型组学习记忆能力降低、炎症介质含量增加,说明模型组小鼠因为aβ堆积而引起学习记忆能力降低、炎症介质含量增加。经过中药组合物治疗后,中药组合物高剂量、中药组合物中剂量可以增加血管性痴呆小鼠海马lrp1和apoj蛋白和基因表达,而下调rage、zo-1蛋白和基因表达,通过rage/lrp1系统进行转运aβ出脑,结合中药组合物高剂量、中剂量学习记忆能力正常、炎症介质含量较低,提示中药组合物高剂量、中药组合物中剂量可以通过影响rage/lrp1系统而减少脑内aβ,改善学习记忆能力并降低炎症介质水平。
为了评价中药组合物对血管性痴呆小鼠免疫功能和脑萎缩程度的影响,本实验使用plzoz-s型电子天平(赛多利斯公司)测定小鼠脾指数、胸腺指数和脑指数。结果显示,对照组小鼠脾脏主要产生的b细胞和胸腺主要产生的t细胞较多,体液免疫及其细胞免疫水平较强,同时脑未出现萎缩;模型组小鼠脾脏主要产生的b细胞和胸腺主要产生的t细胞较少,体液免疫及其细胞免疫水平降低,抗感染的能力减弱同时伴有脑出现萎缩。经过中药组合物的治疗后,中药组合物高剂量、中药组合物中剂量可以增加b细胞和t细胞数量,且同时改善脑的萎缩程度,提示中药组合物高剂量、中药组合物中剂量对血管性痴呆小鼠模型的免疫器官及其脑有一定的保护作用。
针对中药组合物的副作用,本实验使用plzoz-s型电子天平(赛多利斯公司)测定了小鼠的心指数、肺指数、肾指数、肝指数和体重。结果表明,与对照组比较,模型组小鼠心指数、肺指数、肾指数、肝指数和体重改变不明显,差异无统计学意义。经过中药组合物高剂量、中剂量治疗后,与模型组比较,中药组合物高、中、低剂量组小鼠心指数、肺指数、肾指数、肝指数和体重改变也不明显,差异无统计学意义,提示中药组合物治疗血管性痴呆不会改变小鼠心指数、肺指数、肾指数、肝指数和体重,提示可以放心使用中药组合物治疗血管性痴呆。
以上实验表明,中药组合物高、中剂量(39.73g/kg、19.86g/kg)可改善血管性痴呆小鼠学习记忆能力和血脑屏障通透性,还可改善海马炎症介质、app相关蛋白、抗氧化能力等,更可改善海马lrp1/rage相关蛋白和基因表达,且中药组合物高、中剂量(39.73g/kg、19.86g/kg)对血管性痴呆小鼠重要脏器的脏器指数和体重无影响,说明该中药组合物高、中剂量(39.73g/kg、19.86g/kg)治疗血管性痴呆有效并且无副作用。
在上述研究的基础上,本发明提出了一种用于治疗血管性痴呆的中药组合物,所述的中药组合物由以下重量份的各原料药组成:丝瓜络8-12重量份、马钱子0.1-0.5重量份、茺蔚子5-10重量份、骨碎补10-20重量份、三叶香茶菜20-25重量份、地肤子8-15重量份、紫花地丁20-25、青木香4-8重量份、青羊参20-30重量份、沙苑子5-10重量份、阴香皮4-8重量份、紫苏梗15-25重量份。
其中,优选的,所述的中药组合物由以下重量份的各原料药组成:丝瓜络10重量份、马钱子0.3重量份、茺蔚子7.5重量份、骨碎补15重量份、三叶香茶菜22.5重量份、地肤子10.5重量份、紫花地丁22.5、青木香6重量份、青羊参25重量份、沙苑子7.5重量份、阴香皮6重量份、紫苏梗20重量份。
进一步的,本发明还提出了一种临床上适宜的用于治疗血管性痴呆的中药制剂,其由本发明所述的中药组合物加入制剂成型所需的辅料,按照制备药物制剂的常规方法制成。
其中,优选的,所述的制剂为水煎剂、粉剂、胶囊剂、丸剂、颗粒剂、片剂或口服液。
进一步的,本发明还提出了一种制备所述的中药组合物的方法,包括以下步骤:
(1)按照本发明所述的重量份称取各原料药,将各原料药混合均匀后放入容器中,加入药物重量10-20倍的蒸馏水,浸泡1-2.5h后,煎煮1-2.5h,冷却;
(2)将步骤(1)冷却后的药液用纱布过滤,得到第一次滤液和药物残渣;
(3)步骤(2)的药物残渣放入容器中,重复步骤(1)和(2)得到第二次滤液,混合第一次滤液及第二次滤液;
(4)干燥,得到所述中药组合物的干膏。
其中,优选的,所述的纱布过滤是指使用4层纱布过滤。
其中,优选的,还包括将得到的干膏放在粉碎机内粉碎,研磨,分子筛处理,得到所述中药组合物的干粉。
其中,优选的,所述的分子筛处理是指分别依次使用10目筛网过滤、40目筛网过滤、100目筛网过滤、200目筛网过滤。
更进一步的,本发明还提出了所述的中药组合物在制备治疗血管性痴呆药物中的应用。
相较于现有技术,本发明的有益效果是:
本发明提出了一种新的用于治疗血管性痴呆的中药组合物及其制备方法。本发明治疗血管性痴呆中药组合物的主要功效为通络活血、化痰祛风、除湿止痛、补肝补肾、温中理气。该中药组合物能够通过作用于多个靶点蛋白及其海马lrp1/rage来治疗血管性痴呆,且无副作用。本发明的提出为治疗血管性痴呆提供了新的技术手段。
附图说明
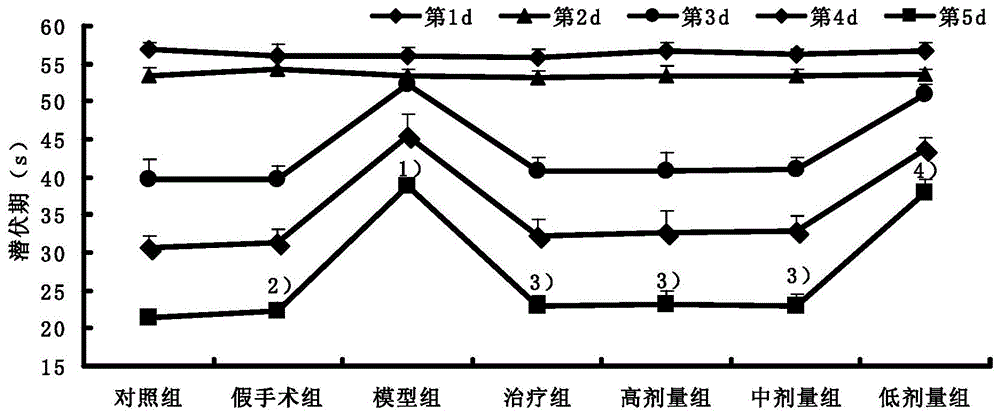
图1为中药组合物对血管性痴呆小鼠学习能力的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图2为中药组合物对血管性痴呆小鼠记忆能力的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图3为中药组合物对血管性痴呆小鼠学习记忆保持能力的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图4为中药组合物对血管性痴呆小鼠脑bbb通透性的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图5为中药组合物对血管性痴呆小鼠海马app相关蛋白含量的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图6为中药组合物对血管性痴呆小鼠海马炎症介质的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图7为中药组合物对血管性痴呆小鼠海马t-aoc的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图8为中药组合物对血管性痴呆小鼠海马sod、gsh-px的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图9为中药组合物对血管性痴呆小鼠海马mda的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图10为中药组合物对血管性痴呆小鼠海马lrp1、apoj、rage、zo-1表达的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图11为中药组合物对血管性痴呆小鼠海马lrp1、apoj、rage、zo-1mrna的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图12为中药组合物对血管性痴呆小鼠脾指数、胸腺指数和脑指数的影响;
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05;
图13为中药组合物对血管性痴呆小鼠心指数、肾指数、肝指数、肺指数的影响;
注:与对照组比较:1)p>0.05;与模型组比较:2)p>0.05;
图14为中药组合物对血管性痴呆小鼠体重的影响;
注:与对照组比较:1)p>0.05;与模型组比较:2)p>0.05。
具体实施方式
下面结合具体实施例和附图来进一步描述本发明,本发明的优点和特点将会随着描述而更为清楚。但这些实施例仅是范例性的,并不对本发明的范围构成任何限制。本领域技术人员应该理解的是,在不偏离本发明的精神和范围下可以对本发明技术方案的细节和形式进行修改或替换,但这些修改和替换均落入本发明的保护范围内。
实施例1一种用于治疗血管性痴呆的中药组合物
所述的中药组合物由以下重量份的各原料药组成:丝瓜络10重量份、马钱子0.3重量份、茺蔚子7.5重量份、骨碎补15重量份、三叶香茶菜22.5重量份、地肤子10.5重量份、紫花地丁22.5、青木香6重量份、青羊参25重量份、沙苑子7.5重量份、阴香皮6重量份、紫苏梗20重量份。
实施例2一种用于治疗血管性痴呆的中药组合物
所述的中药组合物由以下重量份的各原料药组成:丝瓜络8重量份、马钱子0.5重量份、茺蔚子5重量份、骨碎补20重量份、三叶香茶菜22重量份、地肤子10重量份、紫花地丁25、青木香5重量份、青羊参22重量份、沙苑子10重量份、阴香皮5重量份、紫苏梗25重量份。
实施例3一种用于治疗血管性痴呆的中药组合物
所述的中药组合物由以下重量份的各原料药组成:丝瓜络12重量份、马钱子0.1重量份、茺蔚子10重量份、骨碎补12重量份、三叶香茶菜25重量份、地肤子8重量份、紫花地丁20、青木香8重量份、青羊参30重量份、沙苑子5重量份、阴香皮8重量份、紫苏梗15重量份。
实施例4一种用于治疗血管性痴呆的中药组合物粉剂的制备
(1)按照以下重量份称取各原料药:
丝瓜络10重量份、马钱子0.3重量份、茺蔚子7.5重量份、骨碎补15重量份、三叶香茶菜22.5重量份、地肤子10.5重量份、紫花地丁22.5、青木香6重量份、青羊参25重量份、沙苑子7.5重量份、阴香皮6重量份、紫苏梗20重量份。
(2)将各原料药混合均匀后放入容器中,加入药物重量10倍的蒸馏水,浸泡2h后,煎煮2h,冷却;
(2)将步骤(1)冷却后的药液分别依次使用4层纱布过滤,得到第一次滤液和药物残渣;
(3)步骤(2)的药物残渣放入容器中,重复步骤(1)和(2)得到第二次滤液,混合第一次滤液及第二次滤液;
(4)使用干燥箱于65℃下干燥第一次滤液及第二次滤液6d,得到所述中药组合物的干膏;
(5)得到的干膏放在粉碎机内多次粉碎,细心研磨,分别依次使用10目筛网过滤、40目筛网过滤、100目筛网过滤、200目筛网过滤,得到所述中药组合物的干粉。
实施例5中药组合物治疗血管性痴呆的药效试验
1材料
1.1动物
清洁级4月龄雄性昆明小鼠(23±2)g,140只,购买于北京维通利华实验动物技术有限公司(质量合格证号scxk(京)2012-0001)。在黑龙江中医药大学实验动物中心内常温、常湿饲养昆明小鼠,2只/笼,给予昆明小鼠充足饮用水及其饲料。
1.2仪器
tgl-16g型台式离心机(上海安亭科学仪器厂);plzoz-s型电子天平(赛多利斯公司);hmias型高清晰度彩色分析系统(武汉千屏影像技术有限公司);6100型酶标仪(美国rt公司);appliedbiosystems型定量pcr仪(美国应用生物系统公司);bw-mwm101型morris水迷宫(安徽淮北正华生物仪器有限公司);-20℃冰箱(中国青岛海尔电器有限公司);tt30-fw-100型高速万能粉碎机(温岭市林大机械有限公司);超声波清洗器(上海市科导超声仪器公司);mu5100p型超纯水仪(北京科誉兴业科技发展有限公司);fm881-1型远红外鼓风干燥箱(飞马烤箱厂);rsearchuv型超纯水系统(上海和泰仪器有限公司)等。
1.3药品
盐酸多奈哌齐片(中国重庆植恩药业有限公司,批号20141201);中药丝瓜络、马钱子、茺蔚子、骨碎补、三叶香茶菜、地肤子、紫花地丁、青木香、青羊参、沙苑子、阴香皮、紫苏梗由黑龙江中医药大学中医药研究院周忠光教授购买于黑龙江中医药大学附属第一医院,然后由黑龙江中医药大学药学院田明教授进行鉴定原药材;app、aβ1-42、il-1β、tnf-α和il-6试剂盒(南京建成生物工程研究所,20150501);prime
2方法
2.1动物分组
选择4月龄雄性清洁级昆明小鼠140只为研究对象,体重(23±2)g,每组20只,按照随机数字表将昆明小鼠随机分成对照组、假手术组、模型组、多奈哌齐组(简称治疗组)、中药组合物高剂量组(简称高剂量组),中药组合物中剂量组(简称中剂量组)、中药组合物低剂量组(简称低剂量组),共分7组,实验动物昆明小鼠适应饲养1周后开始进行后续实验。
2.2模型复制
(1)aβ1-42注射
本实验参考文献(morronif,sitag,graziosia,etal.neuroprotectiveeffectofcaffeicacidphenethylesterinamousemodelofalzheimer'sdiseaseinvolvesnrf2/ho-1pathway[j].agingdis,2018,9(4):605-622..)制备aβ1-42注射小鼠模型,选择小鼠,麻醉、固定体位、减去头部毛发、消毒头部皮肤、剪开小鼠皮肤,使用zh-c型脑立体定位仪(河北慧采科技有限责任公司)定位小鼠海马区域,暴露小鼠头部颅骨,使用微量加样器对小鼠海马区域双侧脑室一次性注入5μl凝聚态aβ1-42(80pmol/μl),留针2min,封闭颅骨孔,滴加庆大霉素,消毒皮肤,包扎小鼠头部,单笼饲养,避免小鼠之间进行撕咬。
(2)阻断血流
参考文献(夏洪涛,马利刚,赵赟.有氧运动对血管性脑痴呆小鼠学习记忆能力的影响[j].中国动脉硬化杂志,2018,2(12):1233-1238.)制备阻断血流小鼠模型。小鼠脑内注射5μl凝聚态aβ1-42后,小鼠颈部正中切口,分离两侧颈总动脉,0号手术线阻断两侧颈总动脉6min,再灌注6min,需要间歇阻断两侧颈总动脉3次,每次间隔8min,鼠尾放血2滴。
(3)确定模型
实验通过小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,制备出血管性痴呆模型。对照组在昆明小鼠双侧脑室注射等量生理盐水进行处理且不分离两侧颈总动脉,20只昆明小鼠存活;假手术组在昆明小鼠双侧脑室注射等量生理盐水进行处理且分离两侧颈总动脉,19只昆明小鼠存活;模型组昆明小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,17只昆明小鼠存活;治疗组昆明小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,17只昆明小鼠存活;高剂量组昆明小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,16只昆明小鼠存活;中剂量组昆明小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,18只昆明小鼠存活;低剂量组昆明小鼠脑内注射aβ1-42结合阻断两侧颈总动脉,18只昆明小鼠存活。
2.3药物提取
(1)药物组成
每份中药组合物包括丝瓜络10g、马钱子0.3g、茺蔚子7.5g、骨碎补15g、三叶香茶菜22.5g、地肤子10.5g、紫花地丁22.5、青木香6g、青羊参25g、沙苑子7.5g、阴香皮6g、紫苏梗20g,共计购买4份中药组合物原药材。
(2)计算每份中药组合物剂量
中药组合物包括丝瓜络10g、马钱子0.3g、茺蔚子7.5g、骨碎补15g、三叶香茶菜22.5g、地肤子10.5g、紫花地丁22.5、青木香6g、青羊参25g、沙苑子7.5g、阴香皮6g、紫苏梗20g,共计152.8g,此剂量为正常人标准体重每份中药组合物的总体剂量。
(3)配制4份中药组合物
需要分别取丝瓜络10g、马钱子0.3g、茺蔚子7.5g、骨碎补15g、三叶香茶菜22.5g、地肤子10.5g、紫花地丁22.5、青木香6g、青羊参25g、沙苑子7.5g、阴香皮6g、紫苏梗20g各4份,配制4份中药组合物,4份中药组合物共计611.2g。
(4)获取中药组合物第一次滤液
将611.2g中药组合物放入20000ml大容量圆底烧瓶中,加入蒸馏水6000ml,需要蒸馏水浸泡611.2g中药组合物2h,100℃下煎煮中药组合物2h,4层纱布过滤后,获得中药组合物的第一次滤液及药物残渣。
(5)获取中药组合物第二次滤液
将中药组合物残渣放到大容量圆底烧瓶中,加入蒸馏水6000ml,蒸馏水浸泡中药组合物残渣2h,100℃下煎煮2h,过滤后获得中药组合物的第二次滤液。
(6)获取中药组合物干膏
合并第一次滤液及其第二次滤液,fm881-1型远红外鼓风干燥箱(飞马烤箱厂)于65℃下干燥6d,获得中药组合物干膏142.34g,则中药组合物出膏率为(干膏/中药组合物)×100%,即(142.34g/611.2g)×100%=23.29%,即1g中药组合物干膏相当于中药组合物原药材4.29g。
(7)获取中药组合物干粉
使用tt30-fw-100型高速万能粉碎机(温岭市林大机械有限公司)将中药组合物干膏多次粉碎,细心研磨,10目筛网过滤、40目筛网过滤、100目筛网过滤、200目筛网过滤,plzoz-s型电子天平(赛多利斯公司)称重,获得中药组合物干粉131.25g,则该中药组合物出粉率=(干粉/中药组合物)×100%=(131.25g/611.2g)×100%=21.47%。
(8)保存中药组合物干粉
实验使用611.2g中药组合物最终将可以获得中药组合物干粉131.25g,即1g中药组合物干粉相当于中药组合物原药材4.66g。
(9)分装中药组合物干粉
该中药组合物干粉按照13g/袋分装,最后一袋14.25g,所有袋装干粉于-80℃冰箱(日本sanyo公司)保存备用。
(10)使用中药组合物干粉
使用时,需要将中药组合物室温内融化,搅拌该中药组合物,并按照小鼠的体表面积及其体重数值精细换算小鼠中药组合物给药量。
2.4药物剂量的设定
(1)设定中药组合物剂量
中药组合物包括丝瓜络10g、马钱子0.3g、茺蔚子7.5g、骨碎补15g、三叶香茶菜22.5g、地肤子10.5g、紫花地丁22.5、青木香6g、青羊参25g、沙苑子7.5g、阴香皮6g、紫苏梗20g,一共152.8g,此剂量经过黑龙江中医药大学栗明副主任医师评定,是临床患者安全剂量。依据小鼠和人体表面积比值0.0026:1进行换算,计算求得该中药组合物常规剂量为[(152.8g×0.0026)/20g小鼠]×50,即19.86g/kg。此为中药组合物中剂量。最终设定该中药组合物高剂量、中药组合物中剂量、中药组合物低剂量分别是39.73g/kg、19.86g/kg、9.93g/kg。
(2)设定阳性药物剂量
临床上多奈哌齐治疗血管性痴呆的常规可用剂量是(5~10)mg,依据小鼠和人体表面积比值为0.0026:1,计算获得小鼠给药剂量为[5×0.0026×50~10×0.0026×50=1.3mg/kg],即(0.65~1.3)mg/kg或者(0.00065~0.0013)g/kg,本实验选择0.001g/kg多奈哌齐开展实验研究。
2.5实验动物给药
血管性痴呆小鼠模型造模后,对照组20只昆明小鼠存活;假手术组19只昆明小鼠存活;模型组17只昆明小鼠存活;治疗组17只昆明小鼠存活;高剂量组16只昆明小鼠存活;中剂量组18只昆明小鼠存活;低剂量组18只昆明小鼠存活。各组小鼠均需要灌胃给药,其中对照组给予等量生理盐水灌胃,模型组给予等量生理盐水灌胃,假手术组小鼠给予等量生理盐水灌胃,治疗组给予多奈哌齐0.001g/kg灌胃,高剂量组给予相当于中药组合物原药材39.73g/kg灌胃,中剂量组给予相当于中药组合物原药材19.86g/kg灌胃,低剂量组给予相当于中药组合物原药材9.93g/kg灌胃。各组小鼠给药32d。各组小鼠灌胃结束后,对照组19只昆明小鼠存活;假手术组17只昆明小鼠存活;模型组14只昆明小鼠存活;治疗组15只昆明小鼠存活;高剂量组15只昆明小鼠存活;中剂量组15只昆明小鼠存活;低剂量组17只昆明小鼠存活。
2.6检测学习记忆能力
(1)学习能力
本实验各组小鼠灌胃给药结束后第2天开始检测,小鼠学习能力使用潜伏期进行表示,需要使用bw-mwm101型morris水迷宫(安徽淮北正华生物仪器有限公司)检测小鼠学习能力。morris水迷宫(安徽淮北正华生物仪器有限公司)包括圆形水池、电子计算机、摄像机、水迷宫分析软件、可移动平台等,水温控制在(23±2)℃,可移动平台位于第iv象限且低于水平面1.5cm。昆明小鼠头部使用墨汁着色,圆形水池底部及其周边均使用黑色麻布覆盖。圆形水池正上方摄像机同步记录昆明小鼠实验过程,获取实验数据。昆明小鼠训练时间是60s,若昆明小鼠60s内寻找不到可移动平台,需将昆明小鼠放在可移动平台上停留12s。第5d是实验测试时间,将昆明小鼠头朝外侧放入第i、ii、iii象限,获得潜伏期数据,评价昆明小鼠学习能力。
(2)记忆能力
各组小鼠灌胃给药结束后第2天后,昆明小鼠头部使用墨汁着色,圆形水池底部及其周边均使用黑色麻布覆盖。圆形水池正上方摄像机同步记录昆明小鼠实验过程,获取实验数据。昆明小鼠训练时间是60s,若昆明小鼠60s内寻找不到可移动平台,需将昆明小鼠放在可移动平台上停留12s。测试第5d时候,撤去平台,检测小鼠60s内找到平台游泳距离,评价各组昆明小鼠记忆能力。
(3)学习记忆保持能力
各组小鼠灌胃给药结束后第2天后,昆明小鼠头部使用墨汁着色,圆形水池底部及其周边均使用黑色麻布覆盖。圆形水池正上方摄像机同步记录昆明小鼠实验过程,获取实验数据。昆明小鼠训练时间是60s,若昆明小鼠60s内寻找不到可移动平台,需将昆明小鼠放在可移动平台上停留12s。在测试第5d时候撤去可移动平台,测试在60s内小鼠跨越第iv象限移动平台所在位置次数(跨平台次数)及其小鼠在原平台所在象限游泳时间(目标象限停留时间),评价小鼠的学习记忆保持能力。
2.7测定小鼠脑bbb通透性
采用脑伊文氏蓝(eb)渗出量测定各组小鼠脑bbb通透性。需要制备伊文氏蓝(eb)渗出量的标准曲线,以吸光度值(a)为纵坐标,以eb浓度为横坐标,计算获得脑eb标准曲线方程。morris水迷宫实验测定结束后,小鼠尾静脉注射2%eb,10%水合氯醛麻醉小鼠,小鼠固定架上固定小鼠,剪开各组小鼠右心耳,灌注生理盐水约70ml,迅速解剖小鼠,plzoz-s型电子天平(赛多利斯公司)称量小鼠脑重量,即脑湿重。将小鼠脑浸泡于甲酰胺溶液,45℃避光孵育72h,匀浆脑,使用tgl-16g型台式离心机(上海安亭科学仪器厂)3000rpm/min离心10min,使用6100型酶标仪(美国rt公司)630nm处测定各组小鼠脑上清液吸光度值(a)。根据事先已经制备伊文氏蓝(eb)渗出量的标准曲线计算eb含量,本实验eb含量用eb浓度(μg/ml)或eb浓度/脑湿重(μg/g)来表示,将可以评价中药组合物对各组小鼠血脑屏障通透性的干预效果。
2.8检测海马app相关蛋白及炎症介质
各组小鼠morris水迷宫实验测定结束后,抓取小鼠,眼球采血,获得眼部混合血,将小鼠血液滴入离心管内,静置1h,使用tgl-16g型台式离心机(上海安亭科学仪器厂)3000rpm/min离心20min,将血清转移到ep小管内,检测血清app相关蛋白,余下血清保存于-80℃冰箱备用。另外,迅速在冰上取材小鼠脑,去除小脑和脑干,取材海马,匀浆,4℃静置匀浆液1h,tgl-16g型台式离心机(上海安亭科学仪器厂)3000rpm/min离心20min,取上清液,分装,检测各组小鼠海马蛋白含量,余下样品保存于-80℃冰箱备用。按照试剂盒说明书,采用6100型酶标仪(美国rt公司)进行测定450nm波长处吸光度值(od),根据标准曲线方程及各孔吸光度值(od)计算海马app相关蛋白及炎症介质含量。
2.9测定抗氧化能力
各组小鼠morris水迷宫实验测定结束后,使用10%水合氯醛麻醉小鼠,取脑、流水清洗、取材海马、匀浆、静置1h,tgl-16g型台式离心机(上海安亭科学仪器厂)3000rpm/min离心20min,取各组小鼠海马上清液,进行分装,按照试剂盒说明书测定各组小鼠脑海马sod、gsh-px、t-aoc、mda含量.
2.10测定海马蛋白表达
各组小鼠灌胃给药结束后第2天,morris水迷宫实验测定结束后,使用10%水合氯醛麻醉各组小鼠,固定小鼠,剪开皮肤,充分暴露小鼠心脏,剪开右心耳,输液针头刺入左心室心尖处,缓慢匀速点滴各组小鼠生理盐水90ml,缓慢匀速灌注4%多聚甲醛约50ml,取材全脑,去除小脑和脑干,经过固定、脱水、透明、融化、切片,使用db-b2型烤片机(德国leica公司)烘烤后保存,按照试剂盒说明书采用免疫组织化学方法测定各组小鼠脑海马rage、lrp1、apoj、zo-1蛋白表达,采用hmias型高清晰度彩色分析系统(武汉千屏影像技术有限公司)分析,分析海马rage、lrp1、apoj、zo-1蛋白表达。
2.11测定海马mrna的表达
使用appliedbiosystems型定量pcr仪(美国应用生物系统公司),采用real-time-pcr测定各组小鼠海马rage、lrp1、apoj、zo-1mrna的表达。需要将新鲜小鼠脑海马rna,并反转录成cdna,设计各组小鼠海马rage、lrp1、apoj、zo-1mrna的特异性引物,加入特殊sybrgreeni荧光材料,设置参数包括50℃2min,95℃10min,95℃15s,60℃1min,40cycles,采用2-δδct法计算,使用appliedbiosystems型定量pcr仪(美国应用生物系统公司)分析计算小鼠海马rage、lrp1、apoj、zo-1mrna表达量。
2.12测定脏器指数
morris水迷宫实验测试结束后,断头处死小鼠,在超净工作台上解剖小鼠,取材小鼠脾、胸腺、脑、心、肺、肾、肝等脏器,洗涤脏器、吸干水分,使用plzoz-s型电子天平(赛多利斯公司)称量小鼠脏器质量,计算脏器指数,评价中药组合物对各组小鼠副作用。脏器指数(mg/g)=脏器质量(mg)/小鼠体重(g)
2.13测定小鼠体重
morris水迷宫实验测试结束后,测定各组小鼠体重,统计各组小鼠在给药过程中0d、8d、16d、24d、32d体重数据变化,评价中药组合物对各组小鼠副作用。
2.14统计分析
采用spss19.0软件分析小鼠实验数据,小鼠实验数据采用x±s表示,多组间比较采用单因素方差分析,p<0.05表示差异有统计学意义,p>0.05表示差异无统计学意义。
3结果
3.1中药组合物对血管性痴呆小鼠学习能力的影响
小鼠潜伏期可以评价血管性痴呆小鼠学习能力,随着各组小鼠训练时间延长,各组小鼠潜伏期表现出整体下降趋势。分析测试第5d各组小鼠潜伏期,结果表明,与对照组小鼠比较,模型组小鼠潜伏期明显延长(p<0.05),假手术组小鼠潜伏期改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组血管性痴呆小鼠潜伏期明显缩短(p<0.05),而低剂量组血管性痴呆小鼠潜伏期改变不明显(p>0.05)。见表1、见图1。
表1中药组合物对血管性痴呆小鼠学习能力的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.2中药组合物对血管性痴呆小鼠记忆能力的影响
小鼠游泳距离评价血管性痴呆小鼠记忆能力,随着各组小鼠训练时间延长,各组小鼠游泳距离表现出整体下降趋势。分析第5d各组小鼠游泳距离,结果表明,与对照组小鼠比较,模型组小鼠游泳距离明显增加(p<0.05),假手术组小鼠游泳距离改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠游泳距离明显减少(p<0.05),而低剂量组小鼠游泳距离改变不明显(p>0.05)。见表2、见图2。
表2中药组合物对血管性痴呆小鼠记忆能力的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.3中药组合物对血管性痴呆小鼠学习记忆保持能力的影响
小鼠目标象限停留时间和跨平台次数可以评价小鼠学习记忆保持能力。分析第5d各组小鼠目标象限停留时间和跨平台次数,结果表明,与对照组小鼠比较,模型组小鼠跨平台次数明显降低(p<0.05)且目标象限停留时间明显缩短(p<0.05),假手术组小鼠目标象限停留时间和跨平台次数改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠跨平台次数明显增加(p<0.05)且目标象限停留时间明显延长(p<0.05),而低剂量组小鼠目标象限停留时间和跨平台次数改变不明显(p>0.05)。见表3、见图3。
表3中药组合物对血管性痴呆小鼠学习记忆保持能力的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.4中药组合物对血管性痴呆小鼠脑bbb通透性的影响
脑bbb通透性使用eb浓度和eb含量表示。结果表明,与对照组比较,模型组小鼠脑eb浓度和eb含量明显增加(p<0.05),假手术组小鼠脑eb浓度和eb含量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠脑eb浓度和eb含量明显降低(p<0.05),而低剂量组小鼠脑eb浓度和eb含量改变不明显(p>0.05)。见表4、图4。
表4中药组合物对血管性痴呆小鼠脑bbb通透性的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.5中药组合物对血管性痴呆小鼠海马app相关蛋白的影响
结果表明,与对照组比较,模型组血管性痴呆小鼠海马app、海马aβ1-40、海马aβ1-42含量明显增加(p<0.05),假手术组小鼠海马app、海马aβ1-40、海马aβ1-42含量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马app、海马aβ1-40、海马aβ1-42含量明显降低(p<0.05),而低剂量组小鼠海马app、海马aβ1-40、海马aβ1-42含量改变不明显(p>0.05)。见表5、图5。
表5中药组合物对血管性痴呆小鼠海马app相关蛋白含量的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.6中药组合物对血管性痴呆小鼠海马炎症介质的影响
结果表明,与对照组比较,模型组小鼠海马炎症介质il-1β、tnf-α、il-6含量明显增加(p<0.05),假手术组小鼠海马炎症介质il-1β、tnf-α、il-6改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马炎症介质il-1β、tnf-α、il-6含量明显降低(p<0.05),而低剂量组小鼠海马炎症介质il-1β、tnf-α、il-6含量改变不明显(p>0.05)。见表6、图6。
表6中药组合物对血管性痴呆小鼠海马炎症介质的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.7中药组合物对血管性痴呆小鼠海马抗氧化能力的影响
结果表明,与对照组比较,模型组小鼠海马t-aoc、sod、gsh-px含量明显降低(p<0.05)且mda明显升高(p<0.05),假手术组小鼠海马t-aoc、sod、gsh-px、mda改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马t-aoc、sod、gsh-px含量明显升高(p<0.05)且mda明显降低(p<0.05),而低剂量组小鼠海马t-aoc、sod、gsh-px、mda含量改变不明显(p>0.05)。见表7、图7、图8、图9。
表7中药组合物对血管性痴呆小鼠海马抗氧化能力的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.8中药组合物对血管性痴呆小鼠海马lrp1、apoj、rage、zo-1表达的影响
结果表明,与对照组比较,模型组小鼠海马lrp1、apoj平均光密度值明显减少(p<0.05),rage、zo-1明显增加(p<0.05),假手术组小鼠海马lrp1、apoj、rage、zo-1平均光密度改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马lrp1、apoj平均光密度值明显增加(p<0.05),rage、zo-1明显减少(p<0.05),而低剂量组小鼠海马lrp1、apoj、rage、zo-1平均光密度值改变不明显(p>0.05)。见表8、图10。
表8中药组合物对血管性痴呆小鼠海马lrp1、apoj、rage、zo-1表达的影
响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.9中药组合物对血管性痴呆小鼠海马lrp1mrna表达的影响
结果表明,与对照组比较,模型组小鼠海马lrp1mrna相对表达量明显降低(p<0.05),假手术组小鼠海马lrp1mrna相对表达量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马lrp1mrna相对表达量明显升高(p<0.05),而低剂量组小鼠海马lrp1mrna相对表达量改变不明显(p>0.05)。见表9、图11。
表9中药组合物对血管性痴呆小鼠海马lrp1mrna表达的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.10中药组合物对血管性痴呆小鼠海马apojmrna表达的影响
结果表明,与对照组比较,模型组小鼠海马apojmrna相对表达量明显降低(p<0.05),假手术组小鼠海马apojmrna相对表达量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马apojmrna相对表达量明显升高(p<0.05),而低剂量组小鼠海马apojmrna相对表达量改变不明显(p>0.05)。见表10、图11。
表10中药组合物对血管性痴呆小鼠海马apojmrna表达的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.11中药组合物对血管性痴呆小鼠海马ragemrna表达的影响
结果表明,与对照组比较,模型组小鼠海马ragemrna相对表达量明显升高(p<0.05),假手术组小鼠海马ragemrna相对表达量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马ragemrna相对表达量明显降低(p<0.05),而低剂量组小鼠海马ragemrna相对表达量改变不明显(p>0.05)。见表11、图11。
表11中药组合物对血管性痴呆小鼠海马ragemrna表达的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.12中药组合物对血管性痴呆小鼠海马zo-1mrna表达的影响
结果表明,与对照组比较,模型组小鼠海马zo-1mrna相对表达量明显升高(p<0.05),假手术组小鼠海马zo-1mrna相对表达量改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠海马zo-1mrna相对表达量明显降低(p<0.05),而低剂量组小鼠海马zo-1mrna相对表达量改变不明显(p>0.05)。见表12、图11。
表12中药组合物对血管性痴呆小鼠海马zo-1mrna表达的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.13中药组合物对血管性痴呆小鼠脾指数、胸腺指数、脑指数的影响
结果表明,与对照组比较,模型组小鼠脾指数、胸腺指数、脑指数明显降低(p<0.05),假手术组小鼠脾指数、胸腺指数、脑指数改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组小鼠脾指数、胸腺指数、脑指数明显增加(p<0.05),而低剂量组小鼠脾指数、胸腺指数、脑指数改变不明显(p>0.05)。见表13、图12。
表13中药组合物对血管性痴呆小鼠脾指数、胸腺指数、脑指数的影响(
注:与对照组比较:1)p<0.05,2)p>0.05;与模型组比较:3)p<0.05,4)p>0.05
3.14中药组合物对血管性痴呆小鼠心指数、肾指数、肝指数、肺指数的影响
结果表明,与对照组比较,模型组小鼠心指数、肾指数、肝指数、肺指数改变不明显(p>0.05),假手术组小鼠心指数、肾指数、肝指数、肺指数改变不明显(p>0.05);与模型组比较,治疗组、高剂量组、中剂量组、低剂量组小鼠心指数、肾指数、肝指数、肺指数改变不明显(p>0.05)。见表14、图13。
表14中药组合物对血管性痴呆小鼠心指数、肾指数、肝指数、肺指数的影响(
注:与对照组比较:1)p>0.05;与模型组比较:2)p>0.05
3.15中药组合物对血管性痴呆小鼠体重的影响
结果表明,与对照组0d、8d、16d、24d、32d小鼠体重比较,模型组0d、8d、16d、24d、32d小鼠体重改变不明显(p>0.05),假手术组0d、8d、16d、24d、32d小鼠体重改变不明显(p>0.05);与模型组0d、8d、16d、24d、32d小鼠体重比较,治疗组、高剂量组、中剂量组、低剂量组0d、8d、16d、24d、32d小鼠体重改变不明显(p>0.05)。见表15、图14。
表15中药组合物对血管性痴呆小鼠体重的影响(
注:与对照组比较:1)p>0.05;与模型组比较:2)p>0.05
4结论
以上实验表明,中药组合物高、中剂量(39.73g/kg、19.86g/kg)可改善血管性痴呆小鼠学习记忆能力和血脑屏障通透性,还可改善海马炎症介质、app相关蛋白、抗氧化能力等,更可改善海马lrp1/rage相关蛋白和基因表达,且中药组合物高、中剂量(39.73g/kg、19.86g/kg)对血管性痴呆小鼠重要脏器的脏器指数和体重无影响,说明该中药组合物高、中剂量(39.73g/kg、19.86g/kg)治疗血管性痴呆有效并且无副作用。
- 还没有人留言评论。精彩留言会获得点赞!