用于治疗震颤的多模态刺激的制作方法
相关申请的交叉引用
本申请是2018年6月27日提交的美国专利申请no.16/020,876的继续申请,美国专利申请no.16/020,876是2016年9月27日提交的美国专利申请no.15/277,946的部分继续申请,美国专利申请no.15/277,946是2015年7月21日提交的美国专利申请no.14/805,385(现在是美国专利no.9,452,287)的继续申请,美国专利申请no.14/805,385是2014年1月21日提交的国际专利申请no.pct/us2014/012388的继续申请,国际专利申请no.pct/us2014/012388要求2013年1月21日提交的美国临时专利申请no.61/754,945、2013年3月15日提交的美国临时专利申请no.61/786,549、2013年4月25日提交的美国临时专利申请no.61/815,919、2013年5月10日提交的美国临时专利申请no.61/822,215和2013年7月23日提交的美国临时专利申请no.61/857,248中的每一个的优先权;这些专利申请中的每一个出于所有目的(包括在37c.f.r.§1.57下)通过引用以其整体并入本文。在本说明书中提到的所有专利公布和专利申请都以相同的程度通过引用并入本文,就好像每个单独的专利公布或专利申请均被具体地和单独地指出出于所有目的通过引用以其整体并入。
背景技术:
特发性震颤(et)是最常见的运动障碍,在美国估计影响了1000万患者,并且由于人口老龄化,人数不断增长。et的患病率随年龄增长而增加,从65岁以上人口的6.3%上升到95岁以上人口的20%以上。et的特征在于非自愿的振荡运动,通常在4-12hz之间。它(et)会产生声音振荡以及头部和四肢的不需要的移动。手和前臂的震颤尤其普遍,而且由于手和前臂的震颤使书写、打字、进食和饮水变得困难而成问题。与静止时存在的帕金森氏震颤不同,特发性震颤是姿势性和运动性的,这意味着震颤是通过分别在重力作用下或在移动过程中保持肢体引起的。
et伴随的残疾是多变的,并且范围从尴尬到无法独立生活,例如当由于手和手臂的不受控制的移动而无法进行书写和自己进食的任务时。尽管许多et患者患病率高且高度残疾,但仍没有足够的治疗选择来解决震颤。
已经发现,仅在60%的患者中,用于治疗震颤的药物(例如,普萘洛尔和扑米酮)可有效地将震颤幅度降低50%。这些药物的副作用可能很严重,许多et患者无法耐受。替代疗法是使用深部脑刺激(dbs)在脑内进行手术植入刺激物,这能够有效地将震颤幅度降低90%,但它是一种高侵入性的外科手术,其具有很大的风险并且很多et患者都无法耐受。因此,迫切需要针对et患者的替代疗法,这些疗法可减少震颤,而不会产生药物副作用,也不会造成脑部手术的风险。
对于患有站立性震颤、多发性硬化症和帕金森氏病的患者,震颤也是一个重要问题。多种神经障碍包括震颤(例如,中风、酒精中毒、酒精戒断、周围神经病变、威尔逊氏病、克雅氏病、格林-巴雷综合征和脆性x综合征)以及脑肿瘤、低血糖、甲状腺功能亢进、甲状旁腺功能减退、胰岛素瘤、正常衰老和外伤性脑损伤。口吃或结巴也是震颤的一种形式。这些情况下的震颤的潜在病因可能与et不同;然而,其中某些情况的治疗选择也很有限,而需要替代疗法。
技术实现要素:
et被认为是由与移动产生和控制相关联的回路动态中的异常引起的。先前的工作表明,冷却、局部镇痛药和振动可能会暂时改变这些回路动态。先前的工作报道,使用经皮电神经刺激(tens)进行的电刺激不会改善震颤(munhoz2003)。因此,令人惊讶的是,在我们的临床研究中发现,与et相关联的回路动态可通过周围神经刺激改变,从而导致患有et的个体的震颤大大降低。
若干实施例包括新颖的周围刺激设备,其用于沿着感觉神经向中枢神经系统发送信号以便修改异常的网络动态。随着时间推移,这种刺激使异常网络中的神经放电正常化并减少了震颤。在dbs直接刺激大脑时,我们的周围刺激会通过沿将周围神经连接到大脑的感觉神经发送信号来影响异常的大脑回路动态。这种方法是非侵入性的,并且有望避免dbs的手术风险以及与认知、陈述性和空间记忆性构音障碍、共济失调或步态障碍相关联的问题。周围神经刺激可通过移相(dephase)、覆盖或掩盖异常的脑回路动态来有效地治疗震颤。遵循传统dbs机制的假设,覆盖、掩盖或训练大脑以忽略异常的大脑回路动态。
也许与我们的方法最紧密相关的技术是经皮电神经刺激(tens)。高频tens(50至250hz)通常用于治疗疼痛,其假设是,大型的、有髓鞘的周围本体感受纤维(a-β)的激发会阻止传入的疼痛信号。尽管使用tens进行疼痛控制所取得的不一致的临床结果使许多人质疑其在疼痛治疗中的用途,但有充分证据表明,表面电刺激会激发a-β神经元。a-β神经元将本体感受感官信息传送到在包括et和帕金森氏病在内的疾病中为异常的相同的大脑回路中。不受任何提议的作用机制的限制,这使我们提出了神经刺激可用于激发a-β神经并由此改善震颤的观点。这个提议特别令人惊讶,因为munhoz等人的先前研究未能发现在应用tens后所测试的任何震颤参数有任何明显改善。参见munhoz等人的《经皮神经电刺激对震颤的急性作用(acuteeffectoftranscutaneouselectricalnervestimulationontremor)》,刊登于《运动障碍(movementdisorders)》(2003,18(2):191-194)。
本文公开的若干实施例涉及用于治疗震颤的系统、设备和方法,并且更具体地涉及用于通过刺激周围神经来治疗震颤的系统、设备和方法。
在一些实施例中,提供了一种减少患者震颤的方法。该方法包括将第一周围神经效应器放置在相对于第一周围神经的第一位置处;通过第一周围神经效应器向第一周围神经递送第一刺激;以及通过修改患者的神经网络动态来降低震颤幅度。
在一些实施例中,放置步骤包括将第一周围神经效应器放置在患者的皮肤上,并且第一刺激是施加到皮肤表面的电刺激。在一些实施例中,第一刺激具有约0.1ma至10ma或更高(例如,15ma)的幅度和约10至5000hz或更高的频率。在一些实施例中,第一刺激具有小于约15、14、13、12、11、10、9、8、7、6、5、4、3、2或1ma的幅度(例如,在约0.1ma和约1ma之间、在约0.1ma和约2ma之间、在约0.1ma和约3ma之间、在约0.1ma和约4ma之间、在约0.1ma和约5ma之间、在约0.1ma和约6ma之间、在约0.1ma和约7ma之间、在约0.1ma和约8ma之间、在约0.1ma和约9ma之间、在约0.1ma和约10ma之间、在约0.1ma和约11ma之间、在约0.1ma和约12ma之间、在约0.1ma和约13ma之间、在约0.1ma和约14ma之间、在约0.1ma和约15ma之间或在此类值之间的其他范围)。在一些实施例中,第一刺激具有在约10hz和约20khz之间的频率(例如,约10hz、约20hz、约30hz、约40hz、约50hz、约60hz、约100hz、约250hz、约500hz、约1000hz、约2500hz、约5000hz、约10khz、约15khz、约20khz以及在此类值之间的范围)。
在一些实施例中,放置步骤包括将第一周围神经效应器植入患者体内,并且第一刺激是电刺激。在一些实施例中,植入步骤包括将第一周围神经效应器注射到患者体内。在一些实施例中,第一刺激具有小于约3ma的幅度和约10至5000hz的频率。在一些实施例中,第一刺激具有小于约5、4、3、2或1ma的幅度(例如,在约0.1ma和约1ma之间、在约0.1ma和约2ma之间、在约0.1ma和约3ma之间、在约0.1ma和约4ma之间、在约0.1ma和约5ma之间或在此类值之间的其他范围)。在一些实施例中,第一刺激具有在约10hz和约20khz之间的频率(例如,约10hz、约20hz、约30hz、约40hz、约50hz、约60hz、约100hz、约250hz、约500hz、约1000hz、约2500hz、约5000hz、约10khz、约15khz、约20khz以及在此类值之间的范围)。
在一些实施例中,周围神经效应器包括电源。在一些实施例中,该方法还包括通过位于外部的电源为第一周围神经效应器无线供电。
在一些实施例中,第一刺激包括振动触觉的。在一些实施例中,第一刺激包括化学的。在一些实施例中,第一刺激包括机械的、振动的、机电的、热的、辐射的、电的、磁的、电磁的、光的、声的、超声的(例如,聚焦超声的)、化学的、红外的、射频(rf)的、紫外线的、x射线的或微波的。在一些实施例中,第二或第三刺激与第一刺激相同,但是在身体上的不同位置处。在另一些实施例中,第二或第三刺激与第一刺激不同,并且在身体上的相同或不同的位置处。例如,将第一刺激施加到手腕并且将不同的第二刺激施加在不同的位置。替代地,将第一刺激施加到第一位置(例如,手腕)并且将不同的第二刺激施加到相同的第一位置。可以在第一位置上刺激相同或不同的神经。例如,在一些实施例中,刺激一个区域中的不同神经(或多个位置点)。在若干实施例中,代替或除了在皮肤表面上之外,可以在身体内施加刺激或其他神经调节(例如,设备的部分或完全植入、口服递送等)。
通过减少习惯性、提高疗效、改善优先刺激的神经纤维的特异性、利用其他基于非能量的疗法(例如,药物疗法)产生协同作用、提高刺激效率以影响神经回路和/或减少至少一种刺激至少一个的量或持续时间等,在一些实施例中使用多模态方法(无论这种方法是否包括多个位置、相同刺激的多种类型或多个刺激等,或其组合)是有益的。例如,在手腕和第二位置(例如,脚踝、耳朵、手指等)上进行的治疗可能会导致震颤更快的减少、震颤减少的持续时间更长、递送总体减少量的刺激、患者依从性提高等。在另一个示例中,在同一区域中使用不同的点可以提供类似的有益结果(例如,手腕上的不同的点)。在一个实施例中,同一区域中的不同点彼此之间的距离在约5mm、25mm、50mm、100mm和200mm内(例如,在手腕或脚踝上)。在另一些实施例中,同一区域中的不同点彼此之间的距离在约0.25英尺-4英尺内(例如,在腿上)。
在许多实施例中,使用多模态方法来治疗特发性震颤。在一些实施例中,使用多模态方法来治疗肌张力障碍、帕金森氏病和其他运动障碍。在若干实施例中,在同一个人中治疗手、腿、头部、颈部和/或声音震颤。在另一些实施例中,治疗患有手部震颤或腿震颤的患者。
在一些实施例中,与单模式方法或不治疗相比,多模态方法使达到功效(例如,震颤减少)所需的时间减少了10-75%或使治疗效果的时长增加了10-75%。例如,在一些实施例中,多模态方法可以减少刺激期间以及在刺激后30分钟、1-2小时和6小时或更长的时间段内的震颤。在一些实施例中,每天提供一次、两次、三次、四次、五次或更多次刺激。在若干实施例中,提供了使用反馈的多模态优化方法。
在一些实施例中,该方法还包括:使用测量单元来感测患者四肢的移动以产生运动数据;以及从运动数据中确定震颤信息。在一些实施例中,递送包括基于震颤(或其他)信息递送第一刺激。在一些实施例中,该信息(例如,震颤信息)包括与患者四肢的静止位置的最大偏差。在一些实施例中,该信息(例如,震颤信息)包括患者四肢的静止位置。在一些实施例中,震颤信息包括震颤频率、相位和幅度。
在一些实施例中,递送第一刺激包括递送多个刺激突发,在所述刺激突发之间具有可变的时间延迟。
在一些实施例中,该方法还包括:将第二周围神经效应器放置在相对于第二周围神经的第二位置处;以及通过第二周围神经效应器向第二周围神经递送第二刺激。根据若干实施例,效应器被放置在同一大体区域(例如,手腕)上的两个或更多个点上,或者被放置在两个或更多个位置(例如,手腕和脚踝)上。
在一些实施例中,该方法还包括确定患者的震颤或其他功能障碍的时间段,其中递送第二刺激包括使第二刺激的递送与第一刺激的递送的偏移量为震颤或其他功能障碍的时间段的预定分数或倍数。在一些实施例中,该方法还包括使患者大脑中的神经网络的同步性移相。在一些实施例中,第二刺激设置在与第一刺激相同的位置或不同的位置。第二刺激可以与第一刺激相同(例如都是电的或机械的)或不同。第二刺激可以与第一刺激相同,但是具有不同的参数(例如,不同的幅度、持续时间、频率等)。
在一些实施例中,第一位置和第二位置位于相邻的手指上。在一些实施例中,第一周围神经和第二周围神经是相邻的神经。在一些实施例中,第一周围神经是正中神经而第二周围神经是尺神经或桡神经。在一些实施例中,第一周围神经和第二周围神经在体位上相邻。
在一些实施例中,第一刺激具有低于感觉阈值的幅度。在一些实施例中,第一刺激大于15hz。在一些实施例中,第一周围神经携带来自患者四肢的本体感受信息。在一些实施例中,该方法还包括:确定第一刺激对减小震颤幅度的功效的持续时间;以及在功效的持续时间到期之前输送第二刺激。
在一些实施例中,确定效果的持续时间包括分析在预定时间段内施加的多个刺激应用。可以顺序地(例如,串行地或一个接一个地)和/或至少部分地重叠(例如,并行地)施加刺激。
在一些实施例中,确定功效的持续时间还包括确定患者的活动概况。在一些实施例中,确定功效的持续时间还包括确定震颤或其他功能障碍的概况。在一些实施例中,活动概况包括关于咖啡因和酒精消耗的数据。在一些实施例中,该方法还包括将传导通路增强器放置在第一周围神经上。在一些实施例中,传导通路增强器是导电纹身。在一些实施例中,传导通路增强器包括一个或多个导电条。
在一些实施例中,第一位置选自由手腕、前臂、腕管、手指和上臂组成的组。
在一些实施例中,提供了一种用于治疗患者的震颤或其他功能障碍的系统。设备可包括:决策单元;以及适于向周围神经递送电刺激的接口单元,该接口单元包括与决策单元通信的第一周围神经效应器,该第一周围神经效应器包括至少一个电极;其中该决策单元包括处理器和存储指令的存储器,所述指令在由处理器执行时使决策单元:通过第一周围神经效应器向第一周围神经递送第一电刺激,该电刺激由控制器配置以通过修改患者的神经网络动态来减少患者四肢的震颤或其他功能障碍。
在一些实施例中,第一电刺激具有小于约10ma或更高(例如,15ma)的幅度以及约10至5000hz的频率。在一些实施例中,幅度小于约15、14、13、12、11、10、9、8、7、6、5、4、3、2或1ma(例如,在约0.1ma和约1ma之间、在约0.1ma和约2ma之间、在约0.1ma和约3ma之间、在约0.1ma和约4ma之间、在约0.1ma和约5ma之间、在约0.1ma和约6ma之间、在约0.1ma和约7ma之间、在约0.1ma和约8ma之间、在约0.1ma和约9ma之间、在约0.1ma和约10ma之间、在约0.1ma和约11ma之间、在约0.1ma和约12ma之间、在约0.1ma和约13ma之间、在约0.1ma和约14ma之间、在约0.1ma和约15ma之间或在此类值之间的其他范围)。在一些实施例中,第一电刺激具有在约10hz和约20khz之间的频率(例如,约10hz、约20hz、约30hz、约40hz、约50hz、约60hz、约100hz、约250hz、约500hz、约1000hz、约2500hz、约5000hz、约10khz、约15khz、约20khz以及在此类值之间的范围)。
在一些实施例中,接口单元还包括与决策单元通信的第二周围神经效应器,该第二周围神经效应器包括至少一个电极,其中存储器存储指令,所述指令在由处理器执行时进一步使决策单元通过第二周围神经效应器向患者四肢中的第二周围神经递送第二电刺激。
在一些实施例中,所述指令在由处理器执行时使决策单元递送第二电刺激,第二电刺激与第一电刺激在时间上的偏移量为震颤或其他功能障碍的时间段的预定分数或倍数。
在一些实施例中,第一周围神经效应器适用于放置在第一手指上,而第二周围神经效应器适用于放置在第二手指上。
在一些实施例中,第一周围神经效应器包括布置成线性阵列的多个电极。在一些实施例中,所述多个电极间隔开约1至100mm。在一些实施例中,第一周围神经效应器包括布置成二维阵列的多个电极。在一些实施例中,存储器存储指令,所述指令在由处理器执行时进一步使决策单元基于第一周围神经效应器在患者四肢上的位置来选择多个电极的子集,其中每当第一周围神经效应器在四肢上定位或重新定位时,就发生对多个电极的子集的选择。在一些实施例中,所述多个电极沿着第一轴线间隔开约1至100mm,并且沿着垂直于第一轴线的第二轴线间隔开约1至100mm。在一些实施例中,所述电极中的一些彼此相邻以形成带。在一些实施例中,间距能够小于约100、90、80、70、60、50、40、30、20、10、5、4、3、2或1mm(例如,在约0.1mm和约1mm之间、在约1mm和约2mm之间、在约1mm和约3mm之间、在约1mm和约4mm之间、在约1mm和约5mm之间、在约1mm和约10mm之间、在约1mm和约20mm之间、在约1mm和约30mm之间、在约1mm和约40mm之间、在约1mm和约50mm之间、在约1mm和约60mm之间、在约1mm和约70mm之间、在约1mm和约80mm之间、在约1mm和90mm之间、在约1mm和约100mm之间或在此类值之间的其他范围)。
在一些实施例中,该系统还包括测量单元,其中存储器存储指令,所述指令在由处理器执行时进一步使决策单元:使用测量单元来测量患者四肢的运动以产生运动数据;以及基于对运动数据的分析来确定震颤频率和量值(或其他参数)。
在一些实施例中,对运动数据的分析包括对移动数据的频谱功率的频率分析。在一些实施例中,频率分析被限制在约4至12hz之间。在一些实施例中,频率分析被限制在大约一个或多个所关注的震颤的预期频率范围内。在一些实施例中,对运动数据的分析是在运动数据的预定时间长度内完成的。在一些实施例中,决策单元还适于基于运动数据来确定震颤相位信息以及基于震颤相位信息来递送第一电刺激。在一些实施例中,震颤相位信息包括峰值震颤偏差,决策单元还适于在与峰值震颤偏差相对应的时间递送第一电刺激。
在一些实施例中,对于震颤和其他适应症,存储器存储指令,所述指令在由处理器执行时进一步使决策单元将第一电刺激作为多个电刺激突发递送,在所述电刺激突发之间具有可变的时间延迟。在一些实施例中,存储器存储指令,所述指令在由处理器执行时进一步使决策单元基于所确定的震颤频率来设置第一电刺激的参数。在一些实施例中,存储器存储指令,所述指令在由处理器执行时进一步使决策单元基于所确定的震颤量值来设置第一电刺激的参数。在一些实施例中,存储器存储指令,所述指令在由处理器执行时进一步使决策单元将所确定的震颤量值(或其他数据)与预定阈值进行比较;并且其中当所确定的震颤量值(或其他数据)超过预定阈值时,递送第一电刺激。在一些实施例中,电极适于通过患者的皮肤递送第一电刺激。在一些实施例中,电极适于被植入并递送电。在一些实施例中,决策单元包括用户接口,该用户接口适于接收来自用户的用以调整第一电刺激的参数的输入。在一些实施例中,存储器还存储一个或多个预定刺激协议的库。在一些实施例中,接口单元与决策单元集成在一起。在一些实施例中,接口单元和决策单元彼此分开并且具有分开的壳体。在一些实施例中,决策单元被配置为向接口单元无线地提供电力或与其通信。在一些实施例中,该系统还包括位于决策单元中的测量单元。在一些实施例中,该系统还包括位于接口单元中的测量单元。在一些实施例中,决策单元是选自由智能电话、平板电脑和笔记本电脑组成的组的计算设备。在一些实施例中,该系统还包括与计算设备通信的服务器,该服务器被配置为从计算设备接收运动数据以及递送给患者的电刺激的历史。在一些实施例中,服务器被编程为:将所接收的运动数据和递送给患者的电刺激的历史添加到存储来自多个患者的数据的数据库。在一些实施例中,服务器被编程为:将所接收的运动数据和递送给患者的电刺激的历史与数据库中存储的数据进行比较;基于所接收的运动数据与递送给患者的电刺激的历史与数据库中存储的数据的比较,确定修改的电刺激协议;以及将修改的电刺激协议传输到计算设备。在一些实施例中,电子器件是柔性并且设置在柔性基板上,该柔性基板可以是袖套、衬垫、束带或其他壳体。
在一些实施例中,提供了一种用于监测患者四肢的震颤或其他功能障碍的系统。该系统可以包括:接口单元,其具有用于捕获运动数据的惯性运动单元、电源以及无线发射器和接收器,该接口单元适于戴在患者四肢上;以及与接口单元通信的处理单元,该处理单元被配置为从接口单元接收运动数据。在一个实施例中,处理单元被编程为基于对运动数据的分析来确定在预定时间段内的震颤签名和概况(signatureandprofile)。在另一个实施例中,处理单元被编程为基于数据分析来确定在预定时间段内的神经或移动签名和概况。在另一个实施例中,处理单元被设置在设备中或与设备无线通信的远程处理器上,并且被编程为分析神经或移动数据的预定特征。
在若干实施例中,多模态方法基于监测,其中基于在第一模式被激活后接收到的反馈来提供第二模式(例如,在第二身体位置处的相同或不同的刺激、在相同或不同身体位置处的不同刺激等)。在一些实施例中,第二模式可以是不同类型的能量(例如,热的、机械的、化学的等)或具有不同刺激参数(例如,频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、突发等)的相同类型的能量。在一些实施例中,提供了一种设备,该设备基于受试者的先前反应和/或从传感器测量的神经或移动数据的预定特性或特征来调整刺激模态以增强功效。在一些实施例中,提供一个或多个传感器以调整第二(或第三或以上)模式的参数。在一些实施例中,这有利于减少达到治疗效果所需的时间(例如,减少至少10%、25%、50%或更多,或者减少其中重叠的范围)或延长治疗效果(例如,延长至少10%、20%、40%或更多,或者增加其中重叠范围),或改善总体益处(例如,更大程度地降低手部震颤水平)。
在一些实施例中,处理单元是移动电话。在一些实施例中,该系统还包括与移动电话通信的服务器,该服务器被配置为从移动电话接收运动数据。在一些实施例中,处理单元还被编程为将震颤量值或其他数据与预定阈值进行比较。在一些实施例中,处理单元还被编程为当震颤量值或其他因素超过预定阈值时产生警报。在一些实施例中,预定阈值可由患者调整。在一些实施例中,处理单元被编程为提示患者输入活动数据,该活动数据包括对活动的描述和活动发生的时间。在一些实施例中,处理单元被编程为将活动数据与所确定的震颤频率和量值相互关联。在一些实施例中,活动数据包括咖啡因或酒精的消耗。在一些实施例中,活动数据包括药物的消耗。
不同的刺激模式或多模态刺激可包括刺激的不同位置。不同的刺激模式或多模态刺激可包括不同类型的能量以及与基于非能量的疗法(例如,药物疗法)相结合的能量模态。不同的刺激模式或多模态刺激可包括相同类型的能量的不同刺激参数(例如,频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间和/或突发)。不同的刺激模式或多模态刺激可包括不同类型的刺激,以选择性地或优先刺激独特的纤维类型和/或神经类型,包括传入和传出刺激。不同的刺激模式或多模态刺激可包括数个刺激目标或参数以优先影响自主神经系统的四肢之一。不同的刺激模式或多模态刺激可包括数个持续时间。不同的刺激模式或多模态刺激可包括将不同的图案/模式(pattern)应用于设备阵列(例如,成对的电极的线性阵列)。不同的刺激模式或多模态刺激可包括上述不同模式中的两个或更多个的组合。在一些实施例中,多模态系统可包括多个刺激物,所述多个刺激物彼此无线通信并提供同步的模式化刺激。在一些实施例中,数个刺激物可与数个效应器连接以同时刺激数个神经。在一个实施例中,一种系统可包括在手腕上的以正中神经为目标的刺激物以及在耳朵中的以迷走神经耳支为目标的刺激物。
在一些实施例中,提供了一种用于治疗病症(包括但不限于震颤)的系统,该系统包括:第一刺激执行器,其被配置为对第一周围神经(例如,本体感受器、传入神经、a纤维、b纤维、c纤维等)施加第一刺激模式;第二刺激执行器,其被配置为对第二周围神经(例如,本体感受器、传入神经、a纤维、b纤维、c纤维等)施加第二刺激模式;以及控件模块,其与第一刺激执行器和第二刺激执行器通信。在一个实施例中,第二刺激模式不同于第一刺激模式。在另一个实施例中,两种模式是相同的(例如,相同的位置、都为电刺激、都为兴奋性的、都为抑制性的等)。在一些实施例中,可使用三种、四种或更多种模式。除震颤之外,还治疗膀胱过度活动症和心脏功能障碍。在一个实施例中,治疗精神疾病(例如,患有神经传递功能障碍)。
在一些实施例中,第一刺激执行器或第二刺激执行器中的至少一个可包括电执行器(例如,用于递送电刺激的装置,包括例如元件、设备、机构、部件、部分(例如,电极)、影响器或诸如此类)。电部分可以是经皮的。电部分可以是皮下的。第一刺激执行器可包括第一电部分。第二刺激执行器可包括第二电部分。
第一刺激模式可包括参数的第一值。第二刺激模式可包括与该参数的第一值不同的该参数的第二值。
参数可包括刺激频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间或突发中的至少一个。参数可包括刺激连续性。第一刺激模式可包括突发。第二刺激模式可包括连续。参数可包括刺激频率。第一刺激模式可包括介于10hz和30hz之间(例如,20hz)。第二刺激模式可包括介于30hz和50hz之间(例如,40hz)。第一刺激模式可包括介于100hz和200hz之间(例如,150hz)。第二刺激模式可包括介于50hz和150hz之间(例如,100hz)。在一些实施例中,第一刺激和第二刺激可以以交替模式以介于4-12hz之间的频率突发开/关,例如在突发模式中(例如10hz)。参数可包括刺激波形。第一刺激模式可包括第一刺激波形。第二刺激模式可包括与第一刺激波形不同的第二刺激波形。
第一刺激执行器或第二刺激执行器中的至少一个可包括热设备、部件、执行器或者增加和/或降低旁组织的内部温度的部分(诸如用于加热和/或冷却的装置(例如,电阻加热器、压电冷却器、基于流体的温度空间),包括例如元件、设备、机构、部件、部分、影响器或诸如此类)。热设备可被配置为施加冷却效果。热设备可被配置为施加加热效果。温度传感器也可包括在内并且提供与处理器或控件模块的通信,具有或不具有影响冷却或加热的反馈。
第一刺激执行器或第二刺激执行器中的至少一个可包括振动或机械致动执行器(诸如用于振动、产生产生振动并将振动传递到例如皮肤的装置(例如,振动器、声波系统、螺线管、偏置马达),包括例如元件、设备、机构、部件、或部分影响器或诸如此类)。在一些实施例中,被配置为施加非振动的机械能的机械执行器可以被激活以在诸如穴位点的特定位置施加压力。在一些实施例中,具有圆形端部或其他形状的元件的钉可由马达或螺线管驱动,以从穿戴在身体部位周围的束带伸出到皮肤中,以对神经(例如,对于腕带而言为正中神经)施加压力。在一些实施例中,穿戴在身体部位周围的束带可由马达或螺线管驱动,以增加张力或收紧该束带,以对神经(例如,对于腕带而言为正中神经)施加压力。第一刺激执行器或第二刺激执行器中的至少一个可包括磁执行器(诸如用于产生磁场的装置(例如,磁体、电磁体),例如包括元件、设备、机构、部件、部分、影响器或诸如此类)。第一刺激执行器或第二刺激执行器中的至少一个可包括化学物质(例如,药物治疗或利多卡因)。第一刺激执行器或第二刺激执行器中的至少一个可包括超声(例如,聚焦超声)执行器(诸如用于产生超声能量的装置(例如,换能器、压电元件、耦合流体),例如包括元件、设备、机构、部件、部分、影响器或诸如此类)。第一刺激执行器或第二刺激执行器中的至少一个可包括微波执行器(诸如用于产生微波能量的装置(例如,微波发生器),例如包括元件、设备、机构、部件、或部分影响器或诸如此类)。在一些实施例中,第一刺激执行器或第二刺激执行器中的至少一个包括用于产生电磁能、波、场等的电磁执行器。在一些实施例中,除了第二刺激执行器之外,还使用第三、第四或附加的刺激执行器。
第一刺激执行器可被配置为定位在受试者的手腕上。第二刺激执行器可被配置为定位在受试者的手指上。第二刺激执行器可被配置为定位在受试者的脚踝上。第一位置可包括身体的手臂,而第二位置可包括身体的腿。第一位置可以是身体的左臂或左腿,而第二位置可以是身体的右臂或右腿,以提供双侧刺激。
该系统还可包括传感器。控件模块可被配置为在检测到事件时启动第一刺激模式或第二刺激模式中的至少一个。
在一些实施例中,用于治疗受试者的震颤的系统可包括第一刺激执行器和与第一刺激执行器通信的控件模块。第一刺激执行器被配置为向第一周围神经(例如,本体感受器、传入神经、a纤维、b纤维、c纤维等)施加第一刺激模式和第二刺激模式,第一刺激模式包括参数的第一值,第二刺激模式包括与该参数的第一值不同的该参数的第二值。
第一刺激执行器可包括电极(例如,1-6个或更多个电极)。电极可以是经皮或皮下的。
参数可包括刺激频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间或突发中的至少一个。参数可包括刺激连续性。第一刺激模式可包括突发。第二刺激模式可包括连续。参数可包括刺激频率。第一刺激模式可包括介于10hz和30hz之间(例如,20hz)。第二刺激模式可包括30hz至50hz(例如,40hz)。第一刺激模式可包括介于100hz和200hz之间(例如,150hz)。第二刺激模式可包括介于50hz和150hz之间(例如,100hz)。在一些实施例中,第一刺激和第二刺激可以以交替模式以介于4-12hz之间的频率突发开/关,例如在突发模式中(例如10hz)。参数可包括刺激波形。第一刺激模式可包括第一刺激波形。第二刺激模式可包括与第一刺激波形不同的第二刺激波形。
该系统还可包括第二刺激执行器。第二刺激执行器可包括电极。第二刺激执行器可包括热执行器。刺激执行器可包括机械的、振动的、机电的、热的、辐射的、电的、磁的、电磁的、光的、声的、化学的、超声的(例如,聚焦超声)、红外的、射频的(rf)、紫外线的、x射线的或微波的执行器。任选地包括传感器,并且其可改变各种执行器的神经调节。
第一刺激执行器可被配置为定位在受试者的手腕上。第二刺激执行器可被配置为定位在受试者的手指或脚踝上。在一个实施例中(例如,在手腕、手指、脚踝等周围的各个点处)使用例如束带、袖带等来提供圆周刺激。在一些实施例中,脚、脚踝、膝盖、大腿、背部、骶区、腰区、耳朵、头部和/或颈部和/或以神经为目标的位置(包括胫神经、隐神经、骶神经、腓神经、腓肠神经和/或迷走神经)对治疗膀胱过度活动症可能是有益的。
在一些实施例中,一种用于治疗受试者的震颤或其他适应症的系统和方法包括将第一刺激施加到第一周围身体部位,以及将第二刺激施加到与第一周围身体部位不同的第二周围身体部位。第一刺激包括电刺激、振动刺激、热刺激或化学刺激中的至少一种。第二刺激包括电刺激、振动刺激、热刺激或化学刺激中的至少一种。第二刺激不同于第一刺激。
在一些实施例中,一种用于治疗受试者的震颤或其他适应症的系统和方法包括将第一刺激施加到第一周围神经(例如,本体感受器、传入神经、a纤维、b纤维、c纤维等),以及将第二刺激施加到第二周围神经(例如,本体感受器、传入神经、a纤维、b纤维、c纤维等)。第一刺激包括电刺激、振动刺激、热刺激或化学刺激中的至少一种。第二刺激包括电刺激、振动刺激、热刺激或化学刺激中的至少一种。在一个实施例中,第二刺激与第一刺激不同,但在另一些实施例中可以是相同的。在一些实施例中,第一刺激包括电刺激、磁刺激、化学刺激、热刺激、振动刺激、超声刺激(例如,聚焦超声)、射频刺激或微波刺激中的至少一种,而第二或附加的刺激包括电刺激、磁刺激、化学刺激、热刺激、振动刺激、超声刺激(例如,聚焦超声)、射频刺激或微波刺激中的至少一种。
在一些实施例中,第一和第二(以及任选的第三、第四或更多)刺激包括电刺激。第一刺激可包括参数的第一值。第二(及任何附加)刺激可包括与该参数的第一值不同的该参数的第二值。参数可包括刺激频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间或突发中的至少一个。参数可包括刺激连续性。第一刺激模式可包括突发。第二刺激模式可包括连续。参数可包括刺激频率。第一刺激模式可包括介于10hz和30hz之间(例如,20hz)。第二刺激模式可包括介于30hz和50hz之间(例如,40hz)。在一个实施例中,第一刺激小于40hz并且第二刺激为40hz或更高。在另一个实施例中,第一刺激小于20hz并且第二刺激为20hz或更高。第一刺激模式可包括介于100hz和200hz之间(例如,150hz)。第二刺激模式可包括介于50hz和150hz之间(例如,100hz)。在一些实施例中,第一刺激和第二刺激可以以交替模式以介于4-12hz之间的频率突发开/关,例如在突发模式中(例如10hz)。参数可包括刺激波形。第一刺激模式可包括第一刺激波形。第二刺激模式可包括与第一刺激波形不同的第二刺激波形。
在一些实施例中,第一和第二(以及任选的第三、第四或更多)刺激包括化学刺激。第一刺激可包括第一神经调节化学物质。第二(及任何附加)刺激可包括与第一神经调节化学物质不同的第二神经调节化学物质。
在一些实施例中,第一和第二(以及任选的第三、第四或更多)刺激包括机械刺激。在一个实施例中,刺激具有不同的振动持续时间和/或频率。在另一个实施例中,机械执行器被激活以将受控压力施加到特定位置,诸如目标神经或穴位点。机械执行器可包括线性执行器或旋转执行器,其使神经附近的组织移位以施加压力,以便激活目标区域或目标神经中的本体感受器。
在一些实施例中,第一和第二(以及任选的第三、第四或更多)刺激包括同一区域中的不同点处的不同刺激。例如,在第一点处施加一定频率、持续时间和/或幅度的电刺激,并且在第二点处施加不同频率、持续时间和/或幅度的电刺激。这两个点可在手腕上的不同位置处,并且可以刺激相同或不同的神经。刺激可以是同时的和/或顺序的或重叠的。可以从线性或周向布置在束带中或皮肤界面上的多个电极的一边到另一边对刺激进行模式化。在一个实施例中也使用三模态方法,其中,例如刺激手腕上的三个点。代替手腕或除手腕之外,治疗点(无论是两个、三个还是更多个点)可位于脚踝、膝盖、大腿、上臂、手指、脚趾、耳朵、胸部、背部、肩部、头部、颈部等上。
在一个实施例中,以多模态双重方法顺序和/或同时提供电和机械(例如,振动)。在一个实施例中,在同一位置(例如,手腕上的同一点)处提供双重刺激。在另一个实施例中,在同一区域中但在不同点(例如,手腕上的不同点)处提供双重刺激。在又一个实施例中,在不同区域(例如,手腕和脚踝)处提供双重刺激。在一些实施例中,提供了第三、第四或附加刺激。
在一些实施例中,将第一刺激施加到第一位置,将第二刺激施加到第二位置,并且任选地将第三刺激施加到第三位置,并且将第四刺激施加到第四位置。在一个实施例中,一个或多个位置不同于其他位置。
在一个实施例中,第一、第二、第三或附加位置选自手腕、手指、脚趾、耳朵、脚踝、膝盖、大腿、上臂、背部、胸部、手、脚、头部、颈部等。可以使用袖带或束带,并且其可以是柔性的以适应受试者。也可使用贴片。在一些实施例中,可使用1-12个(或更多个)电极(诸如2、4、6、8、10个以及其中的范围)。电极可以排列成阵列(例如,线性阵列)。
在一些实施例中,一种治疗受试者的震颤的方法包括将来自第一执行器的第一刺激施加到所述受试者的身体上的第一位置,以及施加来自第二执行器的第二刺激。第一刺激包括电刺激。第一执行器包括电极。第二刺激包括振动刺激。使用柔性袖带将第一执行器和第二执行器耦接到手臂、手腕、腿、膝盖或脚踝中的一者。施加第一刺激或施加第二刺激中的至少一者响应于智能设备中的控制器并且基于疾病的感测和预定的特性。在施加第一刺激和施加第二刺激之后,疾病症状减轻。
将来自第二执行器的第二刺激施加到身体上的第二位置。第二位置可与第一位置间隔一距离。
在一些实施例中,系统和方法可涉及传入(感觉)刺激与神经、肌肉或两者的运动(传出)刺激的结合,包括但不限于功能性电刺激。在一些情况下,功能性电刺激(fes)能够异相地激活震颤性肌肉以减轻震颤。在另一些实施例中,可以用诸如陀螺仪(例如,旋转偏心块)的工具与如本文其他地方所述的利用能量或其他模态的神经刺激相结合来机械地阻尼(damper)震颤。在一些实施例中,控制器能够从被配置为测量患者的参数(例如,震颤幅度)的一个或多个传感器接收实时或接近实时的反馈,并且在震颤幅度被测量为高于预定阈值水平时施加fes和/或机械阻尼。
我们发明了一种周围神经刺激设备和方法,该设备和方法有效地减少震颤,而没有药物副作用,也没有脑部手术的风险。我们的方法是安全的,并且在一些实施例中是非侵入性的,并且在减轻震颤方面有效。在一些实施例中,该设备可以通过改变与特发性震颤、帕金森氏震颤和其他震颤相关联的神经回路动力学来起作用。该设备易于使用、舒适且可调整以为每位患者提供最佳治疗。在一些实施例中,本文公开的多模态设备和方法还能够用于多种其他非限制性适应症。此类适应症可包括但不限于心脏功能障碍(例如,节律不齐,诸如心房颤动、心房扑动、室性心动过速等)和异常血压(高血压和低血压)。其他非限制性适应症包括泌尿和/或胃肠道功能障碍(包括膀胱过度活动症、夜尿症和/或压力和急迫性尿失禁)以及大便失禁。在一些实施例中,可以治疗具有神经学成分的精神疾病(诸如神经递质功能障碍)。也可治疗偏头痛。
在一个实施例中,在以下一处使用第一电刺激和第二振动刺激以多模态方式治疗膀胱过度活动症:包括脚、脚踝、膝盖、大腿、背部、骶区、腰区、耳朵、头部和/或颈部的位置,和/或以神经为目标的位置,包括胫神经、隐神经、骶神经、腓神经、腓肠神经和/或迷走神经。在一些实施例中,在两个或更多个不同位置处提供电刺激。
在一个实施例中,在以下一处使用第一电刺激和第二振动刺激以多模态方式治疗心脏功能障碍:包括手腕、手臂、手指、肩部、颈部、头部、经颅、耳朵、耳内、耳屏、耳甲艇、背部或胸部的位置,和/或以神经为目标的位置,包括正中神经、桡神经、尺神经、迷走神经、耳迷走神经或三叉神经、正中神经、桡神经、尺神经、腓神经、隐神经、胫神经和/或肢体上可触及的其他神经或经络。在一些实施例中,在两个或更多个不同位置处提供电刺激。
在一个实施例中,在以下一处使用第一电刺激和第二振动刺激以多模态方式治疗神经递质功能障碍(例如,抑郁、焦虑和其他精神疾病):包括手腕、手臂、手指、肩部、颈部、头部、经颅、耳朵、耳内、耳屏、耳甲艇、背部或胸部的位置,和/或以神经为目标的位置,包括正中神经、桡神经、尺神经、迷走神经、耳迷走神经或三叉神经、正中神经、桡神经、尺神经、腓神经、隐神经、胫神经和/或肢体上可触及的其他神经或经络。在一些实施例中,在两个或更多个不同位置处提供电刺激。
对于适应症(诸如膀胱过度活动症、心脏功能障碍、精神疾病和其他适应症)而言,电和振动调节是多模态方法的非限制性示例。其他调节模态包括但不限于磁、化学(药理)、热、超声(例如,聚焦超声)、声波、射频和微波。根据若干实施例,多模态方法还包括在身体上的不同位置处或同一区域中的不同点处使用相同模态。多模态方法还包括在身体的相同或不同位置处或同一区域中的相同或不同点处使用具有不同参数的相同模态,和/或使用不同刺激模式。
在若干实施例中,当在不同位置使用两个或更多个设备时,设备可彼此进行通信,经由有线连接进行通信或经由标准无线通信协议(诸如rf、wifi、蓝牙、蜂窝、或zigbee)进行无线通信。在另一个实施例中,数个设备进行通信以在相同或不同位置中的多个设备之间同步刺激。来自一个传感器的反馈可用于调整在不同位置处的设备的刺激。
在一些实施例中,用于治疗震颤的可穿戴设备包括:处理单元;第一周围神经效应器,其包括被配置为定位成调节第一周围神经通路的至少一个刺激源;第二周围神经效应器,其包括被配置为定位成调节第二周围神经通路的至少一个刺激源;以及至少一个传感器,其被配置为测量疾病状态的特性。处理单元包括控制器和用于存储指令的存储器,所述指令在被执行时致使设备将来自第一执行器的第一刺激施加到身体上的第一位置并且施加来自第二执行器的第二刺激。第一刺激包括电刺激或振动刺激。第二刺激可以包括与第一刺激不同类型的刺激。第二刺激可以包括与第一刺激相同类型的刺激以及不同的刺激参数,包括频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、占空比、开/关时间、突发模式或刺激持续时间中的至少一个。施加第一刺激或施加第二刺激中的至少一者响应于控制器并且基于疾病状态的感测特性。在施加第一刺激和施加第二刺激之后,疾病状态的特性减轻。
第二执行器可被配置为施加到身体上的与第一位置间隔一距离的第二位置。第一刺激能够被配置用于传入神经刺激,而第二刺激被配置用于功能性电刺激。
附图说明
在权利要求和具体实施方式以及附图中特别阐述了几个实施例的新颖特征,具体实施方式阐述了示意性(非限制性)实施例,在其中利用了本文所述的原理,其中:
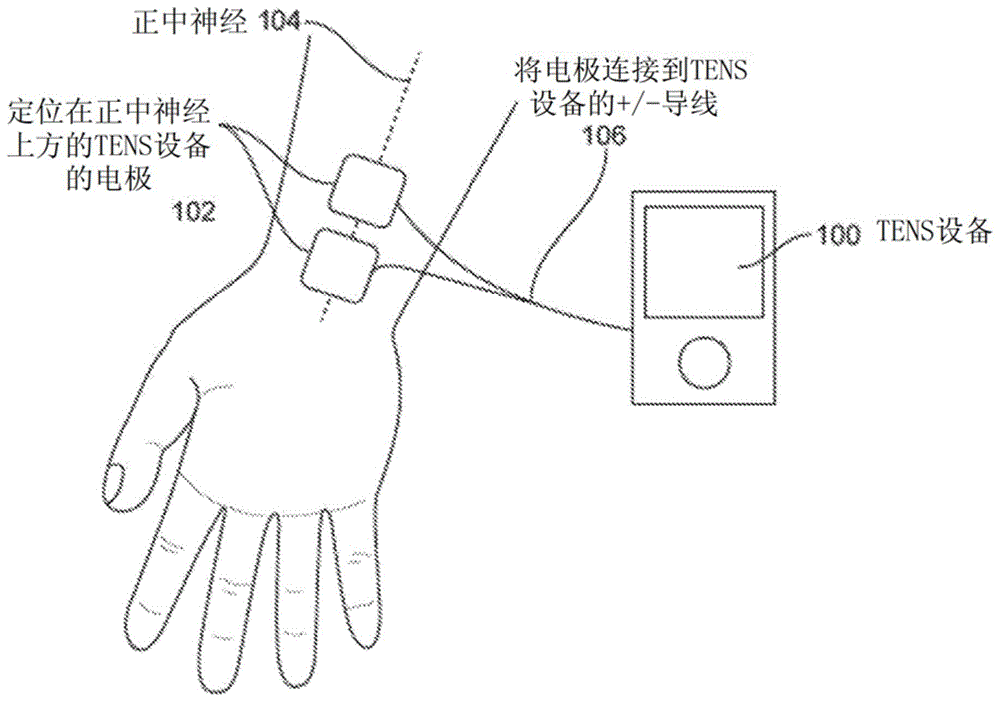
图1示出了将刺激递送到发现要减轻震颤的正中神经的一个实施例。
图2a-2c示出了在轻度(图2a)、中度(图2b)和重度(图2c)et患者中的周围神经刺激的实施例的治疗作用。它展示了一项临床研究的结果,其中患有特发性震颤的患者通过以150hz频率、300μs和40分钟的刺激接通持续时间的刺激配置减小了震颤幅度。通过比较et患者画螺旋的能力示出,在刺激关闭后立即观察到震颤减少。
图3a-3c示出了根据图2a-2c的受试者b中的陀螺仪数据计算出的手腕屈伸。图3a示出了治疗前的震颤;图3b示出了治疗后的即刻震颤减少;图3c示出了在治疗后震颤减少维持二十分钟。
图4示出了中度et患者的无效治疗的示例。
图5a示出了患者身上震颤改变系统能够位于的各种位置。
图6a和图6b示出了支配手的主要神经及其末梢分支。
图7a-7d是示出震颤改变系统的各种实施例的框图。
图8a示出了用于激发不同手指中的神经的电极对的实施例,其中两个电极都定位在手指上。
图8b示出了激发不同手指中的神经的装置,其中第二电极定位在手腕处。
图8c示出了将电极放置在手腕上以便以不同潜在神经为目标的实施例。
图8d和图8e示出了各种刺激位点。
图9a是示出用于使接收来自两根手指的感觉输入的大脑区域移相的激发方案的实施例的图。
图9b是示出用于使接收来自四根手指的感觉输入的大脑区域移相的激发方案的实施例的图。
图10a-10c示出了其中手的位置可以确定最佳刺激占空比和时间安排的实施例。
图11示出了随时间推移而改变频率的可变刺激的实施例。
图12是示出其中刺激物是化学的并且能够混合两种神经调节化学品以提供定制化学刺激的实施例的图。
图13a和图13b示出了各种形式的用户控件。
图14a-14m示出了震颤改变系统的各种非侵入式或侵入式实施例。图14e是示出刺激物是机械的实施例的图。图14h示出了具有腕表的形状因数的设备的实施例。图14i示出了图14h所示的设备的背面,示出与用户接口的电极。图14j和图14k示出了一次性电极接口的实施例,该电极接口卡扣到设备壳体的腕表形状因数的合适位置中。图14l示出了自对准卡扣特征的实施例,该特征允许一次性电极接口卡扣到具有腕表形状因数的设备的壳体中。图14m是示出其中效应器是电的设备的实施例中电极沿脊柱的可能放置的图。
图15a-15c示出了电极阵列的各种实施例。
图16a-16d示出了导电油墨纹身的各种实施例。
图17a-17b是示出将加速度计定位在手或手腕上用于测量患者的活动和震颤的实施例的图。
图18a和图18b示出了针对患有以6.5hz为中心的震颤的患者的陀螺运动数据的频谱分析的示例。
图19示出了姿势性震颤与运动性震颤的相关性。
图20示出了刺激设备的实施例,该刺激设备能够记录数据(诸如震颤特性和刺激历史)并将数据传输到数据门户设备(诸如智能电话),该数据门户设备将数据传输到基于云的服务器。
图21a-21d是示出用于通知用户或改善刺激的数据的监测、集成、分析和显示的流程图。
图22是示出反馈逻辑的流程图。
图23是示出其中刺激物是至少部分皮下植入的电极的实施例的图。
图24a-24d示出了允许无线供电和控制的可植入设备和皮肤表面设备的各种实施例。
图25a-25f示出了用于植入电刺激的电极的各种几何形状。
图26a-26b示出了用于与设备相互作用的控件模块的两个优选实施例。震颤设备的控制系统利用反馈来修改刺激。这是一个闭环,其中基于对活动和震颤的测量来调整刺激。
图27a示出了能够被配置为以定时方式刺激数块皮片的系统的实施例。
图27b示出了用于神经纤维的选择性或优先激活的电极队列(electrodealignment)的实施例。
上面标识的图可与本文提供的其他图和描述结合使用。
具体实施方式
如本文所用,术语“刺激”和“刺激物”通常是指将信号、刺激或脉冲递送到目标区域的神经组织。这种刺激对神经元活动的作用称为“调节”;然而,为简单起见,术语“刺激”和“调节”及其变体有时在本文中互换使用。信号递送到神经组织的作用可能是兴奋性的或抑制性的,并可能增强神经元活动的急性和/或长期变化。例如,“刺激”或“调节”神经组织的作用可包括以下作用中的一者或多者:(a)使神经元去极化以使得神经元激发动作电位,(b)使神经元超极化以抑制动作电位,(c)耗尽神经元离子存储以抑制激发动作电位,(d)随本体感受输入而改变;(e)影响肌肉收缩,(f)影响神经递质释放或摄取的变化,或(g)抑制激发。“本体感受”是指人对自己的身体部位的相对位置或为移动其身体部位所采用的努力的感觉。本体感受可另外被称为躯体感觉、动觉或触觉的感觉。“本体感受器”是向神经系统提供本体感受信息的受体,并且包括肌肉、关节、韧带和肌腱中的拉伸受体,以及针对压力、温度、光和声音的受体。“效应器”是设备通过其调节目标神经的机制。例如,“效应器”可以是神经的电刺激或本体感受器的机械刺激。
“电刺激”是指将电信号施加到目标区域的软组织和神经。“振动触觉刺激”是指通过向目标区域的软组织和神经施加生物力学负载来激发本体感受器。应用“热刺激”是指所引起的目标区域的冷却或加热。应用“化学刺激”是指递送化学药品、药物或药物制剂,所述药物制剂能够刺激暴露于该制剂的神经或神经组织中的神经元活性。这包括影响神经元(通过电信号和化学信号处理和传递信息的可电激发细胞)中的神经递质释放或摄取的局部麻醉剂。“云”是指使用实时协议(诸如互联网)来分析、显示分布式设备中的数据以及与其相互作用的计算机通信的网络。
设备位置
设备刺激感觉神经以便修改异常网络动态。随时间推移,该刺激可使异常网络中的神经放电正常化并减小震颤。优选地,受刺激的神经是承载来自受震颤影响的肢体的感觉本体感受信息的神经。可在沿着或邻近承载本体感受信息的神经的任何地方直接调节神经(诸如通过电刺激)。在一些实施例中,可诸如通过刺激目标神经的本体感受器的激发来间接地调节目标神经。图5a示出了承载来自肢体或声带或喉的本体感受信息的神经的接入点。这些接入点可包括但不限于:包括一个或多个手指和/或拇指的手指510、手520、手腕530、下臂或前臂540、肘部550、上臂560、肩部570、脊柱580或颈部590、脚(例如,包括一个或多个脚趾)、脚踝、下腿或小腿、膝盖和/或上腿或大腿。在一些实施例中,这些接入点可用于直接刺激。在另一些实施例中,这些接入点用于间接刺激。在几个实施例中提供了间接和直接刺激。在一些实施例中,提供了两个、三个或更多个接入点。
影响本体感受的神经可包括,例如手、手臂和脊柱区域中或沿着肌肉或关节内的正中神经、尺神经、桡神经或其他神经。针对神经的这些区域可包括臂神经丛、内侧神经、桡神经和尺神经、皮肤神经或关节间隙神经。这些区域也可针对肌肉组织,包括肩部的肌肉、手臂的肌肉,以及前臂、手或手指的肌肉。作为非限制性示例,肩部肌肉可包括三角肌、大三头肌和棘上肌。手臂的肌肉可包括喙肱肌和肱三头肌。前臂的肌肉可包括桡侧伸腕长肌、拇长展肌、尺侧腕伸肌和尺侧腕屈肌。在一些实施例中,刺激这些区域中的一者、两者、三者或更多者(直接和/或间接)。
可结合使用的设备位置或治疗位点的一些示例包括以下中的两者或更多者:手腕、手、手指、前臂、上臂、肘部、肩部、手臂、脚踝、脚、脚趾、小腿、下腿、大腿、上腿、膝盖、腿、上半身附器、上半身、下半身附器、下半身、脊柱、脖子、头部或其中的任一者的部分。多个位点可与多个模态和/或多个模式组合,每个模态具有多个模式或一个或多个模态具有不同模式。例如,可将第一刺激模态和/或模式应用于手腕530,并且可将第二刺激模态和/或模式应用于手指510。对于另一个示例,可将第一刺激模态和/或模式应用于手腕530,并且可将第二刺激模态和/或模式应用于脚踝。对于又一个示例,可将第一刺激模态和/或模式应用于手臂,并且可将第二刺激模态和/或模式应用于腿。对于又另一个示例,可将第一刺激模态和/或模式应用于上半身,并且可将第二刺激模态和/或模式应用于下半身。可在各个位点处植入(例如,皮下和/或经皮)刺激物。
在一些实施例中,振动或触觉马达设置在设备中并位于目标区域或神经附近,使得振动能量指向目标神经。例如,在手腕穿戴的设备中,可将振动马达设置在束带中,使得其位于手腕的手掌侧,直接邻近正中神经。振动马达的运动可被取向为使得其与目标神经或皮肤表面正交和/或倾斜。马达的运动可以是例如线性的或具有偏心质量的旋转。
在一些实施例中,水凝胶或水基部件(例如,具有悬浮在凝胶中的利多卡因或另一种化学物质的水凝胶贴片,经由电能刺激的电极)可嵌入有化学或药理试剂(诸如利多卡因)。电极可放置在皮肤表面上,并且化学药品以与电极中的化学物质的浓度成比例的预定速率释放。结合悬浮在水凝胶中的化学物质,电极可提供电刺激或者不提供电刺激。在一些实施例中,可将试剂放置在皮肤上,并且电能可协同地刺激一个、两个或更多个目标区域或神经,以及辅助驱动一种、两种或更多种试剂通过皮肤(例如,经由离子电渗疗法)。在一些实施例中,可对离子电渗疗法设备进行修改以促进试剂的皮肤渗透以及经由电极的电刺激的增强(例如,在一些情况下,在促进离子电渗疗法的第一刺激模式与促进神经刺激的第二刺激模式之间交替)。模式可涉及不同的频率、幅度、波形和/或本文其他地方公开的其他参数。
在一些实施例中,与设备接触的周围组织中的热能增加或减少。可通过热电加热元件(例如,具有电阻元件的设备中设置的电池)在与设备接触的组织中增加热能。热量可传递到束带中的例如具有传导元件的特定目标位置,该传导元件将热能传递到与该传导元件接触的组织。可通过热电冷却元件(例如,珀尔帖设备或固态冰箱)或通过使冷却剂或冷却液循环通过与目标组织区域接触的设备的一部分来减少与设备接触的组织中的热能(例如,在手腕穿戴的设备中,束带可设置有管线以使冷却液循环通过束带)。在一些实施例中,设备可具有使冷却剂循环的泵。设备可具有传热元件(诸如散热器或电动风扇)以将热能从周围组织传递到周围空气或环境(例如,设备上的不与组织接触的区域)。
在几个实施例中的优选位置中,设备与用户的震颤上肢的皮肤表面接合并将神经调节信号施加到神经束,该神经束选自由以下组成的组:臂神经丛、内侧神经、桡神经和尺神经,或上肢的肌肉组织中的可激发结构(皮肤上或关节内)。在一些实施例中,将神经调节信号提供给一个、两个或三个或更多个神经束。
根据几个实施例,在将刺激或其他神经调节信号提供到两个、三个或更多个位置的情况下,同时、顺序或重叠地提供信号。
本体感受器可在例如肌肉、肌腱、关节、皮肤和内耳中找到。定义用于直接调节的候选神经的标准包括要减小的震颤的位置,以及神经与皮肤表面的接近程度,本体感受纤维的高密度,以及与可激发疼痛受体或肌肉相距的距离。根据这些标准,针对手腕的正中神经和针对肘部的尺神经排名较高。定义间接本体感受调节的候选位置的标准包括本体感受器的密度和类型。帕西尼氏小体提供关于触摸的信息;当机械门控的离子通道由于肌肉拉伸而打开时,肌肉纺锤通过触发肌肉纺锤传入神经中的动作电位来提供有关肌肉长度变化的信息。高尔基腱器官提供有关肌肉张力的信息。还可刺激这些结构以改变回路动态并减小震颤。
设备针对在异常脑回路上形成突触的特定神经。该突触可以是直接突触,或者通过多个中继突触。图6a和图6b示出了将本体感受信息输送到橄榄-小脑网络(在et中为异常的网络)的一组代表性神经。这些神经包括620正中神经和630尺神经的610远侧分支和主要分支,以及650桡神经的640远侧分支和主要分支。在优选的实施例中,该设备针对从手、手腕和前臂输入本体感受信息的神经。
在另一个实施例中,此处所述的任何部分的组合可用于影响与语音震颤相关的神经,包括但不限于迷走神经的分支,诸如喉上神经或喉返神经。
设备部件:各种实施例
图7a-7d是示出震颤改变系统700的一些实施例的概念图。系统700包括壳体720、一个或多个效应器730、与效应器730电连通的一个或多个控件740以及一个或多个电源750。在一些实施例中,壳体720可包括接口760。接口促进将效应器耦接到患者。例如,接口可提供设备与患者的神经之间的物理、电、化学、热或磁连接。在一些实施例中,壳体720还可包括用于检测震颤的传感器780、存储器770、显示器790和处理器797。该实施例中的设备可包括耦接到效应器的处理器797,其可执行其他部件的计算和控制。设备还可包括存储在处理器797或存储器770上的数字库,该数字库可包含预加载的调节协议。设备可包括控件模块740,该控件模块与处理器797通信并且可由用户用来控制刺激参数。这些控件允许用户调整设备的操作。例如,控件可被配置为开启设备,关闭设备,调整效应器(诸如强度)。设备可包括连接到处理器797的传感器780,其可检测预定义参数的信息并将所述参数信息传输到处理器797。设备可包括连接到传感器780和处理器797的数据存储单元770;并且电源750可连接到处理器。
设备还可包含显示器或指示器790以便与用户通信并报告设备的状态。在一些实施例中,指示器优选地是发光二极管(led)或某种视觉指示器,但可以是音频指示器。信息可能包括电池电量或刺激状态。
设备可缺少或没有效应器730。它可以是诊断性的非治疗性设备。在优选的实施例中,接口单元704将被穿戴在震颤肢体上以随时间推移追踪颤动。向设备的用户提供反馈可使他们意识到其震颤并可随时间推移进行监测。即使没有治疗性刺激,这种生物反馈也可帮助一些个人减轻其震颤。设备可缺少或没有传感器780。它可以是治疗性的非诊断性设备。
为了使设备小且简单,可将这些部件中的许多部件容纳在单独单元中。可在决策单元702中远程完成处理、控制以及可能的感测,从而使得为多种应用提供与患者的治疗性接触的接口单元704是紧凑、简单和柔性的(图7b-7d)。该决策单元702可以是为此应用设计的新设备,或者其可集成到诸如智能电话的现有技术中。这将允许系统成为具有降低的成本和尺寸的坚固的手持式形状因数外形。
在图7b所示的实施例中,接口单元704是植入物;效应器730提供神经的电刺激;从外部设备无线传输指令集和电力。植入的接口单元704可由机载电池供电。植入的接口单元704可包含传感器780,其用于直接检测通过电描记术(eng)或肌电描记术(emg)检测到的震颤或神经肌肉活动。
在图7c所示的实施例中,接口单元704穿戴在身体的表面上;效应器730提供下面神经的电刺激或附近本体感受器的振动触觉刺激。传感器780可包括运动传感器,该运动传感器包括加速度计、陀螺仪和磁力计。
在图7d所示的实施例中,感测运动、温度等的一个或多个传感器单元780可穿戴在身体中的不同位置处。效应器730和决策单元702是穿戴在身体上的与传感器780不同的位置处的单独实体。如果神经的刺激发生在无法轻易或准确地测量出震颤的位置,这是有用的。例如,放置在手腕底侧以用于减小手部震颤的刺激设备700是高度有效的。然而,使用加速度计或陀螺仪来从手腕测量手部震颤可证明是更加困难的;在手套中单独放置在手部的手掌或手背上或作为戒指穿戴在手指之一上的传感器单元由于其位于手腕关节以外而将显示出对手部震颤的更高灵敏度。
效应器:常规
效应器可用来调节刺激指向的上肢区域中的神经组织。例如,效应器可修改神经中的神经元信号和/或修改本体感受信息的流或内容。效应器可经皮或皮下递送。一个或多个效应器可用于影响神经。在一些实施例中,效应器对于神经可以是兴奋性的。在另一些实施例中,效应器对于神经可以是抑制性的。在一些实施例中,系统可用于在治疗的一些部分期间激发神经并且在治疗的其他部分期间抑制神经。
效应器:电刺激
在一些实施例中,效应器可以是电刺激物。电效应器可包括电极、电极对、电极阵列或能够将电刺激递送到期望位置的任何设备。电刺激可以是经皮或皮下的。例如,可通过放置在皮肤表面上的电极来实现经皮电刺激,而可通过定位成靠近神经的植入电极来实现皮下电刺激。
刺激参数可自动调整或者由用户控制。刺激参数可包括开/关、持续时间、强度、脉冲率、脉冲宽度、波形形状以及脉冲开和关的斜率。在一个优选实施例中,脉冲率可以是约50至5000hz、并且优选频率是约50hz至300hz或150hz。例如,频率可介于约10hz和约20khz之间(例如,约10hz、约20hz、约30hz、约40hz、约50hz、约60hz、约100hz、约250hz、约500hz、约1000hz、约2500hz、约5000hz、约10khz、约15khz、约20khz,以及此类值之间的范围)。优选脉冲宽度可在50至500μs(微秒)的范围内,并且优选脉冲宽度可为约300μs(例如,约50μs、约100μs、约150μs、约200μs、约250μs、约300μs、约350μs、约400μs、约450μs、约500μs,以及此类值之间的范围)。电刺激的强度或幅度可从0ma变化到500ma,并且优选电流可为约1ma到6ma(例如,约0ma、约0.1ma、约1ma、约6ma、约10ma、约20ma、约30ma、约40ma、约50ma、约100ma、约200ma、约300ma、约400ma、约500ma,以及此类值之间的范围)。某些优选设置是从上述临床研究导出的,该临床研究提供了持续一定时间段的震颤的有价值减小。可在不同的患者中和通过不同的刺激调节方法来调整刺激。这些优选设置是非限制性示例。强度调整的增量可以是0.1ma至1.0ma(例如,0.1-3ma、3-6ma、6-10ma,以及其中的重叠范围)。在一个优选实施例中,刺激可持续约10分钟至1小时(例如,10-20分钟、20-40分钟、40-60分钟以及其中的重叠范围)。
在一个优选实施例中,电极可在一根或多根神经(包括内侧神经、桡神经和尺神经)上方的皮肤的表面处与用户接触。电极可处于其中存在电极对的配置,其中一个电极在近侧(靠近肘部)并且另一个电极在远侧(靠近手)。电极可与相对电极连通。电极对可具有电流流过的正电荷或负电荷的极性。
效应器可包括两个电极,每个电极具有正极性或负极性,或者电极阵列可包括多个电极对,其中每个电极对被独立地编程或相对于其他电极对相关地编程。作为示例,程序可允许不同神经(诸如尺神经,然后正中神经,然后桡神经,或其任何组合)在不同时间的循环刺激。
电刺激可被设计成通过干扰本体感受输入、引起代偿性肌肉收缩、或两种方法的组合来抑制震颤。电极可由能够通过与上肢的皮肤表面的刺激物接口传导电信号的任何等效材料代替。电极可附接到控制单元740,控制单元可经由电极将电刺激施加到其中放置电极的区域和紧邻的区域中的软组织和神经。在该实施例的另一个变型中,可将若干电极放置到目标区域的组合。
连接到处理器并由处理器控制的函数发生器可用于调节电刺激参数。函数发生器优选是使用直接数字合成技术来产生可由幅度表描述的任何波形的任意波形发生器。这些参数选自包括但不限于频率、强度、脉冲宽度或脉冲持续时间以及总持续时间的组。优选地,输出具有由最大输出电压设定的功率极限。在优选实施例中,数字存储的协议通过各种刺激参数进行循环以防止患者适应环境。电刺激的变化通过函数发生器来实现。
在一些实施例中,电刺激包括一个或多个单频和一个或多个扫描频率(例如,从较低频率连续变为较高频率)的组合。例如,可施加第一单频率持续第一持续时间,并且可施加第一扫描频率持续第二持续时间。第二持续时间可在第一持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第二持续时间可至少部分地与第一持续时间重叠。继续该示例,可施加不同于第二频率的第二单频率持续第三持续时间。第三持续时间可在第二持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第三持续时间可至少部分地与第二持续时间重叠。继续该示例,可施加与第一扫描频率不同的第二扫描频率(例如,具有不同的低频、高频和/或频率变化率)持续第四持续时间。第四持续时间可在第三持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第四持续时间可至少部分地与第三持续时间重叠。该示例可在单频率和/或扫描频率的附加持续时间内继续。可将不同频率施加到相同的振动刺激物或不同的电刺激物(例如,在相同的身体部位上,在不同的身体部位上)。向不同身体部位施加的电刺激可在身体部位之间的某个点汇合并可能形成驻波。在一些实施例中,汇合点可以是目标身体部位(例如,肘部和手指汇合在手腕处)。扫描的幅度可由其他波形(诸如正弦曲线或高斯曲线)包封,或者可随机或伪随机地改变参数。上面对不同频率的讨论也可应用于其他参数,诸如频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、或突发、其组合等。
优化刺激:移相
在优选实施例中,刺激被设计为对大脑中的同步性进行移相。对异常回路进行移相的概念紧随最近工作,其表明神经再训练减小网络陷入异常节律的倾向。有趣的是,运动障碍通常与大脑回路中的异常周期性同步放电相关联。在帕金森氏病中,该回路位于基底神经节中。在et中,它是橄榄-小脑回路。这些异常振荡被认为驱动震颤,如许多研究支持的,这些研究表明在手部和前臂肌肉中观察到的震颤与大脑中的病理性节律放电同步。最新的dbs研究表明,相邻电极对上的低压相移突发(称为协调重置)可减小异常大脑网络中的同步并且这可减小帕金森氏震颤。协调重置理论在治疗耳鸣中的应用支持了使用突触激发以再训练神经网络的概念。
本文公开的设备具有超越高频tens刺激的若干优点,包括使用较低的功率(导致延长电池寿命,减小因运动增长和收缩引起的不适,减小因感觉激发引起的不适),较少抑制相邻神经的活动中的放电(通过耗尽或其他机制),以及维持更持久的作用,使得仅需要间歇性地使用设备来训练或维持对神经回路动态的训练。设备刺激神经集合,方式为使得其针对神经亚群以减小群的同步。例如,这可通过刺激手上的不同手指来实现。
图8a是设备的优选实施例的示意图,其中手指上的阳极810和阴极820电极对用于激发每个手指中的本体感受神经(正中神经、桡神经和尺神经)的分支。阳极810在远侧并且阴极820在近侧的这种布置被设计成引起神经脉冲朝向大脑行进。由于大脑的体组织,每个手指上的独特刺激模式可向大脑中的特定神经元亚群发送独特信号,其中来自不同的相邻或附近身体部位的信号在大脑中的附近位置处形成突触。使用多个独特模式的刺激是多模态刺激的示例,其中使用了相同类型的刺激的多个模式(具有至少一个不同参数)。在一些实施例中,阳极810和阴极820的位置可颠倒以抑制感觉冲动朝向大脑的传递(逆向碰撞)。多个手指的刺激是多模态刺激的示例,其中使用了相同类型的刺激的数个位点。结合独特刺激模式,此类刺激是多模态刺激的示例,其中使用了相同类型的刺激的数个位点和多个模式。在若干实施例中还提供了不同种类的刺激(例如,一个或多个手指上的电刺激和一个或多个其他手指上的振动触觉刺激)。
图8b示出了其中电极830定位在手指上并且第二电极840定位在手腕上的布置。在一个实施例中,手指上仅存在830单电极,并且840第二电极定位在手腕上。手指表示仅一组可能的目标,并且类似地可使用不同的位置作为邻近神经元亚群的目标。在一些实施例中,一个或多个手指上的电极可包括阳极和阴极,例如如相对于图8b所述,并且阳极和阴极可定位在手腕上。一个或多个手指和手腕的刺激是使用数个位点的多模态刺激的另一个示例。在一些实施例中,一个或多个手指上的电极可以是经皮的,并且手腕上的电极可以是皮下的。将电极放置在皮肤的不同位置是多模态刺激的示例。在一些实施例中,在一只手上的一个手指(包括拇指)上并且另外在另一只手上的一个手指(包括拇指)上提供多模态治疗。
在图8c所示的实施例中,电极位于手腕上的不同位置850、860、870上以针对正中神经(靠近位置850)、尺神经(靠近位置860)和桡神经(靠近位置870)。本领域技术人员将认识到,输入可位于输入到异常脑回路的神经的其他位置或分支上。位置可能在有震颤的肢体的相同侧或相对侧。位置可在皮肤的表面上,穿过皮肤和/或被植入。
图8d示出了各种刺激位点,这些位点可经受刺激,该刺激延迟或偏移了震颤周期t的预定分数或倍数,例如图9a和图9b所示。这些位点靠近正中神经和尺神经。图8e示出了靠近桡神经的刺激位点。手腕的第一侧(例如,图8d)和手腕的第二侧(例如,图8e)的刺激是其中使用数个位点的多模态刺激的另一个示例。
设备使用被设计成对异常网络进行移相、覆盖或掩盖的刺激方案。图9a是示出样本激发方案的概念图,该样本激发方案用于使接收来自两个位点的感觉输入的大脑区域移相。例如,两个位点可以是图8a-8e中所示的两个手指。第二位点处的刺激在第一位点的刺激之后延迟时间t/2,其中t是自然震颤的周期。例如,如果震颤是以8hz并且周期t为125ms,则第二位点的刺激将延迟62.5ms。刺激被设计成重置神经元的相位,这可使用高频刺激(高于100hz)或dc脉冲来实现。
图9b是示出样本激发方案的概念图,该样本激发方案用于使接收来自四个位点的感觉输入的大脑区域移相,其中后续位点延迟t/4。在另一个实施例中,不同位置处的刺激在除了定时之外的参数(诸如频率或脉冲宽度或它们的组合)上是可变的。这些变化被类似地设计成通过消除、覆盖或掩盖异常网络动态来再训练大脑。在又一个实施例中,刺激可出现在单个位置,但其参数随时间推移而变化。例如,它的频率可能每隔几秒钟变化一次或者其可开启和关闭。在又一个实施例中,刺激是恒定的并且在单个位置。在这些的优选实施例中,位置在靠近手腕的正中神经处。
优化刺激:次感觉
以低于感觉阈值的强度进行刺激将避免可能与周围神经刺激相关的不适(刺痛、麻木、疼痛)。因为确切的电极位置、尺寸和表面接触对刺激水平和接受刺激的解剖结构产生很大影响,所以可能需要针对每个患者以及甚至每个阶段校准感觉阈值。可通过用户手动设置刺激参数或以其他方式指示其感觉阈值来完成此校准。设备的另一种可能机制是自动扫过一系列刺激参数,并且患者选择一组最舒适的参数值。另一个可能机制是使患者从一组先前选择的参数值中进行选择,从而提供有效且舒适的刺激。在一些实施例中,电极垫可包括局部镇痛药诸如利多卡因以减轻刺激的不适感,由此增加患者耐受的感觉阈值。在一些实施例中,可使用控释形式来递送局部镇痛药以在将要穿戴电极垫的持续时间(可以是几天,几周或几个月)内提供疼痛缓解。由于更大的刺激强度和/或与局部止痛剂的协同作用,这样的方法可提供更大的舒适度或更大的治疗效果,从而可减小一些患者的震颤。
优化刺激:高频
替代地或附加地,刺激波形可能是非常高的频率(通常以khz为单位或更高),使得用户感觉不到刺激或者感觉到很少的刺激。人们认为,非常高频率的刺激会导致传导封锁。然而,在封锁之前,存在包括强烈神经去极化的开始响应。为了有效地实现非常高频率的刺激而不引起患者的不适,优选消除这种开始响应。这可通过在初始刺激期间冷却神经来完成。运动神经通常由约15hz及以下的刺激激发,而感觉神经通常由约50hz及以上的刺激激发。在一些实施例中,可能期望具体地在运动神经元刺激的15hz阈值以上进行刺激以避免引起肌肉收缩。
优化刺激:触发
替代地或附加地,针对震颤阶段触发刺激可改善有效性。这种刺激的目的是打破运动单元的节奏性夹带。更有效的治疗可允许以较低的水平进行刺激以便实现类似的治疗益处,同时伴随较少的不适感。本质上,震颤是谐振回路中的反馈的问题。与震颤异相定时的刺激可通过更改回路动态(例如,通过改变反馈环路上的增益)来减小震颤。
如图10b所示,当手腕处于其最大屈曲或伸展时(图10a),可能会定时发生高频刺激的突发。在示例(图10c)中,突发已被移至随机相位。手的位置(图10a)可确定最佳的刺激占空比和时序,诸如(图10b)通过最大震颤偏差或(图10c)使用可变时间延迟的突发来刺激非谐振以避免与震颤谐振。
在一些实施例中,第一刺激可包括突发刺激(例如,具有指定的开启周期和关闭周期的刺激)并且第二刺激可包括连续刺激。第一刺激可在第二刺激之前、期间和/或之后。第一刺激可由与第二刺激相同的电极或电极组施加,或者由与第二刺激不同的电极或电极组施加。在一些实施例中,可将突发刺激施加到身体上的第一位置,并且可将连续刺激施加到第二位置(同时或顺序地)。
替代地或附加地,刺激可以是混沌的或可变的。混沌、随机或可变的刺激的目标是抑制或防止习惯化并减小回路中的谐振。例如,这可通过随时间推移改变刺激频率和/或通过叠加较高和较低的频率分量来实现,如图11所示。
替代地或附加地,刺激可以是高频交流电。这表明在动作电位沿轴突传递时阻止动作电位并且可调整回路动态。
在一些实施例中,可根据预定顺序循环上述刺激参数以确定最佳刺激参数。在一些实施例中,可随时间推移监测刺激参数的有效性,以确定一组特定刺激参数是否正在丢失有效性。在一些实施例中,当一组特定刺激参数的有效性已减小预定量时,可根据预定顺序来改变或循环刺激参数。例如,如果对于震颤阶段触发刺激,则可以以随机或可变的时间延迟递送刺激,或者如果刺激使用设置的幅度和/或频率,则可将刺激改变为混乱、随机或可变的模态以防止或破坏习惯化。在一些实施例中,可根据预定例程利用随机或可变类型的刺激参数,诸如每天持续预定小时数,或者每周持续预定天数,或者以某个其他预定间隔(包括一天中的时间)。
效应器:振动触觉刺激
效应器可通过包括振动触觉或触觉的感觉来机械地激发本体感受器。机械刺激可能包括力、振动和/或运动。效应器通过激发高尔基体腱器官(gto)或帕西尼氏小体来引起目标神经中的动作电位。机械效应器可包括例如小型马达;压电体;一个或多个振动触觉单元,其由质量块和效应器组成,该效应器用于使该质量块移动以使得将振动刺激施加到身体;偏心质量块,其安装在轴上以使得在轴旋转时产生振动刺激;超声马达;磁流变流体(mrf)效应器或电活性聚合物(eap)效应器;和/或扬声器(例如,触觉扬声器、压电扬声器、电活性聚合物换能器、电磁线圈扬声器)。
在一些实施例中,振动刺激可为250hz,对应于帕西尼氏小体(也称为环层小体)的最佳灵敏度。帕西尼氏小体是皮肤中的感测触摸和振动的神经末梢。小体的变形打开压敏钠离子通道以引起动作电位。在一个实施例中,振动可低于50hz以激发手指中的对轻触敏感的迈斯纳小体(也称为触觉小体)。在一些实施例中,振动刺激可以是例如至少约、大约或不超过约10hz、20hz、30hz、40hz、50hz、60hz、70hz、80hz、90hz、100hz、110hz、120hz、130hz、140hz、150hz、160hz、170hz、180hz、190hz、200hz、210hz、220hz、230hz、240hz、250hz、260hz、270hz、280hz、290hz、300hz、350hz、400hz、450hz、500hz,或更高或更低,或包括前述参数中任何两个的范围。
在一些实施例中,振动刺激包含一个或多个单频率的组合。例如,可施加第一单频率持续第一持续时间,并且可施加第二单频率持续第二持续时间。第二持续时间可在第一持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第二持续时间可至少部分地与第一持续时间重叠。继续该示例,可施加不同于第二频率的第三单频率持续第三持续时间。第三持续时间可在第二持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第三持续时间可至少部分地与第二持续时间重叠。第三持续时间可至少部分地与第一持续时间重叠。第三持续时间可至少部分地与第一持续时间和第二持续时间重叠。该示例可在单频率的附加持续时间内继续。可将不同频率施加到相同的振动刺激物或不同的振动刺激物(例如,在相同的身体部位上,在不同的身体部位上)。向不同身体部位施加的振动刺激可在身体部位之间的某个点汇合并可能形成驻波。在一些实施例中,汇合点可以是目标身体部位(例如,肘部和手指汇合在手腕处)。
在一些实施例中,振动刺激包括一个或多个单频和一个或多个扫描频率(例如,从较低频率连续变为较高频率)的组合。例如,可施加第一单频率持续第一持续时间,并且可施加第一扫描频率持续第二持续时间。第二持续时间可在第一持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第二持续时间可至少部分地与第一持续时间重叠。继续该示例,可施加不同于第二频率的第二单频率持续第三持续时间。第三持续时间可在第二持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第三持续时间可至少部分地与第二持续时间重叠。继续该示例,可施加与第一扫描频率不同的第二扫描频率(例如,具有不同的低频、高频和/或频率变化率)持续第四持续时间。第四持续时间可在第三持续时间之后(例如,紧接在其后,在暂停持续时间之后)。第四持续时间可至少部分地与第三持续时间重叠。该示例可在单频率和/或扫描频率的附加持续时间内继续。可将不同频率施加到相同的振动刺激物或不同的振动刺激物(例如,在相同的身体部位上,在不同的身体部位上)。向不同身体部位施加的振动刺激可在身体部位之间的某个点汇合并可能形成驻波。在一些实施例中,汇合点可以是目标身体部位(例如,肘部和手指汇合在手腕处)。扫描的幅度可由其他波形(诸如正弦曲线或高斯曲线)包封,或者可随机或伪随机地改变参数。
上面对不同频率的讨论也可应用于其他参数,诸如频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、或突发、其组合等。在若干适用的实施例中,以上对振动刺激的讨论也适用于其他模态及其组合。
在一些实施例中,对身体上的第一位置进行电刺激,同时向第二位置提供振动刺激(例如,手腕和脚踝、手腕和耳朵、脚踝和耳朵、手臂和腿等)。代替第二位置,或者除了第二位置之外,在第一位置处(同时或顺序地)提供电刺激和振动刺激。例如,针对手腕使用提供电刺激和振动刺激的束带(或其他设备),并且针对耳朵、脚踝、腿、手臂等使用提供电刺激和振动刺激的束带(或其他设备)。在一个实施例中,两个位置都提供电刺激和振动刺激。也可刺激第三、第四或其他位置。尽管在若干实施例中公开了刺激,但在多个实施例中考虑了包括刺激或抑制的神经调节。
这种机械类型(例如,振动)的刺激物可通过若干方法来减小震颤。一种方法可以是将本体感受信号传输到大脑,该信号会遮盖或修改从震颤肌肉传输的驱动本体感受信号。另一种方法可以是阻抗控制。关节阻抗可通过经皮神经刺激来改变共同收缩的肌肉,从而影响肌肉的僵硬程度并且进而影响肌肉的收缩。另一种方法可以是通过神经刺激来产生对抗震颤性收缩的代偿性肌肉收缩。在一些实施例中,刺激物优选例如通过弹性或velcro束带(或其他可调整的、可适配的带)来抵靠皮肤表面牢固地固定。
效应器:化学、热及其他
本文的示例主要将刺激描述为电的或振动触觉的。然而,可另选地使用其他效应器来实现刺激,这些效应器可带来患者舒适度、便携性、安全性或成本方面的明显益处。
在该实施例的另一个变型中,效应器可以是提高或降低神经元放电阈值的神经调节化学物质。在一些实施例中使用的化学物质可以是局部麻醉剂,包括但不限于“卡因”族。“卡因”族的麻醉药可包括但不限于苯佐卡因、布比卡因、丁卡因、卡比卡因、氯普鲁卡因、西卡普因、地丁卡因、依托卡因、庚烷、左旋布比卡因、利多卡因、盐酸利多卡因、丙哌卡因、美卡因、普鲁卡因、美卡因、普罗卡因和丁卡因。其他化学族可包括薄荷醇族的那些、或来自花椒的α-羟基椒素、或辣椒素,其都已知会影响周围感觉神经。
图12示出了可通过贴片和/或通过显微注射经皮递送化学刺激的化学刺激物。预加载的协议可优选地是一种或多种化学物质的预定组合物。在若干实施例中,局部麻醉剂对于其他适应症可能是已知的。推荐的刺激剂量可能已经过测试并被批准用于其他适应症的治疗。例如,局部麻醉剂利多卡因可以以2-10重量%进行施用。利多卡因可与其他麻醉剂结合施用。如图12所示,将两种神经调节化学物质1202、1204混合以提供定制的组合物。化学刺激物可作为组合物施用,该组合物包括作为第一化学物质1202的2.5重量%的利多卡因和作为第二化学物质1204的2.5重量%的丙胺卡因。化学刺激物可作为组合物施用,该组合物包括作为第一化学物质1202的0.1-5重量%的利多卡因和作为第二化学物质1204的0.1-5重量%的丙胺卡因。
化学刺激物可包括来自花椒的α-羟基椒素。α羟基椒素可包含在赋形剂或载体中。赋形剂可包括凝胶、乳膏、油或其他液体。如果递送方法是经皮贴片,则化学试剂的形式可优选是乳膏或凝胶。用户可通过控制模块(例如,图7的控制模块740)选择组合物。如果递送方法是显微注射,则形式可优选是溶液。
在一些实施例中,效应器可以是引起冷却和/或加热的温度或热效应器(例如,图7的温度效应器732)。效应器可直接通过冷却神经或间接通过冷却手臂的相邻肌肉、皮肤或其他组成来调节神经元放电。温度效应器可包括例如压电材料(例如,珀尔帖冷却砖)、循环流体、压缩的可膨胀气体、冷却或加热的固体材料或蒸发材料。冷却效应器的一个示例可如美国公开号2010/0107657中公开的,该公开通过引用并入本文。加热和/或冷却可被施加作为贴片,该贴片通过将刺激物附着到皮肤表面的附接件(诸如臂带)或通过植入物来附连到皮肤表面。
在具有热刺激物的实施例中,预加载的协议可能优选地是刺激的预定温度和相关联的刺激持续时间。优选地,预加载的协议可要求热冷却的15分钟的持续时间以及在15-25℃的范围内的冷却温度(例如,约15℃、约17.5℃、约20℃、约22.5℃、约25℃,此类值之间的范围等)。刺激的持续时间可被预编程为(但不限于)约5分钟至约30分钟(例如,约5min、约10min、约15min、约20min、约25min、约30min,此类值之间的范围等)。刺激的最大长度应很好地由用户耐受并且不会造成任何肌肉或神经性损伤。在刺激物是热刺激物的实施例中,温度传感器可用于检测有效冷却温度。有效的冷却或加热温度可以是用户所感觉的温度,并且这不一定与施加的温度相同。如果温度传感器确定有效温度达到阈值(该阈值的范围可比特定协议的施加温度大或小5℃),则处理器797(来自图7)可修改所述协议以比最初编程更多地冷却或加热,以便补偿有效冷却和预期冷却之间的差异。
在一些实施例中,效应器可以是相控阵超声(例如,聚焦超声)效应器。例如,相控阵超声效应器可包括多个超声换能器元件。元件可各自具有宽度和厚度。厚度可与宽度相关(例如,厚度是宽度的分数(例如,1/2、1/3、1/4、1/5、1/10,此类值之间的范围等)或倍数(例如,2×、3×、4×、5×、10×,此类值之间的范围等))。每个元件可具有宽度,并且元件之间的空间可与该宽度相关(例如,与该宽度相同、该宽度的一半、该宽度的两倍)。元件之间的间距可以是可调整的。在一些实施例中,元件具有在约0.5mm与约2mm之间的宽度以及在约0.1mm与约2mm之间的间距。元件可以以一维阵列或二维阵列进行布置。元件可以是长方体、矩形、圆柱形、棱柱形、金字塔形或任何适当的形状。例如,超声信号可在约20khz和约2ghz或更高之间(例如约20khz、约50khz、约100khz、约500khz、约1mhz、约1.5mhz、约2mhz,此类值之间的范围等)。元件中的至少一个可传输不同的频率。每个元件可传输不同的频率。每个元件可传输相同的频率。在一些实施例中,由超声效应器施加的剂量水平介于约0w/cm2和约2w/cm2之间(例如,约0w/cm2、约0.1w/cm2、约0.25w/cm2、约0.5w/cm2、约1w/cm2、约1.5w/cm2、约2w/cm2,此类值之间的范围等)。超声换能器元件中的一者、一些或全部可以是发散的、聚焦的、散射的、平坦的等。在一些实施例中,换能器元件可以以用于聚焦能量(例如,来自不同元件的能量导致相长干涉)的方式布置在皮肤表面下方靠近目标神经或组织区域的位置。
超声换能器元件可布置在印刷电路板上。超声换能器元件可布置在柔性电路上。柔性电路可包括例如超声换能器元件和一种或多种其他类型的效应器。某些电路板、柔性电路等可能包括效应器的其他组合。
在一些实施例中,效应器可以是一个磁体或多个磁体。例如,可将具有第一极性的第一磁体施加到第一位点,并且可将具有第二极性的第一磁体施加到第二位点。第一极性可与第二极性相同(例如,正-正、负-负)。第一极性可与第二极性不同(例如,正-负、负-正)。第一位点可靠近第二位点(例如,约10cm内、约8cm内、约6cm内、约5cm内、约4cm内、约3cm内、约2cm内、约1cm内或更靠近)。第一磁体可包括与第二磁体相同的材料。第一磁体可包括与第二磁体不同的材料。第一磁体可具有与第二磁体相同的尺寸(例如,厚度、长度、宽度直径)。第一磁体可具有与第二磁体不同的至少一个尺寸(例如,厚度、长度、宽度直径)。第一磁体可具有与第二磁体相同的质量。第一磁体可具有与第二磁体不同的质量。
磁体可包括电磁体,该电磁体的材料只有在将电流施加到围绕磁体缠绕的导线时才能变为磁性,以产生可使材料的磁场强度倍增的磁场。在包括电磁体的实施例中,可在不移动效应器的情况下开启和关闭磁效应器。
在一些实施例中,可使用与目标神经正交取向的mini-tms线圈来施加磁能以在目标神经附近输送电磁能突发。经颅磁刺激(tms)线圈包括环形形状,该环形形状包含导线的多个绕组。在向导线施加电流时,正交于环形线圈的平面形成磁场。电流可随时间推移变化,例如当连接到刺激物时。磁场致使电流在身体的邻近tms的区域中流动。mini-tms可以是被配置为穿透组织的tms的较小版本,例如与头骨相对。
若干实施例可以替代地应用其他效应器,包括声学(使用超声激发来激发指尖处的感觉神经)、振动、触觉、发光(例如,光遗传学修饰的神经中的曝光)、磁性(例如,通过快速切换rf场)或机制的组合。可组合使用的模式的一些示例包括以下中的两者、三者或更多者:电刺激、磁刺激、化学刺激、热刺激(热和/或冷)、机械(例如,振动触觉)刺激、聚焦超声(聚焦、高和/或低强度、相控阵列)、射频刺激、或微波刺激。此类模态可在相同区域或不同区域中使用。在一些实施例中,不同的模态用于针对单个区域治疗震颤或实现其他神经调节,即使调节了两个或更多个身体区域也是如此。例如,可调节手腕和前臂以协同减小手部震颤。在另一些实施例中,不同的模态用于针对多个区域治疗震颤或实现其他神经调节。例如,可调节手腕和脚踝以减小手部震颤和腿震颤两者。除震颤外,还使用本文所述的设备来治疗其他适应症,包括但不限于:心脏功能障碍(例如,心脏节律不齐诸如心房颤动、心房扑动、室性心动过速等)、血压异常(高血压和低血压)、泌尿和/或胃肠道功能障碍(包括膀胱过度活动症、夜尿症和/或压力和急迫性失禁)以及大便失禁,以及有关神经性组成部分的精神疾病(诸如神经递质功能障碍)。
在一些实施例中,振动刺激与电刺激结合使用。在一些实施例中,振动刺激和电刺激位于相同位置或不同位置。在一些实施例中,振动刺激用于优先刺激本体感受器(例如,a纤维),并且电刺激用于优先刺激不同类型的感觉纤维,诸如疼痛或触觉感觉纤维(例如,c纤维),或反之亦然。
在一些实施例中,化学刺激与电刺激结合使用。在一些实施例中,化学刺激和电刺激位于相同位置或不同位置。在一些实施例中,电刺激用于优先刺激本体感受器(例如,a纤维),并且化学刺激用于优先刺激不同类型的感觉纤维,诸如疼痛或触觉感觉纤维(例如,c纤维),或反之亦然。
改变模式的事件可包括疾病状态的生物标志物(例如,患者报告症状、活动水平、震颤运动特性、神经完整性)。模式可由开处方的医师控制。模式可由终端用户或患者控制。可针对一天中的特定时间对模式进行预编程。可通过自主活动的度量(包括hrv、gsr、msna等)来控制模式。
可结合使用的模式的一些示例包括两个或更多个不同的刺激参数(例如,频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、突发等)。多个模式可与多个模态组合,每个模态具有多个模式或一个或多个模态具有不同模式。第一刺激可包括突发刺激并且第二刺激可包括连续刺激。第一刺激可包括第一频率(例如,约20hz)并且第二刺激可包括第二频率(例如,约40hz)。第一刺激模式可包括介于100hz和200hz之间(例如,150hz)。第二刺激模式可包括介于50hz和150hz之间(例如,100hz)。在一些实施例中,第一刺激和第二刺激可以以交替模式以介于4-12hz之间的频率突发开/关,例如在突发模式中(例如10hz)。第一刺激可包括第一波形并且第二刺激可包括与第一波形不同的第二波形。在一些实施例中,在相同区域中在相同神经束处、在相同区域中但在不同神经束(例如,不同点)和/或在不同位置处使用不同刺激参数。
形状因数:通用可穿戴刺激物
参照图14a-14e,来自图7的系统700可以是非侵入性的、完全可植入的、或部分可植入的。例如,非侵入性实施例可包括非侵入性壳体,诸如套筒1400、或贴片1410或手套。在此类非侵入性实施例中,壳体的接口与患者的外部部分连通。在一些实施例中,系统部件中的一者或多者可被植入1420。例如,当电源在患者外部时,可在接触点将效应器和/或壳体接口的至少一部分植入患者体内。
非侵入性系统壳体可促进将接口和/或效应器维持在患者附近。套筒可覆盖一长段手臂或者可以是狭窄束带。套筒可覆盖肢体的任何部分的圆周的至少一部分,或者套筒可覆盖肢体的任何部分的整个圆周。套筒的功能可以是维持外部设备相对于植入物的位置。维持位置的目的可包括实现良好的电力传输、可靠的通信或其他目的。
壳体可由适合于实现期望性能的任何材料制成。例如,壳体材料可以是柔性和/或可拉伸的材料、聚合物或织物。壳体可包括紧固件诸如velcro、系带、肘节和/或扎带以将设备固定到患者。壳体可包括被配置为保持本文所公开的系统的各种部件的多个层和/或袋。
系统可由患者在有或没有护理人员辅助的情况下进行定位。在一些实施例中,系统可具有用于将其定位在手臂上的辅助机构,诸如压力响应卡扣和/或自对准磁体。在一些实施例中,诸如套筒1400,系统可在肢体的端部上滑动(类似于运动套筒)或围绕手臂缠绕或围绕手臂自缠绕(类似于卡扣束带)。
在一些实施例中,壳体可采用贴片1410的形式。例如,可使用可移除或可降解的粘合剂将壳体贴片1410固定到患者的皮肤。贴片可穿戴多次,包括但不限于仅在刺激周期期间穿戴的贴片和留在原地持续几天、几周或几个月的贴片。贴片也可被机械地附接、化学地附接或电附接。此类实施例包括但不限于将贴片固定在期望位置的钉、线或磁体。
在一些实施例中,非侵入式系统可包括与患者通信但壳体未附接到患者的接口。例如,系统可以是患者与其相互作用的外部设备。例如,壳体可以是患者可在其中放置肢体的开放或封闭的管状结构。如图14d所示,另一个示例包括类似于垫1430或支撑结构(诸如手腕垫或支撑件)的外部设备,患者可在其上放置肢体的至少一部分。
在一个实施例中,壳体1450可具有穿戴在用户的手腕或手臂上的手表的配置,如图14h-14l所示。壳体1450可包含接口1452,该接口与壳体分离、部分分离或连接并且可与用户相互作用。接口1452可连接到壳体1450并且在使用一定时间段后可丢弃。接口的电极1454可布置成条并且可布置成阳极/阴极对。也可使用本文所述的其他电极配置。时间段可以是在单次使用之后,或者几分钟、几小时、几天、几周或几个月的时段内的多次使用之后。接口本身可以是腕带的整个部分或者可以是腕带的一部分或可附接到腕带。腕带本身可以是接口的一部分或者可以是壳体的一部分或者可以是两者。在一个示例中,具有或不具有接口的腕带可通过包括弹性材料的特征来围绕手腕卡扣,该特征略微弯曲以使得当移动时,腕带围绕手腕缠绕成圆形形状。在另一个示例中,存在具有形状记忆的温度敏感材料(例如镍钛诺),使得当设备与皮肤接触时,具有或不具有接口的腕带可改变形状以围绕患者的手腕缠绕。在另一个示例中,具有或不具有接口的腕带在腕带内部或外部具有一条或多条金属线,该腕带在移动时保持新形状以允许用户将设备放置在手腕上并增加力量以便将腕带成形到用户的独特解剖结构上。在另一个示例中,具有或不具有接口的腕带部分或完全围绕手腕缠绕。该缠绕可在相同轴线上或者可以是螺旋缠绕。
一次性或非一次性接口可以以多种不同方式连接到壳体,包括但不限于卡扣特征、velcro、压配合、磁体、温度、胶粘剂,其可包括或可不包括自对准特征。连接可在一个或多个尺寸或轴线上。作为示例,图14j-14l示出了一个可能实施例,其中存在可以是磁体的自对准件,该自对准件在3个尺寸上将接口连接到身体。对准件的圆形形状可允许一个平面中的第一尺寸对准。可从对准件的圆形特征偏移的对准件的杆状部分可沿适当轴线对准接口。对准件的总体形状可允许在最终尺寸上对准接口,该最终尺寸在实施例的该特定示例中是深度。壳体可具有该形状的匹配特征,连接部可连接到该特征。可能的是,可反转连接特征,并且可将对准件放置在壳体上,并且可将形状的匹配特征放置在接口上。对准件的这些连接部可在壳体或接口部件中的一者或两者或任一者上具有或不具有磁体。
在一些实施例中,外部设备可以是未穿戴在身体上的物体。例如,它可具有手机的形状因数,并且患者在其口袋、包、手中或以运输和支撑手机的其他方式(诸如在台面上)来携带设备。它可被设计成坐置在患者想要控制其震颤的位置中的家具表面上,诸如在餐桌处、厨房中或其更衣室中。
如图14m所示,另一个优选实施例可包括刺激设备,该刺激设备具有沿脊柱施加的一个或多个电极1460。刺激设备可用于刺激神经递质的释放并且通过对沿着脊柱定位的神经的神经调节来减小震颤。刺激可影响神经递质的释放和摄取,由此影响神经支配震颤区域。电极优选放置在颈椎根部的皮肤表面上,优选地从c1至c8,但最优选地介于c5和c8之间。电极优选是贴片电极。操作单元优选地可附连到用户,并且将电极连接到操作单元的引线优选地被磁化以便于连接。操作单元可连接到处理器并由处理器控制。由于电极优选地沿着脊柱(用户的后侧)放置,因此分离且便携式的控件模块对于用户操作而言可更加方便。
在一些实施例中,神经递质(诸如多巴胺、血清素、gaba等)经由本文所述的神经调节设备(例如,电、振动、超声(例如,聚焦超声)、射频等)增加或减少以治疗震颤、膀胱过度活动症、心脏功能障碍、抑郁症、焦虑、偏头痛和其他疾病。尽管脊椎可以是一个位置,但其他位置包括手腕、手(包括手指)、上臂、头(包括头皮、耳朵、面部、太阳穴)、腿、脚(包括脚趾)和其他位置。两个、三个或更多个位置可用于产生协同治疗效果。
在一个实施例中,电极可在脊柱的任一侧放置在脖子和肩部的c2至c8区域附近。电极可放置在距脊柱约100cm至1cm的位置,并且可放置在彼此相距200cm至5cm的位置。刺激参数可包括介于500与30μs之间的相位持续时间,其可优选地为300-60μs(微秒)。脉冲率的范围可以是10hz至5000hz或更高(例如,20khz),并且优选的范围可以是50hz至200hz或150hz。周期时间可以是连续的,或者可在5秒到1小时的范围内内。优选的周期时间可为约5秒至20秒或10秒。电刺激的持续时间的范围可从每天5分钟到24小时。优选范围可包括每天重复约10次的30分钟至60分钟,或者优选范围可以是每天约40分钟至1小时并且每周重复一次至每天重复一次。幅度(其可与强度互换使用)可在0.1ma至200ma的范围内,并且优选的范围可包括1ma至10ma。用户在对用户的震颤产生影响之前可使用设备的时间长度可以是一天到一个月,或者可以优选是2天到4天。
形状因数:对于电刺激
常规的tens设备通常难以定位、笨重且不舒服。以下创新是可轻松快速应用、调整刺激物以控制et并使患者能够独立舒适地使用它的解决方案。
使用常规tens设备,难以正确设置粘贴电极的尺寸和位置以最佳地针对期望神经。较小电极增加目标神经处的电流密度,但利用较小垫时,它们很可能将错过神经,并且来自较小电极的较高电流密度可引起不适。较大垫更易于放置,但需要更多的电力并且更有可能无意间刺激相邻组织。以下创新解决了这些挑战并且实现一致、有效、舒适和安全的刺激。
如图15a-15c所示,设备可包含电极1500的阵列,而不是仅将单个电极用作阴极以及将单个电极用作阳极。尽管为清楚起见,在患者的皮肤上单独地示出了电极,但实际上,电极阵列可集成到套筒、柔性垫或基板、或本文所述的其他形状因数中。在每次重新定位设备时或基于检测的刺激需求,将选择适当的电极组合。刺激可使用单个电极作为阳极和阴极,或者可使用电极的组合来对刺激场进行成形。电极的选择可基于来自设备中的传感器的反馈而自动进行(参见下文)。在一些实施例中,电极选择可由用户手动完成。例如,用户可循环通过电极组合,直到他们发现提供最佳震颤减小或获得正确放置的替代的组合,诸如伴随正中神经感觉刺激发生的第1手指(食指)和第2手指中的麻刺感。图15a示出了离散电极1500的二维阵列。在一些实施例中,一些电极可被组合成线性行,使得二维阵列由多个电极行形成。图15b示出了电极1500的线性阵列,其可被穿戴为如图所示的束带或贴片、垫、套筒等。图15c示出了可用于保持电极1500的阵列的壳体1502。
在一些实施例中,可通过修改电极和目标神经之间的传导通路,将来自较差定位的电极的电刺激重定向到目标神经。例如,可由导电材料制成的传导通路增强器1600可放置在患者的皮肤上、嵌入皮肤中、被植入或以上方法的组合,以便增强电刺激从电极1602到目标神经1604的传导,如图16a-16d所示。传导通路增强器可在神经上方和/或跨神经放置。例如,在一个实施例中,导电油墨的纹身可将偏离目标的刺激引向正中神经。比相邻结构(例如,血管、神经)导电性更高的纹身将提供最小电阻的路径并重引导电流。为了放置或定位导电纹身,首先要主动确定目标神经。然后将导电纹身放置在目标神经上。如图16a-16d所示,导电纹身可包括跨过神经的多个导电条带。在一些实施例中,条带可彼此平行并且横向跨过神经。在另一些实施例中,条带可形成为星形或交叉影线图案,其中心位于神经上方。在另一些实施例中,条带也可放置在神经(未示出)上方并平行于神经。
为了供用户采用,可穿戴设备应当是分立且舒适的。在图14b和图14f所示的优选实施例中,例如,效应器是电的,并且皮肤贴片具有以预定图案印刷到柔性基板上以形成“第二皮肤”的单个电极或多个电极的电子设备(类似于创可贴)。为了最佳的舒适度和表面附着,机械特性诸如弹性和刚度应与皮肤匹配。可将用于表面电刺激的电路和布线印刷或蚀刻到柔性材料中,使得设备符合身体或身体内的组织。例如,它可以是印刷在柔性基板(诸如塑料)上的铜。
在如图14g所示的另一个实施例中,设备可定位在身体的表面上,但包含经皮穿透元件1470以改善对神经的影响。这些元件可以是微针,其用于改善刺激和/或药物递送。在一些实施例中,经皮穿透元件可形成微电极阵列,其放置在皮肤表面上并穿透皮肤。微电极阵列可像微针一样起作用,并且可改善从电极到神经的信号传输并且改善皮肤的渗透性,从而改善局部药物递送。
传感器:传感器类型
设备或系统可包括传感器。用于监测震颤的传感器可包括以下的组合:单轴或多轴加速度计、陀螺仪、倾角仪(用于测量和校正由设备取向的缓慢变化而导致的重力场变化)、磁力计;光纤电测角仪、光学跟踪或电磁跟踪;用于检测震颤肌肉的肌电图(emg);电神经图(eng)信号;通过诸如脑电图(eeg)技术的皮层记录,或在紧邻神经的植入物上的直接神经记录。图17a至图17b示出了运动传感器在1710手或1720手腕上的代表性位置。其他跟踪位置可包括手指或其他身体部位。
来自这些震颤传感器的数据用于测量患者当前和历史的震颤特性(诸如幅度、频率和相位)。这些传感器还可用于确定活动,诸如用于区分非自愿运动(例如,震颤)与自愿运动(例如,喝水、写作)或相对于一天中的时间或其他检测到的活动(诸如睡眠/清醒周期)的震颤的存在或不存在。
设备还可包括用于提供性能和使用数据的传感器,包括何时穿戴设备(例如,来自温度传感器)、设备的位置(例如,来自gps)、电池电量或视频记录。在另一个实施例中,传感器是用于测量冷却的肢体的温度的温度传感器。在另一个实施例中,传感器包括视频记录。在另一个实施例中,使用来自诸如智能电话的现有硬件的传感器。例如,可使用智能电话上的加速度计或者使患者参与诱发震颤的书写任务(通过分析在智能电话屏幕上绘制的线条)来测量震颤。
传感器:用于提取震颤的算法
在若干实施例中,算法将用于从传感器所提供的数据流中提取有关震颤的信息。可基于其时域信号、频域信号、幅度或放电模式(例如,突发、尖峰)来识别震颤。例如,在图18a至图18b中,对陀螺运动数据的频谱功率的频率分析指示,震颤的中心在约6.5hz处(参见下曲线图中的最大功率)。
可获取运动数据作为每个原始传感器信道,或者通过将多个传感器的原始信号融合在一起来获取运动数据。作为一个示例,可将多轴加速度计数据组合成单个数值以进行分析。算法将提取4到12hz范围内的运动数据以移除不归因于震颤的运动。这可使用陷波滤波器、低通滤波器、加权频率傅立叶线性组合器或小波滤波器的任意组合来完成。由于每位患者具有占优势的震颤频率,因此基可于患者的震颤或震颤史的具体了解来缩小此范围。例如,对于患有6hz震颤的患者,分析算法可仅提取5至7hz范围内的运动数据。如果已知患者的震颤使手腕屈曲和伸展最大5度,则分析算法将确定45度手腕屈曲的测量运动很可能是由于有意的总体运动而非震颤。在一些实施例中,算法将通过识别可能对应于姿势保持或运动性精细运动任务的时间段来对运动数据进行采样。
一旦已经提取了适当的运动数据,算法将分析震颤的关键特性,包括幅度、中心频率、扩频、幅度、相位和频谱功率。
传感器融合技术还可用于分析震颤的不同方面。例如,可组合附接到手背的多轴加速度计和陀螺仪以减小噪音和漂移,并确定手在空间中的准确取向。如果在手腕上还使用了第二对多轴加速度计和陀螺仪,则在震颤期间可确定手腕的关节角度和位置。这可隔离哪些神经的何种刺激引起控制震颤的不同肌肉群的阻尼。
et患者具有其震颤的两个组成部分。运动性震颤在有意运动期间存在,并且对生活质量产生重大影响,因为它们影响人完成日常任务(如喝水、饮食、写作和穿衣)的能力。在抵抗重力保持的静态位置期间存在姿势性震颤。尽管它们对生活质量的影响较小,但它们可能会令人尴尬。姿势性震颤通常在疾病进程中较早存在并被认为会引起运动性震颤。两个组成部分通常都在4至12hz的范围内,其中老年患者经历较低频率的震颤。
检测姿势性震颤和运动性震颤比检测静止性震颤更具挑战性。静止性震颤存在于其他运动障碍中,包括帕金森氏病,并且可通过分析仅在肢体静止时存在的震颤来轻松识别。从运动数据中提取运动性震颤具有挑战性,因为有必要将由于震颤引起的运动与由于任务引起的运动区分开。
识别姿势性震颤可能比运动性震颤更容易,因为运动性任务期间的加速度计/陀螺仪数据会因任务中的运动而损坏。人们认为姿势性震颤可导致运动性震颤,因为人们在生命中通常比运动性震颤更早地患有姿势性震颤并且它们以约相同的频率。如图19所示,我们在临床研究中发现的姿势性震颤和运动性震颤的相关性支持使用姿势性震颤数据来分析或治疗运动性震颤的该理论。
在若干实施例中提供了基于反馈和/或算法的定制处理。
传感器:资料存储与使用
如图20所示,刺激设备2000可包含硬件、软件和固件以记录数据(诸如震颤特性、刺激历史、设备的性能、使用和/或控制)并将其传输到数据门户设备2002(诸如智能电话、手机、平板计算机、膝上型计算机、台式计算机或使用无线通信协议(诸如蓝牙)的他电子设备)。
使用et患者所使用的设备来记录的数据可存储在智能电话上,然后该智能电话将该数据传输到基于云的数据库/服务器2004,或者et患者所使用的设备可直接将数据传输到基于云的数据库/服务器2004,从而实现许多活动,包括跟踪震颤、优化刺激、与护理人员和医师共享以及建立社区。数据可向控制器提供信息,向患者、护理人员和/或临床医生提供实时反馈,或者可存储数据以向患者、护理人员和临床医生提供历史数据。可由多个用户2008在多个平台2006上查看存储在云2004上的数据。此外,云2004上的数据可由计算设备2010池化和分析。
通常每隔几个月,或每年一次,在患者拜访医师时会监测患者的震颤。这种监测通常是高度主观的。另外,震颤严重性可受到许多因素的显著影响,包括睡眠模式、情绪状态、先前体育锻炼、咖啡因摄入量、食物、药物等。
这种不频繁且不准确的监测限制患者、其护理人员和医师了解患者的et的严重性和进展以及各种治疗和行为的影响的能力。这些因素可与设备所提供的刺激的影响相互作用,并且可能难以检测到这些相互作用。可识别这些相互作用以优化治疗并且帮助患者更好地了解其行为如何影响其震颤。
在图21a所示的一个实施例中,使用可能是imu、电极或先前讨论的任何其他传感器的传感器来监测2100震颤。监测可以是连续的或在离散时间段期间。分析2110来自这些传感器的数据以识别震颤特性(幅度、频率等)随时间推移的变化。记录结果并向用户显示2120结果。分析2110和/或显示2120可在刺激设备本身上完成,或者通过将原始数据或经分析数据传送到诸如智能电话或计算机的辅助设备来完成。
在另一个实施例中,也可收集2101行为数据,使得分析可检查震颤历史记录与用户行为之间的关系。行为数据可包括咖啡因、酒精、药物的消耗和焦虑水平。然后,系统可提醒患者行为与震颤之间的相互作用。
在设备具有治疗性(例如,如果它具有效应器)的另一个实施例中,可收集2102刺激历史记录,使得分析可检查刺激历史记录和震颤特性之间的关系。
图21b所示的实施例将上传2140添加到云。可交换上传2140和分析2110的顺序,使得在上传之前在机器上完成分析(未示出)。云的使用使得能够在各种联网设备(包括智能电话、平板电脑、笔记本电脑和台式计算机)上向用户显示2120结果;向其他用户诸如医师或护理人员显示2150结果;或针对多个患者进行池化分析2160。
图21c示出了池化数据的一些潜在用途,包括基于特征(诸如患者的震颤特性、地理、年龄和性别)将患者与类似患者连接2170,或者改善2180刺激算法。
图21d示出了如何可在闭环中使用图21a-c所示的数据监测和分析来调整刺激参数。以这种方式,算法检测变量之间的相互作用以优化治疗。
设备可包含刺激的闭环控制以自适应地响应于所检测的震颤或活动水平。设备通过活动传感器、数据记录和刺激参数的系统调整来实现震颤的感觉以实现最佳震颤减小。图26a是示出该检测和响应系统的基本部件的控制图。目标2650定义预期概况。例如,在et患者中,此概况可为没有震颤,并且在pd患者中,此概况可为没有震颤或僵硬。目标2650和检测2660之间的误差2670被馈送到控制器2680,该控制器修改输出2690。控制器2680可包括处理器和存储器。除了误差和测量值之外,控制器2680的算法还可将测量历史、刺激和活动输入到其算法中。输出2690修改刺激。如果效应器是电的,则这可包括修改刺激的波形、频率、相位、位置、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、突发和/或幅度。在优选实施例中(图15),设备包含小电极的阵列并且输出修改要用作阳极和阴极的电极的选择。然后由测量设备检测2660修改的影响并且重复该过程。检测2660和/或输出2690修改可实时连续发生,以预定义时间之间(例如,每小时或每天)之间的周期性延迟发生,或者响应于用户产生的信号(诸如运动的预定义序列或按钮按下)而发生。在一些实施例中,控制器可警告患者手动修改刺激参数。该闭环可用于自动的自校准。
图26b示出了显示此检测和响应系统的基本部件的控制图,该图类似于图26a所示的描述,但现在关于位于内部和外部的部件。
控制还可考虑其他行为模式,更像是前馈控制器2640。例如,进食时间的典型模式可致使效应器在特定时间更积极地放电以减小这些活动的震颤。而且,人可基于他们的当天活动在时间表中指示他们是否希望在某些时间段增加治疗,例如,他们是否有演讲或其他引起焦虑的事件。随着时间推移,这种类型的信息也可由控制单元获得和学习。通过其他移动技术和应用程序(诸如azumio、jawbone、fitbit等)收集的其他数据(诸如睡眠、食物摄入量(尤其是酒精和咖啡因的摄入量)、运动史、情绪状态(尤其是焦虑水平)和药物使用)可集成到基于云的患者数据库中,如图20和图21所示。可提示用户输入此类数据,即诸如使用成像处理应用程序来拍摄膳食照片以确定食物摄取量。数据库将离散事件(例如,咖啡因摄入的时间和数量)与时间序列数据(例如,震颤测量)组合。算法将检查患者行为、刺激和震颤之间的关系。这些将优化刺激并警告患者影响震颤的行为。这将允许对震颤进行单独优化的治疗并前馈送到系统中。
在一些实施例中,设备或手机可在预定时间提示用户执行特定任务,该任务可针对折磨患者的震颤的类型进行定制,诸如对于et以特定姿势保持手臂,或者对于帕金森氏症将手臂置于静止位置。在该时间期间,传感器可记录震颤。在一些实施例中,可附加地或替代地指示患者饮用咖啡因或记录自从他们上次饮用咖啡因以来已经过去的时间段。该数据可用于确定咖啡因如何影响震颤、治疗方案和刺激参数的有效性、有效性的持续时间等。在一些实施例中,可在刺激之后的预定时间量(诸如10分钟、20分钟、30分钟和/或60分钟)提示患者。可取决于所测量的刺激之后的震颤减小的持续时间来调整时间。
设备将具有机载数据记录并且可将此信息传输到外部数据门户设备,诸如智能电话或支持互联网的充电与同步站。该传输可以是无线的或直接的。外部设备将具有更大的存储容量并允许传输到云中的数据库。外部设备可在机器上分析此数据并且在屏幕上或使用诸如led灯的指示器来呈现信息,或者可在刺激设备本身上示出数据。
可在多个平台(包括智能电话、平板电脑和计算机)上查看云中的数据。数据将可由包括用户、他或她的医师、护理人员或家庭成员在内的多个人查看。这样将更全面地了解患者的震颤并且实现治疗的优化。在一些实施例中,查看数据的用户还可向数据添加评论和注释,可用做出评论或注释的用户的身份以及做出评论或注释的时间来对数据进行标记。在一些实施例中,做出注释的能力可限于医疗保健提供者(诸如患者的医师)和患者。
在一些实施例中,对数据的访问限于医疗保健提供者和患者。可通过要求用户设置安全的用户名和密码以访问数据来限制访问。在一些实施例中,患者还可向其他人(诸如家人和朋友)提供对数据的访问。
用于优化的算法
我们的数据指示,使用tens设备的刺激在一些患者中高度有效,在其他患者中稍微有效,并且在其他患者中无效。然而,对刺激参数(刺激强度(例如,幅度)、频率、相位、波形(例如,形状、对称性)、占空比、定相、脉冲宽度、脉冲间隔、持续时间、开/关时间、突发等)的优化使得设备在每个患者中以最大舒适度实现最大震颤减小,并且允许设备响应于电路动态、设备位置、患者状态等的变化而随时间推移调整。图22示出了用于设备的决策算法/控制器。
在一个实施例中,优化算法通过初始化一个或多个参数2200来开始,该多个参数可包括刺激幅度、预期频率、开启时间持续时间、关闭时间持续时间和预期刺激效果延迟时间。接下来,传感器检测2202并记录震颤特性,包括震颤幅度、频率、相位和本文所述的其他特性。将所检测的震颤特性2202与期望的目标震颤特性2204进行比较,该目标震颤特性可以是无震颤或减小的震颤。比较步骤2206可确定所检测的震颤特性与目标震颤特性之间的误差或差异,并且确定是否存在震颤或减小的震颤2208,或者换句话说,所检测的震颤是否满足或超过目标状况。如果没有检测到震颤,或更一般地,如果未超过预定的目标震颤状况,则算法循环回到检测步骤2202。如果检测到震颤,或更一般地,如果超过了预定的目标震颤状况,则可开启刺激2210。一旦刺激已经超过设置的开启时间持续时间2212,则关闭刺激2214,并且算法行进回检测步骤2202。当刺激开启时,设备可将所记录的数据2218上传到云或另一个设备以进行进一步处理。一旦已经关闭刺激2214,该算法可监测关闭时间持续时间2216,并且一旦关闭时间持续时间已经过去就可继续上传数据2218。在一些实施例中,甚至可在关闭时间过去之前就上传数据。用户报告的事件2220(其可包括咖啡因或酒精的摄入、焦虑感以及可能影响震颤的其他事件)也可被输入到系统中并发送到云。数据可由控制器2222处理,该控制器可使用包括机器学习算法在内的各种算法来优化刺激参数。一旦参数被优化,就设置2224新刺激参数。还可将报告2226发送给患者,该报告可突出显示或关联在用户报告的事件中识别出的各种行为与所测量的震颤。
在一个实施例中,刺激算法被设计成优化治疗“开启”时间。优化算法可找到针对输出的最佳解决方案,包括但不限于在特定任务期间,在一天中的特定时间,在特定位置控制震颤,或者仅优化震颤的整体每日最小化。算法可以是自校准的以调整刺激参数,包括但不限于频率、幅度、脉冲宽度、针对阴极和阳极的电极选择和/或开启和关闭刺激的定时。算法可响应用户输入或者可被完全预先编程。算法可以是用于随时间推移定制刺激以根据患者的震颤或患者定义的需求实时调整的学习算法。可响应于输入而触发开关刺激,该输入包括但不限于用户输入(例如,开启或关闭设备)、自上次使用以来的时间、一天中的时间、震颤的检测(例如,通过加速度计)、电子记录、或基于先前所述或其他输入的算法。例如,用户可使用语音激活来关闭设备以利用治疗窗口(例如,关闭刺激后的震颤减小的时间)来提供有意运动所需的稳定的时间间隔。在另一个示例中,用户咬住或使用舌肌(由放置在口腔内部或外部的外部设备检测),这将发出信号以关闭刺激并允许用户稳定手臂,从而能够稳定地执行有意动作。在一些实施例中,系统和算法可基于对震颤参数和所测量的患者活动的分析来检测震颤的类型,诸如区分姿势性震颤和运动性震颤。在一些实施例中,可部分地基于所检测的震颤的类型来确定刺激参数。
在一些实施例中,系统可由事件触发器控制。事件触发器可包括定义的运动、温度、语音激活、gps位置、或基于传感器所接收的数据、或其任何组合。例如,可诸如在震颤已经分别开始或结束之前的有意运动期间开启或关闭设备。在另一个示例中,当达到指定温度时,开启或关闭设备。系统可起作用以实现期望的震颤抑制概况。例如,控制可在期望的震颤抑制的时段期间;在期望的抑制震颤的时段之前,其效果会持续超过设备的使用;和/或响应于震颤的检测而激活设备。
根据若干实施例,系统可使用传感器来确定模态、模态组合或模态设置是否有效并且调整一个或多个模态参数以改善响应。例如,如果可穿戴设备包括电效应器和振动效应器,但设置不是有效的(例如,由于公差累积),则可修改电刺激的参数(例如,频率、幅度、脉冲宽度、占空比、相位、波形形状、波形对称性、脉冲间隔、持续时间、开/关时间、突发等中的一者或多者),和/或可修改振动刺激的参数(例如,频率、幅度、脉冲宽度、占空比、波形形状、相位、波形对称性、脉冲间隔、持续时间、开/关时间、突发等中的一者或多者)。在一些实施例中,模态可停止使用。在一些实施例中,可添加新模态(例如,代替停止的模态或添加到一个或多个现有模态)。
基于社区数据的优化
目前,对震颤的时间进程了解甚少。虽然为单个患者创建数据库将改善我们减小该患者的震颤的能力,但将单独患者数据组合成包括来自许多患者的记录的数据库可使得能够应用更强大的统计方法来识别最佳刺激参数。在一些实施例中,可组合来自患有相同类型的震颤的患者的数据。在一些实施例中,来自每个患者的震颤数据可包括可搜索和可分类的元数据,其允许将数据收集在数据库中以按需进行分类、搜索和/或重组。元数据可包括震颤的类型(震颤幅度、震颤频率、震颤的暂时存在等)、姓名、年龄、种族、性别、位置、时间、食物和饮料消耗(尤其是针对咖啡因和酒精)、活动历史(运动、睡眠等)、药物、过去治疗和当前治疗方法。
上面针对图20和图21所述的系统可适用于进入数据库的来自许多患者的数据,并且算法可对大数据集进行操作。
社区构建
患有et的个体因与其震颤相关联的残疾而感到孤立。因此,他们很积极地结识患有et的其他人。有一个活跃且不断增长的支持小组集合,其组织会议并使得et患者可交谈其问题和讨论可能解决方案。参加这些会议可具有挑战性,因为一些et患者难以驾驶。同样,参加支持小组的特定地理位置内的个体可能会出现彼此不同的症状,并且他们缺乏识别彼此最相似的其他患者的能力。
算法可帮助个体找到具有类似概况的et社区的成员。例如,算法可基于患者的年龄、震颤严重性、震颤特征、治疗的成功、治疗类型、药物类型、位置(基于地址或gps)以及其他特性来表征患者。这将帮助他们彼此交流并共享来自中央社区网站的信息,该中央社区网站是针对患有et的特定个体或护理人员定制的。例如,系统可识别地理位置内的患者或识别与特定患者相距的预定距离内的其他患者。患者可选择加入在线et社区并使得其位置在系统上可搜索。系统可向患者识别预定距离内的现有et社区支持组。
其他处理器、库、数据存储装置
例如,如图7a-7d所示,处理器797可应用对数据进行操作,执行计算,并且控制震颤减小设备的其他部件。它可优选是具有外围设备的微处理器或微控制器。例如,处理器可经由控件模块740从用户接收输入,并且可控制由用户选择的刺激的执行。在另一个实施例中,处理器797可执行由用户选择的预定义刺激协议。这些刺激协议可在刺激协议的数字库798中找到,可将其加载在处理器797中或存储在外部存储器(如eeprom、sd卡等)中。处理器797还可从传感器780接收信息并在机器上处理该信息并相应地调整刺激。处理器的选择由它需要执行的信号处理程度以及需要控制的外围设备的数量和类型确定。例如,可通过任何众所周知的标准诸如usb、uart、spi、i2c/twi执行与外围设备的通信。处理器还可使用蓝牙、wifi等与其他设备部件无线通信。处理器可在设备上,或者经由处理单元和刺激单元之间的无线链路传输震颤数据。
在具有电刺激物730的实施例中,预加载协议798可以是电刺激或电刺激序列。电刺激或电信号是指电脉冲或电脉冲模式。电刺激可包括参数,诸如脉冲频率、幅度、相位、脉冲宽度或持续时间、占空比、波形形状、波形对称性、脉冲间隔、开/关时间或电刺激突发。这些参数可由用户预定义或控制。
数据存储单元770可用于将有关设备的操作统计信息和有关设备的使用统计信息优选地存储在nand闪存存储器中。nand闪存存储器是非易失性的数据存储设备,其不需要电源来保留存储的信息并且可进行电擦除和重写。在一些情况下,能够以micro-sd卡的形式移除此存储器可以是有益的。
电源
效应器可电耦接到一个或多个电源,例如,如图7a-7d所示。电源750用于为设备供电。电源750可连接到处理器797并为处理器运行提供能量。电源可优选地是可再充电的和可拆卸的,因为这允许重新使用设备。电源优选地可以是电池。通常使用若干不同的化学物质组合,包括铅酸、镍镉(nicd)、镍金属氢化物(nimh)、锂离子(li-ion)和锂离子聚合物(li-ion聚合物)。对电池进行再充电的方法优选地是附接到壁式插座或其他供电的设备、太阳能、射频和电化学。在一些实施例中,电源是超级电容器。超级电容器可分为三个不同的系列—双层电容器、伪电容器和混合电容器。超级电容器可优选地由纳米孔材料制成,该纳米孔材料包括活性炭、石墨烯、碳纳米管、碳化物衍生的碳、碳气凝胶、固体活性炭、可调谐的纳米孔碳和矿物基碳。超级电容器的优点是比电池更快的充电,以及更多的充电和放电循环的耐受性。电池和超级电容器可结合使用,因为超级电容器对大量充电-放电循环的耐受性使其非常适合与电池并联连接,并且可在功率密度方面改善电池性能。在一些实施例中,电源可利用来自身体的能量。在一些实施例中,可通过动能、通过热能和/或通过声音来利用电力。在一些实施例中,电源可包括通向外部源(诸如通用设施)的插头。可为单个设备提供两个、三个或更多电源。在一些实施例中使用低轮廓且轻便的设备以增加患者依从性。在一些实施例中提供了抗水或防水的设备。
在一个实施例中,可使用专用充电站或对接站来为设备再充电。专用充电站的益处在于,它还可促进经由wifi或其他通信协议将数据从设备上载到web。
植入物
在一些实施例中,系统的至少一部分是可植入的。植入的刺激物与表面刺激相比可提供更好的控制和舒适性,因为它位于更靠近神经的位置并且避免刺激皮肤传入感觉。
刺激周围神经以控制手部震颤的方法为适当的植入式刺激物提出具体要求。第一,植入物应该很小以最小化用于定位植入物并使其适合植入的过程的侵入性。第二,因为刺激可能会对所检测的震颤或用户输入作出响应,所以植入物应当能够接收来自外部设备的通信。第三,设备应容忍外部设备的位置的变化性。
可植入本文公开的任何数量的系统部件。在一些实施例中,植入了壳体、接口、效应器和电源,并且控制器在患者外部。在此类实施例中,控制器可例如与效应器进行无线通信。在另一些实施例中,电源在患者外部。
设备可皮下植入,部分植入,或可经皮(穿过皮肤),可在皮肤表面上,或可不与身体接触。其可能是这些设备的组件,诸如与已植入的部件通信或为其供电的表面部件。如果植入设备,则可将设备植入在神经、肌肉、骨骼、韧带或其他组织中或周围。
在一个实施例中,将植入物定位在腕管内或附近以影响穿过腕管的神经。在另一个实施例中,植入物位于二头肌之间的上臂中的正中神经上或附近。在另一个实施例中,将植入物定位在前臂或手腕中的正中神经、桡神经或尺神经上或附近。在另一个实施例中,将植入物定位在臂神经丛上或附近以影响从手臂朝向中枢神经系统传递的本体感受神经。
植入部分可在血管内放置或递送以影响植入物作用范围内的区域中的神经。在一个示例中,将设备放置在锁骨下动脉或静脉内或通过锁骨下动脉或静脉以影响臂神经丛。
如图23所示,使用户减小基本震颤的可控制设备的预选实施例包括:由至少部分皮下植入以刺激目标神经的生物相容性材料制成的电极2310;通过导线连接到植入电极2310的包含用户控制界面的外部操作单元2320。设备可包含另外元件,该另外元件可包括:处理器797,其执行计算并控制其他部件;处理器控制的函数发生器;存储在处理器或存储器中的数字库799,其包含预加载的调节协议;连接到处理器797或与处理器通信的传感器780,其检测预定义参数并将该参数信息传输到处理器;连接到传感器和处理器的数据存储单元770;以及电源750。
在该实施例中,植入电极2310可用于将直接电刺激提供给目标神经。由于电极至少部分地植入到身体中并且将保持延长的时间段(优选是几年),因此电极可由具有适当电特性且具有生物相容性的材料制成。电极2310的材料优选地选自包括以下的组:硅树脂、ptfe、聚对二甲苯、聚酰亚胺、聚酯酰亚胺、铂、陶瓷和金,或天然材料诸如胶原或透明质酸。电极2310可具有变化的形状和尺寸,但是重要地接触感兴趣的神经。电极形状包括平面柄、简单且均匀的微丝,以及从较宽基部渐缩到窄尖端的探针。电极可具有近侧端部和远侧端部。远侧端部可接触神经并适于将神经刺激脉冲递送到选定神经。引线的近侧端部可适于连接到由处理器797运行的外部操作单元。
在实施例的变型中,可能有多根引线连接到不同的神经束。在另一个变型中,如图24a-24d所示,可与植入物进行无线通信。可以是微电极或微刺激物的植入物2400可使用针插入来插入到神经附近。可将针2402插入到患者体内从而接近目标神经2404或在其附近,并且然后可从针喷射植入物。植入物2400可与位于外部的设备2406(诸如本文所述的决策单元)通信、传输和接收数据以及由该设备供电。
在一个实施例中,接口可以是植入神经袖带。袖带可完全或部分环绕神经。袖带可通过闭合蝶形手臂电极附接到神经。在另一个实施例中,接口可以是神经桥台。桥台可紧靠神经或可沿着神经放置。袖带的功能可以是提供设备和神经之间的良好接触或紧密接近。在另一个实施例中,接口可被锚定在神经上或围绕神经的鞘上。例如,设备可缠绕神经或神经鞘,绑定到神经或神经鞘,夹紧到神经或神经鞘,用小钩刺拴到或用化学方法融合到神经或神经鞘。袖带、线圈、桥台或锚固件的功能是提供设备和神经之间的良好接触或紧密接近。在图25a-25f中描绘了这些实施例中的一些实施例。袖带或束带可在手腕、手指、脚踝、腿、手臂、耳朵和其他位置上使用。
例如,图25a-25c示出了线圈电极接口的实施例,该线圈电极接口可以是如图所示的多线圈电极或者单线圈电极。在一些实施例中,线圈电极2500可由形状记忆材料诸如镍钛诺制成,并且可在插入和植入之前具有松弛的直配置,并且在暴露于身体温度之后具有卷曲配置。图25d和图25e示出了蝴形袖带型电极2510的实施例,其可至少部分地环绕神经。如在另一些实施例中一样,接口可包括单个或多个电极,并且可由形状记忆材料制成以在递送期间具有开放配置并且在植入之后具有围绕神经缠绕的闭合配置。图25f示出了具有电极2520的线性阵列的接口的实施例,该电极的线性阵列可抵靠神经邻接并沿着神经放置。
插入植入物的方法可涉及局部麻醉或全身麻醉。植入物可通过皮肤上的一个或多个穿孔,诸如针或缝合线进行递送,或者它可以是在皮肤上制成以进入目标区域的开放切口,或者它可包括两种方法。在一个实施例中,可通过将全部或部分的设备穿入神经和/或周围组织(诸如血管或肌腱)周围来植入设备。
在一个实施例中,植入物可包括沿血管通路放置的两个电极。通路可沿着掌弓并且电极可位于肱动脉和腋动脉中。电极之间的流体柱可承载电并刺激相邻的神经。电极可在血管通路的内部(如支架)或者在血管通路的外部(类似于血管包裹物)。在一个实施例中,设备可以是能够与外部设备进行双向通信的植入物。实施例可包含存储器。外部“监听器”设备也可以是电源。植入物可将诸如其动力储备或使用历史的信息传送到“监听器”。在另一个实施例中,设备是能够感测神经或邻近神经上的活动并将该信息报告给监听器的植入物。
在另一个实施例中,用于放置设备的一个或多个设备可使用超声进行引导。超声可用于测量与血管、神经或其他组织的接近度,或表征相邻组织的类型和位置。
在另一个实施例中,用于刺激的电极可作为液体注入。在另一个实施例中,电极可以是柔性并且在诸如透明质酸的粘性介质中递送。在另一个实施例中,电极可由镍钛诺制成,其在37摄氏度下成形。这将允许以一种配置注入或插入电极,诸如为细长配置以配合在针中,并且然后在加热到身体温度时成形。在图25中描述了这些示例中的一些示例。
植入物可包含必要的部件以用于植入物、外部动力传输、通信系统和/或电子设备之间进行单向或双向通信以存储可编程刺激参数。设备可包含通过来自外部天线的射频感应耦接来接收命令和电力信号的无线微模块。如果效应器是电的,则传入通信信道可包含包含刺激频率、延迟、脉冲宽度和开/关间隔的信息。
经皮充电或供电可通过消除对大型电源(例如电池)的需求来减小植入物尺寸,并且无需通过重复手术来更换电源。外部部件可用于诸如通过射频(rf)功率传输对内部部件进行无线供电。例如,外部设备可发射内部部件通过谐振线圈接收的rf电力。可以各种波长传输电力,包括但不限于射频和微波频谱,其范围从3khz到300ghz。在一些实施例中,内部设备可包含电池。外部设备可穿戴或承载在身体上,或者其可在附近周围环境中,诸如在附近桌子或墙壁上。它可以是便携式的或固定的。设备可包含在放电时进行刺激的电容式能量存储模块电极。如果对电子器件供电驱动刺激配置文件,则可显著简化电子器件。电容器阻止直流电通过,但允许交流电通过。当电容器达到其绝缘击穿电压时,它放电并释放刺激脉冲。
植入物还可诸如通过使用电子神经电图(eng)或肌电图(emg)信号或加速度计或上述的组合来直接感测震颤。在这种情况下,植入物可包括多个电极,因为微电极和大电极分别优选用于感测和刺激。设备还可包括传出通信信道以传送所检测的事件。
用于泌尿和/或胃肠道功能障碍的多模态治疗的其他实施例
在一些实施例中,多模态方法可涉及恢复自主(交感和副交感)神经系统活动的平衡,包括但不限于减小与神经膀胱回路相关的交感神经和/或副交感神经系统激活。一些实施例可利用本文公开的任何多模态方法,并且可被使用或修改以与wong等人的pct公开wo2017/132067中的用于治疗膀胱疾病的系统和方法一起使用,该专利以其整体通过引用并入本文。
在一些实施例中,本文公开了用于改善状况(包括但不限于泌尿和/或胃肠道功能障碍)的多模态周围神经刺激物。刺激可针对与膀胱功能相关联的一、二、三或更多条神经。神经可包括例如胫神经或胫后神经(其可分支成内侧和外侧足底神经分支)以及跟骨神经。隐神经是股神经的皮肤分支。其他神经包括例如阴部神经、骨盆神经、生殖器背神经、外肛门括约肌神经和生殖器背神经。在一些实施例中,可以以类似于经皮胫神经刺激的方式穿皮刺激胫(例如,后胫)神经,但以非侵入方式并且以更长久的方式。在一些实施例中,系统和方法仅包括经皮元件,而没有任何植入和/或穿皮的部件。在一些实施例中,待刺激的神经仅是下肢周围传入神经,而不是脊神经。
不受理论的限制,对膀胱的自愿控制在很大程度上可由自主神经系统(ans)介导。ans维持平衡,这对于身体器官的正常运行而言可以是重要的。例如,下腹神经(交感神经)和骨盆神经(副交感神经)都将有关膀胱充满度的信息承载到大脑,并且还共同作用以实现控制排尿的放松收缩机制。
桥脑排尿中心(pmc)的激活导致膀胱的副交感神经的激活。这继而使膀胱中的肌肉收缩并且使尿道中的肌肉松弛。当包括导水管周灰质(pag)的cns结构接收到膀胱不再充满的信号时,排尿命令停止。
对副交感神经和交感神经系统的不适当激活和抑制可导致膀胱充满、紧迫感、感觉不适和/或非自愿排尿。影响自主神经活动的周围刺激可用于调节或中断排尿反射回路以纠正异常膀胱功能。这种调节可通过例如隐神经、胫神经或两者的组合的多模态刺激来实现。在一些实施例中,系统和方法使用多模态刺激方案,该多模态刺激方案被设计成对异常网络进行移相、覆盖或模糊。在一些实施例中,系统和方法使用被设计为恢复排尿反射回路的交感神经和副交感神经活动平衡的多模态刺激方案。有利地,某些实施例利用一、二或更多条周围神经的多模态经皮传入刺激来调节与膀胱功能相关联的脑或脊髓通路和/或远离刺激位点的器官或目标。
在一些实施例中,系统和方法涉及多模态刺激参数,包括远侧肢体表面上的频率和空间选择性,以选择性地或优先地调节和平衡交感神经系统和副交感神经系统。
不受理论限制,第一目标神经(诸如隐神经)的刺激可提供膀胱回路的交感神经调节。具体地,被调谐以激发目标神经(例如,隐神经)中的大有髓纤维的刺激可向腰神经丛提供躯体传入输入,从而经由下腹神经介导通向膀胱回路的交感神经输入。交感神经通过释放去甲肾上腺素,从而激活β肾上腺素能受体来使膀胱的逼尿肌放松,并且通过激活α-肾上腺素能受体来使固有尿道括约肌收缩。使膀胱放松并使固有括约肌收缩可在膀胱循环的填充和储存阶段提供舒适感。第二目标神经(例如,胫神经)的刺激可提供膀胱回路的副交感神经调节。具体而言,被调谐以刺激胫神经中的大有髓纤维的刺激向神经丛(骶排尿中心)提供躯体传入输入,并且经由释放胆碱能递质通过盆腔神经介导通向膀胱回路的副交感神经输入。骨盆底的体细胞传出物也可能输入到尿道外括约肌并调节膀胱充满的传入感觉。由于这些回路的广泛连接和基于回路的机制,在一些实施例中,上述所有机制都可调节对信号进行协调和计时的中央皮质和桥脑排尿中心。
系统可在一系列预先指定的程序上运行,这些程序改变刺激参数并单独或组合地针对一条或多条神经以改善特定患者的膀胱过度活动症的症状,例如,其挑战主要是白天的尿急、夜间醒来(夜尿症)还是失禁和/或胃肠道功能障碍。另选地,系统可在许多参数上闭环,包括:受试者的症状史,包括夜间醒来事件、或设备或辅助设备上指示的手动输入排尿;膀胱或一般回路中的交感神经和副交感神经紧张的直接检测,包括hrv和皮肤电反应;和/或基于设备的先前使用的闭环。
在一些实施例中,多模态神经刺激可与膀胱过度活动症的一种/两种或更多种药物治疗协同结合,包括但不限于抗胆碱能药(例如,奥昔布宁、托特罗定、曲司氯胺、达非那新、索非那新和/或非索罗定)、β-3肾上腺素能药(例如,米拉贝隆)、抗痉挛药(例如,黄酮哌酯)和/或抗抑郁药(例如,三环抗抑郁药诸如地昔帕明或丙咪嗪)、激素(诸如雌激素和/或孕酮)或肉毒杆菌毒素。
在一些实施例中,效应器对于神经可以是兴奋性的。在另一些实施例中,效应器对于神经可以是抑制性的。在一些实施例中,系统可用于在治疗的一些部分期间激发神经并且在治疗的其他部分期间抑制神经。
在一些实施例中,可随时间推移修改包括本文所述波形的波形以便最大程度地减小某些影响(诸如习惯化)。减少习惯化的一种方法是修改刺激的频率、脉冲宽度、幅度、占空比、相位、波形、波形对称性、脉冲间隔、持续时间、开/关时间或突发模式。例如,随机化或伪随机化参数(例如,频率或脉冲宽度)可减小习惯化。使用高斯分布以进行随机化在一些情况下可能是有效的,并且可用于诸如随机波形的波形中。减小习惯化的另一种方法是将频率降低到低于某个阈值,例如,不超过约60hz、55hz、50hz、45hz或40hz,其中人类倾向于不会习惯化。
改变其他参数诸如幅度可以是用于改善波形舒适度的方式。例如,可基于产生强烈的感觉感知和感觉异常而不引起运动收缩所必需的阈值来调整刺激的幅度。在一些实施例中,对肌肉的激发可导致不愉快的痉挛感觉。也可在整个阶段中将此幅度调节为适当的舒适值,具体取决于人的位置或动作。
例如,本文所述的刺激波形可连续地施加到目标神经(诸如胫神经和/或隐神经),或者可以以适应于施加各种持续时间的刺激的方式或者通过响应于系统中的不同输入而调整刺激波形的特性(包括但不限于幅度、频率、脉冲宽度、占空比、相位、波形形状、波形对称性、脉冲间隔、持续时间、开/关时间和突发)来提供。在一些实施例中,系统可包括闭环控制,其使用由设备测量的一个或多个信号或由患者或医师输入到设备的反馈来调节刺激以改善功效。信号或输入可包括例如任意数量的以下各项:设备上或连接在数字生态系统中的传感器;使用心率变化性来评估自主神经功能、反射回路完整性或兴奋性,测量肌肉交感神经活动(msna)和/或通过发送刺激信号并使用emg测量反应来测量h反射。在一些实施例中,信号或输入还可包括睡眠传感器组(包括但不限于加速度计、陀螺仪、基于红外线的运动传感器和/或床垫下的压力传感器)以测量夜间运动作为夜尿事件的量度。例如,患者可在睡眠时穿戴刺激物并且夜间不安可能触发治疗,夜间不安是即将发生夜尿症事件的指示器。运动传感器组(例如,加速计、基于ir的运动传感器等)可测量通常在人有紧迫感时看到的腿的快速来回运动。eeg头带可用于测量不同的睡眠状态。患者和/或医师的输入可向设备或另一个连接的设备提供有关治疗效果和/或满意度的反馈。同样,可跟踪刺激设备的使用;并且可基于患者出现的症状或治疗结果来改变特定的刺激模式(例如,指定的刺激参数集)。可依次和/或同时或重叠地触发多个模式。
在一些实施例中,刺激物可以是具有传感器的系统的一部分以评估睡眠状态并根据穿戴者的睡眠状态调节刺激。传感器可包括运动传感器(例如,身体穿戴的加速度计和陀螺仪,或者经由视频或红外进行的无线运动跟踪)、用于测量身体温度的温度传感器、床垫下的用于测量运动的压力传感器、用于测量hrv的心率传感器、用于测量交感神经和副交感神经活动的其他传感器,和/或用于测量大脑活动的eeg传感器,以评估穿戴者的睡眠状态。例如,如果夜尿事件在慢波睡眠(此时副交感神经活动可升高)期间发生,则调节刺激参数以影响副交感神经活动,反之亦然。
在一些实施例中,多模态刺激可以是可为短期益处提供的第一刺激频率,以及可为长期益处提供的第二刺激频率,该第二刺激频率与第一刺激频率不同(例如,更高或更低)。例如,在一些情况下,10hz刺激可提供短期益处并且20hz刺激可提供长期益处。作为一个示例,可在治疗的初始周期(例如3周)中提供10hz刺激以用于急性治疗,然而可提供20hz刺激以进行长期维护或状况治疗,反之亦然,取决于期望的临床结果。在一些实施例中,特定的交感神经和/或副交感神经系统的目标和回路可取决于患者的潜在自主神经系统活动来具体地用于调节向上或向下的交感神经和/或副交感神经系统活动。直接或间接地测量交感神经和/或副交感神经系统活动的数据和/或传感器的利用(例如,在本文的其他地方公开)可用作到硬件和/或软件控制器中以修改刺激参数的闭环反馈输入,包括以实时基础。
在一些实施例中,治疗(例如,刺激)可被施加持续约、至少约或不超过约5分钟、10分钟、15分钟、30分钟、45分钟、1小时、2小时、3小时、4小时、5小时、6小时或多于一天。在一些实施例中,诸如在睡眠期间和/或在清醒期间,在夜间治疗患者。取决于期望的临床结果,可每天或每周、每隔一天、每三天、每周或以其他间隔重复1、2、3、4、5或更多次治疗。
在一些实施例中,响应能力可取决于一天中的不同时间。例如,患者或医师(或算法)可预先安排全天的不同情景治疗阶段,并且设备可在一天的那些不同时间提供治疗刺激。在一个示例中,在一天中以规则或不规则间隔并以与典型的排尿量有关的频率施加治疗。在夜尿症的治疗中,刺激可被定时为人睡眠期间的定期间隔。在一些实施例中,基于交感神经和副交感神经活动的自然昼夜模式施加刺激方案以恢复自主调节。治疗也可以以不规则的间隔进行,该间隔是人为输入的或者是机器学习从前几天的排尿事件中预测的。在一些实施例中,可在早晨施加第一频率(例如,10hz或20hz)治疗以用于急性白天缓解,并且可在睡前提供第二不同的更高或更低频率(例如,20hz或10hz)治疗以用于更长的夜间缓解。
在一些实施例中,响应能力可取决于活动。例如,在夜尿症中,运动传感器诸如加速度计或陀螺仪可感测人是否在微动,这可指示期望的潜在排尿。在该时间期间,设备可开启以提供适当的刺激。在一些实施例中,一旦排尿完成,设备可关闭。
在一些实施例中,刺激的响应能力可取决于设备中封装的一个、两个或更多个传感器来收集、存储和分析有关穿戴者的生物学度量,包括但不限于运动(例如,加速度计、陀螺仪、磁力计、弯曲传感器)、地面反作用力或脚压力(例如,力传感器或压力鞋垫)、肌肉活动(例如,emg)、心血管测量(例如,心率、hrv)、皮肤电导(例如,皮肤电导反应、皮肤电反应)、呼吸率、皮肤温度和睡眠状态(例如,清醒、轻度睡眠、深度睡眠、rem)。使用标准统计分析技术(诸如逻辑回归或朴素贝叶斯分类器),可分析这些生物学度量以评估穿戴者的活动状态,诸如久坐与活动状态、压力水平和/或膀胱流体体积等,其继而可用作泌尿和/或胃肠道紧迫性增加的预测因子。
交感神经和副交感神经活动可通过若干方法来测量,包括微神经造影(msna)、儿茶酚胺测试、心率、hrv或皮肤电反应。hrv可提供身体中的自主活动的快速且有效的近似。hrv可通过分析心跳之间的时间间隔(也称为rr间隔)来确定。例如,可通过记录设备诸如胸带或手指传感器来准确捕获心率。连续rr间隔之间的差异可提供一个人的心脏健康和自主活动的图像。一般来说,更健康的心脏在连续rr间隔之间具有更大的变化性。这种心跳数据也可用于表示个体的交感神经和副交感神经活动水平。通过频域分析,心跳频率可分为不同频带。高频信号(约0.15-0.4hz)可几乎完全反映副交感神经活动,并且低频信号(约0.04-0.15hz)可表示交感神经和副交感神经活动的混合。因此,获取高频(hf)信号与低频(lf)信号的比率可产生一个人的交感神经紧张的近似值。在一些实施例中,除了频域方法之外,hrv还可例如在时域、几何域方法下进行分析。在一些实施例中,增加的心率变化性可表示增加的副交感反应和/或减少的交感反应。减少的心率变化性可表示减少的副交感反应和/或增加的交感反应。在一些实施例中,系统可感测hrv的大约或超过基准值(或目标期望hrv值)的约5%、10%、15%、20%、25%、30%、35%、40%、45%、50%、75%、100%或更高的增加或减少,并且相应地建立一个、两个或更多个刺激模态参数的变化。在一些实施例中,一个、两个或更多个刺激模态可被配置为调节(诸如增加或减少)对与交感神经系统和/或副交感神经系统相关联的一条或多条神经(例如,周围神经)的刺激,并且可通过感测副交感或交感紧张的增加或减少来确认对治疗的反应,包括但不限于hrv的增加或减少、hrv的高频含量的变化以及hrv的高频含量与低频含量的比率的变化。在一些实施例中,膀胱反射回路的副交感神经和交感神经活动的平衡可通过用脉搏体积描记法测量的心率变化性的频率分析来评估,该脉搏体积描记法利用led光源和设置在设备中的光学传感器,该光学传感器测量针对膝盖周围的主要血管之一的由于血流引起的光水平的波动,该主要血管可包括以下中的一者或多者:股骨、腘、胫、胫后、胫前和/或膝降动脉或静脉。
在一些实施例中,用于非侵入性地测量眼肌运动和/或眨眼反射的系统或方法可用作膀胱过度活跃症或其他状况的诊断的生物标志物(例如,可用于通知疾病状态诊断的生物标志物),对膀胱过度活跃症或其他疾病的治疗的进展或功效的监测,和/或可用作有关治疗的闭环调整的反馈参数。不受理论的限制,排尿控制中涉及的中心(诸如桥脑排尿中心的内侧和外侧区域)位于桥脑被盖的网状结构中,并且在解剖学上与控制眼肌运动和/或用于协调眨眼反射的区域非常接近。因此,此类生物标志物可用于评估整合在脑桥结构中或由脑桥结构介导的功能。例如,与参考值相比增加的眨眼延迟时间(诸如大约或至少约1%、2%、3%、4%、5%、6%、7%、8%、9%、10%、15%、20%、25%或更高)在一些情况下可能与膀胱过度活动症症状相关联。在一些实施例中,可将患者的基线眼肌运动参数诸如眨眼时间与治疗期间或之后的患者的参数/时间进行比较,以进行比较。一些实施例可涉及例如:视频眼睛跟踪或眨眼(诸如经由相机,包括网络相机、平板电脑或智能电话相机,或者包括相机的可穿戴设备,例如头饰诸如帽子、眼镜诸如经修改的googleglass等);基于眼睛的偶极的眼电眼肌记录术;控制眨眼的头部肌肉(诸如眼轮匝肌和上睑提肌)的emg;用于引起眨眼(诸如的进入眼睛亮光或空气喷出)并且然后使用相机或emg来测量眨眼的时间的系统;和/或通过活动刺激信号(诸如经皮施加到眶上神经)来测量眨眼反射并且记录眼轮匝肌的神经活动。
在一些实施例中,如本文所公开的任何形式的刺激可用于将刺激施加到一个、两个或更多个穴位。在一些实施例中,待刺激的穴位可包括以下中的任何一个、两个、三个、四个、五个、六个、七个、八个、九个、十个或任何其他数目:bl18(ganshu)、bl23(shenshu)、bl27(xiaochangshu);bl28(pangguangshu);bl32(ciliao);bl33(zhongliao);bl53(baohuang);cv2(qugu);cv3(zhongji);cv4(guanyuan);cv5(shinen);cv6(qihai);gb34(yanglingquan);ki7(fuliu);ki10(yingu);lr1(dadun);lr2(xingjian);lr8(quan);n-bw-38(xiajiaoshu);sp6(sanyinjiao);sp9(yinlingquan);和/或st28(shuidao)。在一些实施例中,待刺激的穴位包括bl18、bl23、bl28和cv2。在一些实施例中,待刺激的点包括st28、sp6、bl23、bl28、bl32、bl33、bl53、cv3和n-bw-38。在一些实施例中,待刺激的穴位包括sp6、bl23、bl27、bl28、bl33和cv4。在一些实施例中,待刺激的穴位包括sp9、lr1、lr2、cv4和cv6。在一些实施例中,待刺激的穴位包括sp6、sp9、bl23、cv3和cv6。在一些实施例中,待刺激的穴位包括sp9和gb34。在一些实施例中,待刺激的穴位包括sp9、ki7、ki10和lr8。在一些实施例中,待刺激的穴位是单独的cv5或单独的bl39,或其组合。刺激点的其他排列也是可能的,具体取决于期望的临床结果。
心率的光学测量中的大误差源是运动伪像,这是由于光学传感器和被测血管之间的相对运动引起的。在一些实施例中,光学心率传感器在壳体的一侧上具有与穿戴者皮肤接触的粘合剂,以减小传感器与目标血管之间的相对运动。
在一些实施例中,设备中设置了一个、两个或更多个附加传感器,包括与穿戴者皮肤接触以测量心脏活动的电传感器或用于测量血管变化的压力传感器,这些传感器与光学传感器结合使用传感器以改善心率测量的保真度。
在一些实施例中,系统和设备具有存储器和处理器以从传感器数据中提取rr间隔,计算rr间隔的变化性,将数据变换到频域,并计算高频信号,低频信号以及高频率比频率和低频信号。
在一些实施例中,心率传感器可存储在指定时间段收集的数据,以收集足够的数据进行心率变化性计算。在一些情况下,指定时间段的范围可以是1-60秒,并且可延长到10分钟或更长。
在一些实施例中,例如,可使用传感器(诸如电极)来测量皮肤电活动(也称为电皮肤反应或皮肤电导反应)。皮肤电反应是由情绪压力引起的皮肤电阻的变化并且可用例如灵敏电流计来测量。不受理论的限制,皮肤电阻随皮肤中的汗腺的状态而变化。出汗是由交感神经系统控制的,并且皮肤电导可以是心理或生理刺激的指示。如果高度引起交感神经系统,则汗腺活动也会增加,这进而增加皮肤电导。以此方式,皮肤电导可以是可被测量的情绪反应和交感反应的量度,并且反馈数据可被发送到控制器,该控制器进而将调节刺激以例如减少交感神经系统活动。与可被感测的交感神经和/或副交感神经系统活动相关联的其他非限制性参数包括,例如,在白天和/或晚上的特定时间期间的出汗、例如由eeg头带检测到的睡眠状态(以确定交感神经和/或副交感神经活动何时特别高或低,并且可能将睡眠状态诸如阶段1、2、3、4或rem与夜尿症相关联)和/或运动。在一些实施例中,诊断和/或组合诊断/刺激设备可配置为测量人的心率和皮肤电反应以改善对人的自主活动的估计。在一些实施例中,可穿戴设备(诸如和手腕穿戴的设备)可包括皮肤电活动(eda)传感器和光学心率传感器。在一些实施例中,这种数据组合可有利地和协同地提供与单独的单个测量相比改善的对交感神经和副交感神经活动的估计。在一些实施例中,系统可包括多个传感器以结合心率和hrv来测量皮肤电活动。来自多个传感器的数据可由硬件或软件处理器分析,并且进行组合以提供对交感神经和/或副交感神经活动的更准确的估计。在一些实施例中,可将eda和hr传感器放置在手腕穿戴的设备中,该设备经由有线或无线连接与刺激物通信或者将数据发送至集中式远程服务器(例如,云)。可基于交感神经和/或副交感神经活动的估计来调整刺激参数、神经目标位置(例如,胫神经和/或隐神经)或给药方案(例如,刺激阶段的持续时间或频率)。可实时进行调整,或者在后续刺激阶段中进行调整。在一些实施例中,可调整刺激频率以增加或减少由单个特定神经或多个神经调节的自主活动。例如,在一些实施例中,目标神经的相对较低频率的刺激(例如,低于阈值(例如,约5hz))可潜在地抑制神经并且从而减少交感神经活动,而较高频率刺激(例如,高于阈值(例如,约5hz))可潜在地激发神经并且从而增加交感神经活动。可关于相同或其他的目标神经进行相同的作用以调节副交感神经活动。换句话讲,在一些实施例中,目标神经的相对较低频率的刺激(例如,低于阈值(例如,约5hz))可潜在地抑制神经并且从而减少副交感神经活动,而较高频率刺激(例如,高于阈值(例如,约5hz))可潜在地激发神经并且从而增加副交感神经活动。不受理论的限制,例如取决于刺激参数,在一些情况下,刺激目标神经可增加或减少交感神经活动、副交感神经活动或两者。在一些实施例中,隐神经的刺激可影响交感神经活动,并且胫神经的刺激可影响副交感神经活动。
多模态设备还可能对症状发作的数量做出反应,包括膀胱过度活动症。如果一天中发生更多发作,则可例如通过增加刺激的幅度、刺激的持续时间或治疗阶段数量来增加治疗。
可以以多种方式检测症状(诸如膀胱过度活动症)的发作数量以控制系统和设备施加的刺激。在一些实施例中,患者可在移动设备上输入与膀胱过度活动的症状有关的事件,包括但不限于膀胱排尿事件、尿急事件或尿失禁事件。在一些实施例中,设备上的定位服务(诸如gps)可检测人何时进入建筑物或浴室。
在一些实施例中,本文公开了多模态可穿戴系统和方法,其可利用以突发模式(例如,θ突发模式)形式的经皮感觉刺激来改善膀胱过度活动症的症状和各种其他状况,包括但不限于本文所述的那些(例如,震颤和其他运动障碍、高血压、心脏节律不齐和炎症性肠病(例如克罗恩氏病))。非侵入性周围神经θ突发刺激可有效地促进皮质或脊髓可塑性以减小症状并改善个人生活质量。
在一些实施例中,多模态刺激涉及周围神经的电磁刺激的模式。模式化刺激可以是突发刺激,诸如是以规则间隔重复的开/关模式(例如,开启10ms,关闭20ms等),或在一些实施例中可为更复杂的非突发式模式化刺激,诸如是随机模式或正弦包络。电磁刺激可包括例如电能、机械能(例如,振动)、磁能、超声能(例如,聚焦超声)、射频能、热能、光能(例如,诸如红外或紫外能)和/或微波能量、或其组合。在一些实施例中,刺激仅限于电能或电能和机械能(例如,没有施加磁能或其他类型的能量)。周围刺激可包括经皮、穿皮和/或植入的刺激。
在一些实施例中,多模态刺激涉及周围神经(包括传入神经和/或传出神经)的非侵入性经皮模式化或突发刺激。不受理论的限制,但与常规或连续刺激相比,周围神经的突发刺激可能出乎意料地导致以下中的一者或多者:更大的功效;更大的可塑性;增加的容忍性或容忍度;减小的习惯化影响;增加的舒适度;和/或减小的实现相同益处效果所需的治疗时间。在一些情况下,包括传入神经的周围神经的突发刺激可通过远程加速一个或多个中枢神经系统(例如,大脑和/或脊髓)回路的可塑性来递送更有效的治疗,换句话说,在神经回路中产生可塑性持续远长于刺激阶段的持续时间的时间段,例如大约或至少约6小时、12小时、24小时、2天、3天、4天、5天、6天、7天、2周、3周、1个月、2个月、3月、4个月、5个月、6个月、9个月、12个月、18个月、24个月、36个月或更长时间。在一些情况下,周围刺激对用户而言比中央刺激(例如,经颅刺激和/或脊柱刺激)更方便和舒适,并且可能更适合家庭和非住院使用。
在一些实施例中,突发刺激包括θ突发刺激。θ突发刺激(tbs)是重复刺激的模式化形式,其使用通过变化的突发间隔来分离的高频脉冲。最初用于海马学习和记忆研究的长时程增强的引起,以重复磁刺激(rtms)形式的θ突发刺激已被证明可非侵入地引起人类在运动、感觉和视觉皮层中的可塑性。根据各种参数(包括刺激的持续时间和连续性),可观察到长期增强或抑制(ltp/ltd)效应,其是突触功效的替代度量。刺激的阶段数量和单独阶段之间的间隔也可对所引起的响应的持续时间产生影响。刺激之前或期间的肌肉松弛水平也可影响可塑性引起的结果方向或幅度,从而表明存在体内平衡机制,其取决于先前的突触活动来调整可塑性阈值。通过θ突发性刺激证明的神经系统可塑性的有效调节可具有治疗各种神经系统疾病的巨大潜力,并且可对其他中枢神经回路产生影响。
在一些实施例中,θ突发刺激可采取间歇性θ突发刺激(itbs)、连续θ突发刺激(ctbs)和中间θ突发刺激(imtbs)的形式。可取决于期望的临床结果来选择突发模式(或两个或更多个突发模式的组合)。在一些情况下,ctbs可以是抑制性的,itbs可以是兴奋性的,并且imtbs可以既不是兴奋性的也不是抑制性的,但这可取决于参数而变化。在一些实施例中,第一神经(例如,隐神经或胫神经)的抑制性刺激可单独使用或与第二神经(例如,隐神经或胫神经)的兴奋性刺激组合使用,诸如以恢复或改善交感神经和副交感神经平衡。在一些实施例中,可通过调整刺激波形的频率或脉冲宽度来控制神经的抑制性刺激或兴奋性刺激。
在一些实施例中,每个突发可包括多个刺激,诸如大约或至少约2、3、4、5、6、7、8、9、10、11、12、13、14、15、16,17、18、19、20、30、40、50、60、70、80、90、100或更多个刺激。每个突发可具有相同或可变数量的刺激。
在一些实施例中,突发内频率可以是大约或至少约10hz、20hz、30hz、40hz、50hz、100hz、250hz、500hz、1khz或更高。在一些实施例中,突发内频率可在约10hz和约20khz之间变化。突发内频率也可在突发期间以随机或伪随机的方式变化以减小习惯化和/或增加舒适度。在另一些实施例中,突发内频率可介于约10hz和约250hz之间、约50hz和约150hz之间、约10hz和约100hz之间、约100hz和约150hz之间、约50hz和约250hz之间、或约50hz至约1000hz之间,以便最小化震颤减小,改善舒适度,减小习惯化和/或减小刺激物设备的功耗。
在一些实施例中,突发间频率可介于约1hz到约20hz之间,诸如约4hz(每个突发的开始之间有250ms)和约12hz(83ms)之间,诸如约4hz(250ms)和约8hz(142ms)之间(其通常被认为是θ带频率,包括约5hz(200ms)),或在一些实施例中介于约3.5hz和约7.5hz之间,或介于约6hz和约10hz之间。
在一些实施例中,阶段间频率可介于约1分钟和约12小时之间,诸如约5分钟和约120分钟之间、约5分钟和约60分钟之间、约10分钟和约30分钟之间、约5、10、15、20、25、30、35、40、45、50、55,60、75、90、120、180、240、300、360、420、480、540、600、660或720分钟,或合并上述任何两个值的范围。
在一些实施例中,可使用称为四脉冲刺激的重复模式化刺激,其包括在一定时间段(诸如约30分钟)内以约0.2hz重复的以短间隔频率(激励间的间隔为1.5ms)的四个脉冲。已示出四脉冲刺激可引起延长的可塑性。使用此范例的突发内频率的变化可影响所引起的可塑性的方向。这些重复的小脉冲可处于2-10个脉冲之间的任何位置或更多。
替代地或此外,也可使用除θ突发刺激以外的其他突发模式。一些非限制性示例包括δ(0-4hz)、α(8-12hz)、β(12-30hz)和γ(30-100hz)突发间频率。在一些实施例中,周围突发刺激可包括正弦、正方形、矩形、三角形、锯齿形或其他波形。
在一些实施例中,本文公开了一种通过隐神经和胫后神经的双重刺激来治疗患者的泌尿和/或胃肠道症状的多模态方法。在一些实施例中,方法可包括任意数量的以下各项:将第一周围神经效应器定位在患者的皮肤上以刺激患者的隐神经;将第二周围神经效应器定位在患者的皮肤上以刺激患者的胫后神经;通过第一周围神经效应器经皮向隐神经递送第一神经刺激信号;通过第二周围神经效应器经皮向胫神经递送第二神经刺激信号;接收与患者的自主神经系统活动有关的输入;以及基于输入修改与膀胱功能有关的至少一个大脑或脊髓自主反馈回路以平衡患者的副交感神经和交感神经系统活动。在一些实施例中,方法不利用任何可植入的部件并且仅涉及经皮刺激。第一周围神经效应器和第二周围神经效应器都可位于患者的膝盖附近。第一刺激信号可与第二刺激信号不同,包括但不限于不同类型的能量、刺激参数、突发模式、波形形状等。第一刺激信号可具有与第二刺激信号的第二频率不同的第一频率。第一刺激信号可具有与第二刺激信号不同的幅度。第一频率或第二频率可以是例如从约10hz到约20hz。第一频率或第二频率可以是例如从约5hz到约30hz。接收与患者的自主神经系统活动有关的输入可包括任意数量的以下各项:从测量患者的自主神经系统活动的传感器接收数据;从测量患者心率变化性的传感器接收数据;从测量血流特性并设置在靠近患者膝盖的血管附近的光学传感器接收心率变化性数据;从测量患者皮肤电反应的传感器接收数据;接收与患者的尿路和/或胃肠道症状有关的数据;和/或接收与患者的夜尿症发作有关的数据。
本文还公开了一种多模态可穿戴设备,其用于隐神经和胫后神经的双重刺激以及用于治疗患者的泌尿和/或胃肠道症状。在一些实施例中,设备可包括任意数量的以下特征:控制器;被配置为经皮调节隐神经的第一周围神经效应器;被配置为经皮调节胫后神经的第二周围神经效应器;以及被配置为提供反馈信息的至少一个生物医学传感器或数据输入源。控制器可包括处理器和存储器,其用于从传感器接收反馈信息,该反馈信息在由处理器执行时致使设备至少部分地基于该反馈信息来调整第一刺激和第二刺激的一个或多个参数;和/或通过第一周围神经效应器将第一刺激递送到隐神经,并且通过第二周围神经效应器将第二刺激递送到胫后神经,以通过修改与膀胱功能有关的大脑或脊髓自主反馈回路以及平衡交感神经和副交感神经活动来减小泌尿和/或胃肠道症状。在一些实施例中,设备未被配置用于植入在患者体内。反馈信息可包括实时反馈信息。第一刺激可具有例如介于约10hz和约20hz之间的频率。第二刺激可具有例如介于约5hz和约30hz之间的频率。反馈信息可包括患者的自主神经系统活动。反馈信息可包括心率变化性。反馈信息还可包括与患者的夜尿症事件有关的信息。反馈信息还可包括与患者睡眠状态有关的信息。
心脏功能障碍的多模态治疗的附加实施例
在一些实施例中,多模态方法可涉及恢复自主(交感和副交感)神经系统活动的平衡,包括但不限于减小与影响血压以及心脏节律不齐的神经回路相关的交感神经和/或副交感神经系统激活。一些实施例可利用本文公开的任何多模态方法,并且可被使用或修改以与hamner等人的pct公开wo2018/039458中的用于治疗心脏疾病的系统和方法一起使用,该专利以其整体通过引用并入本文。
自主活动不平衡可导致一些心脏病,诸如高血压和心脏节律不齐;这是自主神经系统内的交感神经和副交感神经活动的不平衡。这种不平衡可能是由于自主神经系统的交感神经和/或副交感神经肢体的过度活动或活动不足引起的。包括本文所公开的系统和方法的影响自主神经系统的多模态刺激可通过恢复自主神经系统的平衡来提供治疗益处,从而减小与这些心脏病相关联的症状的负担。
自主神经活动已被证明是导致心脏节律不齐的重要诱因。通过自主神经很好地支配人的皮肤,并且如本文所公开的神经或子午点的刺激可潜在地帮助治疗心脏节律不齐。例如,周围或远侧肢体中的传入神经(包括但不限于正中神经)通过神经回路连接至下丘脑的弓形核。不受理论的限制,弓形核的调节通过以下通路中的任一者或两者来减小升高的交感神经流出:从脑垂体到神经内分泌或激素系统中的递减输入,以及经由腹外侧中脑导水管周围灰质和延髓的缝苍白核到延髓头端腹外侧(rvlm)的递减输入。该通路可经由胆碱能的mu受体。
可选地或除此之外,手臂、腿、颈部或耳屏的周围皮肤纤维的刺激可调节脊髓c8-t1水平的星状神经节活性,以经由颈动脉窦神经减小升高的交感神经外流和/或增加迷走紧张。可调节的周围神经包括肌皮神经(在c5-c7处支配)、桡神经(在c5-t1处支配)、正中神经(在c5-t1处支配)、尺神经(在c8-t1处支配)和内侧皮肤神经(在c8-t1处支配)。延髓可操作地连接到迷走神经,该迷走神经在例如心脏的sa和av结中具有副交感作用。颈神经节是交感神经系统的椎旁神经节。来自胸脊髓的节前神经可进入颈神经节以及具有其节后纤维或神经的突触。颈神经节具有三个椎旁神经节:与c2和c3相邻的上颈神经节;节后轴突突出到目标:(心脏、头部、颈部)经由邻近颈动脉的通路;颈中神经节(最小)-与c6相邻;针对心脏和颈部;以及颈下神经节。下神经节可与第一胸神经节融合以形成单个结构、星状神经节—与c7相邻;针对心脏、下颈部、手臂、颅后动脉。例如,从颈交感神经节出现的神经有助于心脏神经丛。星状神经节(或颈胸神经节)是由下颈神经节和第一胸神经节的融合形成的交感神经节。从胸神经节中出现胸内脏神经节(胸肺神经,较大、较小和最小内脏神经),这些胸内脏神经节有助于向腹部结构提供交感神经支配。
可选地或除此之外,并且不受理论的限制,多模态刺激可通过对上下肢指压点(诸如ht7、pc6、gb34、sp6、ki6等)的肌筋膜或皮肤刺激来调用神经激素反应。神经激素反应可包括去甲肾上腺素、肾上腺素、乙酰胆碱和/或炎性细胞因子的产生的变化(增加或减少)。炎性细胞因子可包括白介素、高迁移率族蛋白b1和/或肿瘤坏死因子α。神经激素反应也可由正中神经、桡神经、尺神经或迷走神经、皮肤神经或交感神经的传入和/或传出神经刺激引起。在一个实施例中,在用本文公开的设备治疗后,去甲肾上腺素、肾上腺素、乙酰胆碱和/或炎性细胞因子中的一者或多者与治疗前相比减小至少约5%、10-20%、20-40%、40-60%或更多(包括重叠范围)。
可选地或除此之外,但不受理论的限制,手臂、腿、颈部或耳屏中自主或内脏传出神经纤维的逆行刺激可调节交感神经流出和/或调节迷走神经紧张。具体而言,通过针对身周围的c纤维,可特异性刺激交感神经传出。
可选地或除此之外,并且不受理论的限制,躯体、自主、传入和/或传出的周围神经的多模态刺激可减小触发并维持心脏节律不齐的肺静脉的零星电活动。
一些实施例涉及提供针对单独神经的周围神经刺激的多模态设备和系统。一些实施例涉及允许定制和优化对个体的治疗的设备和系统。具体地,设备可被配置用于正中神经、桡神经、尺神经或、腓神经、隐神经、胫神经和/或肢体上可触及的其他神经或经络的多模态刺激以用于治疗心脏节律不齐,包括但不限于心房颤动(慢性诸如或阵发性心房颤动)和其他心律不齐,和/或减小心脏不同步和/或高血压。可使用本文公开的系统和方法治疗的心律不齐的其他非限制性示例可包括:例如,长qt综合征、尖端扭转型室速、房性早搏、游走性房性起搏点、多焦点房性心动过速、房扑、室上性心动过速(包括psvt)、房室结折返性心动过速、交接区心律、交接区性心动过速、交界性期前收缩、心室早发性收缩、加速性心室自主节律、单形性室性心动过速、多形性室性心动过速和心室颤动。针对那些特定神经并使用适当定制的刺激产生了更有效的治疗方法(例如,减小的心律失常发作,诸如颤动或颤动发作和/或颤动发作的较短持续时间;减小的心悸/心律不齐的感觉;与治疗前(有或没有停止心律不齐)相比,心律不齐的改善速率控制,诸如心率的大约或至少约10%、20%、30%、40%或更高的减少;预防或减小与心房颤动相关联的诸如中风的栓塞事件发生率;和/或调节,例如,减少收缩压、舒张压和/或平均血压)。在一些实施例中,治疗可预防或减小药物或心脏电复律后的持续性心房颤动(af)患者的纤维性颤动的复发率,或阵发性心房颤动患者的颤动发作的次数和持续时间,包括但不限于减小消融手术后的心律补齐复发性发作的次数。在一些实施例中,治疗可减小或消除患者可能需要为其潜在心律不齐而服用的药物的数量、剂量和/或频率,从而有利地减小副作用/潜在的毒性。在一些实施例中,当与一种、两种或更多种药理剂组合时,治疗可具有意想不到的协同作用,诸如速率控制剂(例如,β受体阻滞剂,诸如阿替洛尔、美托洛尔、普萘洛尔、卡维地洛;钙通道阻滞剂,诸如硝苯地平、氨氯地平、地尔硫卓或维拉帕米;或强心苷,诸如地高辛),和/或抗心律不齐剂(例如,奎尼丁、普鲁卡因酰胺、丙吡胺、利多卡因、美西律、氟卡尼、普罗帕酮、索他洛尔、伊布利特、多非利特、胺碘酮或决奈达隆)。在一些实施例中,强心苷诸如地高辛可与诸如本文所述的周围神经刺激协议一起口服、静脉内或以另一种途径给药,以在治疗心律不齐、心脏不同步和/或高血压中具有意想不到的协同有益作用。不受理论的限制,洋地黄苷和强心苷(有时也称为地高辛或去乙酰毛花苷)可调节人体的动脉压力反射机制。压力感受器反射的减弱可导致连续和过度的交感神经活动,这继而可导致心律、血压的增加以及心脏节律不齐的开始和维持。异常压力感受器功能可与钠钾atpase泵的提升激活有关;洋地黄苷和强心苷的作用是减少这种提升激活,从而导致压力感受器的敏感性增加,包括对刺激的敏感性。因此,调节压力感受器的周围神经(例如,手臂的正中圣经、神经、尺神经或皮肤纤维)的多模态刺激可与洋地黄苷和强心苷具有意想不到的协同作用,从而抑制提升的交感神经活动;糖苷增加压力感受器反射的敏感性并且刺激激活压力感受器反射。通过减小治疗心脏功能障碍(诸如高血压或心脏节律失常)所需的糖苷剂量,这种协同作用可以是有利的,因为地高辛的治疗指标非常狭窄,并且在血浆浓度仅为治疗血浆浓度范围两倍的情况下会产生严重的毒性作用。在一些实施例中,向患者施用的强心苷诸如地高辛的剂量可比常规处方小得多,诸如大约或小于每天约3、2.8、2.6、2.4、2.2、2.0、1.8、1.6、1.4、1.2、1.0、0.8、0.6、0.4或0.2mcg/kg。在一些实施例中,强心苷的剂量可被滴定至小于治疗性的血液水平,例如大约或小于约1.5、1.4、1.3、1.2、1.1、1.0、0.9、0.8、0.7、0.6,0.5、0.4、0.3、0.2或0.1ng/ml。在一些实施例中,以大约或小于约250mcg、125mcg、62.5mcg、31.25mcg、16mcg、8mcg、4mcg、2mcg、1mcg或更少的单剂量施用形式(例如,片剂)提供地高辛。
在一些实施例中,本文公开了用于刺激多个神经以治疗心脏功能障碍的多模态设备系统和方法。2、3或更多个神经或皮片(诸如正中神经、正中皮肤神经、桡神经和/或尺神经)的刺激可用于治疗诸如心脏节律不齐的状况。在一些情况下,双神经刺激可通过对臂神经丛(单独神经在脊髓附近汇聚的近侧位置)的作用来协同提高治疗效果。例如,在一个实施例中,本文公开的设备用于在两个不同的时间刺激距臂神经丛一定距离定位的两条神经(包括但不限于正中神经、桡神经、尺神经或正中皮肤神经),其中,最终,臂神经丛由来自两个或更多个神经的两个信号基本上同时刺激(例如,小于约2ms、1ms、0.5ms、0.4ms、0.3ms、0.2ms、0.1ms、0.09ms、0.08ms、0.07ms、0.06ms、0.05ms、0.04ms、0.03ms、0.02ms、0.01ms或更少),但在一些情况下可能会更高。在一个实施例中,两条神经偏移(就刺激的定时而言)0.1-3.0ms。在一个实施例中,在与目标(包括但不限于臂神经丛)相距一定距离处定位的两条、三条、四条或更多条神经在不同的时间被刺激以便基本上同时击中靶标。在一些实施例中,系统可被配置为分别独立地控制第一目标神经和第二目标神经的刺激(包括刺激参数诸如频率和本文列出的其他参数)。换句话说,可用相同或不同的参数刺激第一目标神经和第二目标神经,并且可同时或以交替或其他方式刺激第一目标神经和第二目标神经。在一些实施例中,刺激系统可包括多个单独的刺激电路,或者具有控制器的公共电路,该控制器被配置为切换一条、两条或更多条神经的刺激参数。
本发明的实施例可包括用于进行以下操作的设备和系统以及方法:测量和收集生物学数据(例如,心率、心率变化性、ecg、皮肤电反应、温度和血压),分析数据以解释这些度量如何影响心律和/或血压,以及提供针对一个或多个神经(诸如正中神经、尺神经和/或桡神经)的周围神经刺激以治疗或预防心脏节律不齐、减小心脏不同步和/或减小血压,其中所施加的刺激可能会或可能不会根据测量数据进行修改。
在一些实施例中,多模态系统和方法可包括监测器单元,该监测器单元可以是具有带用户接口的壳体的可穿戴监测器。壳体可使用多个传感器以收集、存储和分析穿戴者的生物度量,包括但不限于:血压、运动(例如,加速度计、陀螺仪、磁力计、弯曲传感器)、肌肉活动(例如,使用电极的emg)、心血管节律度量(例如,心率、心率变化性,或使用电极以测量ecg、心律异常的心室和/或心房不同步)、皮肤电导(例如,皮肤电导反应、皮肤电反应,使用电极)、呼吸率、皮肤温度、瞳孔直径和睡眠状态(例如,清醒、轻度睡眠、深度睡眠、rem)。可通过基于光学、电气和/或加速度计的传感器来记录心律度量。具体地,研究表明,压力水平升高可增加血压。诸如锻炼的活动也可影响心率和/或节律,和/或影响血压—测量加速度(运动)、心率等可帮助识别这些活动并通过类似活动使测量标准化。此外,高血压与心力衰竭相关—通过ecg传感器测量心室不同步可有助于识别刺激长期减小高血压的有效性。因此,使用标准的统计分析、机器学习、深度学习或大数据技术(诸如逻辑回归或朴素贝叶斯分类器),可对这些生物学度量进行分析以评估人的状态(诸如压力水平),其继而可作为心脏节律不齐、心脏不同步和/或血压的增加的预测因子。在一些实施例中,设备可基于对一种或多种生物学度量的测量值、对人状态的确定和/或对心脏节律不齐、心脏节律不同步和/或血压变化的预测来提供刺激。
在一些实施例中,响应能力可取决于活动。例如,在可能因运动而加剧的心律不齐中,例如,诸如加速度计或陀螺仪的运动传感器可感应到人是否在锻炼。在该时间期间,设备可开启以提供适当的刺激。在一些实施例中,一旦活动完成,设备可关闭。在一些实施例中,传感器可在无活动的时段期间(例如,当受试者正在睡觉时)激活刺激。
在一些实施例中,刺激的响应能力可取决于设备中封装的一个、两个或更多个传感器来收集、存储和分析有关穿戴者的生物学度量,包括但不限于运动(例如,加速度计、陀螺仪、磁力计、弯曲传感器)、地面反作用力或脚压力(例如,力传感器或压力鞋垫)、肌肉活动(例如,emg)、心血管测量(例如,心率、心率变化性(hrv)、光电容积描记术(ppg),或使用电极来测量ecg和/或心律异常的心室和/或心房不同步)、皮肤电导(例如,皮肤电导反应、皮肤电反应)、呼吸率、皮肤温度、瞳孔直径和睡眠状态(例如,清醒、轻度睡眠、深度睡眠、rem)。使用标准的统计分析、机器学习、深度学习或大数据技术(诸如逻辑回归或朴素贝叶斯分类器)可对这些生物学度量进行分析以评估穿戴者的活动状态(诸如久坐与活动、压力水平等),这进而可用作血压、心脏心律不齐、或心脏不同步的变化的预测因子。
交感神经和副交感神经活动可通过若干方法来测量,包括微神经造影(msna)、儿茶酚胺测试、心率、hrv或皮肤电反应,如本文其他地方所述。
与对照组相比,患有心血管疾病的患者的hrv测量值可能存在显著差异。通过频域分析,心跳频率可分为不同频带。高频信号(在约0.15hz和约0.4hz之间)可几乎完全反映副交感神经活动,并且低频信号(在约0.04hz和约0.15hz之间)可表示交感神经和副交感神经活动的混合。在一些实施例中,获取高频(hf)信号与低频(lf)信号的比率产生一个人的交感神经紧张的近似值。也可评估甚低频(vlf)信号(在约0.004hz和约0.040hz之间)以评估副交感神经活动。还可评估hrv在频域中的总功率以评估自主活动。
交感神经和副交感神经功能也可通过例如分析平均正常-正常间隔来评估,例如,测量的心律的相邻qrs复合体之间的所有间隔,包括大于50毫秒的连续nn个间隔的间隔差数;连续nn间隔的均方差的平方根以及nn间隔的标准差。
在一些实施例中,也可使用更传统的技术来评估交感神经活动:诸如在释放之前和开始进行握力运动之前测量血压变化,或者在将手浸入冷水浴中之前和之后测量血压变化(例如,冷压测试)。可通过测量深呼吸期间的心率反应或从躺着或坐着的姿势站立时的心率响应(直立位)或通过使用倾斜桌改变人身体的取向来评估副交感神经活动。交感神经活动和副交感神经活动都可在瓦氏操纵(例如,吹入水银压力计并保持约或至少约40mmhg的压力),或直立位心律反应(例如,从躺着或坐着的姿势站立)期间进行评估。
在一些实施例中,设备中设置了一个、两个或更多个附加传感器,包括与穿戴者皮肤接触以测量心脏活动的电和/或加速度计传感器或用于测量血管变化的压力传感器,这些传感器与光学传感器结合使用传感器以改善心率测量的保真度。
在一些实施例中,系统和设备具有存储器和处理器,以从传感器数据中提取rr间隔,计算rr间隔的变化性,将数据变换到频域,并且计算高频信号、低频信号以及高频信号和低频信号的比率。在一些实施例中,系统可存储心脏事件,诸如心律不齐、心动过速、心动过缓等。
在一些实施例中,心率传感器可存储在指定时间段收集的数据,以收集足够的数据进行心率变化性计算。在一些情况下,指定时间段的范围可以是1-60秒,并且可延长到10分钟或更长。
在一些实施例中,例如,如本文其他地方所公开的,可测量皮肤电活动(也称为电皮肤反应或皮肤电导反应)。在一些实施例中,交感神经和/或副交感神经活动的显著变化可用于预测心室和/或心房不同步或心律异常的发作,并且设备可开始刺激以预防或减小不同步事件的持续时间。可实时进行调整,或者在后续刺激阶段中进行调整。在一些实施例中,可调整刺激频率以增加或减少由单个特定神经或多个神经调节的自主活动。例如,在一些实施例中,目标神经的相对较低频率的刺激(例如,低于阈值(例如,约5hz))可潜在地抑制神经并且从而减少交感神经活动,而较高频率刺激(例如,高于阈值(例如,约5hz))可潜在地激发神经并且从而增加交感神经活动。另外,可调整刺激波形的脉冲宽度以征用更多或更少的特定纤维类型,包括皮肤纤维,这可抑制交感神经活动。可关于相同或其他的目标神经进行相同的作用以调节副交感神经活动。换句话讲,在一些实施例中,目标神经的相对较低频率的刺激(例如,低于阈值(例如,约5hz))可潜在地抑制神经并且从而减少副交感神经活动,而较高频率刺激(例如,高于阈值(例如,约5hz))可潜在地激发神经并且从而增加副交感神经活动。不受理论的限制,例如取决于刺激参数,在一些情况下,刺激目标神经可增加或减少交感神经活动、副交感神经活动或两者。在一些实施例中,隐神经的刺激可影响交感神经活动,并且胫神经的刺激可影响副交感神经活动。
不受理论的限制,迷走神经和交感神经活动的同时放电可触发一些心律失常,包括心房颤动,这导致植物神经系统两臂的不平衡。在一些实施例中,系统和方法可包括使用心率变化性/皮肤电反应和心律不齐(例如,心房颤动)事件的测量值来评估交感神经平衡以确定对周围刺激的反应的可能性。例如,可将设备戴在手腕上,该设备结合用于测量心率的传感器(诸如基于光学的传感器)和/或测量皮肤电反应以评估交感迷平衡并检测心律失常(例如,心房颤动事件)的传感器和刺激设备。设备可测量hrv和/或gsr并且在指定的时段时间(诸如1-3天或1周内)检测心房颤动事件,以基于交感迷走平衡的评估和心律失常事件的检测来调整刺激参数(例如,刺激频率、交替频率、刺激持续时间、一天中的刺激时间、脉冲宽度、幅度、占空比、相位、波形形状、波形对称性、脉冲间隔、开/关时间、突发)。在一些实施例中,可将上肢和/或下肢中的一条、两条或更多条神经的刺激与迷走神经的耳分支(诸如通过耳屏)的刺激组合以调节迷走神经活动并恢复自主神经系统的平衡。
在一些实施例中,多模态系统可包括多个刺激物,其彼此进行无线通信并提供同步的模式化刺激。在一些实施例中,多个刺激物可与多个效应器连接以同时刺激多个神经。在一个实施例中,一种系统可包括针对正中神经的手腕上的刺激物以及耳朵中的针对迷走神经的耳分支的刺激物。系统中的每个刺激物可经由有线或无线连接相互通信。多个刺激物可向多条神经提供同步化刺激。刺激可以是例如多神经之间的突发、偏移或交替。
在一些情况下,设备还可对多种症状发作做出反应,包括胸痛、呼吸困难、头晕和/或心悸,其表明存在心律不齐、心脏不同步和/或血压异常。如果一天中发生更多发作,则可例如通过增加刺激的幅度、刺激的持续时间或治疗阶段数量来增加治疗。
可以以多种方式检测症状的发作数量以控制系统和设备施加的刺激。在一些实施例中,患者可在移动设备上输入与心脏症状有关的事件,包括但不限于胸痛、呼吸困难、头晕和/或心悸事件。
系统的一个实施例可将来自多个穿戴者的生物学度量与有关每个用户的其他相关人口统计数据(包括年龄、体重、身高、性别、种族等)一起集中存储在服务器系统(例如,云)上。可使用标准统计分析、机器学习、深度学习或大数据技术(诸如逻辑回归或朴素贝叶斯分类器(或其他分类器))来分析从多个穿戴者收集的数据,以通过确定生物学度量与其他记录的事件与心脏节律不齐、心脏不同步和/或增加的血压之间的相关性来改善对心脏节律不齐、心脏不同步、血压或血压变化的预测。这些相关性可用于设置治疗单元所施加的刺激波形的参数,确定施加刺激治疗的最佳时间和/或实时调整治疗单元所施加的刺激波形。
在一些实施例中,可穿戴监测器可具有视觉、听觉、触觉(例如,挤压束带)或振动触觉提示以基于生物学度量的分析来通知穿戴者关键事件,包括但不限于预测心脏节律不齐、心脏不同步、血压或增加的血压的预测和/或压力水平、心率、心率变化性或其他参数的增加。提示系统还可向穿戴者由穿戴者设置的其他预定事件或提醒通知。提示系统用于以更谨慎、更个性化的方式向穿戴者传送信息(诸如心律不齐诸如心房颤动、高血压或其他预定事件的存在),而不会引起社交场合其他人的注意。
在一些实施例中,可穿戴监测器和/或治疗单元的形式可以是腕带或手表、戒指、手套、手臂套筒或手臂束带或袖带、膝盖束带、袜子、腿套筒或袖带、耳塞/耳机、头部束带、项链或脖子束带、或符合身体上的多个位置的兼容贴片。
在一些实施例中,可选择性地或优先激活一种或多种神经内的特定纤维类型(例如,在这种特定纤维类型中产生动作电位),以通过专门调节自主神经系统的交感神经和副交感神经肢体(例如,选择性或优先地调节a-α、a-β、a-δ、b和/或c纤维中的仅一者或多于一者)来恢复自主平衡。在一些实施例中,系统和方法不刺激或基本上不刺激a-α、a-β、a-δ、b纤维或c纤维。
不受理论的限制,表层和/或皮肤传入和/或传入神经的刺激可通过抑制孤束细胞核和迷走神经核,抑制主动脉降压神经并由此抑制副交感神经输入来防止心律不齐;深传入神经和/或传出神经的刺激可通过刺激弓形核-腹侧导水管周围灰核缝通路,由此抑制延髓头端腹外侧(rvlm)并且由此抑制交感神经输入来防止心律不齐。表层纤维是较细(例如,较小直径)的传入神经,其将感觉信息传递到表层背角,其是背角和脊髓灰质的明显区域;较深纤维是较粗(例如,较大直径)的传入神经,其将感觉信息传递到深背角。
一些实施例可包括皮肤纤维(例如,a-α、a-β、a-δ和/或c)的优先刺激以抑制经由星状神经节的交感神经活动。在手腕处,选定皮肤纤维的刺激可通过内侧皮肤神经和臂神经丛的内侧索承载感觉信息,其支配在c8-t1的水平的脊髓;刺激继而通过星状或颈胸神经节调节心脏交感神经活动,其是c7-t1水平的交感神经的集合。在一些实施例中,周围神经效应器可例如位于患者的皮肤上诸如前臂内侧上以刺激正中皮肤神经,但不刺激或基本上不刺激正中神经/桡神经或尺神经,或至少优先刺激内侧皮肤神经。在一些实施例中,可优先地或具体性地刺激外侧皮肤神经和/或肌皮肤神经,或其特定纤维。在一些实施例中,仅一种类型的神经纤维被激活,而其他类型的神经纤维不被激活。例如,在一个实施例中,仅激活a-α纤维,但未激活b纤维。在一个实施例中,激活1-5种类型的纤维,而使一种或多种纤维类型失活(或功能上未刺激)。在一些实施例中,失活的纤维不放电或不承载动作电位。在一些实施例中,a-α、a-β、a-δ、b纤维或c纤维中的一者或多者被激活或未被激活。在一些实施例中,优先激活一种或多种纤维,使得相对于该周围神经的其他纤维和/或邻近目标周神经的其他周围神经,刺激特定周围神经的一种或多种纤维类型的更多数量或分数。在一些实施例中,激活神经的一种或多种纤维类型的多于约50%、60%、70%、80%、90%、95%或基本上所有的纤维,而激活另一种纤维类型的少于约50%、40%、30%、20%、10%、5%或更少,使得相对于相同神经和/或邻近目标周围神经的其他周围神经的一种或多种不同纤维类型优先激活一种或多种纤维类型。
各种神经纤维类型的选择性激活或优先激活可通过多种方式完成。在一些实施例中,可控制双相方波的刺激参数诸如脉冲宽度以选择性地或优先地激活特定的纤维类型(例如,而不激活其他纤维类型)。例如,约50-100μs的脉冲宽度可选择性或优先地刺激较大的a-α纤维;约150-200μs的脉冲宽度可选择性地或优先地刺激较小的a纤维;并且约300-400μs的脉冲宽度可选择性或优先地刺激甚至更小的c纤维。
在一些实施例中,可控制正弦波模式的频率以选择性地或优先激活特定纤维类型。例如,约2000hz、约250hz和约5hz的频率可分别选择性或优先地激活a-β、a-δ和c传入纤维。
在一些实施例中,设备可包括周围神经效应器,该周围神经效应器被配置为通过使效应器沿着神经轴突的长度对准来选择性或优先地刺激表层神经纤维(例如,更靠近皮肤表面的纤维)。
一些实施例可涉及一种或多种多模态刺激模式(例如,突发、脉冲模式、随机、伪随机或噪声)以改善刺激的效率和功效。在一些实施例中,可以以突发模式提供刺激,其中突发可以是有节奏的(例如,以规则间隔)或伪随机的。在一些实施例中,可提供将超低刺激频率(0.01-0.1hz)与较高频率刺激(1-200hz)组合或将较低频率(1-200hz)与非常高频率(1000-10khz)组合的刺激波形。
在一些实施例中,本文公开了可利用以突发模式的形式的经皮感觉刺激的可穿戴系统和方法,例如,θ突发模式以改善心脏节律不齐、心脏不同步、高血压和/或多种其他状况,包括但不限于本文公开的那些。在一些情况下,非侵入性周围神经θ突发刺激可比连续刺激更有效地促进皮质或脊髓可塑性以减小症状并改善个人生活质量。关于非限制性突发参数的附加细节在本文其他地方公开。
在一些实施例中,多模态刺激涉及周围神经(包括传入神经和/或传出神经)的非侵入性经皮模式化或突发刺激,如本文其他地方所述。
不受理论限制,在正中神经、桡神经和/或尺神经上的交替突发刺激可通过产生协同作用来防止心律不齐,该协同作用增加经由臂神经丛的星状神经节的输入以抑制交感神经活动或经由颈动脉窦神经调节迷走神经紧张。
在一些实施例中,正中神经、桡神经和/或尺神经刺激可被组合以用于臂神经丛处的协同作用。正中神经、桡神经和尺神经支配臂神经丛处的不同水平的脊髓,其中通路到达不同的目标位置和器官。一些实施例可同时或延迟地向正中神经、桡神经和/或尺神经提供定时刺激以控制臂神经丛内的靶向,从而在臂神经丛处提供神经激活的协同作用,这通向星状神经节和交感神经链。这种协同作用可以以更少的不适感和更少的电流(例如,更少的功率以延长电池寿命)提供更大的治疗益处。刺激的定时可以是同步的,或具有延迟,以解决不同神经的传导速度差异,使得信号同时到达肱神经丛。不受理论的限制,但臂神经丛的同时或几乎同时激活可通过通路增强向星状神经节的刺激,并且增加交感神经系统的作用(例如,抑制)。例如,桡神经、正中神经和尺神经的感觉神经的平均传导速度分别为约51m/s、60m/s和63m/s。基于从手腕到臂神经丛的神经长度(从女性的1%到男性的99%)的变化,这需要约1.3至约1.7毫秒的正中神经和桡神经之间的刺激延迟、约0.3和约0.4毫秒的正中神经和尺神经之间的刺激延迟、约1.6毫秒和约2.1毫秒的桡神经和尺神经之间的刺激延迟。在一些实施例中,第一神经与第二神经之间的刺激延迟可介于约0.3ms与约1.7ms之间、或约0.2ms与约2.0ms之间、约1.2ms与约2.1ms之间、或约1ms与约2ms之间。在正中神经、桡神经和/或尺神经上的较低阈值刺激可有利地要求在单个神经上的较低阈值刺激,从而在臂神经丛上产生协同作用。在一些实施例中,系统可包括神经传导速度测量(其通过在神经的远侧部分施加刺激源以及在神经的近侧部分施加测量电极来测量个体的神经传导速度),并且基于个体化的测量值修改定时延迟。
在一些实施例中,系统可包括周围神经效应器配置以便以可能有节奏或伪随机的交替模式刺激神经(例如,桡神经、正中神经和/或尺神经)。对于有节奏的交替模式,交替频率可在1-100hz的范围内,这可通过促进皮质脊髓回路的可塑性来改善治疗功效。在一些实施例中,设备实施例可包括效应器配置,其用于交替神经(例如,桡神经、正中神经和/或尺神经)的刺激,并且基于自主平衡的评估来调整刺激参数(例如,刺激频率、交替频率、刺激持续时间、一天中的刺激时间、脉冲宽度、幅度、占空比、相位、波形形状、波形对称性、脉冲间隔、开/关时间或突发),例如,通过测量心率变化性(hrv)并分析交感神经平衡,如绝对低频(lf)与绝对高频(hf)功率之比或测得hrv的lf/hf,如本文其他地方所述。
在一些实施例中,本文公开了用于治疗心律不齐或高血压的多模态方法。方法可包括任意数量的以下各项:将第一周围神经效应器定位在患者上肢的患者皮肤上以刺激选自由患者的正中神经、桡神经和尺神经中的一者组成的组的第一周围神经;将第二周围神经效应器定位在患者的耳朵或耳迷走神经的耳屏上(例如,经由耳甲艇)以刺激与患者的副交感神经通路相关联的第二周围神经;向第一周围神经效应器递送第一神经刺激信号以刺激第一周围神经,其足以修改与心律不齐或高血压有关的至少一个大脑或脊髓自主反馈回路;以及向第二周围神经效应器递送第二神经刺激信号以刺激第二周围神经,其足以修改与心律不齐或高血压有关的至少一个大脑或脊髓自主反馈回路。第二神经刺激信号可具有与第一神经刺激信号相同或不同的刺激参数。第一神经刺激信号和第二神经刺激信号可被配置为平衡患者的副交感神经和交感神经系统活动。方法还可包括监测患者中的交感神经和副交感神经活动。方法还可包括在识别患者中的异常交感神经活动时调整第一神经刺激信号。方法还可包括在识别患者中的异常副交感神经活动时调整第二神经刺激信号。
在一些实施例中,本文还公开了一种用于治疗心律不齐或高血压的多模态可穿戴系统。系统可包括任何数量的以下特征,或说明书中其他地方公开的其他特征。系统可包括:第一周围神经效应器,其被配置为定位在患者肢体的患者皮肤上;第二周围神经效应器,其被配置为定位在患者的耳朵或耳迷走神经的耳屏上(例如,通过耳甲艇);和/或至少一个生物医学传感器或数据输入源,其被配置为提供反馈信息。控制器可被配置为产生向第一周围神经效应器的第一神经刺激信号以刺激第一周围神经,其足以修改与心律不齐或高血压有关的至少一个大脑或脊髓自主反馈回路。控制器还可被配置为产生向第二周围神经效应器的第二神经刺激信号以刺激与患者的副交感神经通路相关联的第二周围神经,以修改与心律不齐或高血压有关的至少一个大脑或脊髓自主反馈回路。控制器还可被配置为调整第一神经刺激信号和第二神经刺激信号以平衡患者的副交感神经和交感神经系统活动。控制器可被配置为在识别患者中的异常交感神经和/或副交感神经活动时调整第一神经刺激信号。
本文还公开了一种用于治疗心律不齐或高血压的多模态方法。方法可包括任意数量的以下各项:评估受试者的交感神经和副交感神经活动中的至少一个,并且确定受试者中是否存在异常的交感神经和副交感神经活动;如果存在异常的交感神经活动,则刺激可操作地连接到臂神经丛的第一神经,其足以对心律不齐或高血压产生治疗作用;以及如果存在异常的副交感神经活动,则刺激耳或耳迷走神经的耳屏(例如,经由耳甲艇),其足以对心律不齐或高血压产生治疗作用。在一些情况下,刺激可以是仅经皮刺激,可包括激发或抑制第一神经的神经活动。如果同时存在异常的交感神经活动和异常的副交感神经活动,则刺激可涉及第一神经和耳朵或耳迷走神经的耳屏(例如,经由耳甲艇)。评估受试者的交感神经活性和副交感神经活性中的至少一个包括诸如用手腕穿戴的设备来测量受试者中的hrv,并且还包括测量心率和/或皮肤电活动。第一神经可以是例如本文所讨论的正中神经、桡神经、尺神经、正中皮肤神经、外侧皮肤神经或其他神经。调整可包括能量类型、刺激参数(例如,频率、幅度、脉冲宽度、脉冲间隔、相位、波形形状、波形对称性、持续时间、占空比、开/关时间、突发等)、施加刺激的一天中的时间等。
本文还公开了治疗心律不齐或高血压的多模态方法,其可涉及刺激第一周围神经;评估受试者的交感神经和副交感神经活动中的至少一个,并且确定受试者中的异常的交感神经和副交感神经活动;以及在评估交感神经活动和副交感神经活动中的至少一个后调整刺激。调整刺激可包括识别患者中的异常交感神经和副交感神经活动,并调整第一神经的刺激频率,和/或中断第一神经的刺激;以及启动第二神经的刺激。
在一些实施例中,包括多个周围神经刺激以通过调节交感神经系统的至少一个周围神经和调节副交感神经系统的至少一个周围神经促进交感神经平衡的本文所述的实施例可有利地具有响应于检测到的交感神经和/或副交感神经过度活动而选择性或优先调节自主神经系统的交感神经臂和/或副交感神经臂的能力。
对于特发性震颤和其他运动障碍、心脏功能障碍、膀胱过度活动症、胃肠道疾病、炎性肠病、精神病和其他适应症,第一刺激物可包括电刺激物并且第二刺激物可包括磁刺激物。第一刺激物可包括电刺激物并且第二刺激物可包括化学刺激物。第一刺激物可包括电刺激物并且第二刺激物可包括热刺激物。第一刺激物可包括电刺激物并且第二刺激物可包括机械刺激物。第一刺激物可包括电刺激物并且第二刺激物可包括超声刺激物(例如,聚焦超声)。第一刺激物可包括电刺激物并且第二刺激物可包括射频刺激物。第一刺激物可包括电刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括磁刺激物并且第二刺激物可包括化学刺激物。第一刺激物可包括磁刺激物并且第二刺激物可包括热刺激物。第一刺激物可包括磁刺激物并且第二刺激物可包括机械刺激物。第一刺激物可包括磁刺激物并且第二刺激物可包括超声刺激物,例如聚焦超声刺激物(例如,聚焦超声)。第一刺激物可包括磁刺激物并且第二刺激物可包括射频刺激物。第一刺激物可包括磁刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括化学刺激物并且第二刺激物可包括热刺激物。第一刺激物可包括化学刺激物并且第二刺激物可包括机械刺激物。第一刺激物可包括化学刺激物并且第二刺激物可包括聚焦超声刺激物(例如,聚焦超声)。第一刺激物可包括化学刺激物并且第二刺激物可包括射频刺激物。第一刺激物可包括化学刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括热刺激物并且第二刺激物可包括机械刺激物。第一刺激物可包括热刺激物并且第二刺激物可包括聚焦超声刺激物(例如,聚焦超声)。第一刺激物可包括热刺激物并且第二刺激物可包括射频刺激物。第一刺激物可包括热刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括机械刺激物并且第二刺激物可包括聚焦超声刺激物(例如,聚焦超声)。第一刺激物可包括机械刺激物并且第二刺激物可包括射频刺激物。第一刺激物可包括机械刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括聚焦超声刺激物(例如,聚焦超声)并且第二刺激物可包括射频刺激物。第一刺激物可包括超声(例如,聚焦超声)刺激物并且第二刺激物可包括微波刺激物。第一刺激物可包括射频刺激物并且第二刺激物可包括微波刺激物。
图27a示出了一种系统,该系统可配置为通过以规则间隔刺激相邻电极对来以定时方式刺激多个皮片(利用跨手臂嵌入在套筒中的电极阵列),使得沿神经的特定点被刺激。电极可以以线性阵列布置,例如以提供空间模式化刺激。多模态刺激可包括将不同模式施加到电极阵列(例如,电极对的线性阵列)。手臂中的可被刺激的承载感觉信息的皮片包括,例如,c5(肘部及以上的上肢外侧);c6(手的前臂和桡骨侧);c7(中指);c8(小指上的皮肤和每只手的内侧);t1(前臂内侧);以及t2(手臂的内侧和上部以及腋窝区域)。
一些实施例可涉及刺激模式(例如,突发、脉冲模式、随机、伪随机或噪声)以改善刺激的效率和功效。在一些实施例中,例如如图27a中示意性示出的,电极阵列可沿着神经的轴突对准并且可以以规则间隔刺激相邻的电极对,使得以例如约1cm/s和约10cm/s之间的速度(例如约1cm/s、约2cm/s、约3cm/s、约4cm/s、约5cm/s、约6cm/s、约7cm/s、约8cm/s、约9cm/s、约10cm/s,以及介于此类值之间的范围)刺激沿着神经的特定点。在一些实施例中,可以以突发模式提供刺激,其中突发可以是有节奏的(例如,以规则间隔)或伪随机的。在一些实施例中,可提供将超低刺激频率(0.01-0.1hz)与较高频率刺激(1-200hz)组合或将较低频率(1-200hz)与非常高频率(1000-10khz)组合的刺激波形。
横向电极配置可在皮肤表面以下的位置处提供干扰性刺激。可使用多种模式来创建不同的干扰模式。干扰可以是建设性的或破坏性的。每个电极对可具有相同的刺激参数或不同的参数。例如,不同的刺激频率可产生相消干扰,其以新拍频刺激(例如,两个不同频率之间的差异)。
在一些实施例中,电极对可在肢体上隔开,如图27b所示,使得刺激波形在特定交叉点处组合以通过产生频率为是两个波形频率之差的刺激的干扰模式来针对深纤维,例如,频率介于约2hz和约20khz之间(例如,约2hz、约4hz、约6hz、约8hz、约10hz、约12hz、约15hz、约20hz、约30hz、约40hz、约50hz、约60hz、约100hz、约250hz、约500hz、约1000hz、约2500hz、约5khz、约10khz、约15khz、约20khz,以及此类值之间的范围)。更高和更低的频率也是可能的。
示例
以下示例仅是示意性的并且不旨在限制本发明。
我们在临床研究中评估了使用周围神经刺激来改变与et相关联的回路动态的方法。使用位于手腕掌侧的表面电极102来递送经皮电神经刺激(tens)的设备100用于通过方波刺激正中神经104持续40分钟,该方波处于150hz的频率并具有300微秒的脉冲宽度,如图1所示。在该实施例中使用导线106来将设备100连接到电极102。令人惊讶的是,发现减小了震颤,因为先前研究报道使用tens的周围神经刺激不会改善震颤。
这种电刺激有效地减小患有轻度至重度震颤的受试者的震颤。使用广泛使用的运动性震颤的测量方法来评估运动性震颤:fahntolosamarin测试的阿基米德螺线绘制任务。通过测量戴在手背上的陀螺仪的角速度来评估姿势性震颤。
三名患者(在图2中分别表示为受试者a、b和c)示出了在刺激之前和之后由患有轻度、中度和重度et的受试者绘制的螺线。在患有轻度、中度和重度震颤的受试者中,姿势性震颤减小分别为70%、78%和92%。通过电刺激也可减小姿势性震颤,并且这种作用在治疗结束后最多维持45分钟。图3a-3c示出了对手腕屈伸的影响,该手腕屈伸是由图2的受试者b中的陀螺仪数据确定的,作为代表性示例。治疗十五分钟将震颤幅度从0.9度(图3a)减小到0.2度(图3b)。在治疗的40分钟内,这种震颤幅度的减小得以维持。治疗后20分钟进行的测量显示,震颤幅度持续减小并保持在0.2度(图3c)。震颤减小在受试者之间是可变的。如图4所示,一些受试者对治疗没有反应。
通过施加电刺激来减小患有et的受试者的震颤,从而实现了出色的治疗结果。刺激能够在治疗期间、立即在治疗之后以及治疗后长达二十分钟的时间内减小震颤。为了实现长期使用并允许患有et的患者将治疗整合到他们的生活中,在许多实施例中,使该系统易于使用并且长期有效。在若干实施例中,本文所述的创新和设备用于实现该目标。
在另一个示例中,将使用多模态方法,在一些实施例中,该多模态方法将使用算法学习和/或反馈。将从以下组中选择至少两种刺激:振动触觉、化学、机械、热、电、超声(例如,超声、聚焦超声)、rf和微波,并且将其施加到身体上或身体内的相同或不同位置。例如,要将第一刺激施加到手腕并且要将不同的第二刺激施加在不同的位置(脚踝、手指、耳朵、腿、手臂等)。另选地,要将第一刺激施加到第一位置(例如,手腕)并且要将不同的第二刺激施加到相同的第一位置。在另一个示例中,使用相同区域中的不同点也可提供协同作用(例如,手腕上的不同点)。可在第一位置上刺激相同或不同的神经。例如,在一些实施例中,将刺激一个区域中的不同神经(或多个位置点)。
上面已经公开了各种疾病改变设备及其方法的各种实施例,包括但不限于震颤改变设备及其使用方法。这些各种实施例可单独使用或组合使用,并且在不脱离本发明的范围的情况下,可对实施例的单独特征进行各种改变。例如,在一些情况下,可改变各种方法步骤的顺序,和/或可将一个或多个任选特征添加到所描述的设备或从中消除。因此,以上提供的实施例的描述不应被解释为对本发明范围的不当限制,如其在权利要求中所阐述的那样。
在单独实施例的上下文中在本说明书中描述的某些功能也可在单个实施例中组合实现。相反,在单个实施例的上下文中描述的各种特征也可分别或以任何合适的子组合在多个实施例中实现。而且,尽管以上可将特征描述为以某些组合起作用并且甚至最初如此要求保护,但在一些情况下可从组合中切除所要求保护的组合中的一个或多个特征,并且所要求保护的组合可针对子组合或子组合的变型。
已经阐明前面的描述和示例以根据各种实施例说明本发明,并且不旨在为不适当限制。本文提供的标题仅用于组织目的并且不应用于限制实施例。本公开的每个公开方面和示例可被单独考虑或与本公开的其他方面、示例和变型组合考虑。此外,除非另有说明,否则本公开的方法的步骤均不限于任何特定的执行顺序。本文引用的参考文献通过引用整体并入本文。将实施例描述为“优选”并不限制替代实施例的使用或范围。
尽管本文描述的方法和设备可易于进行各种修改和替代,但其特定示例已在附图中示出并在本文中进行了详细说明。然而,应当理解,所公开的实施例应当覆盖落入本文和所附权利要求书中描述的各种实施例的精神和范围内的修改、等同形式和替代形式。
取决于实施例,本文描述的任何算法、方法或过程的一个或多个动作、事件或功能可按不同的顺序执行,可添加、合并或省去(例如,并非全部的所描述的动作或事件对于算法的实施是必要的)。在一些示例中,动作或事件可例如通过多线程处理、中断处理、或多个处理器或处理器核或在其他并行架构上同时执行,而不是顺序执行。
除非另有明确说明或在所使用的上下文中另外理解,否则顺序或按时间排列的语言诸如“然后”、“下一个”、“之后”、“随后”等的使用通常旨在促进文本的传递并且不是旨在限制执行的操作顺序。
结合本文所公开的实施例描述的各种示意性逻辑块、模块、过程、方法和算法可被实现为电子硬件、计算机软件或两者的组合。为了清楚地说明硬件和软件的这种可互换性,各种示意性部件、块、模块、操作和步骤在上面已经大体上根据其功能进行描述。将这种功能性实现为硬件还是软件取决于特定应用和施加在整个系统上的设计约束。可针对每个特定应用以各种方式实现所描述的功能,但此类实现决策不应被解释为导致脱离本公开的范围。
结合本文所公开的实施例描述的各种示意性逻辑块和模块可由机器实现或执行,诸如通用处理器、数字信号处理器(dsp)、专用集成电路(asic)、现场可编程门阵列(fpga)或其他可编程逻辑设备、离散门或晶体管逻辑、离散硬件部件或被设计成执行本文描述的功能的其任何组合。通用处理器可以是微处理器,但在替代方案中,处理器可以是控制器、微控制器或状态机、它们的组合等。处理器也可被实现为计算设备的组合,例如,dsp和微处理器的组合、多个微处理器、与dsp核心结合的一个或多个微处理器、或任何其他这样的配置。
结合本文所公开的实施例描述的方法、过程或算法的框、操作或步骤可直接体现在硬件中、由处理器执行的软件模块中或两者的组合中。软件模块可驻留在ram存储器,闪存存储器,rom存储器,eprom存储器,eeprom存储器,寄存器,硬盘,可移除磁盘,光盘(例如cd-rom或dvd)或本领域已知的任何其他形式的易失性或非易失性计算机可读存储介质。可将存储介质耦接到处理器,使得处理器可从该存储介质读取信息以及可向该存储介质写入信息。在替代方案中,存储介质可与处理器成一体。处理器和存储介质可驻留在asic中。asic可驻留在用户终端中。在替代方案中,处理器和存储介质可作为离散部件驻留在用户终端中。
除非另有明确说明或在所使用的上下文中另外理解,否则本文使用的条件语言(诸如“可”、“可能”、“可以”,“例如”等)通常旨在传达一些示例包括某些特征、元件和/或状态,但一些示例不包括它们。因此,此类条件语言通常不旨在暗示一个或多个示例以任何方式需要特征、元件、框和/或状态,或者一个或多个示例必须包括用于决定(具有或没有作者输入或提示)在任何特定实施例中是否包括或将要执行这些特征、元件和/或状态的逻辑。
本文公开的方法可包括从业人员所采取的某些行动;然而,这些方法也可包括这些动作的任何第三方说明,无论是明示还是暗示的。例如,动作诸如“定位电极”包括“指示电极的定位”。
本文公开的范围还涵盖任何和所有的重叠、子范围及其组合。语言诸如“至多”、“至少”、“大于”、“小于”、“之间”等包括所列举的数字。之前有术语诸如“约”或“大约”的数字包括所列举的数字,并且应基于情况进行解释(例如,在这种情况下尽可能合理地准确,例如±5%、±10%、±15%等)。例如,“约1小时”包括“1小时”。之前有术语诸如“基本上”的短语包括所引用的短语并且应根据情况进行解释(例如,在这种情况下尽可能合理)。例如,“基本上垂直”包括“垂直”。除非另有说明,否则所有测量均在标准条件下进行,包括温度和压力。短语“至少一个”旨在需要后续列表中的至少一项,而不是后续列表中的每项中的一种类型的每项。例如,“a、b和c中的至少一个”可包括a、b、c、a和b、a和c、b和c、或a、b和c。
- 还没有人留言评论。精彩留言会获得点赞!