一种水凝胶粘合剂及其制备方法和应用与流程
本发明涉及生物材料及生物医学领域,具体涉及一种水凝胶粘合剂及其制备方法和应用。
背景技术:
所有急性创口都需要立即闭合、修复和防止感染。缝线因其抗拉强度大、开裂率低,仍是创口逼近和修复的常用闭合技术。但是,缝线的放置可能需要麻醉;缝线可诱导高感染率、神经损伤、炎症反应、肉芽肿形成和疤痕组织形成;过强的缝线拉扯不利于创口的愈合。缝钉和胶带作为缝线的替代品,虽然使用快速简便、感染率低于缝线,然而,缝钉会产生不精确的创口近似,且干燥环境会使表皮细胞移行减慢胶带因其拉伸强度低、缺乏粘附性而无法用于湿创口和多毛区域创口。
近年来,临床上能够替代或补充创口修复中常规闭合技术的粘合剂,受到研究者的广泛关注。基于凝胶聚合的水凝胶粘合剂已经成为创口管理和修复的潜力材料。水凝胶是一类具有三维网络交联结构的聚合物材料,由于其具有优异的生物相容性及一定的机械强度,因此广泛应用于组织工程和再生医学。原位固化的水凝胶具有优异的组织赋型能力,根据其成胶机理可分为温敏型、双组份注射型和光敏型等。光敏型水凝胶由于具有时空精确可控的优势而更具备临床的实际操作性。朱麟勇等人提出的非自由基光化学交联技术(yunlongyang;jieyuanzhang;zhenzhenliu;qiuninglin;xiaolinliu;chunyanbao;yangwang;linyongzhu.adv.mater.2016,28,2724.;linyongzhuet.al.pct.no.wo2016082725a1,issuedjun2,2016),该技术基于邻硝基苄醇受紫外光照产生醛基,进一步交联多胺基高分子衍生物制备水凝胶,同时,邻硝基苄醇受光照产生的醛基也会与组织表面富含的蛋白胺基交联,实现胶层与组织的化学键键连固定。但该技术的力学强度和组织的结合力不够。中国专利文献cn108187130a公开了一种用于生物损伤修复或止血的试剂及其应用,其通过增加邻硝基苄基类光扳机修饰的天然生物大分子的浓度,可以增加生物胶水的粘性,以改善现有生物胶水材料组织结合力不佳的问题。但是中国专利文献cn108187130a提供的生物胶水材料存在生物兼容性和高机械强度之间无法平衡以及凝胶容易破裂的问题。如果保证水凝胶机械强度足够的前提下,则牺牲细胞/组织增殖分化环境;如果“胶”与组织基质结合强度大于“胶”内部的结合强度,那么“胶”会被撕裂,反之亦然。这两种情况极大地限制了此类材料于创口愈合方面的应用,不足以代替缝线使用。而且中国专利文献cn108187130a提供的生物胶水主要是用于止血,其粘合力和强度远远不能满足缝合应用。此外,现有水凝胶用于生物损伤修复或止血时,创口表面比较干燥、不透气,不利于创口愈合,无法做到创口环境管理。
技术实现要素:
因此,本发明的目的是提供一种水凝胶粘合剂及其的高分子衍生物,光响应交联基团修饰的高分子衍生物以及多孔组织工程支架;
所述高分子衍生物为亲水或水溶性聚合物。
所述光响应交联基团为甲基丙烯酰胺;
所述高分子衍生物包括透明质酸、明胶、海藻酸盐、硫酸软骨素、丝素、壳聚糖、羧甲基纤维素和胶原中的一种以上;
所述多孔组织工程支架为丝素蛋白多孔组织工程支架。
优选地,所述邻硝基苄基类光扳机修饰的高分子衍生物为邻硝基苄基修饰的透明质酸;所述邻硝基苄基修饰的透明质酸中邻硝基苄基修饰的取代率为5-30%;
所述光响应交联基团修饰的高分子衍生物为明胶-甲基丙烯酰胺;所述明胶-甲基丙烯酰胺中甲基丙烯酰胺的取代率为60-100%;
所述多孔组织工程支架的孔径为5-40μm,其用于多级凝胶缠绕及细胞黏附生长。
优选地,所述多孔组织工程支架中,5-30%的多孔组织工程支架的孔径为5-20μm,30-80%的多孔组织工程支架的孔径为20-35μm,5-40%的多孔组织工程支架的孔径为35-40μm;优选地,8-15%的多孔组织工程支架的孔径为5-20μm,60-80%的多孔组织工程支架的孔径为20-35μm,10-25%的多孔组织工程支架的孔径为35-40μm。
所述水凝胶粘合剂还包括辣根过氧化物酶。
所述水凝胶粘合剂还包括促进伤口愈合、减少疤痕形成的生长因子,优选为重组碱性成纤维细胞生长因子;
所述生长因子以缓释微球作为载体;
所述缓释微球包括丝素蛋白缓释微球、聚乳酸-羟基乙酸共聚物(plga)缓释微球、聚乳酸(pla)缓释微球、聚乙醇酸(pga)缓释微球、壳聚糖缓释微球或海藻酸钠及其衍生物缓释微球,优选为丝素蛋白缓释微球;
所述水凝胶粘合剂还包括光引发剂、磷酸缓冲盐溶液和/或助悬剂;
所述助悬剂为水溶性助悬剂;优选地,所述水溶性助悬剂包括羧甲基纤维素、山梨醇和甘露醇中的至少一种。
一种水凝胶粘合剂的制备方法,包括,
将含有邻硝基苄基类光扳机修饰的高分子衍生物、光响应交联基团修饰的高分子衍生物以及多孔组织工程支架的反应体系进行光照处理,即得所述水凝胶粘合剂。
所述水凝胶粘合剂的制备方法,包括,
向所述丝素蛋白和邻硝基苄基类光扳机修饰的高分子衍生物的共混溶液中加入致孔剂,得到混合液;
以排列均匀、彼此轻微粘连的微球为模板材料;
以所述混合液浇注所述模板材料,待支架初步形成后,去除致孔剂和模板材料,接着用邻硝基苄基类光扳机修饰的高分子衍生物溶液浸润补充,冷冻干燥,得到紧密结合邻硝基苄基类光扳机修饰的高分子衍生物的多孔组织工程支架;
将所述紧密结合邻硝基苄基类光扳机修饰的高分子衍生物的多孔组织工程支架和光响应交联基团修饰的高分子衍生物加入溶剂中,进行光照处理,即得所述水凝胶粘合剂。
所述微球为聚苯乙烯微球;所述聚苯乙烯微球的粒径为5-40μm;
优选地,所述聚苯乙烯微球中,5-30%的聚苯乙烯微球的粒径为5-20μm,30-80%的聚苯乙烯微球的粒径为20-35μm,5-40%的聚苯乙烯微球的粒径为35-40μm;优选地,8-15%的聚苯乙烯微球的粒径为5-20μm,60-80%的聚苯乙烯微球的粒径为20-35μm,10-25%的聚苯乙烯微球的粒径为35-40μm;
将聚苯乙烯微球均匀排列于模具中,然后置于73-76℃恒温干燥,即得所述排列均匀、彼此轻微粘连的聚苯乙烯微球。
所述共混溶液由1-15wt%的丝素蛋白溶液和1-15wt%的邻硝基苄基类光扳机修饰的高分子衍生物溶液组成;所述丝素蛋白溶液和邻硝基苄基类光扳机修饰的高分子衍生物溶液的体积比为3:1-1:7.5;
所述致孔剂为正丁醇;所述致孔剂与所述丝素蛋白溶液的体积比为3:1-1:7.5;
所述单分散微球与丝素蛋白溶液的质量体积比(g/ml)为3:1-1:7.5;
浸润用的邻硝基苄基类光扳机修饰的高分子衍生物溶液的浓度为1-15wt%;所述浸润用的邻硝基苄基类光扳机修饰的高分子衍生物溶液与丝素蛋白溶液的体积比为1:5-3:1;
所述光响应交联基团修饰的高分子衍生物的浓度为5-30wt%;
所述紧密结合邻硝基苄基类光扳机修饰的高分子衍生物的多孔组织工程支架和光响应交联基团修饰的高分子衍生物的质量体积比(mg/ml)为0.005:1-3:1;
所述光响应交联基团修饰的高分子衍生物与溶剂的体积比为5:1-1:50。
所述反应体系中还包括生长因子缓释微球;
所述生长因子缓释微球的粒径为0.2μm-20μm;
所述缓释微球为丝素蛋白缓释微球;
所述生长因子与丝素蛋白缓释微球的质量比为1:1-20:1。
所述的水凝胶粘合剂的应用,包括如下应用:
所述水凝胶粘合剂在制备外伤引起的创口创面封闭材料或敷料中的应用;
所述水凝胶粘合剂在制备手术缝合材料或敷料中的应用;
所述水凝胶粘合剂在制备急性止血材料或敷料中的应用;
所述水凝胶粘合剂在制备组织渗漏封堵材料或敷料中的应用;
所述水凝胶粘合剂在制备浅表创口敷料中的应用。
本发明技术方案,具有如下优点:
1、本发明以高度有序的多孔组织工程支架为介质,光响应交联基团修饰的高分子衍生物、邻硝基苄基类光扳机修饰的高分子衍生物围绕其展开,由此得到的水凝胶粘合剂既提高了水凝胶的整体机械强度,又因引入高度有序的多孔组织工程支架,保证了水凝胶的整体强度均一,解决现有水凝胶机械强度不均导致的凝胶破裂问题,代偿“胶”内部与“胶-组织“外部机械强度分配不均引起的机械强度“木桶效应”影响。
水凝胶在吸水膨胀时可能会损失机械强度,导致水凝胶在创口完全愈合前破裂或最终溶解,所以控制水凝胶的吸水程度成为了关键,根据实验发现高生物兼容性的水凝胶吸水性较强,机械强度相应降低,反之亦然。本发明引入多孔组织工程支架,解决了水凝胶的生物兼容性和高机械强度之间的平衡问题。
英国皇家医学会winter博士的观点“适当湿度环境会有利于创口愈合”已逐渐被证实。本发明提供的水凝胶在粘附组织的同时可以吸收/封闭创口渗出物并保持创口适当程度的湿润,提供创口完全的封闭环境作为细菌、异物感染的屏障,利于创口的愈合。湿润的环境可以防止敷料与创口粘连,避免在换药、拆线时引起创口二次撕裂,减少患者疼痛。
2、本发明进一步在水凝胶中加入生长因子,并以缓释微球作为载体,避免生长因子在制备、光交联等过程中生物活性被破坏,保证其功能得以正常行使,参与整个伤口愈合进程,在既定时间内稳定、持续的释放生长因子,在诱导、促进创口愈合的同时,可以较大程度程度上减少疤痕的形成,且支架、交联凝胶、缓释微球释药之后空球降解可为细胞/组织生长提供营养。
3、本发明提供的水凝胶粘合剂的制备方法所用材料和试剂对人体安全,且在人体中可自降解、无残留。聚苯乙烯微球模板的引入为后续细胞组织增殖分化与水凝胶的紧密结合预留适宜空间,同时以此为模板的高度有序的组织工程支架整体的保证了“胶”的整体稳定性。
附图说明
为了更清楚地说明本发明具体实施方式中的技术方案,下面将对具体实施方式描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
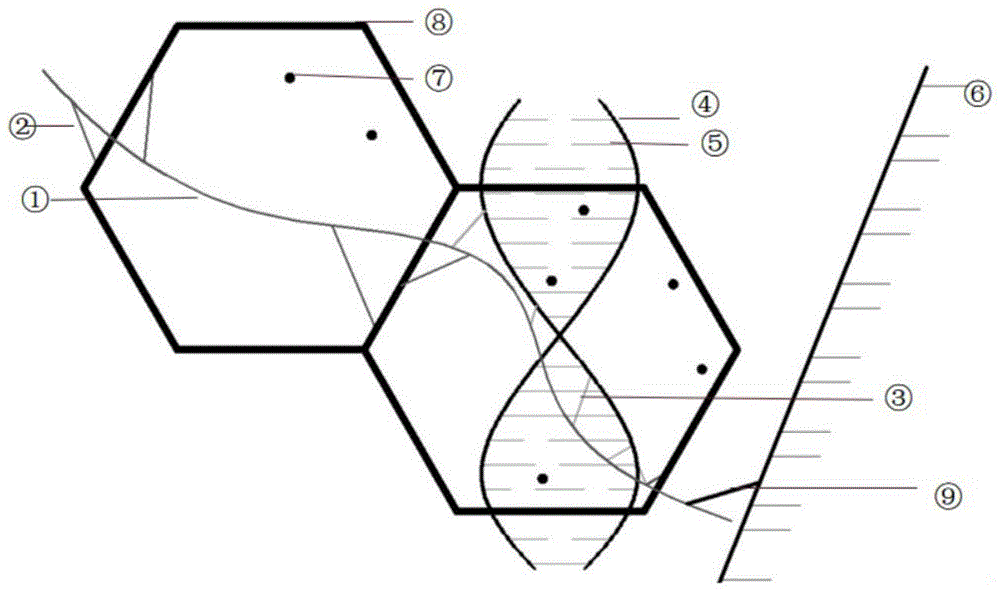
图1是本发明水凝胶形成的原理示意图;其中,①-ha-nb,②-nb-sf,③-ha-(nb-gelma),④-gelma,⑤gelma-gelma,⑥创口基质,⑦-bfgf缓释微球,⑧-sf支架,⑨-以schiff’base为主的多结合方式;
图2是本发明水凝胶的扭转模量结果,其中,图2-a为含多孔组织工程支架水凝胶的扭转模量,图2-b为不含多孔组织工程支架水凝胶的扭转模量;
图3是本发明实施例3制备的水凝胶中bfgf的缓释曲线。
具体实施方式
提供下述实施例是为了更好地进一步理解本发明,并不局限于所述最佳实施方式,不对本发明的内容和保护范围构成限制,任何人在本发明的启示下或是将本发明与其他现有技术的特征进行组合而得出的任何与本发明相同或相近似的产品,均落在本发明的保护范围之内。
实施例中未注明具体实验步骤或条件者,按照本领域内的文献所描述的常规实验步骤的操作或条件即可进行。所用试剂或仪器未注明生产厂商者,均为可以通过市购获得的常规试剂产品。
本发明提供的水凝胶粘合剂,包括邻硝基苄基类光扳机修饰的高分子衍生物,光响应交联基团修饰的高分子衍生物以及多孔组织工程支架;所述高分子衍生物为亲水或水溶性天然高聚物或合成聚合物。本发明提供的优选实施方式中,所述邻硝基苄基类光扳机修饰的高分子衍生物为邻硝基苄基修饰的透明质酸(ha-nb),所述光响应交联基团修饰的高分子衍生物为明胶-甲基丙烯酰胺(gelma),所述多孔组织工程支架为丝素蛋白多孔组织工程支架(sf支架)。
水不溶性、稳定的丝素蛋白纤维支架为水凝胶粘合剂整体提供介质,其具有透气性、持水性、低免疫原性和抗炎抗感染的优秀性能,为细胞和组织的迁移、生长、增殖、分化提供场所,也为交联网络的“生物兼容性/机械强度平衡”提供解决方案。三维网状支架降解性可控,可根据创口情况选择合适的降解周期。其优势在于:a.既保证了整体材料的整体强度均一,不会存在某处机械性能过高/过低的情况导致整体强度失衡,凝胶破裂。b.“胶”系统的整体机械强度有所提升。c.将ha-nb与支架紧密结合的同时为ha-nb与下文所述的gelma材料形成的nb-gelma,gelma-gelma形成的多级网状结构提供了“缠绕”介质。
gelma的改性,以明胶为长链骨架,明胶与甲基丙烯酸酐的含量比决定了其兼容程度和机械性能。在光引发剂引入自由基的前提下,以甲基丙烯酰胺中的碳碳双键为引发中心发生交联反应,生成网状聚合物。gelma与细胞外基质的基本结构高度相似,允许细胞于gelma中扩散增殖,机械性能、生物兼容性二者之间的平衡成反比。细胞允许增殖、分化于sf支架和gelma柔性支架,本发明最主要的是缝合作用,强调更高的机械强度,所以于柔性支架适当合理地牺牲了其生物兼容性,选取gelma的取代度在70-100%,将其功能性转驾于sf支架。ha-nb部分亦是如此。
ha-nb的改性,先与sf紧密结合,以ha为长链骨架,nb取代度为5-30%。以nb为桥梁,围绕核心schiff’sbase点击化学反应机制,活性光醛基与胺基形成席夫碱结构。而r-n=cph结构很大程度上提升了该结构的稳定性,可以使组织基质-sf及交联网络形成整体协同达到生物兼容性-机械强度的最优值。nb的pic效应(phototriggered-imine-crosslinking)下产生活性光醛基中间体(phcoh于uv条件下产生phc=o活性光醛基),继而展开后续的连锁反应。这样可使整体“胶材料”固化成为高度均一整体。
如上文所述,这种协同作用会使整体机械性能达到最佳。“胶”材料中除最主要的schiff’sbase为核心结合机制外,还会与人体基质存在亚胺基/酰胺基/联氨/迈克尔加成/缩氨脲/氢键等多种结合方式。
经紫外光照射可将若干水凝胶从无粘性液体变成稳固强度的固体达到缝合作用。
固体支架上附着ha-nb,可与创口结合,且ha-nb可与ha-nb、nb-gelma、gelma-gelma于自身形成多级网,而且而这种成网方式不冲突,可同时存在并随机成比较复杂的网,而不是简单的各自分别成网,这也很大程度上提升了其整体强度。其水凝胶形成的原理如图1,各凝胶会像多级穿线一样紧紧将其连成一个整体(创口-该球状支架-内部支点相连-穿线再次成网)达到一个高强度网状整体来提高机械性能。同时因水凝胶的特性,也可达到止血功能,以及封闭、吸收创口渗出液的作用。
除结构上,于功能性引入了促进创口修复、愈合的生长因子。它的引入可诱导组织中由中、外胚层分化出组织、器官的修复,包括但不限于一定深度的创口及表面,也可作用于体内器官修复、浅表创口敷料。同时可减少皮下纤维的无序性,进而减少疤痕的形成。但实验发现,不可将生长因子直接暴露于光固化过程,会导致该生长因子失效,所以需要隔离该环境却不能过于缓慢释放错失生长因子诱导愈合修复的最佳时期。为解决上述问题,本发明引入了具有加速愈合、减少疤痕形成的缓释微球。
本发明水凝胶的特性正契合于与适宜的湿润环境对于创口愈合的正向促进。
另一方面,水凝胶粘合剂最外层选择透气且防水的表面封锁,优选为拉索设计,封闭创口表面与外界直接接触,提供拉力用于敛合,胶布与单向封口扎带结合。纵向(与创口平行)相连,横向(与创口垂直)可以以扎带调节方向和牵引力大小。
gelma中掺入光引发剂2-羟基-4’-(2-羟乙氧基)-2-甲基苯丙酮(i2959)或苯基(2,4,6-三甲基苯甲酰基)磷酸锂盐(lap),本发明实施例中gelma中掺入i2959。
实施例1
本实施例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)、明胶-甲基丙烯酰胺(gelma)和丝素蛋白多孔组织工程支架(sf)。
本实施例水凝胶粘合剂的制备方法,包括如下步骤:
取1g30μm左右的聚苯乙烯(ps)微球分散于5ml的乙醇中清洗,室温干燥后置于聚苯乙烯模具中,并用振动器振动使其均匀排列,然后将模具置于73℃的恒温干燥箱中干燥,使得ps微球彼此轻微粘连,从而制得ps微球模板。备用。
取1ml6wt%的丝素蛋白溶液、2ml4wt%的ha-nb溶液(18%取代)形成共混溶液。向共混溶液加入0.8ml正丁醇,室温(25℃)下100r/min转速下搅拌5min得到混合液,将混合液浇注于上述灌有ps微球模板的模具中,抽真空处理3h,浸泡12h,自然晾干后用无水乙醇浸泡1h,再置于乙酸丁酯中浸泡24h以去除致孔剂和ps微球模板,接着用超纯水浸泡二次15min,抽真空带出残留有机溶剂,加入1.5ml4wt%的ha-nb溶液(取代率为18%),超低速摇床浸润30min,然后将其置于-20℃冷冻12h,最后冷冻干燥24h,即得到紧密结合ha-nb的丝素蛋白多孔组织工程支架。备用。
取10wt%的gelma溶液(85%取代),备用。
取上述紧密结合ha-nb的丝素蛋白多孔组织工程支架50mg加入上述20mlgelma溶液中,同时加入20mlph7.4、0.1m的pbs溶液,轻微摇匀,所得混合物以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
水凝胶粘合剂在具体应用时,如作为缝合材料的应用时,将ha-nb的丝素蛋白多孔组织工程支架、gelma溶液和pbs溶液的混合物置于消毒后的创口处,以365nm波长紫外光光照处理,待材料完全固化,即可实现对创口的缝合。
实施例2
本实施例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)、明胶-甲基丙烯酰胺(gelma)、丝素蛋白多孔组织工程支架(sf)和重组碱性成纤维细胞生长因子(bfgf)。
本实施例水凝胶粘合剂的制备方法,包括如下步骤:
取1g30μm左右的聚苯乙烯(ps)微球分散于5ml的乙醇中清洗,室温干燥后置于聚苯乙烯模具中,并用振动器振动使其均匀排列,然后将模具置于73-76℃的恒温干燥箱中干燥,使得ps微球彼此轻微粘连,从而制得ps微球模板。备用。
取1ml6wt%的丝素蛋白溶液、2ml4wt%的ha-nb溶液(18%取代)形成共混溶液。向共混溶液加入0.8ml正丁醇,室温下100r/min转速下搅拌5min得到混合液,将混合液浇注于上述灌有ps微球模板的模具中,抽真空处理3h,浸泡12h,自然晾干后用无水乙醇浸泡1h,再置于乙酸丁酯中浸泡24h以去除致孔剂和ps微球模板,接着用超纯水浸泡二次15min,抽真空带出残留有机溶剂,加入1.5ml4wt%的ha-nb溶液(取代率为18%),超低速摇床浸润30min,然后将其置于-20℃冷冻12h,最后冷冻干燥24h,即得到紧密结合ha-nb的丝素蛋白多孔组织工程支架。备用。
取10wt%的gelma溶液(75%取代),备用。
取8.8230mgbfgf冻干粉,按w(bfgf)/v(sf)=10:1加入至2ml3wt%的sf溶液中,于8ml无水乙醇中100r/min转速下搅拌5min,-20℃冷冻24h,40000r/min离心5min,去上清,去离子水洗涤二次,10000r/min离心3min,冻干,得到于7天bfgf缓释微球。备用。
取上述紧密结合ha-nb的丝素蛋白多孔组织工程支架50mg、bfgf缓释微球30mg加入至上述20mlgelma溶液中,同时加入20mlph7.4、0.1m的pbs溶液和30ml1wt%的羧甲基纤维素(cmc)溶液,轻微摇匀,以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
水凝胶粘合剂在具体应用时,如作为缝合材料的应用时,将ha-nb的丝素蛋白多孔组织工程支架、bfgf缓释微球、gelma溶液和pbs溶液的混合物置于消毒后的创口处,以365nm波长紫外光光照处理,待材料完全固化,即可实现对创口的缝合。
实施例3
本实施例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)、明胶-甲基丙烯酰胺(gelma)、丝素蛋白多孔组织工程支架(sf)和重组碱性成纤维细胞生长因子(bfgf)。
本实施例水凝胶粘合剂的制备方法,包括如下步骤:
取1g30μm左右的聚苯乙烯(ps)微球分散于5ml的乙醇中清洗,室温干燥后置于聚苯乙烯模具中,并用振动器振动使其均匀排列,然后将模具置于73-76℃的恒温干燥箱中干燥,使得ps微球彼此轻微粘连,从而制得ps微球模板。备用。
取1ml6wt%的丝素蛋白溶液、2ml4wt%的ha-nb溶液(18%取代)形成共混溶液。向共混溶液加入0.8ml正丁醇,室温下100r/min转速下搅拌5min得到混合液,将混合液浇注于上述灌有ps微球模板的模具中,抽真空处理3h,浸泡12h,自然晾干后用无水乙醇浸泡1h,再置于乙酸丁酯中浸泡24h以去除致孔剂和ps微球模板,接着用超纯水浸泡二次15min,抽真空带出残留有机溶剂,加入1.5ml4wt%的ha-nb溶液(取代率为18%),超低速摇床浸润30min,然后将其置于-20℃冷冻12h,最后冷冻干燥24h,即得到紧密结合ha-nb的丝素蛋白多孔组织工程支架。备用。
取10wt%的gelma溶液(85%取代),备用。
取25.2996mgbfgf冻干粉,按w(bfgf)/v(sf)=1:10加入至2ml8.25wt%sf溶液中,按照v(sf):v(正丁醇):v(peg,20wt%)=4:2:1加入正丁醇、peg,于25℃下100r/min转速下搅拌2min,然后于冰箱预冻48h,完全解冻后8000r/min离心20min,沉淀用去离子水洗涤3次,得到于21天缓释的bfgf缓释微球。备用。
取上述紧密结合ha-nb的丝素蛋白多孔组织工程支架50mg、bfgf缓释微球30mg加入至上述20mlgelma溶液中,同时加入20mlph7.4、0.1m的pbs溶液和30ml1wt%的羧甲基纤维素(cmc)溶液,轻微摇匀,以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
水凝胶粘合剂在具体应用时,如作为缝合材料的应用时,将ha-nb的丝素蛋白多孔组织工程支架、bfgf缓释微球、gelma溶液和pbs溶液的混合物置于消毒后的创口处,以365nm波长紫外光光照处理,待材料完全固化,即可实现对创口的缝合。
实施例4
本实施例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)、明胶-甲基丙烯酰胺(gelma)和丝素蛋白多孔组织工程支架(sf)。
本实施例水凝胶粘合剂的制备方法,包括如下步骤:
取1g30μm左右的聚苯乙烯(ps)微球分散于5ml的乙醇中清洗,室温干燥后置于聚苯乙烯模具中,并用振动器振动使其均匀排列,然后将模具置于73-76℃的恒温干燥箱中干燥,使得ps微球彼此轻微粘连,从而制得ps微球模板。备用。
取3ml1wt%的丝素蛋白溶液、1ml15wt%的ha-nb溶液(5%取代)形成共混溶液。向共混溶液加入9ml正丁醇,室温下100r/min转速下搅拌5min得到混合液,将混合液浇注于上述灌有ps微球模板的模具中,抽真空处理3h,浸泡12h,自然晾干后用无水乙醇浸泡1h,再置于乙酸丁酯中浸泡24h以去除致孔剂和ps微球模板,接着用超纯水浸泡二次15min,抽真空带出残留有机溶剂,加入1.5ml1wt%的ha-nb溶液(取代率为18%),超低速摇床浸润30min,然后将其置于-20℃冷冻12h,最后冷冻干燥24h,即得到紧密结合ha-nb的丝素蛋白多孔组织工程支架。备用。
取5wt%的gelma溶液(85%取代),备用。
取上述紧密结合ha-nb的丝素蛋白多孔组织工程支架5mg加入上述1000mlgelma溶液中,同时加入20mlph7.4、0.1m的pbs溶液,轻微摇匀,所得混合物以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
水凝胶粘合剂在具体应用时,如作为缝合材料的应用时,将ha-nb的丝素蛋白多孔组织工程支架、gelma溶液和pbs溶液的混合物置于消毒后的创口处,以365nm波长紫外光光照处理,待材料完全固化,即可实现对创口的缝合。
实施例5
本实施例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)、明胶-甲基丙烯酰胺(gelma)和丝素蛋白多孔组织工程支架(sf)。
本实施例水凝胶粘合剂的制备方法,包括如下步骤:
取1g30μm左右的聚苯乙烯(ps)微球分散于5ml的乙醇中清洗,室温干燥后置于聚苯乙烯模具中,并用振动器振动使其均匀排列,然后将模具置于73-76℃的恒温干燥箱中干燥,使得ps微球彼此轻微粘连,从而制得ps微球模板。备用。
取1ml15wt%的丝素蛋白溶液、7.5ml1wt%的ha-nb溶液(30%取代)形成共混溶液。向共混溶液加入7.5ml正丁醇,室温下100r/min转速下搅拌5min得到混合液,将混合液浇注于上述灌有ps微球模板的模具中,抽真空处理3h,浸泡12h,自然晾干后用无水乙醇浸泡1h,再置于乙酸丁酯中浸泡24h以去除致孔剂和ps微球模板,接着用超纯水浸泡二次15min,抽真空带出残留有机溶剂,加入3ml15wt%的ha-nb溶液(取代率为18%),超低速摇床浸润30min,然后将其置于-20℃冷冻12h,最后冷冻干燥24h,即得到紧密结合ha-nb的丝素蛋白多孔组织工程支架。备用。
取30wt%的gelma溶液(85%取代),备用。
取上述紧密结合ha-nb的丝素蛋白多孔组织工程支架30mg加入上述10mlgelma溶液中,同时加入500mlph7.4、0.1m的pbs溶液,轻微摇匀,所得混合物以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
水凝胶粘合剂在具体应用时,如作为缝合材料的应用时,将ha-nb的丝素蛋白多孔组织工程支架、gelma溶液和pbs溶液的混合物置于消毒后的创口处,以365nm波长紫外光光照处理,待材料完全固化,即可实现对创口的缝合。
对比例1
本对比例提供的水凝胶粘合剂,包括邻硝基苄基修饰的透明质酸(ha-nb)和明胶-甲基丙烯酰胺(gelma),不添加丝素蛋白多孔组织工程支架(sf)。
本对比例水凝胶粘合剂的制备方法,包括如下步骤:
取4wt%的ha-nb溶液(取代率为18%),备用。
取10wt%的gelma溶液(85%取代),备用。
取50mlha-nb溶液加入上述20mlgelma溶液中,同时加入20mlph7.4、0.1m的pbs溶液,轻微摇匀,所得混合物以365nm波长紫外光光照处理30s,即得水凝胶粘合剂。
实验例1
为了测试实施例1(含多孔组织工程支架)和对比例1(不含多孔组织工程支架)水凝胶的机械强度,于半径为4cm,厚度为1cm的模具中,分别加入实施例1和对比例1中待光照的混合物,于紫外光下使两种凝胶完全固化,在两凝胶中相同位置的边缘、中心、内部各打孔取样3次,测定其最终扭转模量。结果如图2所示,其中图2-a为含多孔组织工程支架水凝胶的扭转模量,图2-b为不含多孔组织工程支架水凝胶的扭转模量。
结果表明,加入多孔组织工程支架的水凝胶的整体机械强度均一,且水凝胶的整体机械强度增强。
实验例2
将3g实施例3制备的水凝胶置于0.1mph7.4的pbs缓冲溶液中进行37℃缓慢振荡缓释试验,以4h为区间取样以考察21天内投入量所对应的载bfgf缓释微球的缓释性能,如图3所示。可以看出,实施例3制备的水凝胶bfgf于2天释放了37.02%,于至21天的19天内平稳释放,于21天达到95.62%。
显然,上述实施例仅仅是为清楚地说明所作的举例,而并非对实施方式的限定。对于所属领域的普通技术人员来说,在上述说明的基础上还可以做出其它不同形式的变化或变动。这里无需也无法对所有的实施方式予以穷举。而由此所引伸出的显而易见的变化或变动仍处于本发明创造的保护范围之中。
- 还没有人留言评论。精彩留言会获得点赞!